胃癌肝转移患者预后列线图的建立与危险分层
2022-09-30许雅洁龙泉河杜文涛姜相君
许雅洁 龙泉河 杜文涛 姜相君
胃癌是最常见的恶性肿瘤之一,是癌症相关死亡的第4大原因。肝脏是胃癌最常见的血行转移部位,且胃癌肝转移是造成晚期胃癌患者死亡最主要的原因,胃癌肝转移患者1、3和5年的总生存率分别为33%、6%和4%。近年来,随着化疗、靶向、放疗及手术治疗的发展,胃癌肝转移(gastric cancer liver metastasis,GCLM)的诊疗虽取得了重大进展,但患者的生存期仍然很短,如何制定全方位的治疗策略也成了临床医生关注的焦点。
TNM分期系统是常用的预测肿瘤患者预后的工具。然而,仅用TNM分期评估肿瘤患者的预后具有一定的局限性,因其还与患者年龄、肿瘤部位、是否手术、术后放化疗等多种因素相关。目前迫切需要一种能结合患者的病情和肿瘤的特点来预测患者预后的方法。列线图是一种新的且已被广泛用于评估多种肿瘤预后的方法,它以更直观的图形方式展现,能准确预测单个患者的预后。可用作评估患者预后风险及受益的工具,并有助于临床医生制定个性化的诊疗策略。
对象与方法
1.数据来源:SEER(surveillance epidemiology and end results)数据库是美国国家癌症研究所建立的肿瘤相关登记数据库,包括了全美28%的癌症患者的临床相关信息。使用SEER*Stat8.3.9软件获取了2010~2015年经病理学或影像学诊断为GCLM的患者的信息,包括年龄、性别、种族、肿瘤部位、肿瘤直径、组织学分级、病理类型、TNM分期、原发肿瘤手术情况、肝外转移、放疗、化疗、生存时间、生存状况和死因。此外,回顾性收集2010年1月~2021年7月在青岛市市立医院诊断为GCLM的患者的临床资料作为外部验证组。最后一次随访时间为2021年8月1日。
2.纳入与排除标准:(1)纳入标准:①胃癌为原发肿瘤;②经病理或影像学证实发生了肝转移。(2)排除标准:①1种以上原发肿瘤;②临床信息缺失较多;③生存信息缺失或不完整患者。
3.统计学方法:各变量的构成以百分比表示,通过单因素和多因素回归分析确定影响预后的变量。使用R4.0.4软件构建列线图,即对每个变量分别赋分,将各个变量的分值相加得到的总分在总分标尺上定位,即得到1、3和5年肿瘤特异性生存期(cancer-specific survival,CSS)的概率。使用C指数评估模型的预测能力;AUC评价列线图的敏感度和特异度;校准曲线比较实际结果和预测结果之间的差异。另外,使用X-tile软件计算列线图得分的最佳截断值,据此对患者进行危险分层,使用-法和对数秩检验比较不同风险患者的生存差异,以<0.05为差异有统计学意义。
结 果
1.人口统计学及临床病理特征:从SEER数据库中共筛选出8998例GCLM患者。根据纳入排除标准,最终共有4081例患者纳入了本研究,以白色人种(2993例,73.34%)、中老年(3859例,94.56%)、男性(2947例,72.21%)为主。将上述患者按照7∶3随机分为训练组(=2857)和内部验证组(=1224),此外,从青岛市市立医院收集了119例GCLM患者作为外部验证组。所有患者的信息详见表1。

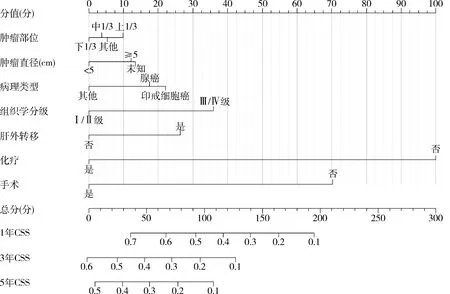
2.变量筛选和列线图构建:对各变量进行单因素回归分析,结果显示,年龄、肿瘤直径、肿瘤部位、组织学分级、病理类型、化疗、原发肿瘤手术、肝外转移与患者的CSS相关(<0.05,表2)。将上述变量纳入多因素回归分析,得出肿瘤部位、肿瘤直径、病理类型、组织学分级、化疗、原发肿瘤手术以及肝外转移是GCLM患者的独立预后因素(表2)。基于上述结果,建立预测预后的列线图(图1)。

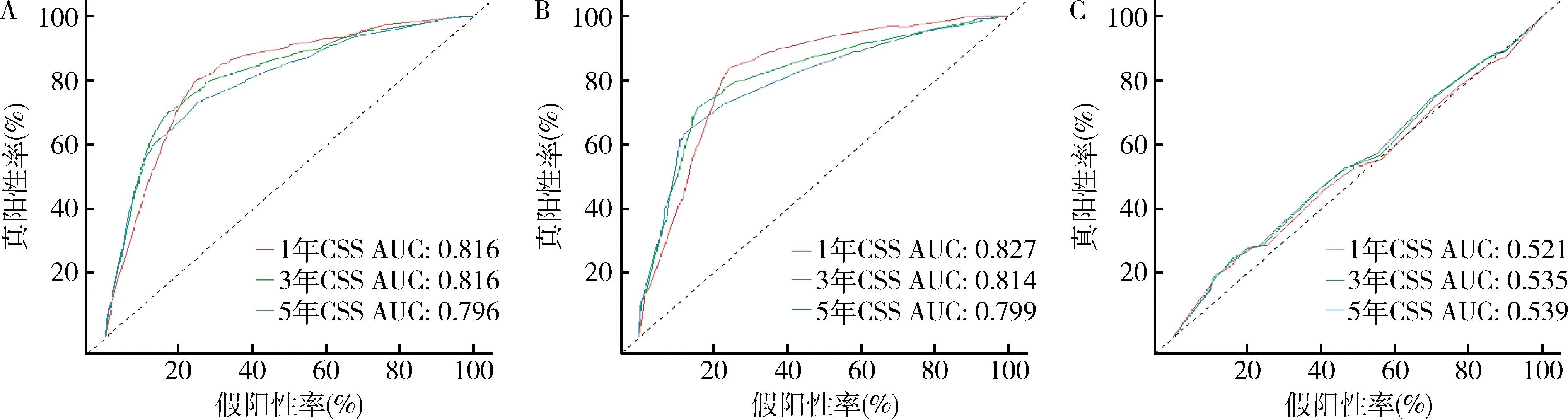
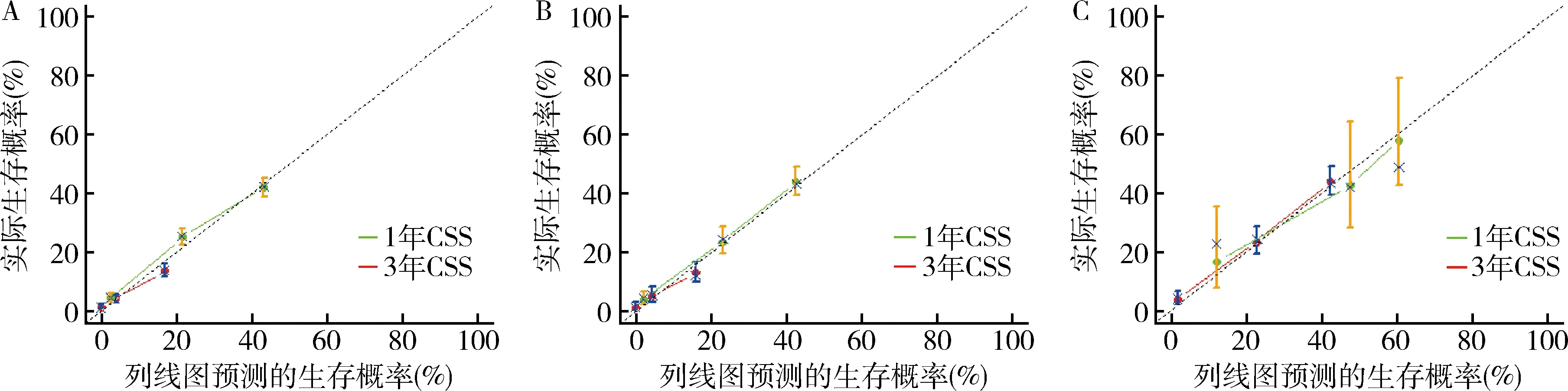
3.列线图验证:训练组C指数为0.720(95% CI:0.710~0.730,=0.005),内部验证组和外部验证组C指数分别为0.724(95% CI:0.708~0.740,=0.008)和0.711(95% CI:0.640~0.784,=0.037),均高于TNM分期系统的C指数(0.557,95%CI:0.543~0.571,=0.007)。训练组1、3和5年CSS的AUC分别为0.816、0.815和0.769(图2中A);内部验证组为0.827、0.814和0.799(图2中B),高于TNM分期的AUC(0.521、0.535和0.539,图2中C),说明列线图预测的准确性较高。校准曲线结果显示列线图预测值与实际值具有良好的一致性(图3)。
4.危险分层:使用X-Tiles软件计算出列线图总分的最佳截断值为164和277(图4),据此将患者分为低、中和高风险组。生存曲线结果显示不同风险层患者的生存概率比较,差异有统计学意义(<0.001,图5)。列线图可以成功区分高危、中危和低危患者的预后。


讨 论
本研究结果显示肿瘤部位、肿瘤直径、病理类型、组织学分级、肝外转移、化疗及手术情况是GCLM患者预后的独立影响因素。据此构建了直观的列线图,且列线图对患者预后的预测能力优于TNM分期。在临床实践中,列线图对评估患者的预后优势突出,能帮助临床医生更好地识别患者的预后风险并做出临床决策。
影响胃癌患者预后的因素众多,但很少有研究探究胃癌原发部位对患者预后的影响。近期有研究显示发生于胃近端1/3的胃癌患者常并发上消化道出血、吞咽困难、胃部不适等症状,且胃癌更容易转移,往往预后较差。Riihimäki等研究发现,与非贲门癌比较,贲门癌更容易向肝脏转移,且贲门癌患者的生存率更低。与上述研究相一致的是,本研究将胃底、贲门部的胃癌定义为上1/3,胃体定义为中1/3,胃窦和幽门定义为下1/3。在训练组和内部验证组中,胃上1/3部肿瘤均占比最多(48.5%和48.3%)。此外相较于胃上1/3部的肿瘤,胃下1/3部位肿瘤的死亡风险更低(HR=0.874,95% CI:0.775~0.987,=0.029)。列线图中胃上1/3部肿瘤得分也较其他部位更高,这可能与胃上1/3部肿瘤的侵袭性更高、更容易发生淋巴结转移和复发有关。从而也证实了胃上1/3部肿瘤是GCLM患者不良预后因素。
肿瘤直径对胃癌患者预后的影响目前仍存在争议,一些研究认为肿瘤直径与胃癌组织学类型、Borrmann分型、TNM分期有关,是影响胃癌患者预后的重要临床指标。另一方面,一些研究者认为肿瘤直径是一个不可靠的指标,通过肉眼或组织学只能粗略测量肿瘤的直径,肿瘤直径不能作为影响预后的独立危险因素。近年来有研究认为,胃癌大于5cm应被视为是预后不良的危险因素。本研究以5cm为分界值,单因素和多因素分析均得出肿瘤直径≥5cm与GCLM患者预后不良相关。可能由于肿瘤越大,往往分期越晚,且较大的肿瘤具有较强的侵袭性和转移性,从而导致预后不良。
GCLM患者出现肝脏以外部位的转移预示患者进入肿瘤的更晚期阶段,提示患者的预后更加不良。而化疗是目前进展期胃癌的标准一线治疗方法,NCCN临床实践指南推荐进展期胃癌的化疗药物主要包括氟尿嘧啶、铂类化合物、紫杉醇等。在本研究构建的列线图中,未化疗的得分最高,说明化疗在影响GCLM患者的预后中非常重要。然而,尽管目前开发了新的化疗药物及分子靶向药物,进展期胃癌的预后仍然不乐观。单独化疗并不能维持部分晚期胃癌患者的长期生存,中位总生存时间仅为13.8个月。
手术在GCLM患者治疗中仍存在诸多争议。一方面,切除癌组织可以减轻肿瘤负荷、消除新发转移的来源、改善胃癌所引起的症状,延长患者的生存时间。Lasithiotakis等的Meta分析结果显示,接受胃癌切除术的晚期胃癌患者与非手术治疗的患者比较,1年的OS显著延长(OR=2.6,95% CI:1.7~4.3,<0.001),且患者术后的生活质量和症状均有改善。而另一方面,一项多中心的REGATTA研究显示胃癌切除可能会导致免疫抑制从而促进转移,术后并发症的出现也将会延迟全身化疗的时间,降低化疗的耐受性,在有单一不可治愈因素的晚期胃癌患者中,姑息性胃切除手术与单纯化疗比较,没有显著的生存益处。本研究所构建的列线图中,未行手术治疗得分仅低于未化疗,说明手术在GCLM患者的重要性仅次于化疗。手术是GCLM患者预后的保护性因素,也是预测GCLM患者预后的重要预测因子。
综上所述,本研究利用SEER数据库数据构建了可靠的预后列线图并对患者进行了危险分层。列线图可以成功区分不同风险患者的CSS,对临床诊疗有一定的指导意义。本研究尚存在一些局限性。首先,SEER 数据库中缺乏患者的具体化疗及手术方案,其次,作为一项大型回顾性研究,患者的选择可能会受到选择偏差的影响。最后,笔者纳入的所有变量都是已知的危险因素,还有许多与GCLM患者预后相关的危险因素仍需要开展进一步研究予以证实。
