煤气化细渣高温碱活化制备高性能孔雀石绿吸附材料的研究*
2022-09-23郭飞强白家明毛松波白永辉
舒 锐 郭飞强 白家明 毛松波 钱 琳 白永辉
(1.中国矿业大学低碳能源与动力工程学院,221116 江苏徐州;2.宁夏大学省部共建煤炭高效利用与绿色化工国家重点实验室,750021 银川)
0 引 言
孔雀石绿是一种人工合成的有机化合物,被广泛应用于工业印染行业。但孔雀石绿具有一定毒性,进入人体后容易在体内产生致癌的代谢物,严重危害身体健康,因此对孔雀石绿废水污染的治理至关重要。孔雀石绿废水普遍的处理方法为催化降解法和吸附法等。VERMA et al[1]采用溶胶/凝胶法制备了柠檬酸和油酸改性的氧化钴纳米材料,并通过光催化降解对染料的降解率达到了91.2%,但催化降解成本高、处理速度慢,无法大规模应用。吸附法作为一种经济环保与治理高效的方法受到大多数研究者的关注。ZHANG et al[2]通过碳化固化的氧化镁/氰酸酯树脂混合物来制备双重氧化镁负载碳泡沫,对孔雀石绿的吸附量达到了1 874.18 mg/g。
煤气化细渣是煤炭气化过程中产生的固体废弃物,对环境有一定的污染性。为响应绿色发展战略,国家开展了对煤气化细渣的综合利用研究[3],合成的材料用于污水治理[4]效果显著,达到了以废治废的理想效果。RODWIHOK et al[5]采用一锅水热法制备了碱/锌活化煤气化细渣纳米复合材料,通过纳米复合材料与染料分子的静电吸附力达到处理污水的目的。CHEN et al[6]用盐酸和氢氧化钠溶液对煤气化细渣进行改性研究,改性后其比表面积增加,孔隙结构得到改善,改性材料对污水中有机物的吸附能力大大提高。
对煤气化细渣进行活化改性可以改善其孔隙结构,增强表面官能团活性,从而大幅提升吸附效果。煤气化细渣的活化改性工艺有酸改性活化[7]、碱改性活化[8]和沸石合成[9-10]等。酸改性活化可以增大其比表面积,进而增强吸附能力[11],但其官能团容易被破坏。沸石的孔隙结构好,但合成工艺复杂、成本高。高温碱活化法相比于传统的沸石合成工艺[12-13]产生的洗涤废水极少,同时具有经济性好、处理效果更佳的优势,此方法更适合推广应用。
本研究通过高温条件下碱活化[14]煤气化细渣制备高性能的吸附剂。本实验旨在探究合成吸附材料的最佳活化温度,并将合成的吸附剂应用于孔雀石绿的吸附实验,验证其对于孔雀石绿的吸附特性,同时进行相应的吸附动力学研究和吸附原理分析。
1 实验部分
1.1 原料
本实验所用煤气化细渣取自宁夏回族自治区某煤气化公司GSP气化设备,命名为FS@GSP。原料的工业分析和元素分析分别按照GB/T 212-2008和GB/T 31391-2015中的方法测量,结果如表1所示,其化学成分分析如表2所示。由表1可知,经气化后的FS@GSP主要组分为灰分,并含有一定量的无定形碳。由表2可知,FS@GSP的XRF分析结果显示,其主要组分为SiO2和Al2O3,同时还含有一定量的Fe2O3和MgO等金属氧化物。一般认为SiO2和Al2O3是构成吸附材料基体结构的重要成分,丰富的金属氧化物有助于提高吸附活性,因此,FS@GSP具有制备良好吸附材料的潜力。

表1 FS@GSP的工业分析和元素分析Table 1 Proximate and ultimate analyses of FS@GSP

表2 FS@GSP的化学成分分析(%*)Table 2 Chemical composition analysis of FS@GSP(%*)
1.2 煤气化细渣合成吸附剂实验
FS@GSP在原始的GSP气化设备经过了高温反应及冷凝,无机组分逐渐缩聚成球形结构。金属氧化物附着在球体表面,堵塞了FS@GSP表面孔隙,不利于吸附的进行。高温加碱煅烧[15]能有效活化FS@GSP,碱性活化剂在高温下呈现熔融状态,与FS@GSP反应更充分,能有效增强反应强度,达到充分反应活化的目的[16]。因此,本研究设计了NaOH高温活化的方法,并在不同温度下制备了吸附材料。
首先将FS@GSP过300目筛,然后放置于鼓风干燥箱干燥24 h。称取5 g FS@GSP干料与5 g NaOH固体于刚玉舟,加入20 mL去离子水使其溶解。然后用磁力搅拌器以60 r/min搅拌5 min,保证其充分混合,随后放置于鼓风干燥箱中干燥至不流动状态。最后转移至管式卧式炉中,通入流量为300 mL/min的N2,以10 ℃/min的升温速率升温至预定温度后保温90 min。结束反应后在N2保护下冷却至室温,将活化后的材料取出,在研钵中研磨后过300目筛。取筛分后的材料用去离子水多次洗涤、抽滤直至pH稳定。再将滤饼置于鼓风干燥箱中干燥24 h,取出过300目筛后得到吸附材料,合成的材料命名为FS@GSP-AC-x(AC代表活化(activation),x代表活化处理温度)。NaOH的熔点为318.4 ℃、沸点为1 390.0 ℃。因此,反应温度应设置在318.4 ℃~1 390.0 ℃之间。综合设备情况以及能耗考虑,本次实验选择的活化温度范围为300 ℃~900 ℃。通过对孔雀石绿的吸附脱除情况确定制备吸附材料的最优活化温度。
1.3 表征方法
将材料研磨并过300目筛,干燥24 h后进行各项表征。本研究采用Quqnta 400 FEG型扫描电镜(美国,FEI公司)研究FS@GSP和FS@GSP-AC-x的微观结构,观测其表面形貌的变化。采用SmartLab(3 kW)型X射线衍射仪(日本,Rigaku公司)对样品进行X射线衍射,分别在5°~90°的2θ范围内获得FS@GSP和FS@GSP-AC-x的X射线衍射谱,以确定材料的成分组成。利用3Flex型快速比表面积和孔隙率分析仪(美国,Micromeritics公司)在77 K下测量N2吸附-解吸等温线。根据Brunauer-Emmet-Teller方程,基于p/p0=0.99的相对压力下的氮气吸附值,计算样品的比表面积(SBET)和总孔隙体积(VT),用t-plot法计算了微孔比表面积(Smic)和微孔体积(Vmic),基于吸附分支的Barrett-Joyner-Halenda(BJH)方法得到介孔比表面积(Smes)和介孔体积(Vmes),并用密度泛函理论(NLDFT)计算样品的孔径分布。用Nicolet iS50型傅立叶变换红外吸收光谱仪(美国,Thermo公司)分析吸附实验前后样品的表面官能团变化,并记录了450 cm-1~4 000 cm-1范围内的光谱。
1.4 吸附实验
首先,配制100 mg/L~500 mg/L的孔雀石绿溶液,使用UV-1800型紫外分光光度计在618 nm波长下分别检测其吸光度,绘制孔雀石绿的标准曲线,用以计算不同吸光度的孔雀石绿溶液质量浓度。
吸附实验包含两部分内容,首先开展不同活化温度对材料吸附性能的影响研究,本实验以单因素实验为基础,考察活化温度对FS@GSP-AC-x吸附值的影响。测定FS@GSP-AC-x对同一质量浓度孔雀石绿溶液的吸附值,以吸附值表示其吸附性能的高低。温度组以100 ℃为梯度,共设置300 ℃~900 ℃的7个实验组别。同时,将未经处理的FS@GSP作为对照组。在吸附实验中,称取0.02 g不同温度条件下制备的FS@GSP-AC-x和原材料FS@GSP,投加至200 mL初始质量浓度为500 mg/L的孔雀石绿溶液中。放入振荡频率为130 r/min的恒温振荡器中,在25 ℃下振荡720 min基本达到吸附平衡。待吸附过程结束,取约3 mL的孔雀石绿溶液过滤并测定滤液吸光度。然后计算溶液浓度,并随之计算FS@GSP-AC-x对孔雀石绿的吸附量和脱除率,筛选出性能相对较优的样品。
其次,针对筛选出的样品开展吸附动力学实验。在动力学实验中,称取0.02 g的FS@GSP-AC-x投加至200 mL初始质量浓度分别为100 mg/L,200 mg/L和500 mg/L的孔雀石绿溶液中。并设置对照组,具体为称取0.02 g的FS@GSP投加至200 mL初始质量浓度为500 mg/L孔雀石绿溶液中。放入振荡频率为130 r/min的恒温振荡器中,在25 ℃下吸附1 440 min。其间在第5分钟、第10分钟、第15分钟、第30分钟、第60分钟、第90分钟、第120分钟、第180分钟、第240分钟、第300分钟、第360分钟、第420分钟、第540分钟、第720分钟、第900分钟、第1 080分钟、第1 260分钟、第1 440分钟18个时刻取出3 mL的孔雀石绿溶液,过滤并测定滤液吸光度,检测完倒回继续吸附过程。计算以上时刻的溶液浓度,并计算FS@GSP-AC-x样品对孔雀石绿的吸附量以及最终的脱除率,将t(min)时刻和对应的吸附量Qt(mg/g)数据输入Origin软件,并进行准一阶和准二阶吸附动力学拟合,完成后输出拟合的各项数据结果,最后进行动力学分析。
在吸附实验中t时刻的吸附量Qt由公式(1)计算得出,脱除率ηt由公式(2)计算得出。
(1)
(2)
式中:ρ0和ρt分别为孔雀石绿溶液的初始质量浓度和震荡过程中t时刻的质量浓度,mg/L;V是孔雀石绿溶液的体积,L;m代表FS@GSP-AC-x的投加量,g。
2 结果与讨论
2.1 活化温度对吸附性能的影响
为探究活化温度对FS@GSP-AC-x对孔雀石绿吸附性能的影响,本实验设计了完全相同的5次吸附实验,并测量吸附值,同时以误差棒分析测量值偏差。记录的7个实验组FS@GSP-AC-x与对照组FS@GSP的平均吸附值、脱除率与误差分析,结果如图1所示。

图1 活化温度对吸附量的影响Fig.1 Effect of activation temperature on adsorption value
由图1可知,FS@GSP-AC-x对孔雀石绿溶液的吸附值随着活化温度提高逐步升高。与FS@GSP 472.3 mg/g的吸附值和9.50%的脱除率相比,FS@GSP-AC-x的吸附性能通过高温碱活化后得到了极为明显的提升,然而当活化温度达到800 ℃后,继续升高温度对材料的吸附值提升不明显。综合分析,800 ℃在本研究中是最优活化温度。因此,本实验选择FS@GSP-AC-800进行表征与吸附动力学分析。
2.2 FS@GSP与FS@GSP-AC-800的表征分析
选取FS@GSP与FS@GSP-AC-800为样本分析其表面形貌,其SEM照片如图2所示。由图2和表2可知,FS@GSP中的球状物质为SiO2微珠[17],Al2O3和Fe2O3等金属氧化物包覆于SiO2微珠外表面,无定形碳存在于金属包覆的SiO2微珠间隙。经800 ℃下NaOH活化处理后,FS@GSP-AC-800的表面形貌发生了巨大改变。由于SiO2和Al2O3与NaOH发生了化学反应,使得球状结构遭到了破坏,反应从SiO2微珠外表面反应至内部,最终形成了连通的孔道,呈现规则的多孔结构。

图2 样品的SEM形貌特征Fig.2 SEM morphological characteristics of samplesa,b—FS@GSP;c,d—FS@GSP-AC-800
FS@GSP与FS@GSP-AC-800的XRD谱如图3所示。由图3可知,在FS@GSP样本中,呈现以20.80°和26.57°为中心的衍射峰,该衍射峰对应于SiO2晶体结构,在43.29°表现为Al2O3较弱的衍射峰。经800 ℃的NaOH活化处理后,FS@GSP-AC-800在20.91°,34.47°,49.49°和61.62°等位置出现了强度较高的NaAlSiO4特征峰,并且SiO2和Al2O3特征峰完全消失,说明活化过程中原始物质结构遭到了完全的破坏并生成了新物质NaAlSiO4(霞石),该物质是一种具有良好吸附性能的材料[18],合成的材料与数据库标准卡片(Na-Nepheline PDF#11-0221)高度吻合,表明实验成功合成了具有高结晶度的霞石。一般认为,在FS@GSP活化的过程中,Al2O3,SiO2和NaOH在高温下发生了化学反应,进行了结构重组,最终合成了霞石,发生的化学反应如公式(3)所示。

(3)
FS@GSP与FS@GSP-AC-800的比表面积和孔体积参数如表3所示。由表3可知,FS@GSP的孔隙主要是其二氧化硅微球的介孔,其比表面积为105.601 m2/g,孔体积达到0.144 cm3/g,平均孔径为5.473 nm。图4所示为FS@GSP和FS@GSP-AC-800的孔径分布。由图4可知,FS@GSP-AC-800孔径更大。这是因为在活化过程中发生了化学反应,原有的孔隙结构遭到破坏,结构重组后形成了较大的介孔,最终生成了霞石。FS@GSP-AC-800的比表面积降低到64.117 m2/g,孔体积提升至0.218 cm3/g,平均孔径为13.619 nm。根据孔径分布可以看出,两种材料有明显的差异,对孔雀石绿的吸附机理也不同。FS@GSP的吸附能力主要依靠其SiO2的介孔的范德华力,属于物理吸附。活化过后FS@GSP-AC-800的孔径和孔体积变大,有利于吸附质分子在吸附剂的内部扩散。FS@GSP-AC-800中的霞石是产生吸附作用的主要物质,霞石的孔径大、表面官能团丰富,利于发生化学吸附,相比于FS@GSP的物理吸附,FS@GSP-AC-800的吸附性能更强。

图3 FS@GSP与FS@GSP-AC-800的XRD谱Fig.3 XRD patterns of FS@GSP and FS@GSP-AC-800

表3 FS@GSP与FS@GSP-AC-800的孔隙结构参数Table 3 Pore structure parameters of FS@GSP and FS@GSP-AC-800

图4 FS@GSP与FS@GSP-AC-800的孔径分布Fig.4 Pore size distributions of FS@GSP and FS@GSP-AC-800
为具体分析两种材料的孔隙结构特征,采用了N2吸脱附对其进行测试,FS@GSP与FS@GSP-AC-800的N2吸附-解吸等温线如图5所示。由图5可知,根据IUPAC的分类[19],两种材料的迟滞环(p/p0范围在0.40到0.99之间)对应于H3迟滞环的Ⅳ型,表明材料以介孔结构为主。FS@GSP-AC-800相比于FS@GSP在饱和区具有更高的氮气吸附量,说明FS@GSP-AC-800的孔体积更大,孔隙结构更发达。
根据吸附量与比表面积参数建立比表面积和吸附能力之间的关系式(4),ES为单位比表面积吸附量,mg/m2;Qe为平衡吸附量,mg/g;SBET为材料的比表面积,m2/g。
(4)
根据公式(4)计算得FS@GSP与FS@GSP-AC-800单位比表面积吸附量分别为4.45 mg/m2和74.57 mg/m2。表明经活化处理后的材料吸附能力得到极大增强,推测是霞石的表面官能团产生化学吸附作用,后面将根据FTIR表征对其吸附原理具体说明。

图5 FS@GSP与FS@GSP-AC-800的N2吸附-解吸等温线Fig.5 N2 adsorption-desorption isotherms of FS@GSP and FS@GSP-AC-800
2.3 FS@GSP-AC-800对孔雀石绿的吸附动力学
孔雀石绿的吸附量随时间的变化情况如图6所示。由图6可知,随着吸附过程的进行, 孔雀石绿分子到达FS@GSP-AC-800表面并扩散至其孔道内,吸附量呈不断上升趋势。吸附至一定时间,溶液浓度与吸附剂表面浓度差降低,传质推动力减小,使其吸附速率不断降低。曲线在720 min左右趋于平坦,可以判断吸附过程基本达到动力学平衡,认为此刻的吸附量接近饱和吸附量[20]。由图6还可知,在吸附温度同为25 ℃和恒温振荡器振荡频率同为130 r/min情况下,随着初始浓度升高,孔雀石绿的吸附量有明显升高。这是由于FS@GSP-AC-800投加量固定不变,随着孔雀石绿溶液初始质量浓度增加,孔雀石绿的分子数量随之增加,吸附质分子向定量的吸附剂的传质量增加,从而提升了吸附值。

图6 孔雀石绿吸附量与吸附时间和初始质量浓度的关系Fig.6 Relationships between adsorption value and adsorptiontime of malachite green with different mass concentrations
本实验采用准一阶动力学模型(Pseudo first-order model)和准二阶动力学模型(Pseudo second-order model)来描述FS@GSP-AC-800对孔雀石绿的吸附过程,具体如公式(5)和公式(6)所示。
ln (Qe-Qt)=lnQe-K1t
(5)
(6)
式中:Qe为通过模型拟合求出的理论值平衡吸附值,mg/g;t为吸附过程所对应的时刻,min;K1为一阶方程吸附速率常数;K2为二阶方程吸附速率常数,其取值与温度有关。
对图6中的吸附过程使用以上两种模型进行动力学拟合,其拟合模型如图7所示,计算得到的动力学参数见表4(其中Qexp表示实验测得的真实吸附值)。由表4可以看出,对于FS@GSP-AC-800的吸附过程,采用准二阶动力学模型(PSO)拟合的相关系数(R2)高于准一阶动力学模型(PFO)。通过准二阶动力学方程计算得出的平衡吸附量Qe更接近实验值。因此,选择准二阶动力学模型更适用于描述FS@GSP-AC-800对孔雀石绿的吸附过程[21]。根据准二阶动力学模型假设,FS@GSP-AC-800对孔雀石绿的吸附主要受化学吸附机理影响,吸附剂与吸附质之间的吸引力主要依靠静电引力和化学键形成等产生。而FS@GSP对孔雀石绿的吸附过程更符合准一阶动力学模型,通过准一阶动力学方程计算得出的平衡吸附量Qe更接近实验值。其吸附过程受物理吸附机理影响,主要依靠FS@GSP自身孔隙结构的范德华力。对比同为500 mg/L的孔雀石绿溶液,FS@GSP-AC-800的吸附量(4 740.05 mg/L)远高于FS@GSP的吸附量(472.30 mg/L),表明合成材料的吸附能力得到巨大提升。

图7 吸附孔雀石绿的动力学非线性拟合曲线Fig.7 Nonlinear fitting curves of adsorption kinetics of malachite green
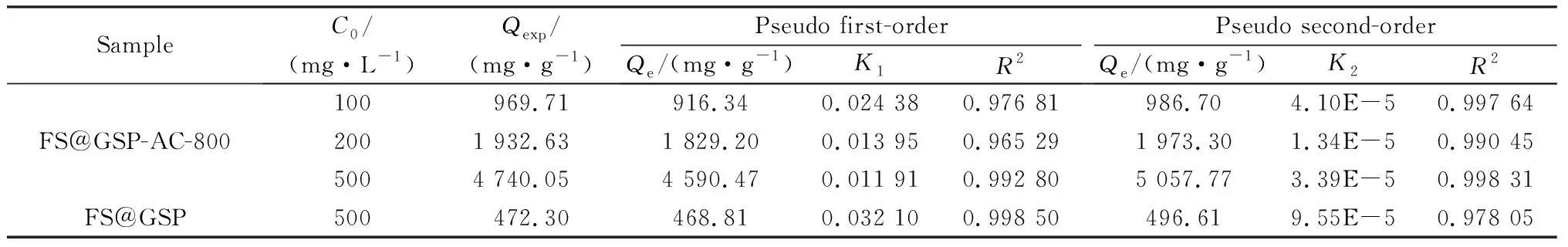
表4 FS@GSP与FS@GSP-AC-800吸附孔雀石绿的动力学参数Table 4 Kinetic parameters of adsoring malachite green by FS@GSP and FS@GSP-AC-800
2.4 FS@GSP-AC的吸附机制分析
根据原料的物质组成与结构分析,可以推测原料FS@GSP对孔雀石绿的吸附能力来自SiO2微珠的孔道结构。由于SiO2微珠表面被金属氧化物包覆,导致其孔道部分被阻塞,致使FS@GSP的吸附能力在一定程度上被抑制。此外,FS@GSP中含有大量SiO2和Al2O3,SiO2晶体的晶格中具有稳定的≡Si—O—Si≡网络结构,使其化学活性较低。采用NaOH活化提高FS@GSP的活性,其原理为Na—O离子键的键强明显小于SiO2的Si—O共价键和Al2O3的Al—O共价键的键强,使得Na—O中的O易于被Si4+和Al3+夺去,活性低的共价键转变成高活性的离子键,其一半的Si被Al代替,空间结构中心的Na+与晶体空间结构以离子键配合,生成霞石(NaAlSiO4)。霞石具有类似SiO2的晶体结构,具有极佳的吸附性能。SiO2与Al2O3和NaOH的化学反应由SiO2微珠的表面至内部,使FS@GSP-AC-800的孔隙容积有明显提升,为吸附提供足够的场所,提升了FS@GSP-AC-800对孔雀石绿的吸附性能。
FS@GSP-AC-800对孔雀石绿的吸附动力学结果显示了其极佳的吸附效果,与准二阶吸附动力学高度拟合,表明吸附过程受化学吸附机理控制。化学吸附机理一般伴随官能团的变化,与FS@GSP-AC-800和孔雀石绿的官能团[22-23]相关。为进一步分析吸附原理,对吸附前的材料FS@GSP-AC-800和吸附后的材料FS@GSP-AC-800-Adsorption进行FTIR表征[24],其红外光谱见图8。由图8可以看出,吸附前后材料的光谱在波数1 000 cm-1和3 400 cm-1处发生了明显变化。在3 400 cm-1处的吸收峰归属于霞石表面丰富的O—H基团,在液相环境中与孔雀石绿易形成氢键(N—O),造成O—H吸收峰的强度变化,其形成化学键的吸附原理如图9所示。由图9可知,O—H在溶液中极易失去H+变成带负电的O-,与失去Cl-后的阳离子孔雀石绿分子(MG+)产生静电吸引。在1 000 cm-1处的吸收峰属于材料的中的—Si—O—Si—键,位于波数小于1 600 cm-1的区域,属于红外光谱指纹区,当分子结构稍有不同时,该区吸收峰就有显著的差异。FS@GSP-AC-800与孔雀石绿分子以氢键或静电吸引的方式结合,造成材料分子结构产生了变化,使得—Si—O—Si—的峰强改变。
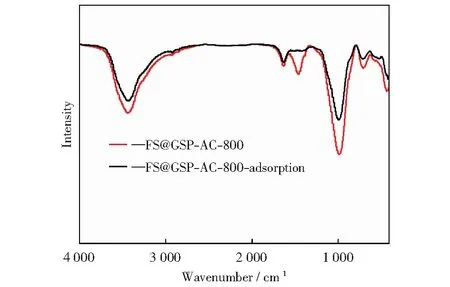
图8 FS@GSP-AC-800在吸附前后的红外光谱Fig.8 Infrared spectra of FS@GSP-AC-800 before and after adsorption

图9 FS@GSP-AC-800对MG的吸附原理Fig.9 Adsorption schematic diagram of MG by FS@GSP-AC-800
3 结 论
1) 选择活化温度800 ℃可以得到吸附性能最佳的FS@GSP-AC-800,吸附实验中对500 mg/L的孔雀石绿的吸附值可达4 784.1 mg/g,脱除率可以达到95%。
2) FS@GSP的吸附能力较低,而FS@GSP-AC-800具有极强的吸附性能,其原因在于FS@GSP的吸附能力主要依靠其中的SiO2微珠的介孔的物理吸附,FS@GSP-AC-800则依靠其中的新物质霞石的化学吸附,其丰富的官能团为其提供了大量的吸附活性位点,使得吸附值显著提升。
3) FS@GSP-AC-800对孔雀石绿的吸附结果表明,其吸附动力学模型更接近于准二阶模型,吸附过程主要受化学吸附机理的影响,分析了吸附前后的官能团变化,发现FS@GSP-AC-800与孔雀石绿之间的吸附是依靠静电引力和新形成的氢键。
