含水硅酸盐熔体中铜溶解度的实验研究
2022-08-31刘星成熊小林邢长明
刘星成, 许 婷, 熊小林, 李 立, 王 煜, 邢长明
含水硅酸盐熔体中铜溶解度的实验研究
刘星成1, 2, 3, 许 婷1, 2, 3, 熊小林1, 2, 3, 李 立1, 2, 王 煜1, 2, 邢长明1, 2
(1. 中国科学院 广州地球化学研究所, 同位素地球化学国家重点实验室, 广东 广州 510640; 2. 中国科学院深地科学卓越创新中心, 广东 广州 510640; 3. 中国科学院大学, 北京 100049)
富Cu岩浆是形成大型‒超大型斑岩型Cu矿床的有利条件, 但形成富Cu岩浆的有利物理化学条件尚不清楚。为了制约温度、压力、熔体成分、氧逸度等因素对含水硅酸盐熔体中Cu溶解度的影响, 本次研究采用Pt95Cu05作为样品管, 使用活塞圆筒装置开展了一系列高温高压实验。实验初始物成分涵盖镁铁质到长英质, 实验温度范围为850~1250 ℃, 压力范围为8~30 kbar, 氧逸度范围约为FMQ–5~FMQ+5。实验结果表明长英质熔体中Cu溶解度主要受温度和熔体成分控制, 受压力影响不明显。在相似氧逸度条件下, 当温度从1250 ℃下降到850 ℃时, Cu溶解度降低了约两个数量级。在相同温度和相似氧逸度条件下, 玄武质、安山质和英安质熔体中Cu溶解度差别较小。但当熔体演化为花岗质或流纹质熔体时, Cu溶解度骤降约一个数量级。因此, 当中酸性岩浆演化到晚期, 随着温度的降低和熔体成分变化, 其运移Cu的能力会迅速降低, 不利于富Cu岩浆的产生。在中酸性岩浆演化过程中, 如果流体过晚出溶, 将不利于形成富Cu流体, 难以为大型矿床的形成提供足够的成矿元素。
铜溶解度; 硅酸盐熔体; 高温高压实验; 斑岩型铜矿床
0 引 言
斑岩型Cu矿床提供了全世界绝大部分的Cu产量, 它们大多形成于汇聚板块边缘, 直接或间接地受俯冲板片影响(Sillitoe, 2010; Sun et al., 2015; Hou et al., 2015)。在俯冲带地区, 俯冲板片脱水交代上覆地幔楔, 形成含水玄武质母岩浆, 其在下地壳经历岩浆演化最终形成中酸性的成矿岩浆。这些岩浆一般具有埃达克质特征(高Sr/Y值)且具有富水和氧化等特点(Audétat and Simon, 2012; Richards, 2013; Chen and Wu, 2020; Xiong et al., 2020)。然而同一构造背景下常见成矿和不成矿岩浆活动共存现象, 这些岩浆中仅有一小部分能够形成具有经济价值的矿床(Chen and Wu, 2020)。这表明斑岩型Cu矿床的形成, 特别是大型矿床的形成需要同时具有多个有利成矿条件。
斑岩型Cu矿床属于岩浆‒热液型矿床, 当流体从岩浆中饱和出溶时, Cu总是倾向于进入流体相(Liu and Xiong, 2018; Audétat, 2019), 意味着富Cu的母岩浆有利于形成富Cu热液。通过质量平衡计算可知, 大型或者超大型斑岩型矿床的产生需要成矿热液从一个超大岩浆房或者富Cu母岩浆中高效萃取足够的Cu。虽然富Cu岩浆不是形成岩浆‒热液矿床的必要条件, 但富Cu中酸性岩浆是大型、超大型矿床形成的一个有利条件, 甚至可能是必要条件。Cu在岩浆中的溶解度会影响其在岩浆、硅酸盐矿物、硫化物和流体间的分配行为(Zajacz et al., 2013, Liu et al., 2021)。而含水中酸性岩浆作为成矿过程中Cu运移的重要载体, 它们溶解和运移Cu的能力直接影响岩浆成矿潜力。因此, 查明俯冲带温压条件下, 控制Cu在含水岩浆中溶解度的主要因素、厘清形成富Cu岩浆的有利物理化学条件, 有助于理解成矿过程中岩浆阶段成矿金属的运移和富集。针对硅酸盐熔体中Cu溶解度的实验研究, 前人多聚焦于低压、高温、不含水的基性‒中性体系(Holzheid and Lodders, 2001; Ripley and Brophy, 1995; Ripley et al., 2002; Zajacz et al., 2012; 2013; Liu et al., 2014; 2015), 而对含水中酸性岩浆体系中Cu溶解度研究较少且并未得到较好的限定, 这也制约了全面理解斑岩型Cu矿床成矿过程中Cu的运移与富集。
为了定量研究温度、压力、熔体成分和氧逸度(O2)对Cu在含水中酸性硅酸盐熔体中的溶解度, 本次研究开展了一系列活塞圆筒实验。实验初始物采用人造花岗岩、英安岩与玄武岩, 实验温度为850~1250 ℃, 压力为8~30 kbar, 氧逸度范围约为FMQ–5~FMQ+5(FMQ为铁橄榄石‒磁铁矿‒石英氧逸度缓冲对)。结合前人数据和本次研究的实验结果, 对斑岩型Cu矿床成矿过程中形成富Cu岩浆的有利条件进行了系统评估。
1 实验和分析方法
1.1 实验初始物与样品容器
为了研究硅酸盐熔体成分对Cu溶解度的影响, 本研究使用了三种不同组成的初始物(表1), 包括合成的人造花岗质(HG)和英安质(Dacite)玻璃以及玄武岩粉末(Xiong et al., 2005)。初始物粉末合成步骤如下: ①首先将所需元素的氧化物或碳酸盐(SiO2、 Al2O3、Fe2O3、MgO、TiO2、MnO、NiO、P2O5、Cr2O3、CaCO3、Na2CO3和K2CO3)化学试剂按比例称量后混合; ②加入丙酮后在玛瑙研钵里研磨15分钟; ③再将粉末置于Pt坩埚里后放入马弗炉, 加热到1000 ℃并保持10小时以去除碳酸盐中的CO2; ④升温到1500 ℃并保持2小时; ⑤将Pt坩埚迅速取出并放入蒸馏水中淬火; ⑥将淬火玻璃加入丙酮后在玛瑙研钵里研磨至少2 小时。为了使初始物充分混合均匀, 重复步骤③~⑤进行第二轮混合。同时, 在进行第二轮研磨前, 取一小块淬火玻璃用于电子探针分析以确定初始物成分。

表1 实验初始物组成(%)
注:初始物玻璃均由电子探针测定, 平均每个初始物测试十个点。括号里为1σ标准偏差。
采用Pt95Cu05合金管作为样品容器(由贵研铂业有限公司制造, Pt为95%, Cu为5%), 这些合金管提供了实验中Cu旳来源。使用传统双管技术控制氧逸度(Chou, 1987): 内外管均为Pt95Cu05合金管, 外管为5.0 mm OD(外径), 4.7 mm ID(内径); 内管为3.0 mm OD, 2.7 mm ID(图1a)。先将15 mg左右的初始物粉末加入5%~12%水后直接装入内管, 然后夹紧并使用LAMPERT PUK U3钨针弧焊机焊封。焊封前后对内管进行称量, 确保焊封时没有明显的水损失; 随后将焊封好的内管放入烘箱数小时, 再次称量以确保成功焊封; 最后将焊封好的内管、固体氧逸度缓冲剂和水共同放入外管并焊封。同样, 焊封前后与放入烘箱前后进行称量, 确保焊封完成且没有明显水损失。如果称量前后样品管重量发生明显变化, 表明焊封失败, 这些未焊封好的样品将弃之不用。在大部分实验中, 一个外管只放入一个内管, 但为了对比不同熔体组成在相同温度、压力和氧逸度条件下Cu溶解度的差异, 分别在实验XT168N-9中放入了两个内管, 其分别封装了一个玄武质玻璃和一个英安质玻璃初始物(与Liu et al., 2015中MDS实验一致)。
本次研究使用了多种固体氧逸度缓冲剂控制氧逸度, 包括IW(铁‒方铁矿)、NNO(Ni-NiO)、MMO (MnO-Mn3O4)、HM(赤铁矿‒磁铁矿), 氧逸度变化范围为FMQ-5~FMQ+5(Haas and Robie, 1973; O’Neill, 1987; Frost, 1991; O’Neill and Pownceby, 1993a, 1993b)。实验中, 水分解形成的H2将在内外管间扩散平衡, 以达到氢逸度(H2)的平衡, 从而控制样品的氧逸度。
1.2 活塞圆筒高温高压实验
高温高压实验在中国科学院广州地球化学研究所和德国拜罗伊特大学巴伐利亚州地质研究所(Bayerisches Geoinstitut)的单向加压、固体传压型活塞圆筒上完成。实验采用1/2英寸组装(碳酸钡/NaCl套+石墨炉+氧化镁套), 具体尺寸描述见阮梦飞等(2020)。实验温度为850~1250 ℃, 压力为8~30 kbar,实验运行时间为24~150小时, 实验条件见表2。
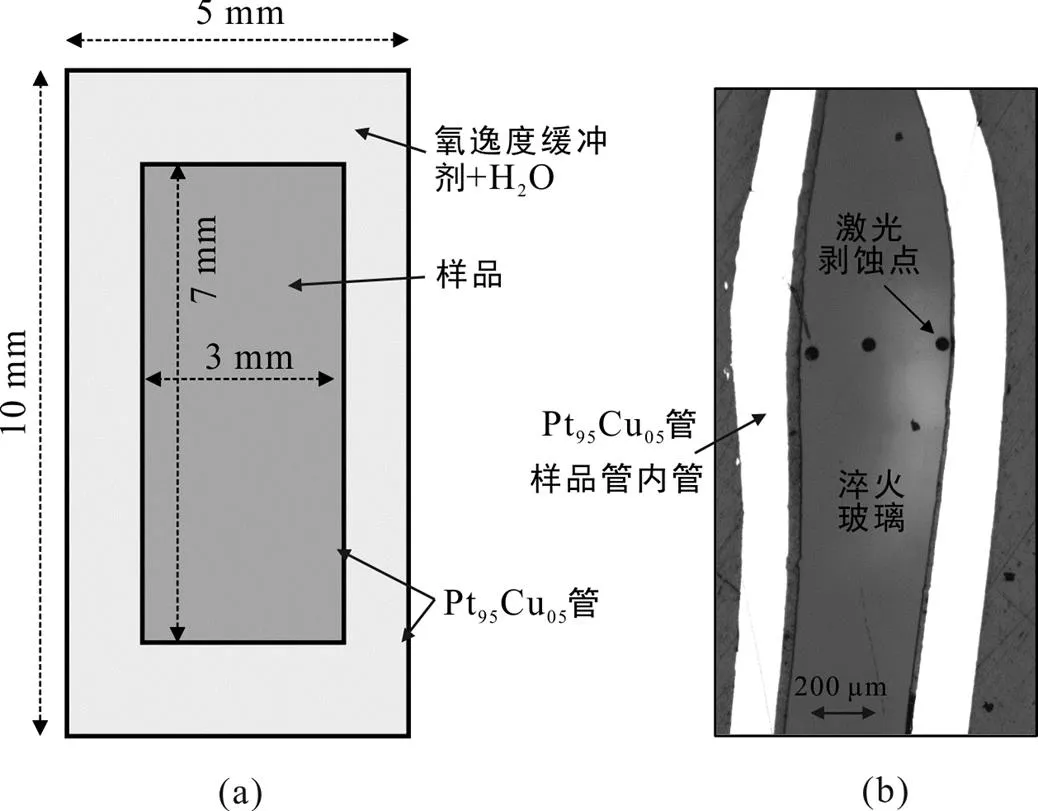
图1 实验样品管组装设计示意图(a)与代表性实验产物图(b)
活塞圆筒实验的压力控制采用自动控压系统。中国科学院广州地球化学研究所的活塞圆筒摩擦校正为13%, 拜罗伊特大学的仪器为18%; 温度并未做校正, S型热电偶(Pt-Pt90Rh10)接到Eurotherm控温器上, 实验中温度变化大致为±2 ℃, 整个样品内管的温度梯度约为±15 ℃(Liu et al., 2015)。实验结束后直接关掉加热开关以达到淬火的目的。样品取出后用线锯纵向切开, 用环氧树脂镶嵌固定实验产物, 最后抛光用于后续岩相观察和分析测试。
1.3 分析测试方法
采用电子探针对实验产物进行化学组成分析, 分析测试分别在中国科学院广州地球化学研究所(仪器型号为JEOL JXA-8100)和德国拜罗伊特大学巴伐利亚地质研究所(仪器型号为JEOL JXA-8200)完成。分析测试加速电压为15 kV; 测试矿物或样品管时电流为20 nA, 电流束斑直径为1 µm; 测试淬火玻璃时电流为10~15 nA, 电流束斑为20 µm。Cu、Na和K采峰(peak)时间分别为40 s、10 s和10 s, 主要是为了尽可能提高Cu的检出限和降低Na、K易挥发元素在测试中的损失。每个产物相都进行了多次测量(>10)再计算平均值和标准偏差, 以反映样品真实成分。原始数据采用PAP法进行校正。分析过程中用到的元素标样为钙铁榴石(Si)、MnTiO3(Ti)、尖晶石(Al)、磁铁矿或石榴石(Fe)、MnTiO3(Mn)、镁橄榄石(Mg)、硅灰石(Ca)、钠长石(Na)、正长石(K)、磷化镓(P)、金属镍(Ni)、金属铬(Cr)和氧化铜(Cu)。由于电子探针测试中, 含水硅酸盐玻璃中Na含量容易丢失, 因此对实验产物淬火玻璃中Na含量进行了质量平衡校正。
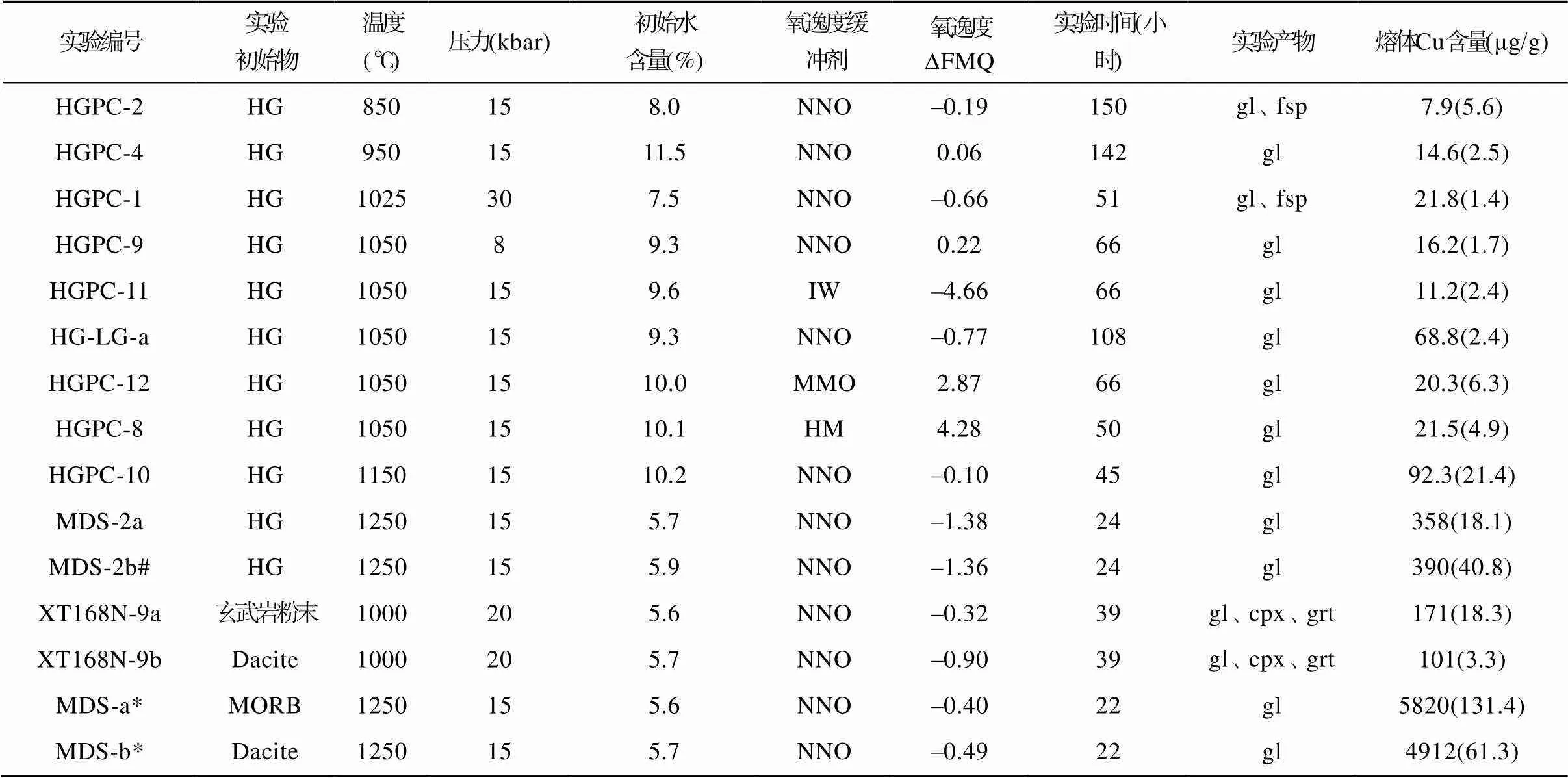
表2 实验条件和产物
注:#实验初始物加入了1% Fe3O4; *实验来自Liu et al. (2015); 实验氧逸度由熔体水活度计算得出; 熔体Cu含量由LA-ICP-MS测定。氧逸度缓冲剂缩写: IW. 铁‒方铁矿; NNO. 镍‒氧化镍; MMO. 氧化锰‒四氧化三锰; HM. 赤铁矿‒磁铁矿。实验产物缩写: gl. 淬火玻璃; fsp.长石; cpx. 单斜辉石; grt. 石榴石。
为了准确测定实验产物中的Cu含量, 采用激光剥蚀电感耦合等离子体质谱仪(LA-ICP-MS)进行了分析, 测试分析在中国科学院广州地球化学研究所和德国拜罗伊特大学巴伐利亚地质研究所完成。前者的分析仪器为Resonetic 193 nm ArF激光器与Agilent 7500a型质谱仪联机; 后者为Geolas M 193 nm ArF激光器与Elan DRC-e型质谱仪联机。剥蚀激光能量为80 mJ, 频率为5~10 Hz, 束斑直径为33~40 µm。载气为Ar气和He气, 中间以5 mL/min速率通入H2以提高Cu的分析测试精度。Cu测试选用的同位素为65Cu, 采峰时间为30 ms。分析时, 主要监控23Na、25Mg、28Si、27Al、39K、43Ca、49Ti、55Mn和57Fe。测试中用NIST SRM 610作为外标; 电子探针测试所得的Si(或Ca或Al)作为内标校正数据。大多数元素检出限<0.1 μg/g, 分析误差<10%。
1.4 实验产物组成与成分
本次研究成功开展了13个活塞圆筒实验, 实验产物主要为光滑的淬火硅酸盐玻璃(图1b), 少数实验中出现了矿物(表2)。淬火玻璃中未观察到流体包裹体, 表明实验中可能没有发生流体饱和。11个HG实验中(初始物为人造花岗岩), 除了HGPC-2和HGPC-1实验中结晶了长石, 导致熔体成分稍有变化外, 其他实验中淬火玻璃成分与初始物基本一致(表3)。需要注意的是, 由于电子探针分析含水淬火玻璃时, 分析过程中Na容易丢失, 导致分析结果低估熔体真实Na含量, 因此分析测试导致的这部分差值需要通过质量平衡计算获得: 实验产物中Na含量总和与实验初始物中Na含量需相等, 差值通过计算校正补齐。电子探针结果显示含水淬火玻璃SiO2变化范围为60.84%~69.41%, Al2O3为14.81%~16.26%, Na2O为5.47%~6.11%(质量平衡校正后), K2O为4.78%~5.6%。需要注意的是, 虽然在实验MDS-2b的初始物中加入了1% Fe3O4, 但是该实验的淬火玻璃仅测得FeO含量为0.04%±0.02%, 这可能是由于该实验氧逸度较低(NNO缓冲), 熔体中的Fe更易与Pt95Cu05合金样品管络合, 导致熔体Fe损失(Liu et al., 2014, 2015)。初始物为富钾玄武岩(XT168N-9a)和英安岩(XT168N-9b)的实验产物中, 除了淬火玻璃, 还有单斜辉石和石榴石(成分见表4)。XT168N-9a实验由于基性矿物结晶, 熔体成分由初始的玄武质变为了安山质(表3)。经过Na质量平衡校正后, XT168N-9a与XT168N-9b实验中淬火玻璃的NBO/T值分别为0.26和0.05。
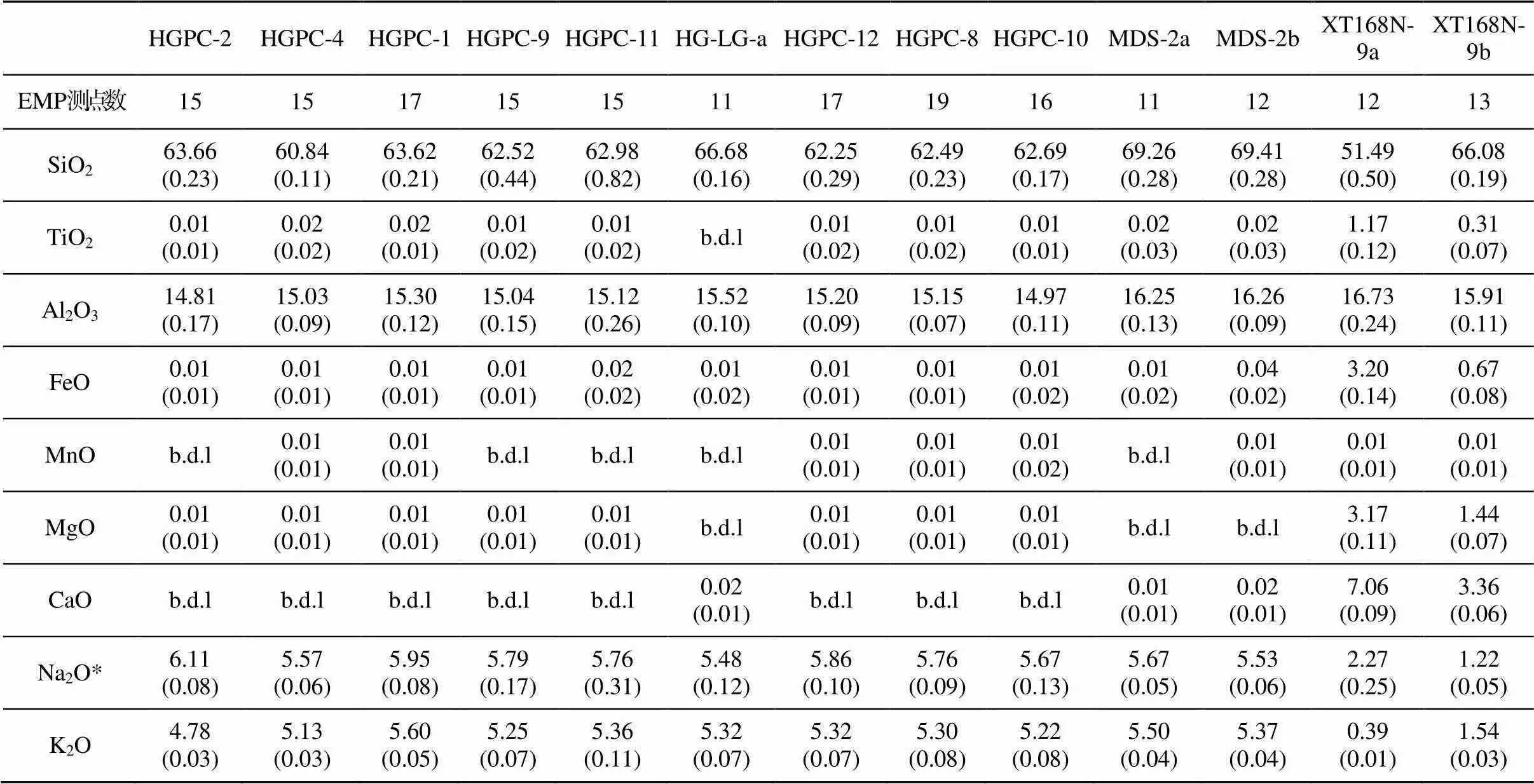
表3 实验淬火玻璃组成

续表3:
注:括号里为1σ标准偏差; b.d.l.为测试值低于检测限; n.a.为未进行分析测试; NBO/T为熔体聚合程度, 即每个四面体所含非桥氧离子数。*Na2O含量经过质量平衡校正。

表4 实验产物中矿物组成
注:括号里为1σ标准偏差。
通过电子探针所测总量与100%的差值, 可以估算硅酸盐熔体中水含量。在人造花岗岩实验中, 淬火玻璃水含量变化范围为3.21%~13.33%, 大部分为10%左右。其中, HGPC-2和HGPC-1实验由于矿物结晶导致熔体水含量略微上升; HG-LG-a实验水含量明显减少(可能由于H丢失导致), 其他实验中淬火玻璃含水量与初始值基本一致。在富钾玄武岩(XT168N-9a)和英安岩(XT168N-9b)的实验中, 由于不含水矿物结晶, 导致熔体中水含量也显著上升: 初始物中水含量为5.6%和5.7%, 实验后含水玻璃水含量为14.02%与9.37%。
1.5 硅酸盐熔体中Cu含量
如表2所示, 人造花岗岩实验(850~1250℃, 8~ 30 kbar)中Cu在淬火玻璃中含量为7.9±5.6 μg/g~ 389.8±40.8 μg/g; 富钾玄武岩实验(1000 ℃, 20 kbar)中淬火玻璃Cu含量为170.8±18.3 μg/g; 英安岩实验(1000 ℃, 20 kbar )中Cu含量为101.4±3.3 μg/g。
虽然本次实验中均采用Pt95Cu05合金管作为样品管, 这些合金管在实验中充当了Cu的来源, 但需要注意, 实验得到的是相似Cu活度下熔体中Cu的表观溶解度(apparent solubility), 为了表达方便, 下文均简称为溶解度。因为只有Cu活度为1才能直接得到Cu在熔体中的溶解度, 而实验中Pt95Cu05合金管提供的Cu活度远小于1(Zajacz et al., 2013; Liu et al., 2014, 2015)。如果实验中合金管成分没有发生明显变化, 那么可以认为实验中Cu活度不变, 由此得到的Cu在硅酸盐熔体中表观溶解度规律可以推导出Cu溶解度规律。但在高温高压实验中, 硅酸盐熔体和氧逸度缓冲剂与合金样品管直接接触, Fe、Ni等亲铁元素难免与合金管发生络合, 从而改变合金管的成分与Cu的活度。为了评估实验中Cu的活度, 我们使用电子探针测试了实验后合金管的成分(表5)。结果显示, 富钾玄武岩(XT168N-9a)和英安岩(XT168N-9b)实验中, 1000 ℃、2.0 GPa、NNO缓冲条件下, 接触到硅酸盐熔体的合金管内壁, 合金管Cu含量为3.7%±0.6%~4.5%±0.7%, Fe含量为3.9%±1.1%~ 4.6%±0.7%, Ni含量为0~0.1%; 而合金管壁中央Cu、Fe、Ni含量未发生明显变化。实验表明硅酸盐熔体中的Fe扩散进入了合金管(仅发生在合金管壁内侧有限区域, 平均小于50 μm), 而氧逸度缓冲剂中的Ni未扩散进入合金管中央。由于合金管中Fe的加入, 导致Cu含量与活度小幅下降。在Liu et al. (2015)开展的相似初始物、压力和氧逸度条件的实验中(表2中MDS-a与MDS-b实验), 其样品Fe损失比此次实验XT168N-9a和XT168N-9b要少, 合金管Cu、Fe含量未发生明显变化(表5), 表明合金管中的Cu含量与活度变化可能主要取决于实验中熔体的Fe损失。在人造花岗岩实验中, 除了MDS-2b实验中加入了1% Fe3O4, 其余实验均不含Fe, 因而这些不含Fe的人造花岗岩实验中, 样品管Cu的含量与活度在实验中发生的变化较小, 不会显著影响Cu溶解度研究。此外, 在MDS-2a与MDS-2b实验中, 除了后者初始物加入了1% Fe3O4, 其余实验条件如温度、压力、氧逸度均相同, 但两组实验最终获得了非常近似的熔体成分(MDS-2b淬火玻璃几乎不含Fe, 表明初始的Fe进入了合金管)与Cu含量(分别为357.5 μg/g和389.8 μg/g),表明合金管中少许Fe的加入不会显著影响Cu活度与熔体中的Cu溶解度。
2 讨 论
2.1 实验平衡与氧逸度探讨
Cu在含水硅酸盐熔体中扩散迅速(Liu et al., 2014, 2015; Ni et al., 2018), 本次实验时间为24~150小时,足以达到平衡或者接近平衡。理由如下: ①实验初始物至少含5%的水, 水的加入有利于促进Cu扩散平衡。根据Ni et al. (2018)实验结果, 850 ℃实验中Cu在含水硅酸盐熔体中的扩散速率估计高于7.6 μm/s,意味数小时就足够达到样品管中Cu扩散的平衡。②绝大部分实验中的矿物和淬火玻璃主量元素成分均一, 表明实验达到了主量元素的化学平衡(表3、4)。③实验使用了Pt95Cu05合金管, Cu元素来源于这些合金管。Cu从合金管向硅酸盐熔体扩散, 避免了前人实验中Cu源源不断地从硅酸盐熔体向不含Cu的贵金属管扩散丢失的问题。实验前后Cu的活度变化不大, 因此在一定温度、压力和氧逸度情况下, 实验中熔体的Cu含量能被缓冲到一个定值。所有熔体里的Cu含量都是均一的, 指示Cu的溶解达到了平衡。
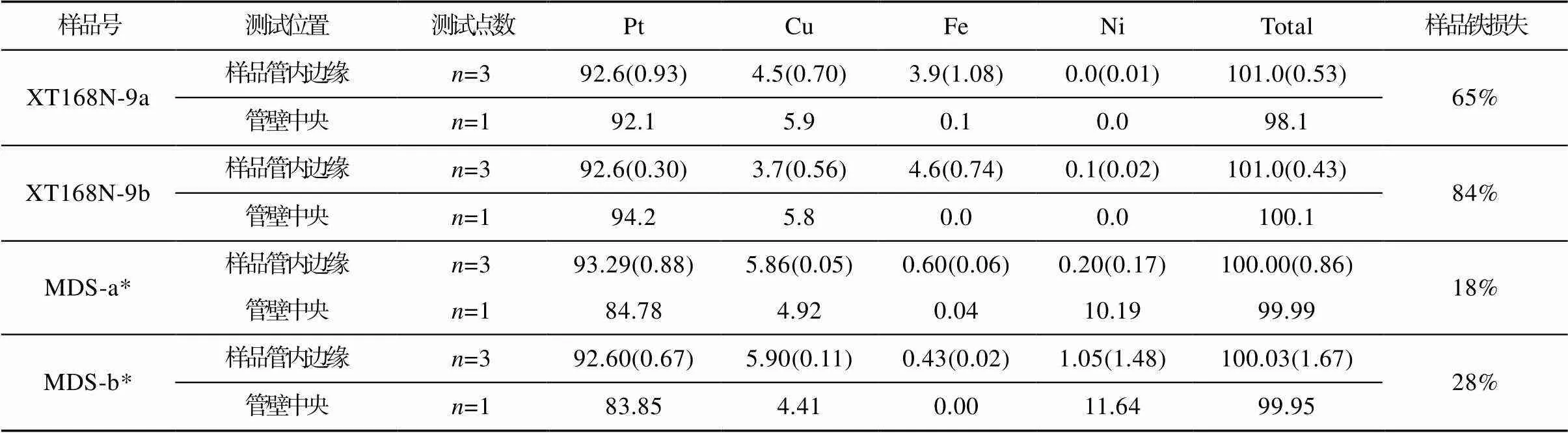
表5 Pt95Cu05样品管管壁电子探针成分分析(%)
注:样品铁损失为实验后相对于初始物的铁损失。*实验来自于Liu et al. (2015)。
高温高压实验, 特别是活塞圆筒实验, 精准控制氧逸度比较困难。本次实验使用了双管技术控制氧逸度, 理论上氧逸度范围应该是FMQ–5~FMQ+5, 但实验产物中未出现可以计算氧逸度的矿物对(如橄榄石‒斜方辉石‒尖晶石, 钛铁矿‒磁铁矿等), 因此只能通过固体缓冲剂实验后氧化剂和还原剂共存情况以及样品水含量推导实验实际氧逸度。双管技术控制氧逸度原理为: 在内外管与氧逸度缓冲剂中均加入水, 高温高压实验中可发生反应2H2O=2H2+O2(1), 而仅有H2这种小分子可以自由扩散穿透贵金属管, 促使内外管达到氢逸度平衡。不同固体氧逸度缓冲剂可以产生对应的氧逸度, 如HM缓冲剂, 4Fe3O4+O2=6Fe2O3(2)。由反应式(1)与(2)可知内管的氧逸度最终将由内管样品的水活度(H2O)和外管氧逸度控制。当H2O=1(如纯水达到饱和)且实验平衡时, 内管的氧逸度等于外管氧逸度; 但更多情况下, 内管H2O≠1, 此时, 可以通过公式∆logO2=2log(H2O)算出实际氧逸度(Matjuschkin et al., 2015)。通过镜下观察发现, 外管具有流体留下的孔洞, 表明外管实验过程中水是饱和的; 并且外管氧逸度缓冲剂中氧化剂和还原剂共存, 表明氧逸度缓冲成功, 因此通过实验产物淬火玻璃的探针数据以及Burnham and Davis (1974)和Burnham et al. (1969)提供的拟合公式估算了本次实验中样品的水活度和对应的氧逸度(表2、3)。
实验初始物采用了不含Fe的人造花岗岩和含Fe的玄武岩与英安岩。含Fe初始物在高温高压实验中, 低氧逸度或还原条件下(如NNO缓冲剂缓冲的实验), 硅酸盐熔体中的Fe会进入Pt95Cu05合金管, 造成熔体的Fe损失。富钾玄武岩(XT168N-9a)和英安岩(XT168N-9b)实验中, 通过质量平衡算出样品的Fe损失分别为65%与84%(表5), 与估算的较低的氧逸度值FMQ–0.32与FMQ–0.9(表2)吻合。
2.2 硅酸盐熔体中Cu溶解度的受控因素
2.2.1 硅酸盐熔体中Cu的种型以及氧逸度的影响
对于Cu在硅酸盐熔体中的种型和溶解度, 前人实验研究不多, 特别是高压实验很少, 大部分都是一个大气压下的溶解度实验(Ripley and Brophy, 1995; Holzheid and Lodders, 2001; Ripley et al., 2002; Zajacz et al., 2012, 2013)。Ripley and Brophy (1995)测定了Cu在不含硫的基性硅酸盐熔体中的溶解度(实验条件为=1245 ℃和1300 ℃;=1 bar;O2=FMQ–3.8~FMQ+5.6), 结果显示Cu的溶解度随氧逸度增加而增加, 表明Cu是通过Cu金属+0.5O2= CuO硅酸盐熔体这一形式溶解在硅酸盐熔体中。Cu溶解度和氧逸度线性拟合直线的斜率为0.31左右(如斜率为0.5时, 则=1, 即以Cu2+存在; 如斜率为0.25时,则=0.5, 即以Cu1+存在), 所以熔体里超过75%的Cu是以Cu1+存在的。Liu et al. (2014)发现基性熔体在1250~1300 ℃和10 kbar条件下, 当O2>FMQ+1.2时, 硅酸盐熔体中可能开始出现Cu2+。Holzheid and Lodders (2001)的实验考虑了S对Cu在玄武质熔体中溶解度的影响, 发现在温度不变时, Cu的价态近乎等于+1, 且溶解度随氧逸度升高而增加(无论是否含S)。当氧逸度为10–11.7bar时, 硫逸度(S2)变化为10–6.29~10–2.84bar时, Cu溶解度没有随硫逸度变化而发生明显变化。这表明Cu的溶解度只与氧逸度直接相关(主要以氧化物形式进入到硅酸盐熔体里), 与硫逸度无关。然而理论上Cu可以同时通过氧化物和硫化物的形式溶解在硅酸盐熔体中, 他们认为与硫逸度无关的原因可能是实验硫逸度太低, 不足以达到Cu以硫化物的形式进入到硅酸盐熔体中。Ripley et al. (2002)对S饱和玄武岩体系开展了 Cu溶解度实验(=1245 ℃;=1 bar;O2=FMQ–3.7~ FMQ–0.7(10–11~10–8bar);S2=10–3.05~10–1.07bar), 发现在硫化物饱和的玄武质熔体中, Cu溶解度主要与共存硫化物成分、氧逸度、硫逸度有关。在相同氧逸度下, 硫逸度越高, Cu溶解度越小; 随着硅酸盐熔体的S含量增加, Cu在硅酸盐熔体里的含量降低。而随着S在硅酸盐熔体里的减少, 当没有足够的S与Cu结合时, 将出现Cu-O-S的化合物。Zajacz et al. (2012, 2013)开展了高压下(2 kbar)Cu在含水硅酸盐熔体中的溶解度实验, 发现在1000 ℃和2 kbar的条件下, Cu在含水安山质熔体中的溶解度与熔体S、Cl含量只有弱正相关关系, 表明Cu在硅酸盐熔体中主要以CuO0.5形式存在。只有当熔体Cl含量特别高时(远超出天然样品范围), Cu与Cl的络合才变得重要。
前人实验研究表明, 在地壳与上地幔条件下, Cu主要为Cu1+, 并主要以CuO0.5形式存在。基性和中性熔体中Cu的溶解度随着氧逸度升高而增大(Ripley and Brophy 1995; Holzheid and Lodders, 2001; Zajacz et al. 2012; Liu et al. 2014, 2015; Ni et al., 2018)。但在本次研究的人造花岗岩实验的酸性熔体中, Cu溶解度并不随氧逸度增加发生明显变化。例如实验HGPC-11、HG-LG-a、HGPC-12与HGPC-8, 温度均为1050 ℃, 压力均为15 kbar, 初始物为含水人造花岗岩, 缓冲剂分别为IW、NNO、MMO与HM, 氧逸度变化范围为FMQ–4.66~FMQ+4.28, 而Cu溶解度变化范围为11.2±2.4 μg/g~68.8±2.4 μg/g (表2、图2a), 远小于前人实验中跨越2~3个数量级的变化(Ripley and Brophy, 1995; Liu et al., 2014, 2015)。在酸性熔体中, 氧逸度对Cu溶解度的影响较小可能是因为酸性熔体结构上非常聚合: 硅酸盐熔体里的氧多为桥氧(NBO/T值低), 没有多余非桥氧来结合Cu, 导致氧逸度变化并不明显引起Cu溶解度变化。这可能也解释了在所有的人造花岗岩实验中, 虽然温度与氧逸度变化较大, 但是Cu溶解度最高不超过400 μg/g, 明显低于其他熔体的Cu溶解度(表2)。这一结果与Zajacz et al. (2013)的实验结果一致, 他们发现当熔体成分为流纹质时, Cu溶解度相较其他熔体成分明显降低。
2.2.2 温度和压力的影响
本次研究实验温度范围设置为850~1250 ℃, 结果表明酸性硅酸盐熔体中Cu溶解度受温度的影响显著(图2b)。如表2所示, 15 kbar, NNO缓冲实验中(O2=FMQ–1.38~FMQ+0.06), 花岗质熔体中Cu溶解度从850 ℃的7.9±5.6 μg/g增加到1250 ℃的357.5±18.1 μg/g, 得到Cu溶解度与温度的拟合公式: lnCu=–4300/+5.88(=850~1250 ℃),2=0.95。前人实验中同样观察到了Cu溶解度与温度的正相关关系(Holzheid and Lodders, 2001; Zajacz et al., 2012, 2013)。但需要注意的是, 由于本次实验中与前人实验中Cu活度不同, 相同条件下Cu溶解度数值有所差异。另外, Ripley and Brophy (1995)发现Cu的溶解度随温度增加而减小, 解释为高温情况使金属氧化物分解所致, 但这与其他人实验结果不一致。
相比温度而言, 压力对酸性熔体中Cu溶解度影响有限。NNO条件下, 开展了三个压力不同但温度相似的实验, HGPC-1(1025 ℃, 30 kbar)、HGPC-9 (1050 ℃, 8 kbar)和HG-LG-a(1050 ℃, 15 kbar), 熔体Cu含量分别为21.8±1.4 μg/g、16.2±1.7 μg/g和68.8±2.4 μg/g。因此, 至少在上地幔条件下, 酸性熔体的Cu溶解度受压力影响较小。
2.2.3 熔体成分的影响
为了对比不同熔体成分对Cu溶解度的影响, 使用了三种不同成分的硅酸盐玻璃作为实验初始物(表1)。在XT168N-9a和XT168N-9b实验中, 将富钾玄武岩和英安岩初始物(加入近似含量的H2O)分别装入两个Pt95Cu05样品内管后, 再将这两个内管置于同一个外管中, 确保这两个实验的温度、压力和氧逸度一致, 便于对比熔体成分的影响。XT168N-9a和XT168N-9b实验分别产生了安山质和英安质含水淬火玻璃, Cu含量分别为170.8±18.3 μg/g和101.4±3.3 μg/g (表2、3)。但需要注意的是, 它们的样品管内壁在实验后Fe含量分别增加了3.9%±1.1%和4.6%±0.7% (与样品Fe损失程度一致, 相对比例分别为65%和84%), 而Cu含量分别为4.5%±0.7% 和 3.7%±0.6% (表5), 暗示实验中Cu的活度由于Fe的稀释作用而下降。因此Cu在安山质熔体中溶解度高于英安质熔体可能是Cu活度的差异造成的, 而非熔体成分的原因。在Liu et al. (2015)的高温实验中(MDS-a和MDS-b实验), 他们发现如果实验中Cu活度一致, 那么在相同的温度、压力和氧逸度下, 对于基性和中酸性熔体而言, 熔体成分对Cu溶解度几乎没有影响(表2)。因此Cu在基性到中酸性熔体中的溶解度主要受温度和氧逸度控制, 随温度和氧逸度增加而增大。
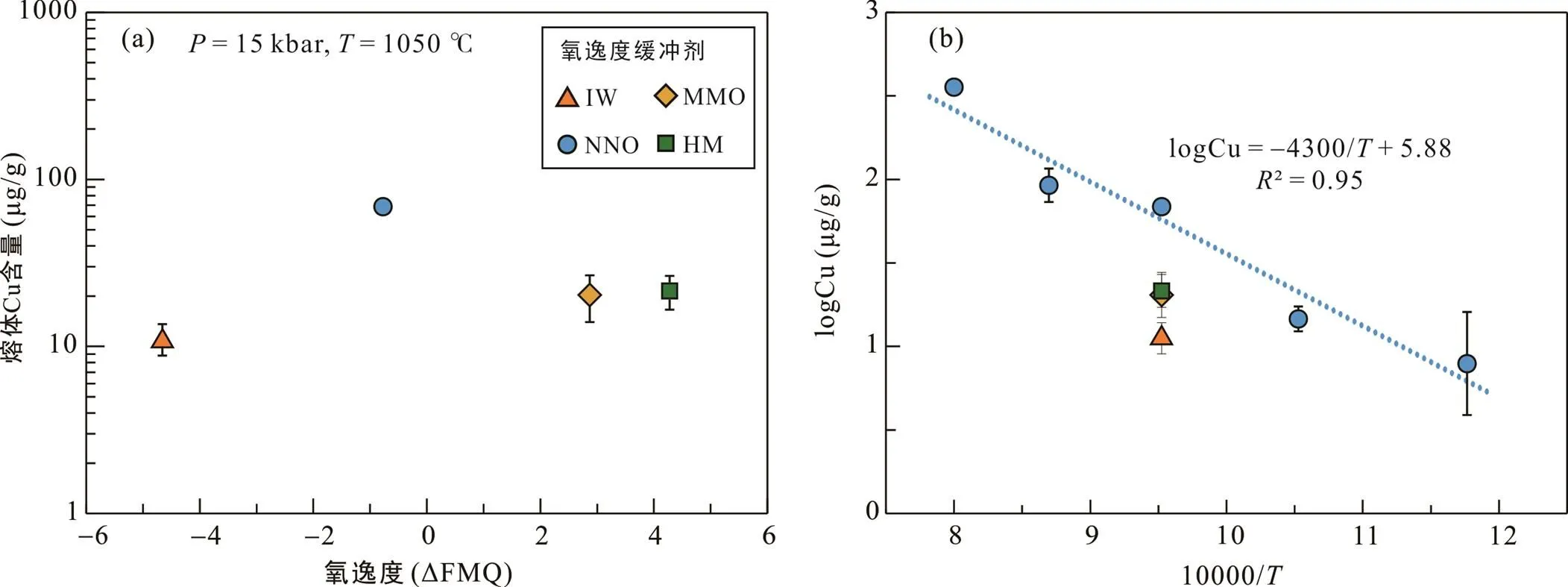
相同温度情况下, 氧逸度的变化对Cu溶解度影响不大。P=15 kbar, NNO氧逸度缓冲条件下, 随着温度升高, 花岗质熔体中Cu溶解度指数增加。
通过相似氧逸度的实验进行对比, 发现Cu溶解度除了受温度影响, 也受熔体聚合程度影响。如图3所示, 相似氧逸度条件下, 当熔体NBO/T>0.2时, Cu溶解度主要受控于温度, 而受成分影响较小; 当熔体NBO/T<0.2时, 除了温度的影响, 熔体成分影响变得显著: 相较于基性熔体, Cu在酸性熔体中溶解度骤减90%。这与前人实验结果一致, Zajacz et al. (2013)也发现温度、压力和氧逸度一定时(800~1030 ℃, 2 kbar,O2=NNO–0.8), 不含S的玄武质、安山质和英安质熔体对应的Cu溶解度差异小于50%, 硅酸盐熔体成分影响有限, 但流纹质熔体中Cu的溶解度下降了1.5~2.5倍。因此, 随着中酸性熔体的演化, 熔体结构进一步聚合(成分变得更酸性), 熔体成分开始成为影响Cu溶解度的重要因素。
2.3 硅酸盐熔体中Cu溶解度对Cu运移及成矿的启示
斑岩型Cu矿床矿化发育在2~5 km深的小型侵入体顶部, 富矿流体来自于5~15 km深的岩浆房, 而这些岩浆房的岩浆与成矿物质则来自20~50 km的深部岩浆房(Sillitoe, 2010; Audétat and Simon, 2012; Wilkinson, 2013)。形成斑岩型Cu矿床的岩浆一般为中酸性岩浆, 并往往具有高的Sr/Y值, 通常由富水玄武质弧岩浆分离结晶形成(Richards, 2013; Xiong et al., 2020), 也可以形成于俯冲板片中含水变质玄武岩(Sun et al., 2015), 或者加厚地壳基底的部分熔融(Hou et al., 2015)。Liu et al. (2014, 2015)研究表明在硅酸盐矿物中Cu属于中等到强不相容元素, 因此, 如果岩浆过程中不含硫化物或者只含有少量硫化物, Cu将会在结晶分异或者部分熔融过程中迅速富集, 形成富Cu母岩浆。然而, 随着成矿母岩浆上升演化, 总是伴随着降温过程和硅酸盐矿物结晶分异, 导致岩浆成分演化为酸性。本次实验结果显示酸性岩浆中Cu溶解度受温度和熔体成分影响最大, 随着温度的降低和熔体聚合程度增加而降低; 受氧逸度影响有限, 受压力影响不明显。这意味着当酸性岩浆演化到后期, 无论氧逸度高低, 运移Cu的能力将快速下降, 如果此刻流体才饱和出溶, 那么无法形成富Cu流体, 导致成矿潜力降低。另一方面, 随着温度的降低和熔体成分向流纹质演化时, 无论Cu在硅酸盐矿物/岩浆间还是硫化物/岩浆间的分配系数都将上升(Liu et al., 2015; Li and Audétat, 2015), 可能导致岩浆亏损Cu。因而流体在岩浆演化到中酸性时出溶, 才有利于形成富Cu流体, 增加成矿潜力。值得一提的是, 俯冲洋壳本身Cu含量较高且氧逸度较高(Sun et al., 2015), 但Cu在低温含水酸性岩浆中溶解度较低, 因此冷俯冲洋壳低程度熔融产生的酸性岩浆成矿潜力非常有限, 这可能解释了中安第斯地区巨型斑岩型矿床与热俯冲(如洋脊俯冲)的关系; 而对于西太平洋的冷俯冲而言, 俯冲洋壳产生的熔流体难以提供Cu, 与岛弧俯冲系统Cu同位素研究结果一致(Wang et al., 2021)。
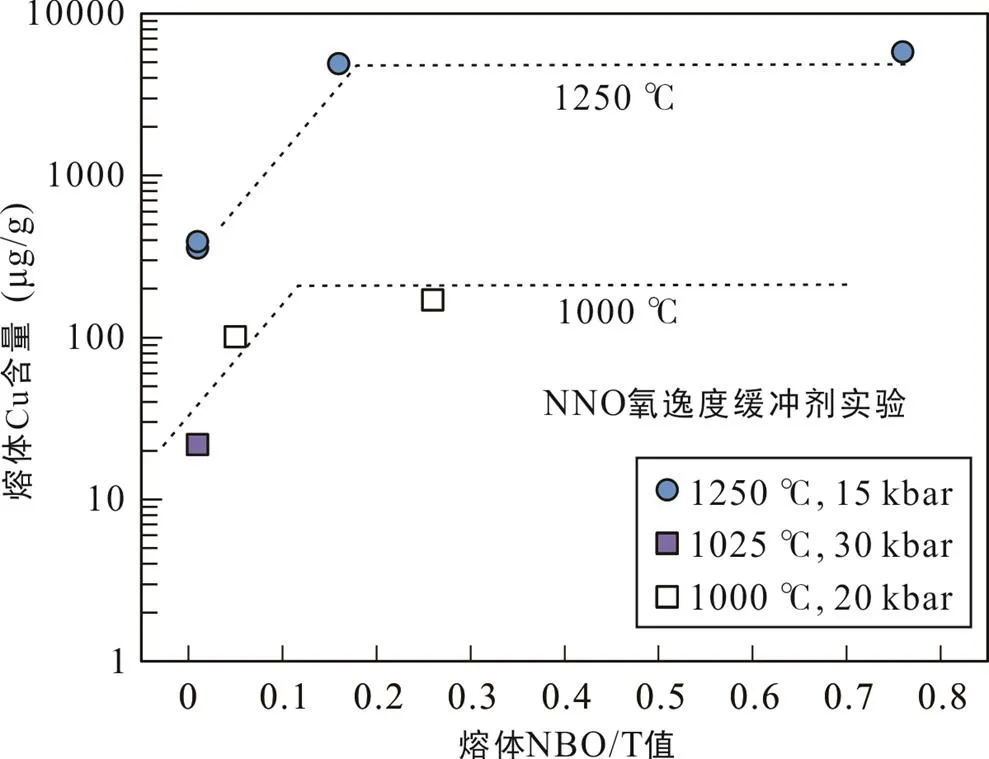
NBO/T反映熔体聚合程度, 其值越小代表熔体聚合程度越大; 酸性岩浆相较于基性岩浆熔体聚合程度更大。NNO氧逸度缓冲条件下, 熔体Cu含量除了受温度影响, 也受熔体聚合程度影响。当NBO/T < 0.2时, Cu溶解度急剧下降。
3 结 论
(1) 采用Pt95Cu05合金样品管, 系统研究了850~ 1250 ℃、8~30 kbar、FMQ–5~FMQ+5条件下, Cu在含水花岗质、英安质和玄武质熔体中的溶解度。
(2) 中酸‒酸性含水硅酸盐熔体中, Cu溶解度主要受温度和熔体成分控制, 压力没有明显影响, 随着温度降低和熔体聚合程度增加, Cu溶解度降低。当岩浆演化为流纹质或者花岗质时, 氧逸度对Cu的溶解度影响较小。
(3) 斑岩型Cu矿成矿过程中, 岩浆演化到后期, 运移Cu的能力迅速降低, 因此流体过晚出溶, 不利于形成富Cu流体, 也不利于形成大型矿床。而如果流体在岩浆演化到中酸性时出溶, 则有利于形成富Cu流体, 增加成矿潜力。
致谢:本研究工作LA-ICP-MS分析测试得到了德国拜罗伊特巴伐利亚地质研究所Andreas Audétat博士的帮助和支持; 中国科学院广州地球化学研究所陈华勇研究员、丁兴副研究员与另一位匿名审稿人提出了宝贵建议和意见, 在此表示衷心的感谢!谨以此文庆祝中国科学院青年创新促进会成立十周年!
阮梦飞, 王锦团, 李立, 熊小林. 2020. 榴辉岩部分熔融过程中钒分配系数的实验测定. 大地构造与成矿学, 44(3): 514–526.
Audétat A. 2019. The metal content of magmatic-hydrothermal fluids and its relationship to mineralization potential., 114: 1033–1056.
Audétat A, Simon A C. 2012. Magmatic controls on porphyry copper genesis.,, 16: 553–572.
Burnham C W, Davis N F. 1974. The role of H2O in silicate melts: Ⅱ. Thermodynamic and phase relations in the system NaAlSi3O8-H2O to 10 kilobars, 700 ℃ to 1100 ℃., 274: 902–940.
Burnham C W, Holloway J R, Davis N F. 1969. Thermodynamic properties of water to 1000 ℃ and 10000 bars., 132: 1–96.
Chen H Y, Wu C. 2020. Metallogenesis and major challenges of porphyry copper systems above subduction zones.:, 63: 899–918.
Chou I M. 1987. Oxygen buffer and hydrogen sensor techniques at elevated pressures and temperatures // Ulmer G C. Hydrothermal Experimental Techniques. Wiley: 61–99.
Frost B R. 1991. Introduction to oxygen fugacity and its petrologic importance // Lindsley D H. Oxide Minerals: Petrologic and Magnetic Significance., 25: 1–9.
Haas J L, Robie R A. 1973. Thermodynamic data for wustite, Fe0.947O, magnetite, Fe3O4and hematite, Fe2O3., 54: 483.
Holzheid A, Lodders K. 2001. Solubility of copper in silicate melts as function of oxygen and sulfur fugacities, temperature, and silicate composition., 65: 1933–1951.
Hou Z Q, Li Q Y, Gao Y F, Lu Y J, Yang Z M, Wang R, Shen Z C. 2015. Lower-crustal magmatic hornblendite in North China Craton: Insight into the genesis of porphyry Cu Deposits., 110: 1879–1904.
Li Y, Audétat A. 2015. Effects of temperature, silicate melt composition, and oxygen fugacity on the partitioning of V, Mn, Co, Ni, Cu, Zn, As, Mo, Ag, Sn, Sb, W, Au, Pb, and Bi between sulfide phases and silicate melt., 162: 25–45.
Liu X C, Xiong X L. 2018. Copper Encyclopedia of Geochemistry. Springer International Publishing: 303–305.
Liu X C, Xiong X L, Audétat A, Li Y. 2015. Partitioning of Cu between mafic minerals, Fe-Ti oxides and intermediate to felsic melts., 151: 86–102.
Liu X C, Xiong X L, Audétat A, Li Y, Song M S, Li L, Sun W D, Ding X. 2014. Partitioning of copper between olivine, orthopyroxene, clinopyroxene, spinel, garnet and silicate melts at upper mantle conditions., 125: 1–22.
Liu X C, Xu T, Xiong X L, Li L, Li J W. 2021. Gold solubility in silicate melts and fluids: Advances from high-pressure and high-temperature experiments., 64: 1481–1497.
Matjuschkin V, Brooker R A, Tattitch B, Blundy J D, Stamper C C. 2015. Control and monitoring of oxygen fugacity in piston cylinder experiments., 169: 1–16.
Ni H W, Shi H F, Zhang L, Li W C, Guo X, Liang T. 2018. Cu diffusivity in granitic melts with application to the formation of porphyry Cu deposits., 173: 1–10.
O’Neill H S C. 1987. Quartz-fayalite-iron and quartz-fayalite- magnetite equilibria and the free energy of formation of fayalite (Fe2SiO4) and magnetite (Fe3O4)., 72: 67–75.
O’Neill H S C, Pownceby M I. 1993a. Thermodynamic data from redox reactions at high temperatures.Ⅰ. An experimental and theoretical assessment of the electrochemicalmethod using stabilized zirconia electrolytes, with revisedvalues for the Fe-“FeO”, Co-CoO, Ni-NiO and Cu-Cu2O oxygen buffers, and new data for the W-WO2buffer., 114: 296– 314.
O’Neill H S C, Pownceby M I. 1993b. Thermodynamic data from redox reactions at high temperatures.Ⅱ. The MnO-Mn3O4oxygen buffer, and implications for the thermodynamic properties of MnO and Mn3O4., 114: 315–320.
Richards J P. 2013. Giant ore deposits formed by optimal alignments and combinations of geological processes., 6: 911–916.
Ripley E M, Brophy J G. 1995. Solubility of copper in a sulfur-free mafic melt., 59: 5027–5030.
Ripley E M, Brophy J G, Li C. 2002. Copper solubility in a basaltic melt and sulfide liquid/silicate melt partition coefficients of Cu and Fe., 66: 2791–2800.
Sillitoe R H. 2010. Porphyry copper systems., 105: 3–41.
Sun W D, Huang R F, Li H, Hu Y B, Zhang C C, Sun S J, Zhang L P, Ding X, Li C Y, Zartman R E, Ling M X. 2015. Porphyry deposits and oxidized magmas., 65: 97–131.
Wang Z C, Zhang P Y, Li Y B, Ishii T, Li W, Foley S, Wang X, Wang X, Li M. 2021. Copper recycling and redox evolution through progressive stages of oceanic subduction: Insights from the Izu-Bonin-Mariana forearc., 574, 117178.
Wilkinson J J. 2013. Triggers for the formation of porphyry ore deposits in magmatic arcs., 6: 917–925.
Xiong X L, Adam J, Green T H. 2005. Rutile stability and rutile/melt HFSE partitioning during partial melting of hydrous basalt: Implications for TTG genesis., 218: 339–359.
Xiong X L, Liu X C, Li L, Wang J T, Chen W, Ruan M F, Xu T, Sun Z X, Huang F F, Li J P, Zhang L. 2020. The partitioning behavior of trace elements in subduction zones: Advances and prospects.:, 12: 1938–1951.
Zajacz Z, Candela P A, Piccoli P M, Sanchez-Valle C, Wälle M. 2013. Solubility and partitioning behavior of Au, Cu, Ag and reduced S in magmas., 112: 288–304.
Zajacz Z, Candela P A, Piccoli P M, Wälle M, Sanchez-Valle C. 2012. Gold and copper in volatile saturated mafic to intermediate magmas: Solubilities, partitioning, and implications for ore deposit formation., 91: 140–159.
An Experimental Study of the Solubility of Copper in Hydrous Silicate Melts
LIU Xingcheng1, 2, 3, XU Ting1, 2, 3, XIONG Xiaolin1, 2, 3, LI Li1, 2, WANG Yu1, 2, XING Changming1, 2
(1. State Key Laboratory of Isotope Geochemistry, Guangzhou Institute of Geochemistry, Chinese Academy of Sciences, Guangzhou 510640, Guangdong, China; 2. CAS Center for Excellence in Deep Earth Science, Guangzhou 510640, Guangdong, China; 3. College of Earth and Planetary Sciences, University of Chinese Academy of Sciences, Beijing 100049, China)
Cu-rich magma favors the formation of large-giant porphyry Cu deposits. However, the favorable physicochemical conditions for Cu-rich magma generation are not well constrained. In order to investigate the effects of temperature, pressure, melt composition, and oxygen fugacity on Cu solubility in hydrous silicate melts, we employed Pt95Cu05alloy capsule with starting materials ranging from mafic to felsic glasses and performed experiments with piston-cylinder apparatus at 850 – 1250 ℃, 8 – 30 kbar, and oxygen fugacity (O2)in range of FMQ–5 – FMQ+5. The result shows that the effects of temperature and melt composition are significant on Cu solubility in felsic melts, whereas the influence of pressure is limited. The Cu solubility decreases by about two orders of magnitude as temperature drops from 1250 ℃ to 850 ℃ at similarO2conditions. There is no substantial variation of Cu solubility in basaltic, andesitic, and dacitic melts at the same temperature and comparableO2. Nevertheless, the Cu solubility in the more evolved magmas, such as granitic or rhyolitic melt, is lower by about one order of magnitude. Therefore, it can be inferred that the capacity of Cu transport of magma decreases rapidly in the late stage of magmatic processes. If the fluid saturation occurs too late, the generation of Cu-rich fluid will be largely hampered, which will low the potential for porphyry Cu mineralization.
copper solubility; silicate melt; high pressure and high temperature experiment; porphyry copper deposit
P589.1
A
1001-1552(2022)04-0803-011
10.16539/j.ddgzyckx.2022.02.014
2022-01-18;
2022-03-10;
2022-04-02
国家自然科学基金项目(42073057、41573053)和中国科学院青年创新促进会项目(2019344)联合资助。
刘星成(1987–), 男, 研究员, 主要从事实验地球化学研究。E-mail: liuxingcheng@gig.ac.cn
