伪狂犬病毒感染对BHK-21悬浮细胞内质网应激和未折叠蛋白反应的影响
2022-08-23倪敏舒庄腾寒郭美锦
陈 丽,倪敏舒,徐 悦,鲍 熹,庄腾寒,冯 磊,3,4,5,郭美锦
(1.华东理工大学生物反应器工程国家重点实验室,上海 200237;2.江苏省农业科学院动物免疫工程研究所,南京 210014;3.江苏省动物重要疫病与人兽共患病防控协同创新中心,扬州 225009;4.江苏大学药学院,镇江 212013;5.江苏省食品质量安全重点实验室——省部共建国家重点实验室培育基地,南京 210014)
病毒在感染过程中会把内质网(ER)作为复制场所,并利用宿主细胞内质网的膜和蛋白系统合成自身的病毒蛋白。内质网是真核细胞器的重要组成部分,由脂类和蛋白质构成,是蛋白质合成、翻译后修饰、加工和折叠的重要场所,同时还参与Ca2+储存和脂类物质的合成[1]。在缺氧、氧化应激、毒性物质刺激等情况下[2],内质网的微环境发生改变,大量未折叠或者错误折叠蛋白在内质网中聚集,使内质网处于生理功能紊乱,进而诱发内质网应激。为缓解应激压力,细胞会启动未折叠蛋白反应(UPR)以维持细胞稳态[3]。为了能够达到在宿主体内增殖,病毒需通过调控UPR以减少对其增殖的不利因素,创造出有利条件。同时,病毒还可以通过调控UPR与细胞凋亡、细胞自噬和病毒先天免疫之间的关系,以应对病毒感染引起的内质网应激,最终达到致病的目的[4-5]。UPR活化由3个不同的内质网跨膜蛋白介导,分别是蛋白激酶样内质网激酶(PERK)、ER跨膜蛋白激酶1(IRE1)和活化转录因子6(ATF6)[6-7]。跨膜蛋白具有抑制病毒蛋白的合成、降解驻留在内质网的病毒蛋白量或诱导促折叠伴侣分子表达等功能[8-9]。活化的PERK催化真核转录起始因子2(eIF2α)磷酸化,磷酸化eIF2α(P-eIF2α)上调活化转录因子4(ATF4)基因的表达,ATF4激活生长停滞和DNA损伤诱导蛋白(GADD34)、C/EBPα-同源蛋白(CHOP)等相关蛋白的表达[10]。活化的IREl能够去除X盒结合蛋白1(XBP1)mRNA的26 bp内含子,形成翻译框移码,编码新蛋白sXBP1[11-12]。XBP1被IRE1切除的26 bp核苷酸序列中含有1个PstⅠ酶切位点[13]。剪切形式的sXBP1诱导内质网相关降解途径(ERAD)中伴侣分子和内质网相关降解蛋白(EDEM)的表达。活化的ATF6(90 ku)转运至高尔基体后降解为有转录活性的ATF6蛋白(50 ku),进入细胞核调节内质网应激响应元件(ERSE)的表达,如葡萄糖调节蛋白78(GRP78)、葡萄糖调节蛋白94(GRP94)、钙连蛋白(Calnexin)和钙网蛋白(Calreticulin)等[14]。多种疱疹病毒可以引起内质网应激,如单纯疱疹病毒1型(Herpes simplex virus 1,HSV-1)通过PERK通路应对内质网应激[15-16];鸭瘟病毒(Duck enteritis virus,DEV)感染可以激活PERK和IRE1通路,并通过小干扰RNA(siRNA)检测发现这2个通路有助于诱导细胞自噬[17]。
伪狂犬病(pseudorabies,PR)是一种由伪狂犬病毒(Pseudorabies virus,PRV)引起的急性传染病[18-19]。PRV属于α疱疹病毒亚科,具有传播速度快、死亡率高、病原体顽固等特点[20-21],能够引起多种家畜和野生动物感染发病,主要的宿主是猪[22-23]。该病广泛分布于世界各地多个国家和地区,给全球养猪业带来了巨大的经济损失。疫苗的免疫接种是防治和消灭伪狂犬病的主要手段[24]。PRV致病机制目前还不明确,内质网应激研究对PRV与宿主细胞的相互作用机制的研究具有重要意义,可为阐明PRV的致病机制奠定基础。目前有关PRV感染诱导内质网应激的研究较少,Yang等[25]的研究表明,PRV感染PK-15细胞在感染早期可激活IRE1-XBP1通路,但是该通路没有对病毒复制造成影响,并通过CHOP-Bcl2通路诱导细胞凋亡。作者前期对PRV感染BHK-21悬浮细胞的接毒剂量进行了摸索,考察了MOI为0.1,0.01,0.001,0.0001对病毒滴度影响,最终得到在生物反应器中生产PRV的最佳MOI为0.01(未发表)。本研究以PRV灭活疫苗生产中的工程细胞BHK-21悬浮细胞为宿主细胞,以MOI 0.01接毒,考察PRV感染对BHK-21悬浮细胞的内质网应激及UPR信号通路的影响。
1 材料与方法
1.1 材料
1.1.1 细胞和毒株 BHK-21贴壁细胞、BHK-21悬浮细胞和PRV毒株均由江苏省农业科学院动物免疫工程研究所细胞工程创新团队保存。
1.1.2 主要试剂 DMEM培养基、新生牛血清(NBS)均购自Gibco公司;悬浮培养基MD910购自北京清大天一科技有限公司;eIF2α(9722S)、P-eIF2α(3597S)和α-tubulin(2144S)抗体均购自Cell Signaling Technology公司;HRP标记羊抗兔二抗购自Invitrogen公司;内质网应激诱导剂毒胡萝卜素(Tg)和内质网应激抑制剂牛磺熊去氧胆酸(TUDCA)均购自Sigma公司;PstⅠ内切酶购自TaKaRa公司;RNA提取、逆转录、QuantiFast SYBR Green PCR试剂盒和DNA回收试剂盒均购自Qiagen公司;CCK-8试剂盒购自上海碧云天生物技术有限公司。
1.2 PRV在BHK-21悬浮细胞中的增殖
在高压灭菌后的1 L生物反应器中加入500 mL细胞培养液(含1% NBS的MD910悬浮培养基),将BHK-21悬浮细胞以5×105/mL接种,培养温度为37 ℃,搅拌转速为160 r/min,溶解氧(DO)为50%,pH为7.2。当细胞密度达到4×106/mL后再加入500 mL细胞培养液,以MOI为0.01接种PRV,以不接毒细胞作为对照组,分别在12、24、36、48和56 h收集对照组和感染组细胞,用CCK-8法检测细胞存活率,按Reed-Muench法[26]测定病毒滴度,筛选病毒接种处理的合适时间。
1.3 PRV感染对内质网应激及UPR通路相关基因及蛋白表达的影响
1.3.1 样品收集 按1.2方法接种病毒,分别在在12、24、36和48 h收集对照组和感染组细胞,用于检测内质网应激标志分子GRP78及UPR的3种感受蛋白(PERK、IRE1、ATF6)相关通路中基因和蛋白的表达变化。
1.3.2 实时荧光定量PCR检测相关基因mRNA的表达水平 使用RNA提取试剂盒提取1.3.1收集细胞的RNA,并反转录合成cDNA。参照GenBank中叙利亚仓鼠GRP78、ATF4、GADD34、p58IPK、EDEM、ERp57、PDI、Calnexin和Calreticulin基因序列,用Primer Premier 5.0软件设计引物,引物信息见表1,引物均由南京擎科生物科技有限公司合成。以β-actin为内参基因,进行实时荧光定量PCR。PCR反应体系20 μL:SYBR Premix ExTaqⅡ 10 μL,上、下游引物(20 μmol/L)各1 μL,cDNA 1 μL,ddH2O 7 μL。PCR反应条件:95 ℃预变性5 min;95 ℃变性30 s,60 ℃退火45 s,72 ℃延伸45 s,共40个循环。采用2-ΔΔCt法计算各基因的相对表达量。
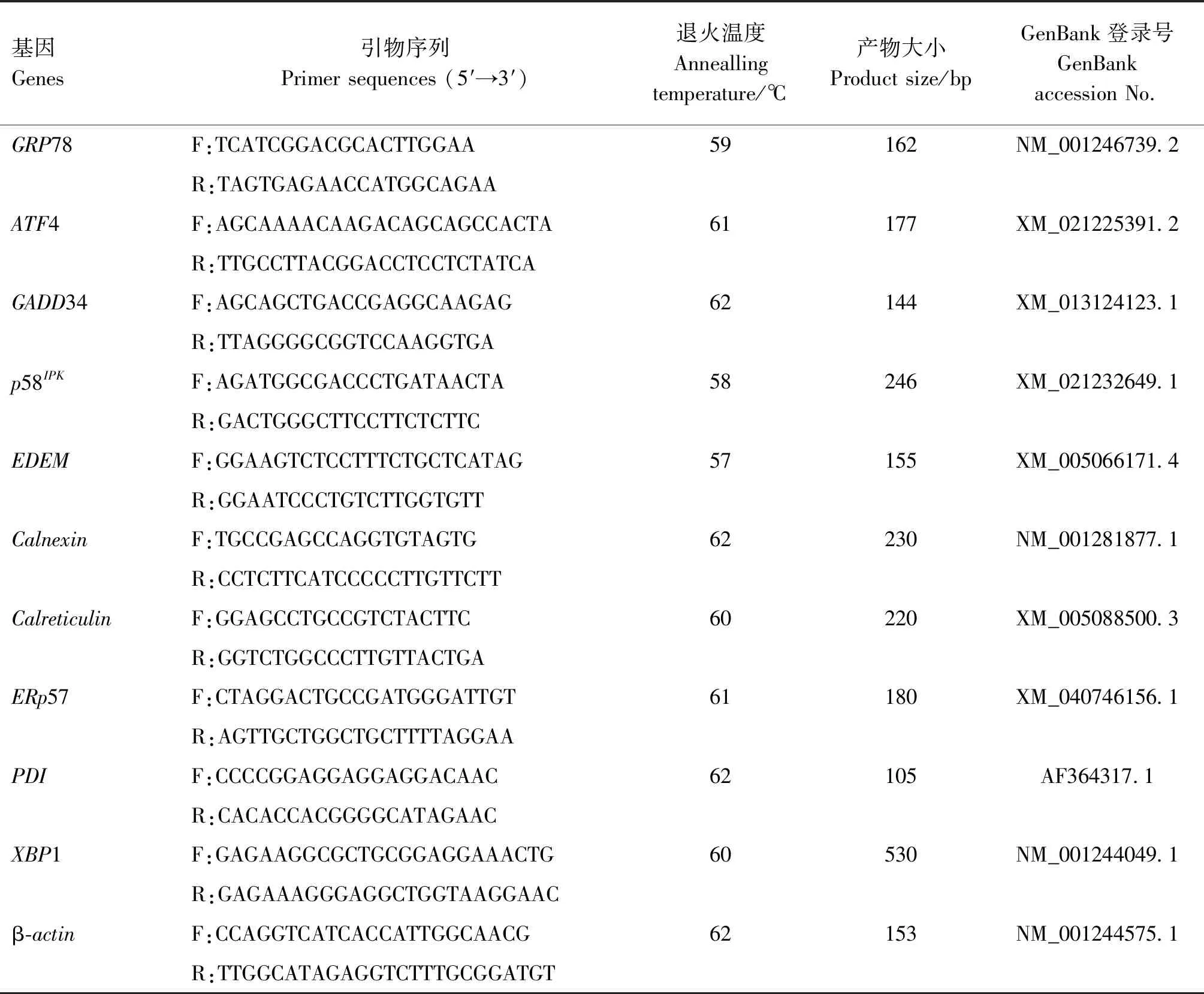
表1 引物序列
1.3.3 Western blotting检测相关蛋白的表达 用RIPA裂解1.3.1收集的细胞提取总蛋白,12% SDS-PAGE分离蛋白,使用湿转法将蛋白转至PVDF膜上。5%脱脂牛奶在37 ℃封闭2 h,4 ℃一抗P-eIF2α(1∶1 000)、eIF2α(1∶1 000)和Tublin(1∶1 000)孵育过夜。然后用TBST洗涤3次,加入HRP标记羊抗兔二抗(1∶5 000)37 ℃孵育1 h,最后用ECL法显示,并使用Tanon 5200系统成像拍照,ImageJ 2.0软件统计蛋白条带灰度值。
1.4 IRE1通路中XBP1剪切分析
用1.3.2中合成的各组细胞的cDNA,进行RT-PCR分析IRE1通路中XBP1剪切情况。根据叙利亚仓鼠XBP1基因序列(登录号:NM_001244049.1),用Primer Premier 5.0软件设计引物,引物信息见表1,引物由南京擎科生物科技有限公司合成。PCR反应体系20 μL:PremixTaq10 μL,上、下游引物(20 μmol/L)各1 μL,cDNA 1 μL,ddH2O 7 μL。PCR反应条件:95 ℃预变性5 min;95 ℃变性15 s,60 ℃退火30 s,72 ℃延伸30 s,共40个循环;72 ℃延伸300 s。PCR产物用2.0%琼脂糖凝胶电泳后进行回收,回收产物用PstⅠ酶消化。sXBPl不含有PstⅠ酶切位点而不能被切开,电泳产物为504 bp,而非剪接形式的uXBPl则被PstⅠ酶切形成大小分别为317和213 bp的片段。
1.5 内质网应激相关化学药物对PRV复制的影响
在BHK-21悬浮细胞上以MOI为0.01接种PRV,同时分别加入0(对照组)、0.001、0.005、0.01和0.02 μmol/L Tg和0(对照组)、20、40、80和160 μmol/L TUDCA,48 h收集细胞,按照1.2中的方法测定细胞存活率和病毒滴度。
1.6 数据统计与分析
用GraphPad Prism 5.0软件进行单因素方差分析,样本间差异采用t检验。结果以平均值±标准差表示。P<0.05表示差异显著,P<0.01表示差异极显著。
2 结 果
2.1 PRV在BHK-21悬浮细胞中的增殖
由图1可知,PRV在BHK-21悬浮细胞中增殖速度较快,12 h病毒滴度达5.0 lg TCID50/mL,48 h病毒滴度最高,达到8.1 lg TCID50/mL,56 h细胞存活率低于70%,病毒滴度和细胞存活率均出现下降。因此后续试验对PRV感染48 h内进行研究,分别在接毒后12、24、36和48 h收集细胞。

图1 PRV感染BHK-21悬浮细胞后病毒滴度和细胞存活率变化Fig.1 Changes of viral titer and relative cell viability of BHK-21 suspension cells infected by PRV
2.2 PRV感染对GRP78表达的影响
由图2可知,与对照组相比,PRV感染组GRP78 mRNA转录水平在36和48 h均极显著上调(P<0.01)。
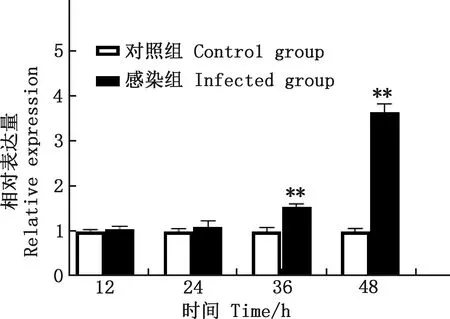
与对照组相比,*,差异显著(P<0.05);**,差异极显著(P<0.01);无*,差异不显著(P >0.05)。下同Compared with control group,*,Significant difference(P<0.05);**,Extremely significant difference(P<0.01);No *,No significant difference(P>0.05).The same as below图2 各组细胞不同时间GRP78的相对表达量Fig.2 The relative expression of GRP78 in each group at different time
2.3 PRV感染对PERK通路相关基因及蛋白表达的影响
由图3可知,与对照组相比,ATF4在PRV感染36、48 h均极显著升高(P<0.01),GADD34在PRV感染36 h显著升高(P<0.05)、48 h极显著升高(P<0.01);PRV感染36、48 h PERK通路中宿主细胞的P-eIF2α蛋白表达水平均极显著增加(P<0.01)。
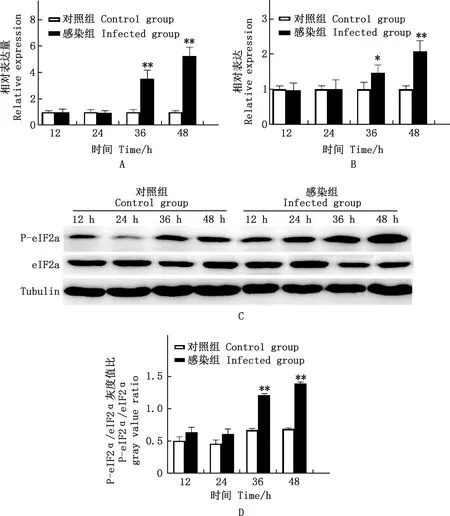
A、B,实时荧光定量PCR分析ATF4、GADD34相对表达量;C,Western blotting分析PERK通路P-eIF2α和eIF2α蛋白表达;D,P-eIF2α/eIF2α灰度值比A and B,The relative expression of ATF4 and GADD34 by Real-time quantitative PCR;C,The expression of P-eIF2α and eIF2α proteins in the PERK pathway by Western blotting;D,The ratio of P-eIF2α/eIF2α gray value图3 各组细胞不同时间PERK通路相关基因及蛋白表达Fig.3 The related gene and protein expression of the PERK pathway in each group at different time
2.4 PRV感染对IRE1通路相关基因表达的影响
由图4可知,与对照组相比,PRV感染组细胞36 h后多以剪切形式sXBP1存在,同时下游p58IPKmRNA水平在36和48 h显著或极显著增加(P<0.05;P<0.01),EDEM mRNA水平在48 h极显著增加(P<0.01)。

A,RT-PCR分析XBP1剪切水平;B、C,实时荧光定量PCR分析p58IPK和EDEM相对表达量A,The level of XBP1 splicing by RT-PCR;B and C,The relative expression of p58IPK and EDEM by Real-time quantitative PCR图4 各组细胞不同时间IRE1通路XBP1剪切水平及相关基因的相对表达量Fig.4 The relative expression of XBP1 splicing and the related gene of the IRE1 pathway in each group at different time
2.5 PRV感染对ATF6通路相关基因表达的影响
由图5可知,与对照组相比,PRV感染组12、24、36、48 h ATF6下游相关效应分子ERp57、PDI、Calnexin和Calreticulin的表达均无显著变化(P>0.05)。

A~D,分别为ERp57、PDI、Calnexin和Calreticulin基因A-D,ERp57,PDI,Calnexin,Calreticulin genes,respectively图5 各组细胞不同时间ATF6通路相关基因的表达Fig.5 The related gene expression of the ATF6 pathway in each group at different time
2.6 内质网应激相关化学药物对PRV复制的影响
由图6可知,BHK-21悬浮细胞药物处理48 h后,与对照组相比,0.01和0.02 μmol/L Tg极显著降低细胞存活率(P<0.01),0.001和0.005 μmol/L Tg及所有试验浓度的TUDCA组细胞存活率均无显著差异(P>0.05);与对照组相比,0.005和0.01 μmol/L Tg均极显著增加了PRV病毒滴度(P<0.01),20、40、80、160 μmol/L TUDCA均极显著降低病毒滴度(P<0.01),且呈剂量依赖性降低。
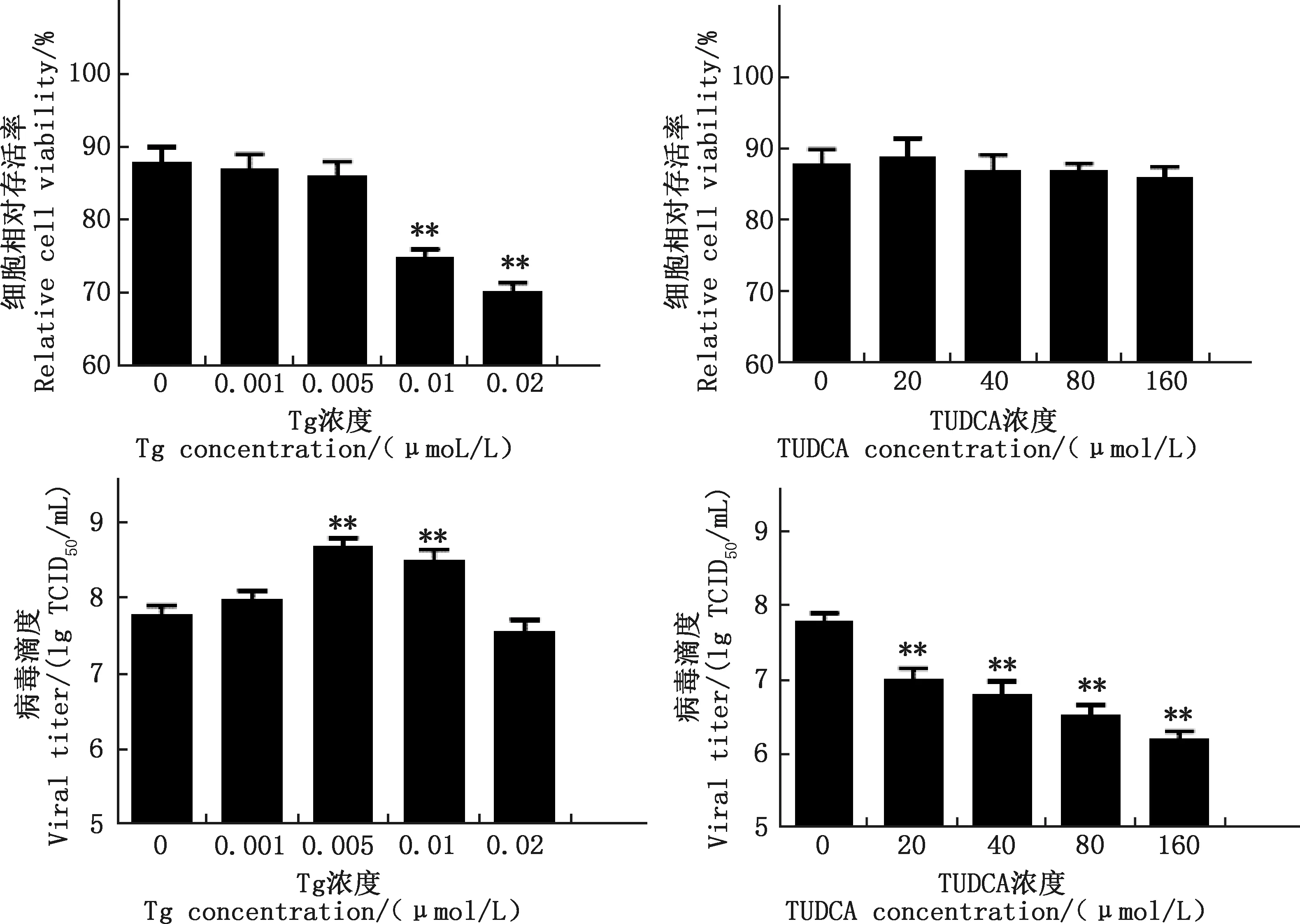
图6 不同浓度Tg和TUDCA组细胞相对存活率及病毒滴度Fig.6 The relative cell viability and viral titers in different concentration groups of Tg and TUDCA
3 讨 论
内质网是宿主蛋白合成的重要场所,病毒感染会引起宿主细胞内质网应激,为缓解内质网应激,宿主细胞会启动UPR[27]。乙型肝炎病毒、流感病毒、猪圆环病毒、疱疹病毒等均可诱导内质网应激[28]。PRV在宿主细胞内可以快速地增殖。本研究发现,BHK-21悬浮细胞以MOI 0.01接种PRV,在48 h可达到最高效价,随后细胞死亡率不断增加,病毒滴度也随之下降。内质网应激时通过UPR可使GRP78大量表达,GRP78可作为内质网应激的标志性分子。本研究中,在PRV感染BHK-21悬浮细胞36 h后,内质网应激标志分子GRP78表达量极显著升高,说明出现内质网应激,UPR被激活。与其他报道相比,本研究中PRV感染BHK-21悬浮细胞后GRP78上调时间延迟,这可能与较低的MOI有关。本研究模拟使用规模化培养的生物反应器为容器,BHK-21悬浮细胞为宿主细胞,生产增殖PRV的MOI为0.01,而其他研究者大部分使用方瓶培养贴壁细胞,接毒的MOI为1.0[29-30]。
活化的PERK主要通过降低蛋白合成速率来缓解内质网应激。本研究检测了PERK通路中eIF2a蛋白的磷酸化水平以及下游分子ATF4、GADD34转录表达水平,结果发现上述分子在PRV感染BHK-21悬浮细胞36 h后均出现表达量上升的现象。活化的IRE1主要通过核酸内切酶对XBP1进行剪切,降解内质网错误折叠蛋白以维持内质网稳态。在PRV感染宿主细胞36 h后,多以sXBPl剪切形式存在,同时下游调节分子p58IPK和EDEM转录水平均有所提高,但是ATF6通路中相关效应分子ERp57、PDI、Calnexin和Calreticulin的表达量并没有明显变化。这些结果说明PRV感染能够激活BHK-21悬浮细胞的PERK和IRE1通路,对ATF6通路没有影响。Yang等[25]报道PRV感染PK15细胞后可激活IRE1通路,但是并没有明确激活PERK通路,造成这种现象的原因可能是不同的宿主细胞对内质网应激产生的反应不同。
病毒感染会产生内质网应激,并通过调节UPR创造对增殖有利的条件,以达到增强自身有效复制的目的。传染性胃肠炎病毒(TGEV)感染可激活ST细胞和IPEC-J2细胞的UPR 3条信号通路,并通过PERK通路抑制TGEV复制[31]。Xu等[32]报道PRV体外感染小鼠神经细胞N2a可以诱导自噬来增强其自身复制。Catanzaro等[33]报道蓝耳病(PRRSV)感染激活UPR的3条通路,但内质网应激抑制PRRSV的复制。经典猪瘟病毒(CSFV)利用内质网应激促进病毒增殖,其中IRE1通路起到了关键作用[34],并且CSFV非结构蛋白p7可以与宿主蛋白相互作用,调节内质网钙离子的通透性[35]。这些研究表明,内质网应激在病毒增殖中具有重要作用。本研究在PRV感染过程中,添加内质网应激诱导剂Tg可明显提高病毒滴度,而添加内质网应激抑制剂TUDCA则抑制病毒增殖,说明PRV可利用内质网应激促进病毒增殖。
4 结 论
PRV感染可以诱导BHK-21悬浮细胞内质网应激和UPR,激活PERK和IRE1信号通路,说明PRV感染可通过调节UPR以利于其在宿主细胞体内增殖。
