双功能金属锌催化剂催化氮杂环丙烷与CO2环加成反应的研究
2022-07-16杨海健胡军成
杨海健,聂 亨,文 勤,余 鹏,彭 静,胡军成
(中南民族大学 化学与材料科学学院,湖北 武汉 430074)
在有机合成当中,杂环化合物由于其独特的结构,具有极为广泛的应用,尤其是在环境化学、药学以及生命科学当中具有重要的作用[1].而氮杂环丙烷由于其独特的结构性质,即有一个含氮的三元环,环张力比较大,具有很高的活性[2],可以应用于有机合成中,做中间体,利用氮杂环丙烷以及其衍生物,可以合成一系列邻氨基化合物和具有生物活性的含氮杂环化合物[3],这些都是具有很高应用价值的产品.例如二氧化碳与氮杂环丙烷发生环加成反应,生成恶唑烷酮类的化合物[4],而恶唑烷酮类的化合物可以作为抗生素类药物,通过抑制细菌蛋白质的合成,从而具备抗菌活性,在医学上具有很高的应用价值[5].正因为氮杂环丙烷具有很高的利用价值,已成为当前研究的热点,而其中研究的重点在于它的环加成反应[6].
因为氮杂环具有以上性质,可以将其与CO2反应,生产出具有工业价值的产品[7].CO2是取之不尽用之不竭的C1资源,然而CO2的过度排放产生了温室效应[8],为了解决这一问题,可以将其转化为尿素、甲醇等具有高附加值的产品[9].由于CO2化学性质不活泼,故需要在转化过程中加入催化剂,以实现CO2的催化转化[10].目前已经开发出了一系列催化剂,例如金属Salen配合物[11]、离子液体[12]、MOFs材料[13]、光催化[14]等一系列催化剂或者催化手段,均取得了不错的效果.
基于氮杂环丙烷和CO2的性质,本文开发了一种双功能金属催化剂,其优点是在无溶剂、无助催化剂的情况下,催化效果很好,原因在于其分子上同时存在Lewis酸中心和Lewis碱中心[15].通过合成一系列的氮杂环丙烷底物,来研究该催化剂的催化活性和底物适用性.
1 实验部分
1.1 实验药品、试剂及仪器
水杨醛、氘代氯仿(百灵威科技有限公司),多聚甲醛、碳酸氢钠、二水醋酸锌、盐酸、甲苯、醋酸、醋酸铵、正戊烷、溴素、苯乙烯、乙腈、乙醚、无水硫酸镁、氯化钠、正丙胺、甲胺(国药集团化学试剂有限公司),三苯基膦、苯偶酰、甲硫醚、乙醇胺、N,N-二甲基乙二胺、异戊胺、4-氯苯乙烯、4-甲基苯乙烯、正丁胺、叔丁胺、苄胺(阿拉丁试剂(上海)有限公司),石油醚、二氯甲烷(上海泰坦化学有限公司),所有试剂均为分析纯.DF-101B 集热恒温加热磁力搅拌器(巩义市英峪华仪器厂),DHG-905311型电热恒温鼓风干燥箱(上海精宏设备有限公司),NEXUS 470型傅立叶红外光谱仪(美国Nicolet公司),PE Lambda 35 紫外可见分光光度计(美国Nicolet公司),PE 2400 II型CHNS/O元素分析仪(Perkin Elmer),核磁共振仪(Bruker A1-400MHz,瑞士布鲁克),DZF-0B型真空干燥箱(上海跃进医疗器械厂),旋转蒸发仪(上海亚荣生化仪器厂).
1.2 氮杂环丙烷合成与表征
参考文献[16],开发出一种合成氮杂环丙烷的方法,如图1所示.

图1 氮杂环丙烷底物的合成
1.2.1 MS1的合成
向单口圆底烧瓶中加入80 mL二氯甲烷,向其中加入0.4 mol甲硫醚,让其处于冰水浴的环境中,同时将0.4 mol溴素和80 mL二氯甲烷的混合溶液缓慢滴入单口圆底烧瓶中,控制好反应速率,则立即产生许多橘黄色沉淀.待全部滴加完毕,进行过滤并用大量的乙醚洗涤,常温干燥,得到MS1固体.
1.2.2 MS2的合成
向单口圆底烧瓶中加入100 mL的乙腈,将已经干燥好的0.3 mol MS1固体加入其中,充分搅拌,使MS1溶解完全,置于冰水浴环境中.将0.3 mol苯乙烯慢慢滴入,对于制备苯环上有取代基的氮杂环丙烷,滴加带有相应取代基的苯乙烯.当滴入完全之后,搅拌20 min,将会产生许多白色沉淀,过滤并用大量的乙醚洗涤,之后对白色固体进行真空干燥,得到MS2固体.
1.2.3 氮杂环丙烷底物的合成
在圆底烧瓶中,将所得的20 mmol MS2完全溶解在80 mL超纯水中,在室温条件下,滴入80 mmol相对应的胺的溶液,搅拌使其反应12 h,待反应完全,加入80 mL的NaCl饱和溶液,然后用80 mL的乙醚萃取3次,加入无水硫酸镁,干燥,过滤,将得到的滤液旋蒸除去溶剂,将得到的液体进行真空干燥,最后得到的液体即为纯的不同的氮杂环丙烷底物.
1.2.4 氮杂环丙烷底物的表征
对于合成的一系列化合物进行结构表征,表征数据如下文所示:
1a:淡黄色液体,产率为99%.1H NMR(400 MHz,CDCl3)δ 7.42~7.21(m,5H),2.58~2.44(m,3H),2.28(m,1H),1.92(t,1H),1.63(t,1H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):3 036,2 970,2 946,1 452,1 385,1 081,696.Elemental analysis cald(%)for C9H11N:C 81.16,H 8.32,N 10.52,Found:C 81.01,H 8.28,N 10.59.
1b:淡黄色液体,产率为99%.1H NMR(400 MHz,CDCl3)δ 7.30~7.25(m,5H),2.52(m,1H),2.36~2.27(m,2H),1.92(d,1H),1.76~1.67(m,3H),0.99(s,3H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):3 035,2 931,2 878,1 458,1 379,1 082,697.Elemental analysis cald(%)for C11H15N:C 81.94,H,9.38,N 8.69,Found:C 81.91 H 9.41,N 8.72.
1c:淡黄色液体,产率为96%.1H NMR(400 MHz,CDCl3)δ 7.38~7.21(m,5H),2.51(m,1H),2.33~2.28(m,2H),1.91(d,1H),1.71~1.63(m,3H),0.93(t,3H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):3 033,2 929,2 818,1 457,1 375,1 085,699.Elemental analysis cald(%)for C12H17N:C 82.23,H 9.78,N 7.99,Found:C 82.27,H 9.75,N 7.96.
1d:淡黄色液体,产率为96%.1H NMR(400 MHz,CDCl3)δ 7.32(d,J=50.8 Hz,10H),2.56(m,J=6.5 Hz,1H),2.03(d,J=8.2 Hz,1H),1.90(d,1H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):3 363,3 030,2 913,1 494,1 453,1 356,699.Elemental analysis cald(%)for C15H15N:C 86.08,H 7.22,N 6.69,Found:C 86.15,H 7.23,N 6.63.
1e:淡黄色液体,产率为96%.1H NMR(400 MHz,CDCl3)δ 7.46~7.29(m,J=46.4 Hz,5H),2.67(m,1H),1.93(m,1H),1.67(m,1H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):2 968,1 471,1 225,989,762,699.Elemental analysis cald(%)for C12H17N:C 82.23,H 9.78,N 7.99,Found:C 82.27,H 9.72,N 7.81.
1f:淡黄色液体,产率为96%.1H NMR(400 MHz,CDCl3)δ 7.33~7.24(m,5H),2.52(m,1H),2.33(m,1H),1.92(d,1H),1.70(m,J=26.7 Hz,2H),1.56(m,J=24.4 Hz,2H),0.94(d,6H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):2 931,2 874,1 492,1 087,1 014,810,654.Elemental analysis cald(%)for C13H19N:C 82.48,H 10.12,N 7.40,Found:C 82.43,H 10.17,N 7.43.
1g:淡黄色液体,产率为96%.1H NMR(400 MHz,CDCl3)δ 7.32~7.23(m,5H),2.73(m,2H),2.37(m,1H),1.92(d,1H),1.73(d,1H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):3 448,2 965,2 812,1 456,1 382,1 080,698.Elemental analysis cald(%)for C14H22N2:C 77.01,H 10.16,N 7.40,Found:C 77.12,H 10.11,N 12.78.
1h:淡黄色液体,产率为98%.1H NMR(400 MHz,CDCl3)δ 7.27(m,J=36.4 Hz,5H),3.76(m,2H),1.96(d,1H),1.77(d,1H),1.21(t,J=7.0 Hz,1H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):3 385,2 934,1 452,1 357,1 063,742,589.Elemental analysis cald(%)for C10H13ON:C 73.59,H 8.03,N 8.58,Found:C 73.65,H 8.09,N 8.52.
1i:淡黄色液体,产率为99%.1H NMR(400 MHz,CDCl3)δ 7.27~7.16(m,5H),2.50(d,J=33.3 Hz,1H),1.90(d,1H),1.66(s,3H),0.98(t,3H).13C NMR(101 MHz,CDCl3)δ 140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):2 930,2 874,1 517,1 378,1 077,790.Elemental analysis cald(%)for C12H17N:C 82.23,H 9.78,N 7.99,Found:C 82.21,H 9.75,N 7.98.
1j:淡黄色液体,产率为99%.1H NMR(400 MHz,CDCl3)δ 7.23(m,J=55.8 Hz,5H),2.48(d,J=26.0 Hz,1H),2.30(d,J=28.7 Hz,2H),1.85(d,1H),0.97(t,3H).13C NMR(101 MHz,CDCl3)δ140.29,128.33,126.88,126.03,77.57,77.25,76.94,47.97,42.37,39.41.Selected IR peaks(KBr,cm-1):3 033,2 859,1 466,1 367,743,697.Elemental analysis cald(%)for C11H14ClN:C 67.52,H 7.21,N 7.16,Found:C 65.57,H 7.28,N 7.12.
1.3 双功能催化剂Zn-PPBCl合成与表征
参考文献[17],合成了双功能催化剂Zn-PPBCl,其合成方法如图2所示.对多聚甲醛,盐酸,水杨醛反应得到的产物进行重结晶和真空干燥,得到PCl.然后,在甲苯中加入PCl和三苯基膦,加热回流,让其反应完全,过滤,真空干燥,得到PPCl.将其和苯偶酰溶解在醋酸中,再加入醋酸铵,加热回流,反应完全之后,加入过量超纯水,抽滤,真空干燥,溶解,干燥,用二氯甲烷和正戊烷重结晶得到PPBCl.最后将其和二水醋酸锌溶解在无水乙醇中,加热回流,得到白色粉末,即为双功能希夫碱锌催化剂,其核磁氢谱数据如图3所示.

图2 双功能催化剂Zn-PPBCl的合成

图3 双功能催化剂Zn-PPBCl的核磁氢谱数据
2 实验结果与讨论
向已经经过真空干燥的高压反应釜中加入磁子,之后再分别加入一定量的催化剂和氮杂环丙烷,控制气瓶开关,置换CO23次,再向其中通入CO2气体到反应所需压力之下,将其放入油浴锅中加搅拌,20 min之后观察气压表是否达到实验值,若未达到,则需继续通入CO2,使气压达到实验所需值,在反应过程中压力值需要保持恒定.当反应达到指定时间之后,将高压反应釜降温至室温,之后将高压反应釜阀门缓慢打开,将剩余的二氧化碳排放干净,取少量反应液作1H NMR表征,计算得到出产率以及表示选择性.
2.1 反应条件优化
本次实验的加成反应如图4所示.以2-苯基1-丙基氮杂环丙烷作为探索条件的反应底物,探索反应的最佳条件,结果如表1所示.

图4 加成反应

表1 双功能金属锌催化剂催化2-苯基1-丙基氮杂环丙烷与CO2环加成反应条件优化a
2.1.1 催化剂用量对产率的影响
催化剂用量对于反应活性有一定的影响(表1条目1,2,4,8),可以看出,当催化剂用量为0.33%(物质的量分数)时,5-取代恶唑烷酮产物的产率为57%,当催化剂用量上升到0.5%(物质的量分数)时,产率上升,但是催化剂用量上升至1%(物质的量分数)时,产率进一步上升,说明适量多的催化剂可以促进氮杂环丙烷和CO2反应,显示出较高的催化活性,故可以看出催化剂的合理比例为催化剂与氮杂环丙烷物质的量之比为1∶100.
2.1.2 CO2压强对产率的影响
CO2压强对催化活性也有很大的影响(表1条目3,4,7),可以看出随着压强由1 MPa升高到3 MPa,产物的产率先增多后减小,可以说明适当的压强可以促进催化剂和底物结合从而使产率升高,但是过高的压强会引起稀释效应,不利于底物和催化剂相结合,使反应活性降低,进而使反应产率降低.因此,通过探究实验可知,最佳的反应压强是2 MPa.
2.1.3 温度对产率的影响
温度对于反应活性也有影响(表1条目4,9~11),随着温度从90 ℃升至110 ℃,再升至130 ℃最后升温至150 ℃时,5-取代产物的产率随着温度的升高而先增加后减少,而4-取代产物的产率则一直增加.但是该反应是以5-取代产物为主,故最后选取的最适温度为130 ℃,而高温情况下4-取代产物产率增加的可能原因是高温促进氮杂环丙烷上亚甲基开环,从而使4-取代产物产率增加,抑制5-取代产物的合成.
2.1.4 时间和溶剂对产率的影响
反应时间对于反应活性的影响也是不可忽视的(表1条目2~4,6),可以看出随着时间从5 h增加到8 h,产率增加的比较多,但是时间增加到12 h时,产率基本保持恒定,故反应的最佳时间为8 h.当加入1 mL的二氯甲烷之后(表1 条目5),产物的产率会减小,说明极性溶剂会影响催化剂的催化活性.
综上所述,双功能金属锌催化剂催化CO2与氮杂环丙烷环加成反应的最佳反应条件为CO2压强为2 MPa、反应温度为130 ℃、催化剂与底物物质的量之比为1∶100,反应时间为8 h.
2.2 底物适用性探讨
由于主要产物是5-取代产物,故只看5-取代产物的产率,结果如图5所示,可以看到取代基是直链烷烃时,随着碳链的增加,5-取代恶唑烷酮产率会随之增加.当取代基为苄基时,转化率值是最大的,但是取代基为叔丁基的时候,几乎没有产率,可能是空间位阻原因导致.当取代基上有支链的时候,产率会相应地降低,可能也是位阻的原因.当取代基上有羟基存在时,产率较低,可能是氮杂环的活性被抑制.针对苯环上有取代基的氮杂环,氯原子会比甲基效果要好,说明苯环上带有钝化基团的底物比活化基团的底物反应性好.

图5 催化CO2与不同种氮杂环丙烷底物环加成反应产率
3 反应机理研究
根据文献[18]和研究结果,提出了图6的反应机理:催化剂中的Zn通过与环胺上N原子配位的方式将其活化,可以使氯离子进攻氮杂环的两种C,从而使三元环开环,生成两种产物,一种是5-取代的恶唑烷酮,另一种是4-取代的恶唑烷酮.由前面的研究数据可知,5-取代产物为主要产物,故可知氯离子会更容易进攻位阻较大的C.但当温度升高到一定值时,则会进攻位阻较小的C,使其能够产生4-取代的恶唑烷酮,最后闭环得到相应的恶唑烷酮产物.
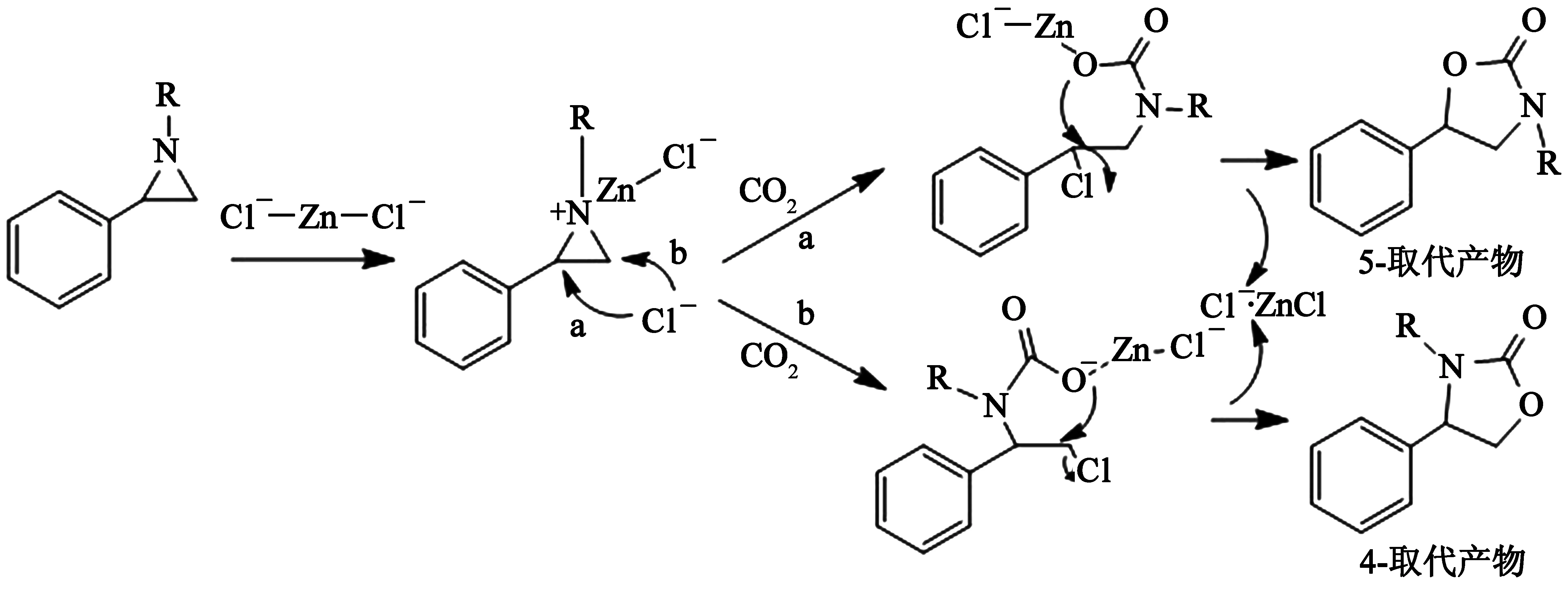
图6 氮杂环丙烷底物和CO2环加成反应的反应机理
4 结语
合成了一系列氮杂环丙烷底物,并对它们的结构进行了表征.随后合成了双功能催化剂Zn-PPBCl,将其用于催化氮杂环丙烷底物与CO2发生环加成反应,以制备化学品恶唑啉酮类化合物.系统研究了压强、时间、温度等参数对催化效率的影响,得到最佳催化条件(130 ℃,2 MPa,8 h,催化剂与氮杂环丙烷物质的量之比为1∶100),在该条件下,CO2可与多种氮杂环丙烷底物反应.最后,根据实验结果和文献报道,推断出了可能的反应机理.该催化体系在工业和医药等领域具有较高的潜在实际应用价值.
