维奈克拉联合阿扎胞苷与地西他滨联合DAG/IAG方案治疗新诊断急性髓系白血病的效果比较
2022-07-12阮敏龙章彪黄震琪吴炜梁兴林梁莉曾庆曙
阮敏,龙章彪,黄震琪,吴炜,梁兴林,梁莉,曾庆曙
安徽医科大学第一附属医院血液科,合肥 230022
维奈克拉是抗凋亡蛋白B细胞淋巴瘤因子-2(BCL-2)的选择性小分子抑制剂。阿扎胞苷是一种同时具有针对 DNA及RNA双重作用的去甲基化药物,多项临床研究肯定了此2种药物联合治疗老年急性髓系白血病(AML)的有效性及安全性[1-3]。地西他滨(DAC)联合预激方案(DAG/IAG)为指南推荐用于不适合标准化疗的患者[4]。目前对于上述2种治疗方案的疗效及不良反应比较未见文献报道,本研究回顾性分析维奈克拉联合阿扎胞苷与DAC联合DAG/IAG方案治疗新诊断不适合标准化疗的AML病患者,比较2组临床疗效及安全性。
1 资料与方法
1.1 一般资料 选取2019年2月至2022年3月在安徽医科大学第一附属医院新诊断的40例AML患者的临床资料。所有患者均行骨髓细胞形态学、免疫分型、染色体等相关检查,该疾病的诊断、疗效及预后判断标准参照第3版《血液病诊断及疗效标准》[5]。本研究通过安徽医科大学第一附属医院伦理委员会审批(编号:PJ2022-03-33)。其中21例患者采用DAC联合DAG /IAG方案治疗为A组,另19例患者应用维奈克拉联合阿扎胞苷方案治疗为B组。
1.1.1 A组临床资料 AML患者21例,男性9例,女性12例;年龄41~69(58.7±7.3)岁;年龄<60岁10例,≥60岁11例。按FAB分型:M1型1例,M2型11例[其中1例为骨髓增生异常综合征(MDS)转化],M4型2例,M5型7例(其中1例为MDS转化)。
1.1.2 B组临床资料 AML 患者19 例,男性9例,女性10例;年龄52~68(61.8±4.8)岁;年龄<60岁5例,≥60岁14例。按FAB分型:M2型5例,M4型1例,M5型12例(2例为MDS 转化),M6型1例。
1.2 治疗方案
1.2.1 A组方案 采用低剂量的DAC联合DAG/IAG方案。DAC(江苏正大天晴药业股份有限公司生产)每日20 mg/m2,静脉滴注,第1~5天。伊达比星[Actavis Italy S.P.A(意大利)生产]每天10 mg,静脉滴注,隔天1次,共2~4次;或柔红霉素(瀚晖制药有限公司生产)每天20~30 mg/m2,静脉滴注,隔天1次,共4次;阿糖胞苷(国药一心制药有限公司生产)10~20 mg/m2,皮下注射,每12 h 1次,连用7~14 d;重组人粒细胞刺激因子(杭州九源基因工程有限公司生产)300 μg,1次/d,皮下注射,白细胞>20×109/L停用。
1.2.2 B组方案 采用阿扎胞苷[Baxter Oncology GmbH(德国)生产,注射剂100 mg/瓶]+维奈克拉片[Abbvie Ireland NL B.V(爱尔兰)生产,100 mg/片]方案。第1疗程维奈克拉片第1天100 mg、第2天200 mg、第3~28天400 mg,口服,1次/d;阿扎胞苷75 mg/m2,1次/d,第1~7天皮下注射,28 d为1个疗程;其后所有疗程,阿扎胞苷同前,维奈克拉片从第1天起即400 mg开始口服,疗程28 d。
上述40例患者均经过1个疗程化疗后根据骨髓细胞学结果及流式微小残留病(MRD)评估疗效,有效者[即完全缓解(CR)或部分缓解(PR)]重复原方案化疗;无效者不再重复原方案。获得完全缓解的患者,根据危险度分层进行巩固治疗或造血干细胞移植。
1.3 支持治疗 化疗期间给予止吐、护胃、水化、碱化、保肝、保肾、防止肿瘤溶解综合征发生;按标准成分输注血制品、白蛋白等;感染时行病原学及影像学检查,及时使用广谱抗生素。
1.4 疗效标准 参照第3版《血液病诊断及疗效标准》[5]。根据患者临床表现、外周血象和骨髓象将疗效分为CR、PR及未缓解(NR)。CR+PR为总有效率(OR)。
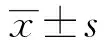
2 结果
2.1 基线资料比较 2组患者在基线年龄、性别、初诊时的白细胞、血红蛋白、血小板、危险度分层、原始细胞数、丙氨酸氨基转移酶、白蛋白、乳酸脱氢酶、血钾、血钙、肌酐、纤维蛋白原、纤维蛋白原降解产物(FDP)、D-二聚体等方面差异均无统计学意义(P>0.05)。
2.2 诱导缓解疗效比较 2组间疗效比较:A组中,28.57%(6/21)患者达CR,33.33%(7/21)患者达PR,38.09%(8/21)患者达NR。B组中,57.89%(11/19)患者达CR,31.58%(6/19)患者达PR,10.53%(2/19)患者达NR。在诱导缓解治疗中,2组间疗效差异无统计学意义(P=0.079)。A组中,61.90%(13/21)患者达OR,38.09%(8/21)患者达NR。在B组中,89.47%(17/19)患者达OR,10.53%(2/19)患者达NR。在诱导缓解治疗中,B组优于A组,2组间OR差异有统计学意义(P=0.044)。
2.3 不良反应分析 2组不良反应方面,主要是骨髓抑制、感染及出血。A组患者中,所有患者均出现骨髓抑制,包括白细胞、血小板及血红蛋白的减低。与A组相似,B组患者大多数出现骨髓抑制,94.74%(18/19)白细胞减低,100.00%(19/19)血小板减低,100.00%(19/19)贫血。A组中90.48%(19/21)患者出现感染,感染部位多为肺部52.38%(11/21)。B组中57.89%(11/19)例患者出现感染,较多感染部位为肺部,达36.84%(7/19)。出血方面,A组患者9.52%(2/21)出现脑出血、9.52%(2/21)出现消化道出血;B组5.26%(1/19出现脑出血,未出现消化道出血。2组中常见的不良反应为胃肠道反应,包括呕吐、腹泻、便秘。其他相对罕见不良反应包括低钾血症与心律失常,多为轻微不良反应。2组不良反应进行比较,A组不良反应发生率略高于B组,但差异无统计学意义(P>0.05)。
2.4 无进展生存比较 在随访期内,A组患者95.24%(20/21)疾病进展,中位无进展生存期5个月,1年PFS率15.38%。B组患者31.58%(6/19)进展,1年PFS率58.56%。B组间无进展生存期优于A组,2组间差异有统计学意义(P=0.044)。见图1。
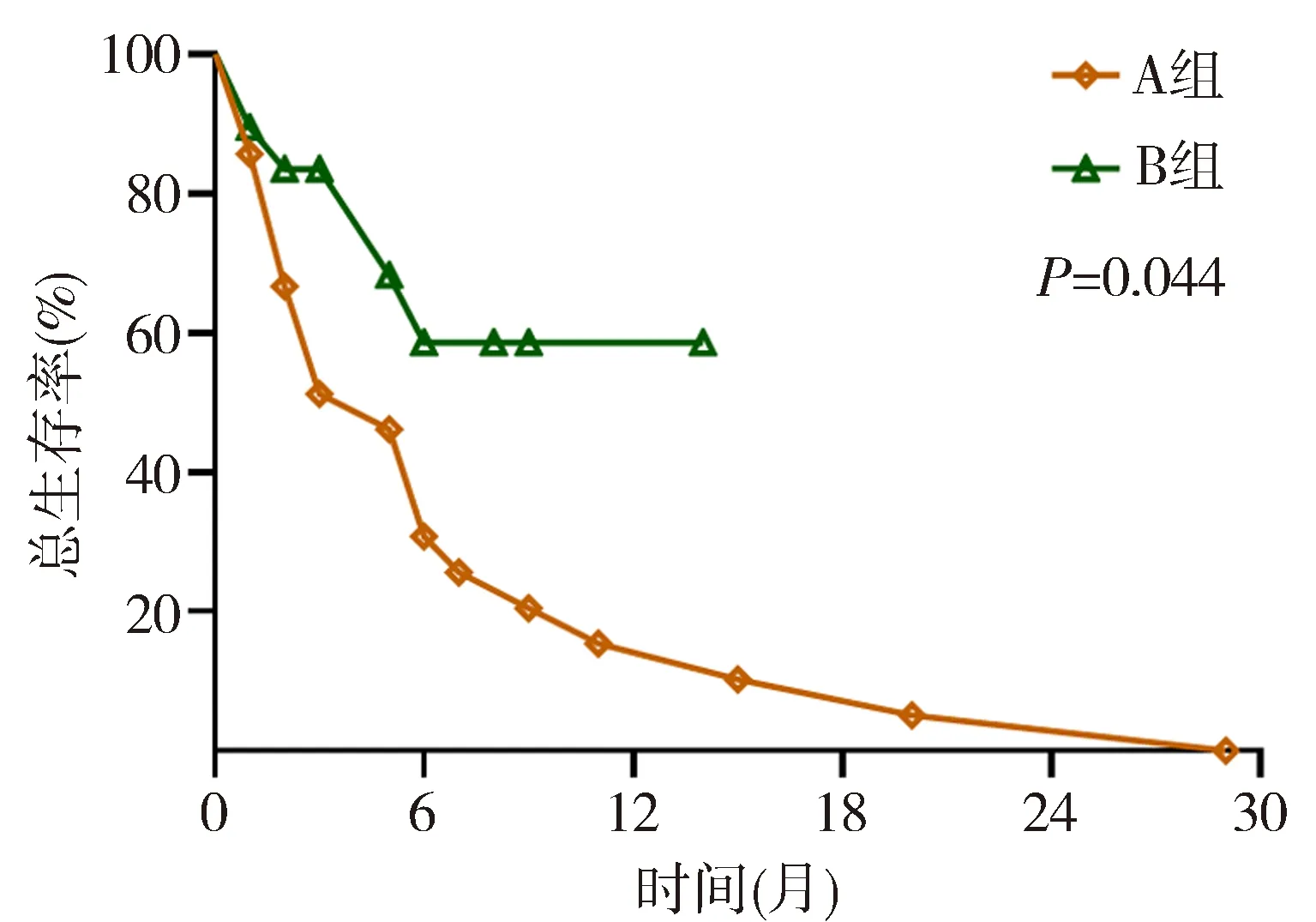
图1 A组与B组患者无进展生存期比较
2.5 总生存率比较 在随访期内,A组患者33.33%(7/21)存活,中位生存期10个月,1年总生存率36.97%。B组患者73.68%(14/19)存活,随访期间中位生存期未达到,1年总生存率62.01%。中位生存期、1年总生存率B组均优于A组,但2组间差异无统计学意义(P=0.327)。见图2。
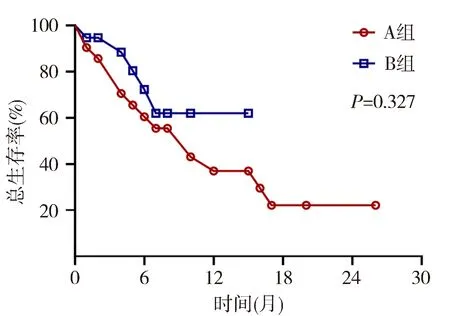
图2 A组与B组患者总生存率比较
3 讨论
维奈克拉是一种强效口服Bcl-2选择性抑制剂,能与Bcl-2家族蛋白的BH3结构域结合,抑制Bcl-2蛋白的表达,激活内源性线粒体凋亡通路,从而使肿瘤细胞快速凋亡。多项研究表明维奈克拉对不适合传统化疗的老年AML患者具有抗肿瘤活性和可耐受的安全性[6-10]。对于不符合强化化疗条件的老年AML患者,NCCN临床实践指南推荐使用维奈克拉和阿扎胞苷治疗作为新的治疗标准[11]。随着白血病检测技术的进步,尤其二代测序技术的发展,DNA甲基化相关基因突变在AML发病检测中的作用越来越受到重视[12]。对体能状态较差的AML患者,不适合标准或强化疗方案,国内多个临床中心探索采用DAC联合小剂量化疗,结果提示疗效提高、不良反应降低。Dinardo等[3,13]进行了2项多中心临床试验,显示维奈克拉联合阿扎胞苷治疗初诊老年AML,起效快、缓解率高。在高危患者中,CR率为60%;中位生存期为17.5个月,且安全、耐受性好。阿扎胞苷或地西他滨单药治疗的应答率较低(10%~50%,包括血液学改善),需要3.5~4.3个月才能达到最佳反应,且不能治愈,中位总生存期小于1年。Yamada等[14]首先设计小剂量阿糖胞苷(Ara-C)、阿克拉霉素(Acla)与G-CSF联合的方案(CAG)预激方案,用于治疗初治、复发和难治性老年AML患者,在临床上取得了令人满意的疗效。研究显示,G-CSF受体几乎在所有AML细胞表达,G-CSF能募集AML细胞进入S期,从而提高S期特异性药物Ara-C的疗效,故G-CSF能有效增强小剂量Ara-C对髓系白血病细胞的诱导凋亡及分化作用,而Acla和Ara-C一样在低浓度时具有诱导分化的作用[15]。目前国内管俊等[16]、张金燕[17]报道DAC联合减量的IAG/HAG,客观缓解率最高为84.62%,最低为54.17%,可能与入组病例疾病状态、治疗方案不完全相同有关[18]。但目前对于维奈克拉联合阿扎胞苷与传统的DAC联合DAG/IAG方案疗效及安全性比较,尚无报道。
本研究中,分别采用维奈克拉联合阿扎胞苷方案(B组)和地西他滨联合DAG /IAG方案(A组)治疗新诊断不适合标准化疗的AML患者,所有患者在基线年龄、性别比例、初诊时的白细胞、血红蛋白、血小板、危险度分层等方面差异均无统计学意义(P>0.05)。在诱导缓解治疗中,B组缓解病例数大于A组,2组间差异有统计学意义。P值接近于0.05。在随访期内,无进展生存B组优于A组,但2组间总生存期差异无统计学意义;显示B组在治疗缓解上有优势,且可获得更优的无进展生存,但并未转换成长期生存优势,故而需要思考维奈克拉联合阿扎胞苷方案治疗AML是否能长期使用,后期治疗过程中是否需更换治疗方案需进一步探讨。
药物安全性方面,2组不良反应均是骨髓抑制、感染及出血。几乎所有患者都发生血液系统不同程度的白细胞减少、血小板减少、贫血等。2组发生感染部位最多为肺部,但没有出现严重肺部感染导致死亡病例。B组感染例数较A组少,感染不良反应更小。较严重的不良反应为脑出血、消化道出血,化疗后血小板极度减低,重要脏器出血为化疗导致死亡的严重并发症,2组病例中出现脑出血经血制品输注度过危险期,故化疗期间血制品输注至关重要,减少严重出血亦是治疗成功的关键。2组中常见的不良反应为胃肠道反应,包括呕吐、腹泻、便秘。肿瘤溶解综合征在2组中均未出现。2组化疗不良反应与总体研究人群的安全性数据一致,没有发现与白细胞减少相关的严重不良事件[19-20]。
综上所述,本研究认为维奈克拉联合阿扎胞苷应用于新诊断AML的老年患者以及身体状态无法耐受标准化疗的年轻患者与DAC联合DAG/IAG相比较疗效更优,安全性好,值得临床推广应用。
