氨曲南联合头孢他啶/阿维巴坦对产新德里金属β-内酰胺酶大肠埃希菌的体外抗菌活性评估*
2022-07-12王艺马可妮刘灵裴瑞景王睿马萍姜飞李洪春徐州医科大学医学技术学院江苏徐州004徐州医科大学附属医院检验科江苏徐州00
王艺,马可妮,刘灵,裴瑞景,王睿,马萍,,姜飞,李洪春,(.徐州医科大学医学技术学院,江苏徐州 004;.徐州医科大学附属医院检验科,江苏徐州 00)
自2009年首次发现产新德里金属β-内酰胺酶(New Delhi metallo-β-lactamase, NDM)的耐碳青霉烯类肠杆菌目细菌(carbapenem-resistant Enterobacterales,CRE)以来,该类细菌引起的感染及全球播散已经成为一个重大的公共卫生问题。我国已有多个城市和地区报道CRE克隆流行[1-3],一项纵向大规模CRE研究的数据显示,NDM金属酶主要存在于大肠埃希菌中[4],据CHINET数据监测网显示大肠埃希菌是引起血流感染和尿路感染最主要的病原菌,产NDM大肠埃希菌通常同时携带多种超广谱β-内酰胺酶(extended-spectrum β-lactamase,ESBLs),导致多重耐药而仅对替加环素和黏菌素等极少数抗菌药物敏感,给临床治疗该类细菌引起的感染带来极大困难。
阿维巴坦是一种新型β-内酰胺酶抑制剂,体外对肠杆菌科细菌产生的ESBLs、KPC 酶和OXA-48酶有活性,但对以NDM为代表的金属β-内酰胺酶(metallo-β-lactamases, MBLs)无抑制作用[5]。而氨曲南对MBLs保持稳定,但被大多数ESBLs水解,两种药物联合使用时,阿维巴坦能保护氨曲南免受ESBLs水解,使氨曲南维持抗菌活性[6],但该组合在国内的临床病例应用报道较少。本研究旨在评估氨曲南联合头孢他啶/阿维巴坦对产NDM金属酶的大肠埃希菌的体外抗菌活性,为该组合治疗产金属酶的碳青霉烯耐药大肠埃希菌引起的感染提供数据支持。
1 材料与方法
1.1菌株来源及鉴定 收集徐州医科大学附属医院2018—2020年临床分离的碳青霉烯耐药[亚胺培南(IPM)最低抑菌浓度(minimum inhibitory concentration, MIC)≥4 μg/mL]大肠埃希菌30株,分离自血液、尿液样本各15株。所有菌株经Vitek 2 Compact GN鉴定卡和质谱确认。
1.2主要仪器与试剂 Vitek 2 Compact全自动细菌分析仪(法国生物梅里埃公司),MALDI-TOF MS仪(德国布鲁克公司),哥伦比亚血琼脂平板、M-H平板(上海科玛嘉公司),头孢他啶/阿维巴坦、氨曲南E-test纸条(温州康泰公司),碳青霉烯酶检测缓冲液(珠海迪尔公司)、PCR扩增仪、GelX1850凝胶成像仪(美国Bio-Rad公司),DYY-8C电泳仪(北京六一仪器厂),1 000 bp DNA marker、PCR mix(日本TaKaRa公司),引物合成(上海生工生物公司),3730XL测序分析仪(美国 ABI 公司)。
1.3药敏试验 用Vitek 2 Compact及配套N335和XN04药敏卡对菌株进行药物敏感性测定,并采用E-test纸条法测定菌株对氨曲南和头孢他啶/阿维巴坦的MIC,结果判读基于美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)2021年判定标准[7]。
1.4联合药敏试验 采用氨曲南和头孢他啶/阿维巴坦双E-test纸条检测二者的体外协同作用[8]。改进方法为:取0.5麦氏浊度单位浓度的大肠埃希菌菌悬液涂布M-H平板,然后将氨曲南和头孢他啶/阿维巴坦E-test纸条完全重合后垂直插入平板中,37 ℃反应18~24 h后,在头孢他啶/阿维巴坦存在条件下读取氨曲南的MIC值[8]。大肠埃希菌ATCC 25922为对照菌株。
1.5碳青霉烯酶表型检测 参照碳青霉烯酶检测缓冲液试剂说明书进行操作。用无菌接种环刮取血平板上过夜培养的至少3个纯菌落配制0.5麦氏浊度单位浓度的菌悬液,涂布M-H平板,干燥3~5 min;贴4张IPM纸片并在其中3张纸片分别滴加10 μL乙二胺四乙酸(EDTA)、10 μL 3′-氨基苯硼酸(3-aminobenzeneboronic acid,APB)以及10 μL EDTA+10 μL APB,各纸片中心距离≥25 mm。35 ℃培养18~24 h后,测量抑菌圈直径大小。结果判读:与单独IPM纸片相比,IPM+APB抑菌圈直径≥5 mm,提示产丝氨酸酶;IPM+EDTA抑菌圈直径≥5 mm,提示产金属酶;IPM+APB和IPM+EDTA抑菌圈无明显扩大,但IPM+APB+EDTA抑菌圈直径≥5 mm,提示同时产丝氨酸酶+金属酶。
1.6细菌DNA提取及耐药基因检测 用煮沸法提取细菌DNA。PCR方法扩增4种碳青霉烯酶基因(NDM、KPC、IMP、VIM)、5种ESBL基因(CTX-M-1group、CTX-M-9group、SHV、TEM、CMY),靶基因引物序列参照文献[9],引物由上海生工生物公司合成。反应体系共50 μL,包括2×PCR Master Mix 25 μL,10 μmol/L上、下游引物各3 μL,DNA模板3 μL,灭菌ddH2O 16 μL。反应参数:94 ℃预变性5 min;94 ℃ 45 s,54 ℃(NDM、KPC、IMP、VIM、SHV、TEM、CMY)/52 ℃(CTX-M-1group、CTX-M-9group)45 s,72 ℃ 60 s,30个循环;72 ℃ 10 min。产物经12 g/L琼脂糖凝胶电泳后,用凝胶成像分析系统分析,阳性条带送上海生工生物公司在3730XL测序分析仪上进行Sanger测序。
1.7多位点序列分型(multi-locus sequence typing, MLST) 采用PCR方法对大肠埃希菌进行MLST。对7个管家基因(adk、fumC、gyrB、icd、mdh、purA、recA)进行扩增,反应体系同1.6,引物序列及退火温度见表1。PCR 产物纯化后送上海生工生物公司在3730XL测序分析仪上进行Sanger双向测序后拼接,将测序数据提交至MLST网站(https://pubmlst.org/bigsdb?db=pubmlst_escherichia_seqdef),确定菌株ST型。

表1 管家基因扩增引物序列
2 结果
2.1药敏结果及氨曲南与头孢他啶/阿维巴坦体外协同作用 30株大肠埃希菌对替加环素和多黏菌素耐药率为0,对阿米卡星耐药率为46.7%(14/30),对氨曲南耐药率为90%(27/30,MIC范围:8~≥256 μg/mL,MIC50≥256 μg/mL,MIC90≥256 μg/mL),对头孢他啶/阿维巴坦的耐药率为100%(MIC范围:128~≥256 μg/mL,MIC50≥256 μg/mL,MIC90≥256 μg/mL)。30株大肠埃希菌均显示出氨曲南与头孢他啶/阿维巴坦之间协同作用,氨曲南MIC50和MIC90分别下降至2 μg/mL和4 μg/mL,其中,27株对氨曲南耐药的大肠埃希菌在头孢他啶/阿维巴坦存在情况下25株对氨曲南敏感(MIC范围<0.064~4 μg/mL),1株对氨曲南中介(MIC=8 μg/mL),1株仍对氨曲南耐药(16 μg/mL)。见表2、图1。
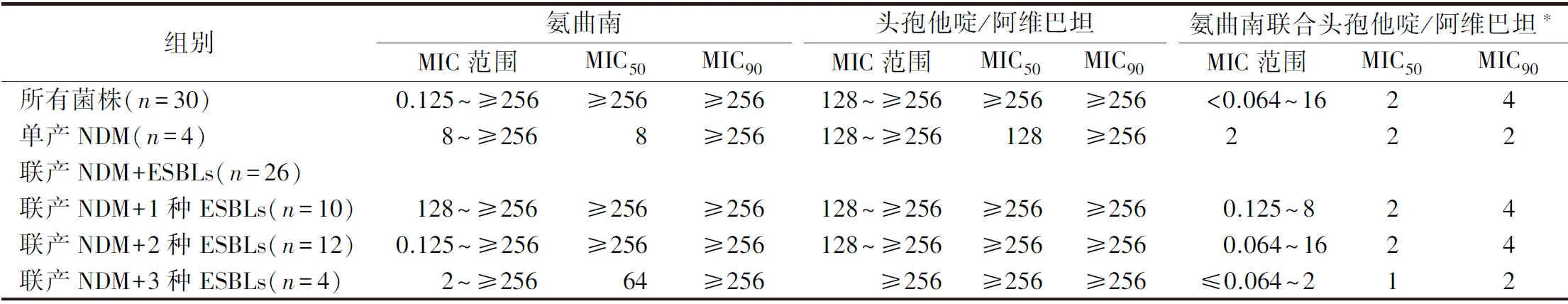
表2 30株大肠埃希菌对氨曲南、头孢他啶/阿维巴坦及氨曲南联合头孢他啶/阿维巴坦的药敏结果(μg/mL)
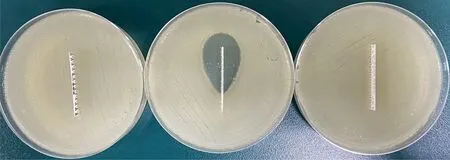
注:左,氨曲南MIC≥256 μg/mL;中,氨曲南联合头孢他啶/阿维巴坦MIC=1 μg/mL;右,头孢他啶/阿维巴坦MIC≥256 μg/mL。
2.2碳青霉烯酶表型检测结果 与单独IPM纸片相比,30株大肠埃希菌IPM+APB抑菌圈直径无明显变化,IPM+EDTA以及IPM+EDTA+APB抑菌圈直径≥5 mm,提示细菌产金属酶。见图2。
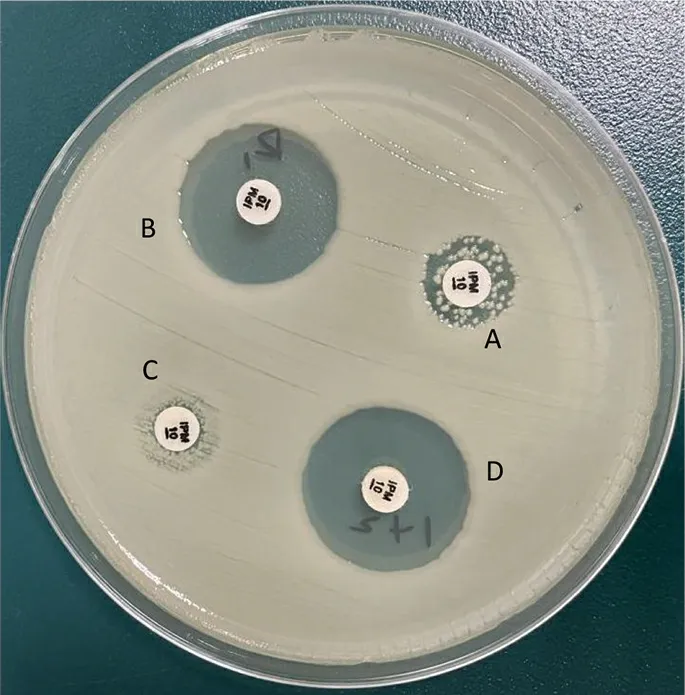
注:A,IPM;B,IPM+EDTA;C,IPM+APB;D,IPM+EDTA+APB。
2.3耐药基因检测结果 30株大肠埃希菌中携带NDM-5基因26株,携带NDM-7基因2株,携带NDM-1和NDM-9基因各1株;15株携带TEM-1基因,22株携带CTX-M-1组基因(10株携带CTX-M-15,12株携带CTX-M-55),9株携带CTX-M-9组基因(均为CTX-M-27)。未检出KPC、IMP、VIM、SHV基因。
2.4MLST分型结果 30株大肠埃希菌共检出8种ST型,其中以ST167为主(n=12,40%),其次为ST405和ST410均6株,ST448 2株,ST744、ST746、ST361、ST2705各1株。见图3。

注:不同颜色点代表不同ST型,点的大小代表菌株数量,线上数字代表不同ST型间管家基因差异数。
3 讨论
头孢他啶/阿维巴坦已被广泛用于治疗以产KPC为代表的丝氨酸酶的革兰阴性杆菌引起的感染[10]。而对于产金属酶的多重耐药革兰阴性杆菌,国外已有多项病例研究表明,氨曲南联合头孢他啶/阿维巴坦的组合能够治疗产NDM-1和OXA-48的肺炎克雷伯菌、产NDM-1和AmpC的铜绿假单胞菌以及产NDM-1和KPC-4的阴沟肠杆菌引起的感染并取得良好疗效[8,11-13],主要是利用阿维巴坦来保护氨曲南免受ESBLs水解,使氨曲南维持抗菌活性。国内一项多中心体外研究显示,94.7%的CRE因携带一种或多种ESBLs对氨曲南耐药,但在联合阿维巴坦之后,氨曲南耐药菌株中96.9%的CRE菌株氨曲南/阿维巴坦的MIC≤1 μg/mL[14]。
本研究对30株CRE进行碳青霉烯酶基因和ESBLs基因检测,结果发现所有大肠埃希菌均产NDM基因,86.7%的菌株(26/30)同时携带NDM基因和1种或1种以上ESBLs基因,其中88.5%的菌株(23/26)对氨曲南耐药,所有菌株对头孢他啶/阿维巴坦耐药。氨曲南联合头孢他啶/阿维巴坦之后,对联产NDM金属酶和ESBLs的大肠埃希菌具有显著的协同作用,氨曲南耐药菌株中91.3%(21/23)的菌株药敏结果由耐药变为敏感,另有2株细菌氨曲南MIC分别下降至8 μg/mL(中介)和16 μg/mL(耐药)。13.3%的菌株(4/30)只携带NDM基因,但仍对氨曲南耐药(MIC≥8 μg/mL),原因可能是携带本研究检测之外的其他类型的ESBLs。在联合头孢他啶/阿维巴坦后,4株细菌氨曲南的MIC由8 μg/mL(耐药)下降至2 μg/mL(敏感)。研究报道,通过体外筛选的对氨曲南联合头孢他啶/阿维巴坦耐药的细菌,其耐药机制与CMY基因突变有关(Tyr150Ser 或Asn346His)[15]。在用微量肉汤稀释法确认E.coli13耐药菌株对氨曲南联合头孢他啶/阿维巴坦MIC为16 μg/mL后进行CMY基因检测,但未检测到该基因,说明氨曲南联合头孢他啶/阿维巴坦耐药还存在其他未知的机制,有待进一步研究。另外,相对于传统的微量肉汤稀释法,本研究采用氨曲南和头孢他啶/阿维巴坦双E-test纸条法检测二者的体外协同作用,为实验室提供了一种简便、快速的检测手段。
30株大肠埃希菌检测出8种ST型,包括国内较为常见的ST167、ST405和ST410及其他少见ST型,氨曲南联合头孢他啶/阿维巴坦均对其表现出协同作用,说明这种药物组合可以广泛应用于治疗不同ST型产NDM金属酶的大肠埃希菌感染。
文献报道,在用头孢他啶/阿维巴坦和氨曲南治疗产金属酶肠杆菌科细菌感染时,需要监测二者的血药浓度,保证给药间隔期间在头孢他啶/阿维巴坦存在的情况下,氨曲南的药物浓度大于MIC,以确保治疗效果[13]。同时,Ⅱ期临床试验也证明在临床许可浓度下,氨曲南联合头孢他啶/阿维巴坦在治疗产金属酶肠杆菌科细菌引起的复杂性腹腔感染方面表现出的良好的安全性和有效性[16]。综上所述,氨曲南联合头孢他啶/阿维巴坦对产NDM金属酶大肠埃希菌表现出较强的体外抗菌活性,可以作为该类耐药菌感染的一种治疗选择。
