仑伐替尼治疗酪氨酸激酶抑制剂经治不可切除肝细胞癌患者的效果及安全性观察
2022-06-23刘晓民魏建莹李文东丁晓燕于明华陈京龙
刘晓民, 孙 巍, 魏建莹, 李文东, 丁晓燕, 于明华, 陈京龙
首都医科大学附属北京地坛医院 肿瘤内科, 北京 100015
原发性肝癌为最常见的消化系统肿瘤,其全球每年新发病例数居恶性肿瘤第6位,死亡病例数居恶性肿瘤第3位[1]。早期、局部晚期、转移性原发性肝癌5年生存率分别为31%、11%、2%[2]。原发性肝癌发病率和病死率均较高,其中约80%为肝细胞癌(HCC)。有研究[3-4]表明,索拉非尼可延长中期晚期HCC总生存期(OS)约3个月,成为中晚期HCC一线用药。之后10年内,HCC的靶向治疗无突破性进展。2018年,REFLECT研究[5]结果显示:在不可切除HCC患者中,仑伐替尼组OS非劣效于索拉非尼组。仑伐替尼成为不可切除HCC的一线用药[6]。索拉非尼治疗失败的HCC患者是否可以选择仑伐替尼治疗为临床工作中的新问题。目前缺乏酪氨酸激酶抑制剂(TKI)经治HCC应用仑伐替尼的数据。本研究旨在观察TKI经治不可切除HCC患者应用仑伐替尼的疗效及安全性。
1 资料与方法
1.1 研究对象 回顾性分析2019年1月—2020年1月于本院就诊并接受仑伐替尼治疗的不可切除HCC患者资料。入组标准:(1)HCC诊断符合中国临床肿瘤学会《原发性肝癌诊疗指南2020》[7];(2)随访超过4周;(3)影像学资料为增强CT/MRI;(4)具有可评价病灶。排除标准:(1)临床资料记录不完整;(2)具有仑伐替尼治疗禁忌证。
1.2 研究方法 根据治疗方式将纳入患者分为TKI初治组和TKI经治组。所有患者均口服仑伐替尼8 mg(体质量<60 kg)或12 mg(体质量≥60 kg),1次/d。观察时间截止至入组后1年或调整治疗方案或肿瘤进展或死亡。
1.3 疗效及安全性评价 疗效评价:本研究主要观察指标为无进展生存期(PFS);次要观察指标为客观缓解率(ORR)和疾病控制率(DCR),其中ORR=完全缓解(CR)+部分缓解(PR)病例数/观察总病例数,DCR=CR+PR+稳定(SD)病例数/观察总病例数。研究根据mRECIST标准[8]进行疗效评价。安全性评价:记录治疗中不良事件,包括临床症状(如腹泻、乏力)、实验室指标异常(如转氨酶升高)等,并根据常见不良事件评价标准(CTCAE)5.0版[9]进行分级。
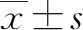
2 结果
2.1 一般资料 共纳入76例患者,其中TKI初治组49例,TKI经治组27例。TKI初治组均为一线治疗;TKI经治组包括25例二线治疗(均为索拉非尼经治)和2例三线治疗(1例为索拉非尼、瑞戈非尼经治,1例为索拉非尼、FOLFOX化疗)。两组基线资料比较差异均无统计学意义(P值均>0.05)(表1)。
2.2 疗效评价 76例患者中位PFS为91(53.18~128.82)d,ORR为30.3%,DCR为61.8%。TKI初治组中位PFS为115(68.58~161.42)d,TKI经治组中位PFS为72(45.07~98.93)d,两组间PFS比较差异无统计学意义(P=0.148)(图1)。TKI初治组CR 1例,PR 17例,SD 14例,疾病进展(PD) 14例,未评价(NE)3例;TKI经治组CR 1例,PR 4例,SD 10例,PD 11例,NE 1例。两组ORR(36.7% vs 18.5%,P=0.098)及DCR(65.3% vs 55.6%,P=0.402)比较,差异均无统计学意义。

图1 两组PFS生存曲线比较
2.3 安全性评价 TKI初治组任何水平的不良事件发生率与TKI经治组相近(93.9% vs 96.3%,P>0.05)。TKI初治组与TKI经治组3级及以上不良事件的发生率比较,差异无统计学意义(24.5% vs 18.5%,P=0.550)。两组常见不良事件包括:乏力(53.0% vs 77.7%)、食欲减退(42.9% vs 44.4%)、高血压(36.7% vs 37.0%)、手足综合征(26.5% vs 40.7%)、腹泻(14.3% vs 40.7%)、血尿(26.5% vs 18.5%)。TKI初治组3级及以上不良事件:乏力6例,高血压4例,食欲减退3例,TBil水平升高3例,腹泻2例,肝性脑病、ALT升高、AST升高、消化道出血各1例。TKI经治组3级及以上不良事件:乏力3例,高血压2例,腹泻2例,另有蛋白尿、手足综合征、TBil水平升高、关节痛各1例。
3 讨论
索拉非尼、仑伐替尼均为口服、小分子、多靶点的TKI,是晚期HCC的一线用药。目前缺乏这两种药物在不可切除HCC患者中互为二线或后线治疗疗效及安全性的数据。
本研究共纳入49例TKI初治和27例TKI经治不可切除HCC患者应用仑伐替尼治疗。研究结果显示,两组PFS、ORR及DCR均无显著差异,其中TKI初治组PFS有延长趋势,ORR、DCR有增加趋势。Hiraoka等[10]研究纳入不可切除HCC患者,分为TKI初治组和TKI经治组,短期疗效显示两组ORR(50.0% vs 36.8%,P=0.675)和DCR(87.5% vs 84.2%,P=1.000)无显著差异。该研究结果与本研究类似,均提示TKI经治患者可以从仑伐替尼治疗中获益,与TKI初治患者效果相似。此外,有研究[11]观察靶向药物初治及索拉非尼不耐受的不可切除HCC患者应用仑伐替尼治疗效果,结果显示两组ORR(61.8% vs 33.3%,P=0.28)相似,但初治组至疾病进展时间较索拉非尼不耐受组显著延长(P<0.05),与本研究结果两组PFS相似不同。考虑可能原因:上述研究仅纳入9例索拉非尼不耐受患者,样本量小,仍需扩大样本量进行观察。综上,仑伐替尼在TKI初治和TKI经治的不可切除HCC患者中疗效可能相似,既往治疗未接受仑伐替尼HCC患者可选择仑伐替尼。但目前尚无大型、前瞻性研究数据发表。仑伐替尼和索拉非尼存在交叉抗肿瘤作用机制,互为二线及以上治疗中,交叉耐药成为最常见问题。索拉非尼通过抑制血管内皮生长因子受体1~3、血小板衍生生长因子受体来抑制血管生成,同时通过下调Ras/Raf/Mek/Erk信号通路抑制肿瘤细胞生长[12-15]。仑伐替尼通过抑制血管内皮生长因子受体1~3、成纤维细胞生长因子受体1~4以及血小板衍生生长因子受体α、β来抑制血管生成,同时通过抑制KIT和RET来抑制肿瘤细胞增殖[16-19]。Tomonari等[11]研究观察HCC细胞和索拉非尼耐药的HCC细胞,发现索拉非尼耐药的HCC细胞对仑伐替尼存在交叉耐药。然而,另有研究[20-21]表明抑制FGF信号通路可减轻甚至克服索拉非尼耐药,索拉非尼治疗后病情进展的HCC患者仍有可能从仑伐替尼治疗中获益。因此,笔者建议不可切除HCC患者一线治疗可优先考虑仑伐替尼;索拉非尼治疗失败患者,在充分知情同意基础上,仍可以考虑应用仑伐替尼。

表1 两组患者基线资料
李广欣等[22]关于不可切除HCC患者应用仑伐替尼的真实世界研究结果显示,ORR为33.3%,DCR为66.7%,与本研究结果相似,但该研究未分析PFS。本研究为真实世界回顾性研究,中位PFS为91(53.18~128.82)d,显著低于REFLECT研究[5]的7.4(6.9~8.8)个月,考虑可能原因为本研究纳入更多Child-Pugh B级患者(28.9% vs 1%)、AFP水平更高患者(AFP>200 ng/mL,56.6% vs 46%)。多项研究[23-25]表明良好的肝功能与HCC患者良好的结局相关。高AFP水平的HCC患者预后欠佳[5,26],故肝功能与HCC患者预后密切相关。肝功能良好的HCC患者可能更能够从仑伐替尼治疗中获益。
本研究中任何水平不良事件的发生率为94.7%(72例),3级及以上不良事件发生率较低,为22.4%(17例),与仑伐替尼真实世界研究数据相似[27]。
本研究存在一定的局限性。研究为回顾性分析,容易产生选择性偏倚,入组病例相对较少,资料不完整;研究中相当部分病例体力状态评分未予以详细记录,故患者基线特征中该指标未作比较,但是临床工作中根据中国临床肿瘤学会《原发性肝癌诊疗指南(2020)》[7]严格用药。尽管本研究有上述局限性,但研究结论仍可为临床医生工作的开展提供重要参考,故具有一定临床价值。
伦理学声明:本研究于2019年7月25日经由首都医科大学附属北京地坛医院伦理委员会审批,批号:京地伦科字(2019)第049-001号。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突。
作者贡献声明:刘晓民参与课题设计,数据获取及分析,撰写论文;孙巍、陈京龙参与课题设计,修改论文;魏建莹、李文东、丁晓燕、于明华参与数据获取及数据分析。
