HPLC-MS/MS测定动物性食品中氟苯尼考及氟苯尼考胺残留量结果的不确定度评定
2022-06-16韩瑨烜
◎ 韩瑨烜,高 鑫,宋 敏,严 娅
(新疆维吾尔自治区产品质量监督检验研究院,新疆 乌鲁木齐 841100)
氟苯尼考(Florfenicol,FF)是氯霉素类的动物专用广谱抗生素,是畜禽养殖业常用的一种抗菌效果极好的药物[1]。氟苯尼考的主要代谢物为氟苯尼考胺(Florfenicol Amine,FFA),因此标准中计算氟苯尼考残留量时通常是计算以上述两种物质的含量之和。目前,液相色谱-串联质谱法是检测氟苯尼考与氟苯尼考胺残留量的常见方法,《食品安全国家标准 动物性食品中氟苯尼考及氟苯尼考胺残留量的测定 液相色谱-串联质谱法》(GB 31658.5—2021)自2022年 2月1日起开始实施,实施后大部分畜禽肉中氟苯尼考的测定均须按照此标准执行[2]。
测量不确定度的评定可以体现检测结果的可靠性,是食品检测中质量控制的重要内容[3-4]。检测和校准实验室能力认可准则(ISO/IEC17025:2005)要求检测和校准实验室必须建立并实施测量不确定度评估程序。本文依据GB 31658.5—2021、《化学分析中不确定度的评估指南》(CNAS—GL06:2019)、《常用玻璃量器检定规程》(JJG 196—2006)等标准[5],对动物性食品中氟苯尼考与氟苯尼考胺残留量测定的不确定度进行评定,旨在为采用新标准检测时的质量评价以及关键点控制提供重要参考。
1 材料与方法
1.1 材料与仪器
样品为实验室内部质控样品。氟苯尼考(99.8%,BePure);氟苯尼考胺(99.2%,BePure);氯霉素-D5(100 µg·mL-1,BePure)。
LC-MS 8045超高效液相色谱-三重四极杆质谱仪(日本岛津公司);Hettich 380R型高速冷冻离心机(德国海蒂诗公司);YP2002百分之一电子天平(上海越平科学仪器有限公司);AUW120d十万分之一分析天平(日本岛津公司);10~1 000 μL可调微量移液器(艾本德中国有限公司);所有玻璃量器均为A级。
1.2 方法
1.2.1 样品制备
按照GB 31658.5—2021中样品制备方法进行。
1.2.2 液相色谱条件
色谱柱:C18色谱柱;柱温:35 ℃;进样量:1 μL;流动相:A/B=0.1%甲酸-水/乙腈;流速:0.2 mL·min-1。
1.2.3 质谱条件
电喷雾(ESI)离子源;正离子(氟苯尼考胺)、负离子(氟苯尼考、氯霉素-D5)扫描模式;多反应监测(Multiple Reaction Monitoring,MRM);喷雾电压:3 000 V;去溶剂温度:500 ℃;气帘气压力: 240 kPa;雾化器压力:350 kPa。其他参数详见表1。

表1 氟苯尼考和氟苯尼考胺主要质谱参数表
2 测量数学模型
2.1 数学模型的建立
以配制的工作溶液浓度(µg·L-1)为横坐标,以工作液峰面积与其内标峰面积之比(响应值)为纵坐标,绘制标准工作曲线。计算公式为:
式中:X为试样中待测组分的含量,µg·kg-1;c为从标准曲线上测得试液中待测组分的质量浓度,µg·L-1;m为试样质量,g;V为试样提取液总体积, mL;f为样品制备过程中的稀释倍数。
2.2 不确定度来源分析
分析测定过程中不确定度来源,见图1。
3 分量计算
3.1 测量重复性引入的相对不确定度ur()
按照样品处理方法,平行称取质控样品6份(n=6),根据公式,计算出单个样品因测量重复性引入的相对不确定度,结果见表2。
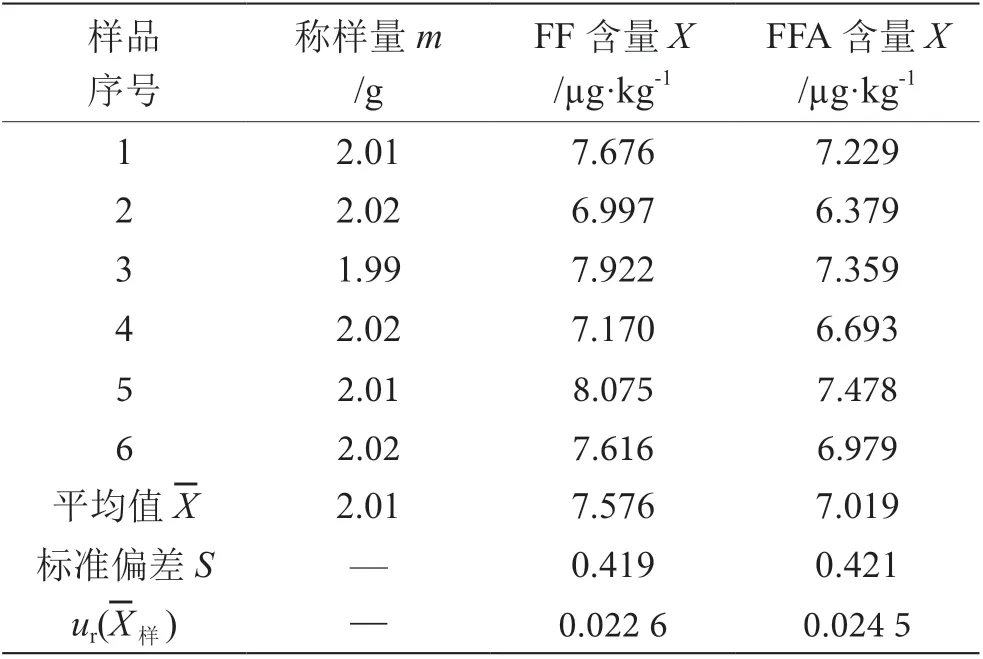
表2 样品重复性测定结果表(n=6)
3.2 样品溶液制备引入的相对不确定度
3.2.1 样品称量引入的相对不确定度ur(W样)
使用精度为0.01 g的天平称取猪肉样品,实际称量待测样品平均质量为m=2.01 g,天平校准证书说明天平最大允许误差M=±0.05 g,假设为均匀分布
3.2.2 样品定容引入的相对不确定度ur(V样)
定容溶剂由可调移液枪吸取500 μL加入,经查《移液器检定规程》(JJG 646—2006)知该移液枪容量允许误差M=±1.0%,假设为均匀分布不考虑温度波动引起的溶剂体积变化,则不确定度,相对不确定度ur(V样)=
3.2.3 内标体积引入的相对不确定度ur(Vis)
内标由可调移液枪吸取100 μL加入,经查《移液器检定规程》(JJG 646—2006)知该移液枪容量允许误差M=±2.0%,假设为均匀分布不考虑温度波动引起的溶剂体积变化,则不确定度,相对不确定度
3.3 混合标准系列溶液配制引入的相对不确定度
3.3.1 标准储备液引入的相对不确定度ur(Cs)
称取FF标准物质0.010 08 g和FFA标准物质 0.010 11 g,分别置于10 mL容量瓶中,乙腈定容至刻度,制成1 mg·mL-1的标准储备液。不确定度主要由标准物质称量u(Ws)、10 mL单标线容量瓶(A级)的容量允许差不确定度u(Cs-容-10mL)及实验室温度波动不确定度u(Cs-温-10mL)引入。
经查万分之一天平检定证书知最大允许误差M=±0.000 05 g,假设为均匀分布,则=0.002 84。
根据《常用玻璃量器检定规程》(JJG 196—2006)知10 mL单标线容量瓶(A级)的容量允许差M=±0.020 mL,假设为均匀分布,则
定容时实验室温度25 ℃,量器校准时温度20 ℃,乙腈的体积膨胀系数为0.001 37 ℃-1,假设为均匀分布,则:
两项合并得:
因此,标准储备液配制引入的相对不确定度ur(Cs-FF)==0.005 00;ur(Cs-FFA)==0.005 00。
3.3.2 内标工作液配制引入的相对不确定度ur(Cis)
用移液器量取1.0 mL氯霉素-D5置于10 mL容量瓶中,用乙腈稀释至刻度并摇匀,制成浓度分别为 10 µg·mL-1的氯霉素-D5内标储备液,再用移液枪从储备液中吸取0.1 mL置于10 mL容量瓶中,制成浓度为0.1 µg·mL-1的氯霉素-D5内标工作液。不确定度主要由移液枪的容量允许误差u(Cis-移)、10 mL单标线容量瓶(A级)的允许差不确定度u(Cis-容)及实验室温度波动不确定度u(Cis-温)引入。
经查《移液器检定规程》(JJG 646—2006)知 1 000 μL移液枪容量允许误差M=±1.0%,假设为均匀分布,则不确定度相对不确定度
已知移液器吸取0.1 mL时相对容量允许差的相对不确定度为0.011 5(3.2.3),10 mL容量瓶定容时相对不确定度为0.004 11(3.3.1),则:
3.3.3 混标中间液配制引入的相对不确定度ur(C混)
使用移液枪分别量取FF、FFA标准储备液0.1 mL,置于同一100 mL容量瓶中,用乙腈定容至刻度并摇匀,制成浓度为1.0 mg·L-1的FF、FFA混合标准中间液。不确定度主要由移液枪的容量允许误差u(C混-移)、100 mL单标线容量瓶(A级)的容量允许差不确定度ur(C混-容-100mL)及实验室温度波动不确定度ur(C混-温-100mL) 引入。
已知移液器吸取0.1 mL时相对容量允许差的相对不确定度为0.011 54(3.2.3)。根据《常用玻璃量器检定规程》(JJG 196—2006)知100 mL单标线容量瓶 (A级)的容量允许差M=±0.10 mL,假设为均匀分布,则定容时实验室温度25 ℃,量器校准时温度20 ℃,乙腈的体积膨胀系数为0.001 37 ℃-1,假设为均匀分布,则=0.395 mL。
两项合并得:
因此,混标中间液配制引入的相对不确定度为:
3.3.4 混合标准系列工作液配制引入的相对不确定度ur(C工)
用移液枪分别量取混合标准中间液20 μL、50 μL定容至100 mL容量瓶中,依次加入氯霉素-D5同位素内标储备液200 μL,再用移液枪分别量取10 μL、20 μL、50 μL、100 μL至10 mL容量瓶中,依次加入氯霉素-D5同位素内标储备液20 μL,均由乙腈定容至刻度,配制成FF、FFA浓度依次为2 µg·L-1、5 µg·L-1、 10 µg·L-1、20 µg·L-1、50 µg·L-1和100 µg·L-1混 合 标准系列工作液,混合标准工作液中含有氯霉素-D5同位素内标浓度为20.0 µg·L-1。不确定度主要由移液枪的容量允许误差u(C工-移)、容量瓶的容量允许差不确定度ur(C工-容)及实验室温度波动不确定度ur(C工-温) 引入。
已知10 mL容量瓶定容时相对不确定度ur(C工-10mL) 为0.004 11(3.3.1),100 mL容量瓶定容时相对不确定度ur(C工-100mL)为0.003 99(3.3.3)。经查《移液器检定规程》(JJG 646—2006)知移液枪各吸液量下容量允许差M,假设为均匀分布,不考虑温度波动引起的溶剂体积变化,各吸液量相对不确定度的计算结果见表3。

表3 ur(Cis)计算结果表
故混合标准系列工作液配制引入的相对不确定度为:
3.3.5 标准曲线拟合引入的相对不确定度ur(C拟)
FF、FFA标准系列工作液每个浓度点平行测定2次,利用工作站绘制标准曲线。标准曲线信息见表4,计算结果见表5。
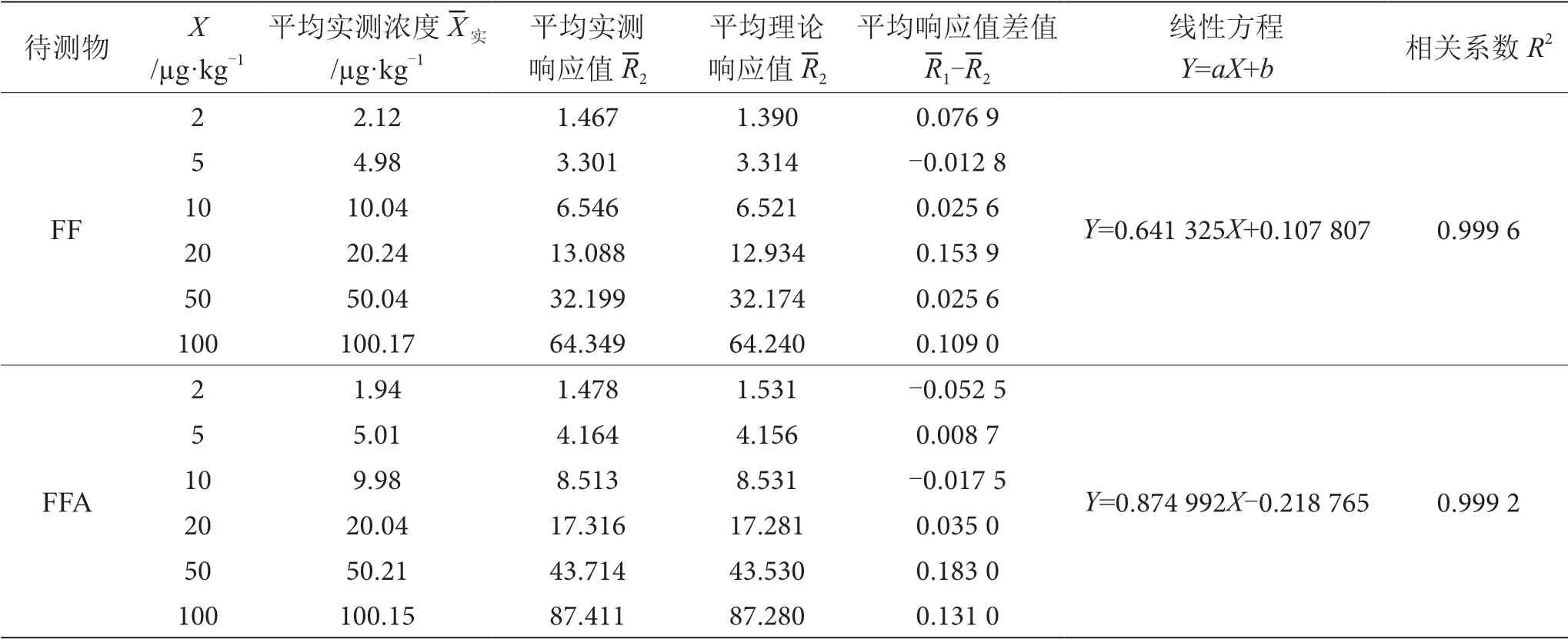
表4 氟苯尼考、氟苯尼考胺线性回归方程及相关系数表
根据公式(2)~(4)计算得到ur(C拟),结果见表5。

表5 ur(C拟)计算结果表
式中:S为标准溶液平均响应值差值的标准偏差;P为样品平行测定的次数,P=6;n为标准溶液测定的总次数,n=12;为样品溶液的平均质量浓度,µg·kg-1;X实为标准溶液的实际质量浓度,µg·kg-1;为标准溶液的平均质量浓度,µg·kg-1;a为工作曲线斜率。
3.3.6 原始标准物质纯度引入的相对不确定度ur(P)
经查询标准物质证书可知,FF的纯度为99.8%,标准不确定度为±1%,k=2,则u(PFF)=0.001/2=0.000 5,ur(PFF)=0.000 5/0.998=0.005 01;FFA的纯度为99.2%,标准不确定度为±2%,k=2,则u(PFFA)=0.002/2=0.001,ur(PFFA)=0.001/0.992=0.002 01。
3.4 仪器分析引入的相对不确定度ur(E)
查询高效液相色谱-质谱联用仪校准证书知,该仪器的测量重复性(RSD)为2%,假设为均匀分布,则仪器分析引入的相对不确定度
3.5 回收率测试随机效应引入的相对不确定度ur(R)
对同一样品分高中低3个浓度合计加标9次(n=9),上机测得FF、FFA的加标回收率,结果见表6。根据公式(5)计算得到9次加标实验的标准偏差S(R),根据公式(6)和(7)计算得到回收率测试过程中引入的相对不确定度ur(R),结果见表6。
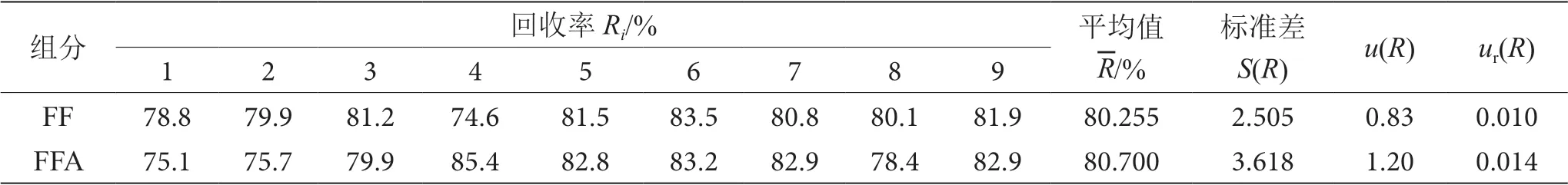
表6 ur(R)计算结果表
用t检验对回收率进行显著性检验,计算公式为取P=0.95,查阅t检验表,t(0.05)=2.57,即当t值大于2.57时,与100%有显著性差异,必须在计算公式中采用以修正结果。计算FF、FFA的t值分别为7.880、5.334,因此计算公式均需要代入回收率。
4 合成标准不确定度
氟苯尼考和氟苯尼考胺的相对不确定度分量见表7。
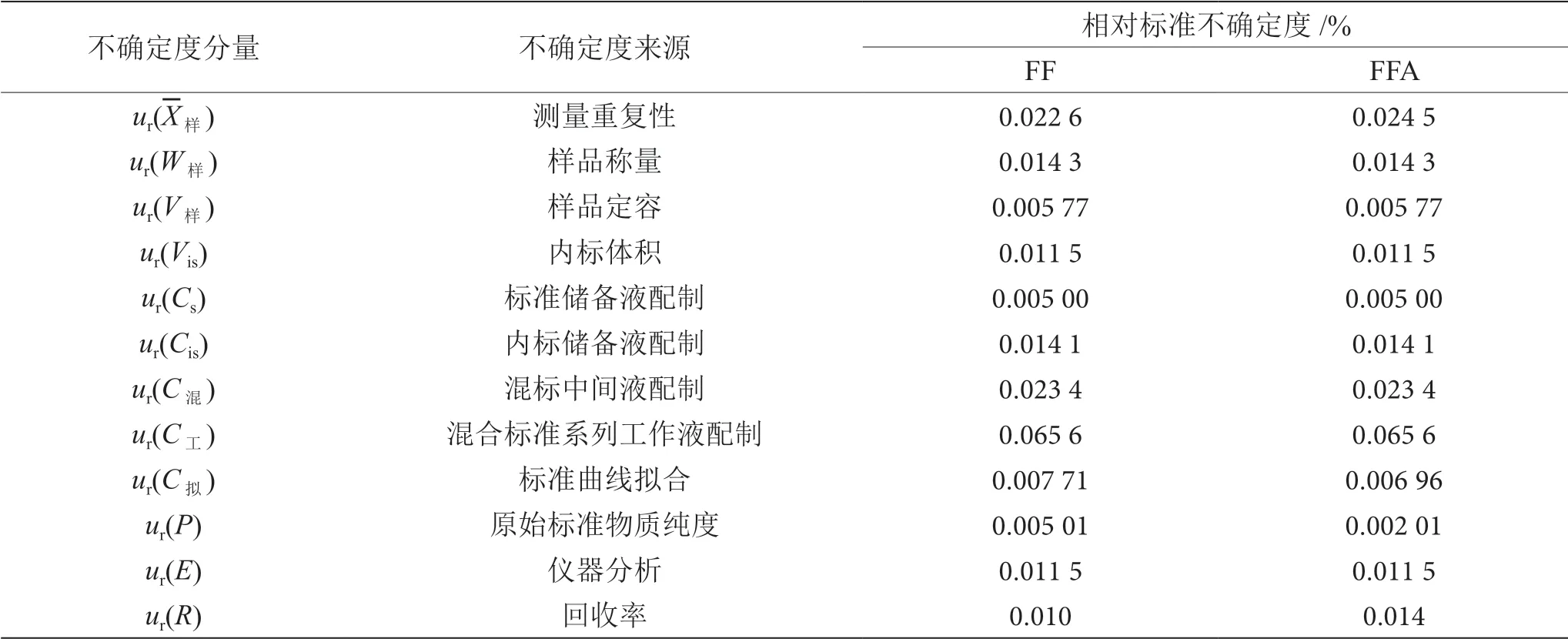
表7 氟苯尼考和氟苯尼考胺相对不确定度分量表
根据表中各不确定度分量,若不考虑不确定的相关性,则FF合成不确定度为:
同理,FFA合成不确定度ur(WFFA)=0.080 2。
5 扩展不确定度及结果表示
根据《化学分析中不确定度的评估指南》(CNAS—GL006:2018),取包含因子k=2时(95%置信度),依据《化学分析测量不确定度评定》(JJF 1135—2005),扩展不确定度UFF=ur(WFF)×2×;UFFA=ur(WFFA)×2×;由此得到动物源性食品中FF、FFA的测定结果,见表8。

表8 猪肉中氟苯尼考和氟苯尼考胺残留量不确定度评定结果表
6 结论
本研究应用《食品安全国家标准 动物性食品中氟苯尼考及氟苯尼考胺残留量的测定 液相色谱-串联质谱法》(GB 31658.5—2021)对猪肉中氟苯尼考与氟苯尼考胺残留量进行测定,并根据数学模型对测定过程中不确定度各分量进行评定[6]。采用该方法,测定结果的不确定度主要来源于混合标准系列工作液的制备、混标中间液的制备、测量重复性3个部分,其中移液枪容量允许差引入的不确定度最显著。因此,在混标梯度工作液的配制过程中应当选择经过检定校准的移液枪,并增加标准溶液的测定次数,尽可能减少因移液枪容量允许差引入的不确定度[18];做好仪器的检定校准工作,使仪器保持足够的精密度与灵敏度;试验应采取双人双样检测,最大程度减少人为因素导致的偶然误差对结果的影响。
