胃癌与慢性萎缩性胃炎的差异基因与中药治疗的生信分析及系统评价
2022-06-15高云霄郭榆西李博林
杨 柳, 李 泽, 高云霄, 郭榆西, 郭 彤, 李博林, 杨 倩, 张 彤
(1.河北中医学院研究生院,河北 石家庄 050011;2.河北中医学院第一附属医院,河北省中医院脾胃病科,河北 石家庄 050090;3.河北医科大学第四医院,河北 石家庄 050035)
慢性萎缩性胃炎(chronic atrophic gastritis,CAG)系指胃黏膜上皮承受反复侵蚀导致固有腺体的减少,伴或不伴肠腺化生和(或)假幽门腺化生的一种慢性胃部疾病[1]。慢性萎缩性胃炎严重影响了患者的生存质量,且在1988年就有研究证实,慢性萎缩性胃炎有向胃癌转变的风险[2]。CAG西医治疗目前缺乏特效药物[3],故寻找慢性萎缩性胃炎与胃癌的差异基因,探索炎癌转化的途径,为特效药物的开发寻找特异性靶点就有着非常重要的意义。近年来,通过分析二代测序平台的基因探针广泛地应用于疾病预后、靶向新药研发等临床研究中。中药治疗萎缩性胃炎具有优势,故而研究萎缩性胃炎向胃癌转化的关键基因、寻找出针对慢性萎缩性胃炎的有效中药,用以指导临床的诊治具有重要意义。本文将分析萎缩性胃炎与胃癌基因探针产生的数据矩阵,研究慢性萎缩性胃炎与胃癌的差异基因和针对靶点的中药,通过系统性评价验证该药的临床疗效,为慢性萎缩性胃炎的中医诊治提供理论依据。
1 资料与方法
1.1 芯片数据的获取 在GEO(geneexpressionomnibus)数据库(https://www.ncbi.nlm.nih.gov/gds)中下载基因芯片数据(GSE116312、GSE55696),2组芯片数据中包含了慢性萎缩性胃炎、胃癌、胃早期癌、滤泡型胃炎等基因表达矩阵,选取其中慢性萎缩性胃炎与胃癌作为研究对象,所有样本均采自病变胃黏膜。
1.2 数据的处理 Bioconductor包是基于R语言开发的用于生物信息学分析的众多工具包的集合,可以快速地进行若干生物信息学相关的分析并将结果可视化。首先对所得数据集进行回归计算,得出其相对标准差(NUSE),并绘制NUSE箱线图,以检验平行试验的一致性。如计算结果具有一致性,说明芯片质量可信,可以进行进一步研究。通过数据的合并、规范基因名称、补充缺失值对数据进行预处理,并应用Lmfit、eBayes函数计算出萎缩性胃炎与胃癌的差异基因,调整P(adj.P)<0.05及|log2FC|≥1为筛选差异基因的标准,其中logFC≤-1说明此类基因在萎缩性胃炎中的表达要低于胃癌中的表达, logFC≥1说明此类基因在萎缩性胃炎中的表达要高于胃癌中的表达。得出结果即为萎缩性胃炎与胃癌的差异表达基因(differentiallyex-pressedgenes,DEGs)。运用gplots包对所得结果可视化。
1.3 慢性萎缩性胃炎与胃癌DEGs的生物富集分析和通路富集分析 将上述所得结果导入DAVID 6.8数据库(https//david.ncifcrf.gov/),设置物种为人类,对慢性萎缩性胃炎的低表达和高表达基因分别进行生物富集分析和通路富集分析。
1.4 慢性萎缩性胃炎与胃癌DEGs蛋白-蛋白相互作用(PPI)网络构建及关键基因分析 将所有差异基因导入STRING数据库(http://string-db.org/),进行蛋白-蛋白相互作用(protein-proteininteraction,PPI)分析,将交互分数大于0.4的基因输入Cytoscape 3.7.2软件绘制蛋白互作图;应用软件中的CytoNCA工具计算蛋白互作图中的节点,得出其在图中的作用度值(Degree)。Degree值越大,说明该节点在网络中承担的生物功能越多,将Dgree值≥2的基因视为慢性萎缩性胃炎向胃癌转变的关键基因。
1.5 治疗慢性萎缩性胃炎中药分析 将基因名输入HERB数据库[4],又称本草组鉴(http://herb.ac.cn/),可得到作用于此基因的中药,将慢性萎缩性胃炎与胃癌的DEGs输入本草组鉴,以P<0.05为标准进行中药筛选[5],将筛选所得的中药进行频次统计,得出频次最高的3味中药。
1.6 中药系统性评价 根据文献的支持程度,再次遴选出1味与该病的治疗最为相关的中药,采用系统评价的方式对以该药为君药的方剂治疗慢性萎缩性胃炎的效果作进一步的验证。
1.6.1 文献检索 在英文数据库及中文数据库中国期刊全文数据库(CNKI)、万方数据库、中文科技期刊全文数据库(VIP)、中国生物医学文献数据库(CMB),检索所有以上中药治疗慢性萎缩性胃炎的文献,选择以该味中药为君药的文献进行系统评价,所有数据库检索时间均为建库至2020年12月。
1.6.2 纳入标准 国内外的盲法与非盲法的随机对照试验,语言仅限于中文与英文。研究对象为慢性萎缩性胃炎,诊断标准参照《中国慢性胃炎共识意见(2017年,上海)》[1],临床表现、内镜及病理检查、实验室检查均提示为慢性萎缩性胃炎,服药方式为口服,不限性别、年龄与病程。试验组给予纯中药汤剂加减口服治疗;对照组给予萎缩性胃炎的常规诊疗手段如吗丁啉、胃复春、质子泵抑制剂等口服治疗。
1.6.3 排除标准 重复文章、经验类、综述类文章、无全文文章及因资料不全无法进行数据提取的文章;试验设计不严谨、动物实验研究。
1.6.4 数据提取与质量评价 由2位研究者分别检索文献,并根据录入排除标准对检索所得文献进行纳排,使用标准资料对纳入文献的数据进行提取,通过第3位研究者对所产生的分歧确定共识意见。运用Jadad量表对纳入临床试验的方法学质量进行评估[6],最低1分,最高5分,1~2分视为低质量研究,3~5分视为高质量研究。采用Rstudio软件的Meta包进行数据分析,分别选取平均差(meandifference,MD)、相对危险度(riskratio,RR)作为连续型变量和二分类变量的疗效分析统计量,以95%CI表示。当P>0.10,I2≤50%时,可认为无异质性,采用固定效应模型分析;当P≤0.10,I2>50时,认为有异质性,使用随机效应模型分析并进行亚组分析或敏感性分析[7]。采用漏斗图进行发表性偏倚的检测,如具有偏倚,运用剪补法检验偏倚的影响性[8];如纳入数据不能进行Meta分析时,则行描述性分析。
2 结果
2.1 数据质量检验 下载慢性萎缩性胃炎和胃癌的基因芯片数据(GSE116312、GSE55696)后,运用R语言的fitPLM函数对数据结果进行回归计算,并绘制GSE116312芯片NUSE箱型图,见图1。经过检验,可以看出基因芯片数据(GSE116312、GSE55696)质量可靠,可进行进一步的研究。
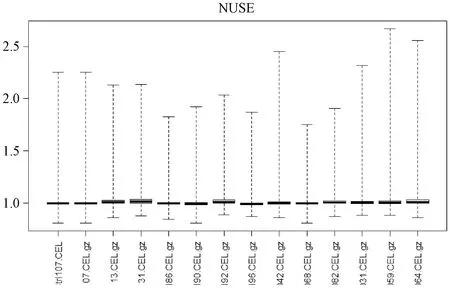
图1 NUSE箱型图
2.2 差异基因 经过初步筛选后发现,GSE116312与GSE55696中共有的慢性萎缩性胃炎与胃癌的差异基因有59个,其中36个基因表达在萎缩性胃炎中低表达,23个基因在慢性萎缩性胃炎中高表达,见图2。
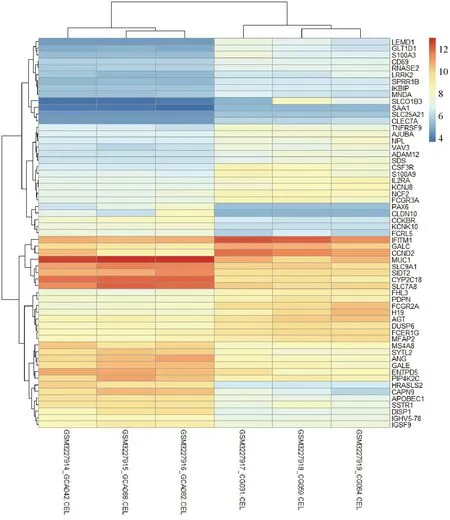
图2 GSE116312热图
2.3 慢性萎缩性胃炎与胃癌DEGs的GO和KEGG分析 运用DAVID数据库分别对低表达基因及高表达基因进行GO和KEGG富集分析,结果显示,下调DEGs的GO分析可见其生物过程(biological process,BP)主要集中在中性粒细胞趋化作用、血小板活化、固有免疫应答、整合素介导的信号通路、MAPK活性的激活、炎症反应的积极调控等方面;细胞组成(cellular component,CC)主要集中在质膜外侧、质膜、胞外区、胞外外体、膜的组成部分等;分子功能(molecular function,MF)主要表现在IgG结合。KEGG富集发现主要集中在吞噬作用、自然杀伤细胞介导的细胞毒性,见表1。上调基因GO分析可见BP主要集中在消化;CC主要集中在膜的组成部分、基底外侧质膜、质膜的组成部分;其KEGG富集在胃酸分泌,见表2。
2.4 PPI网络的构建及关键基因分析 通过Cytoscape软件分析得出PPI蛋白互作图,见图3,得出慢性萎缩性胃炎与胃癌关键的差异基因为免疫球蛋白E高亲和蛋白受体1G(Fc epsilon receptor,FCER1G)、免疫球蛋白G高亲和力受体蛋白2A(Fc gamma receptors 2A,FCGR2A)、免疫球蛋白G高亲和力受体蛋白3A(Fc gamma receptors 3A,FCGR3A)、人髓性细胞核分化抗原(myeloid cell nuclear differentiation antigen,MNDA)、嗜中性粒细胞胞浆因子2(Neutrophil cytoplasmic factor 2,NCF2)钙结合蛋白A9(S100A9)、血管紧张素原(angiotensinogen,AGT)、血清淀粉样蛋白A1(serum amyloid A1,SAA1),生长抑素受体1(somatostatin receptor 1,SSTR1)、VAV家族蛋白3(VAVprotein3,VAV3),见表3。

图3 慢性萎缩性胃炎与胃癌差异基因蛋白互作图

表1 慢性萎缩性胃炎与胃癌的下调差异基因

表2 慢性萎缩性胃炎与胃癌的上调差异基因

表3 慢性萎缩性胃炎与胃癌差异基因中的关键基因
2.5 治疗慢性萎缩性胃炎的相关中药的分析 在本草组鉴(http://herb.ac.cn/)中经过筛选并统计频次,发现与DEGs作用最密切的前3味中药是沙苑子、丹参、甘草,其中丹参具有活血祛瘀、通行血脉的功效,在治疗脘腹疼痛、症瘕积聚等疾病时常以此为主药。久病血瘀是慢性萎缩性胃炎发生发展的重要病机,是胃黏膜萎缩的发生发展乃至恶化的重要因素[9],因而选择中药丹参作为研究目标,采用系统评价的方式作进一步的验证。
2.6 系统评价文献筛选、质量评价及纳入研究的特征 以“丹参”“萎缩性胃炎”“慢性萎缩性胃炎”等关键词在上述数据库中检索,共有相关文献464篇,通过阅读摘要和题目排除重复文献96篇,排除经验类、综述类等不符合研究目的文献330篇,最终对38篇文献进行全文阅读,其中符合丹参为君药的方剂为丹参饮和复方丹参滴丸。丹参饮出自《时方歌括》,陈修园称其“治心痛胃脘诸痛多效”,药物组成精当,药简力专,本方中起主要作用的药物为丹参,因而以丹参饮做系统评价,最后纳入符合纳排条件的文献共7篇[10-16],全部为中文文献,总计640例患者,文献筛选流程及结果见图4。其中5篇文献质量评分为1分[10,12-13,15-16],1篇文献为2分[11],仅有1篇为3分[14],见表4。7个随机对照试验(RCT)的基本特征见表5。
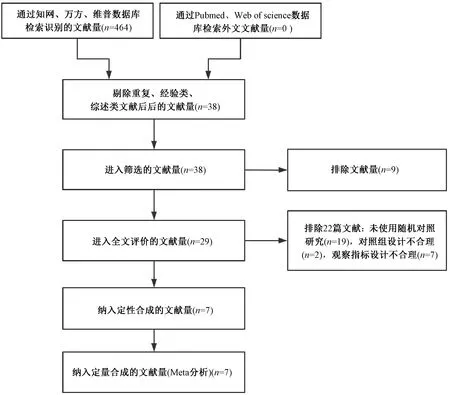
图4 文献筛选流程
2.7 Meta分析
2.7.1 临床总有效率 7个RCT皆对临床总有效指标进行了比较,共有640例患者,其中实验组322例,对照组318例。异质性检验分析显示7个研究之间具备统计学同质性(P=0.39,I2=5%),符合使用固定效应模型的条件。Meta分析结果显示,实验组与对照组临床疗效差异具有统计学意义(P<0.000 01),合并相对危险度(RR)=1.24,95%置信区间为[1.15,1.33]。Meta分析显示可认为丹参饮加减在临床疗效上明显优于对照组,见图5。

表4 纳入文献质量评分
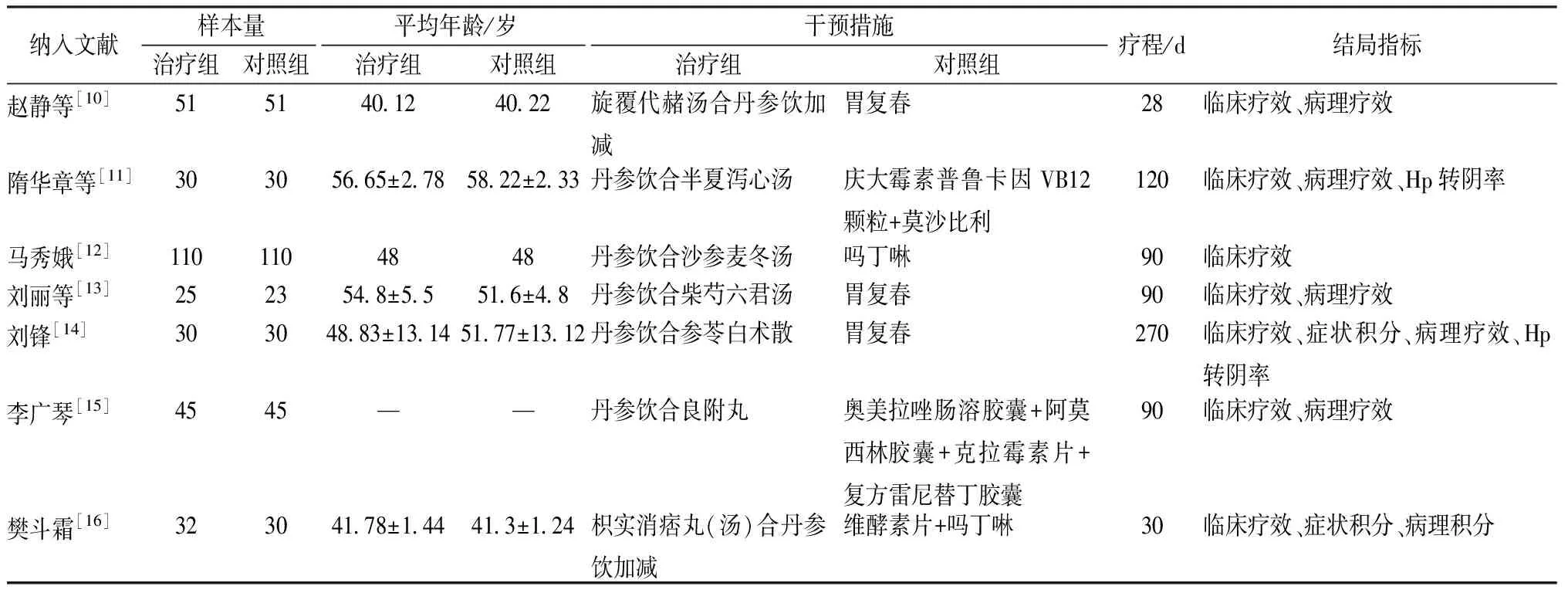
表5 纳入文献的基本特征

图5 临床总有效率Meta分析
2.7.2 病理疗效 5个RCT对病理疗效进行了比较,运用RR、95%置信区间作为效应量的表达方式。统计显示异质性检验显示,P=0.45,I2=0%,说明5个RCT之间异质性较低,故采用固定效应模型进行分析。Meta分析结果显示,实验组与对照组临床疗效差异具有统计学意义(P<0.000 01),合并RR=1.34,95%置信区间为[1.15,1.55]。Meta分析显示可认为丹参饮加减在病理疗效上明显优于对照组,见图6。
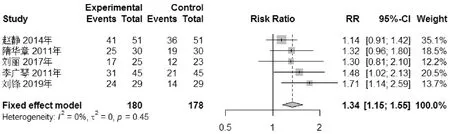
图6 病理总有效率Meta分析
2.7.3 Hp转阴率 2个RCT均对Hp转阴率进行了比较,共有79例患者,其中实验组39例,对照组40例。异质性检验分析显示2个研究之间具备统计学同质性(P=0.35,I2=5%),因此采用固定效应模型进行分析。Meta分析结果显示,实验组与对照组Hp转阴率差异不具有统计学意义(P=0.157 4),见图7。

图7 Hp转阴率Meta分析
2.8 脱落、失访及不良反应 1个RCT报道了脱落和失访情况,但未提及原因;7个RCT均未报道不良反应。
2.9 发表偏倚分析 对临床总有效率为效应指标的研究进行倒漏斗图分析,可见2个数据分布在漏斗图左侧,5个数据分布在漏斗图的右侧,说明纳入的文献存在明显的发表偏倚,见图8。运用剪补法trimfill函数计算缺失值,将缺失值与原有的结果合并,显示异质性仍较低(I2=21.7%,P=0.24),采用固定效应模型,RR=1.24,95%置信区间为[1.11,1.25]。数据变化不明显,说明发表偏倚影响不大,结果真实性好。

图8 偏倚分析
3 讨论
3.1 慢性萎缩性胃炎与胃癌DEGs分析 慢性萎缩性胃炎主要与幽门螺杆菌的感染、胆汁反流、免疫因素有关[17-20]。通过生信分析发现,慢性萎缩性胃炎与胃癌的差异基因有59个,其中36个基因表达下调,23个基因表达上调,关键基因为FCER1G、FCGR2A、FCGR3A、MNDA、NCF2、S100A9、AGT、SAA1、SSTR1、VAV3等。
AGT基因编码的血管紧张素原参与肾素-血管紧张素系统(RAS),可调节和维持人体内环境的相对稳定[21]。Sugimoto等[22]发现幽门螺杆菌会导致RAS成分过度表达,如血管紧张素Ⅱ(AngⅡ)受体。AngⅡ可以诱导VEGF-A的表达,使细胞过度增殖,促使胃黏膜细胞的癌变[23]。血清淀粉样蛋白A(SAA),可由IL-6、TNF-α刺激肝细胞产生[24],SAA受体包括FPRL-1/ALX、SR-BI、RAGE、TANIS等[25-27],SAA与受体结合可发挥调控白细胞迁移、促进炎症等作用[26-28]。FCER与FCGR编码的是免疫球蛋白受体(FcR),免疫球蛋白识别结合抗原后,与先天免疫细胞结合,介导吞噬作用、Ⅰ型超敏反应。故FCER与FCGR与自身免疫性疾病有关,而免疫反应的改变可能使自身免疫性胃炎向胃癌转变[29]。幽门螺杆菌感染可以促进FcR介导的免疫反应,间接导致胃黏膜癌变[30]。SIPR1编码的类固醇受体共激活因子相互作用蛋白受体位于类固醇受体共刺激因子上,可以抑制类固醇受体共刺激因子的活性,阻止类固醇受体进入细胞核,进而起到抑制转录的作用[31]。S100A9编码形成钙卫蛋白[32],钙卫蛋白可通过介导p38细胞分裂素活化蛋白激酶的磷酸化诱导NF-κB的激活,从而促进胃癌细胞的迁移和侵袭[33]。CCND2属于细胞周期素,其含量随细胞有丝分裂的不同时期而变化,可能通过活化周期蛋白依赖激酶调节细胞周期参与细胞的增殖[34],从而导致胃癌的发生。
现有研究成果支持生信分析结果,FCER1G、FCGR2A、FCGR3A、MNDA、NCF2、S100A9、AGT、SAA1、SSTR1、VAV3等基因是慢性萎缩性胃炎向胃癌转化的关键分子。
3.2 慢性萎缩性胃炎与胃癌DEGs富集信号通路分析 自然杀伤细胞(NK)是人体中关键的免疫细胞,它具有抑癌、调节免疫的作用[35]。自然杀伤细胞介导的细胞毒性即NK细胞通过定向释放溶解颗粒或通过诱导相关受体介导的凋亡来杀死癌细胞[36]。在胃炎及胃癌组织中均可见NK细胞表达,但胃癌组NK细胞的表达要高于慢性胃炎组[37],与本文研究结果一致。由于很多治疗癌症的免疫制剂有赖于通过细胞毒性来发挥作用,因此研究此途径的具体机制具有一定的临床意义。
3.3 治疗慢性萎缩性胃炎相关中药分析 慢性萎缩性胃炎后期常有气滞血瘀[38]。通过本草组鉴分析结合专业知识可知以丹参为主药的方剂可作用于慢性萎缩性胃炎的关键基因,故进行丹参饮加减治疗慢性萎缩性胃炎的系统评价,发现丹参饮的临床疗效与病理疗效均高于常规治疗。但也存在诸多问题,①纳入文献的随机方法未作详细报告、均未使用盲法、报告存在偏倚风险; ②缺乏对患者的随访、病例脱落、临床不良反应的报告; ③文献量较少、Jadad评分较低。
综上所述,慢性萎缩性胃炎向胃癌转化过程与FCER1G、FCGR2A、FCGR3A、MNDA、NCF2、S100A9、AGT、SAA1、SSTR1、VAV3等基因及自然杀伤细胞介导的细胞毒性关系密切,中药丹参对治疗慢性萎缩性胃炎临床疗效较好。本研究为疾病的诊断提供了潜在标志物,为临床选药提供了思路。但由于纳入文献数量较少,质量较低,有待今后出现更多高质量循证医学证据后再进行系统评价。
