甘露醇原料药及其制剂中甘露醇的高效液相色谱-电喷雾检测器分析方法*
2022-06-10赵慧王董云吴珺
赵慧,王董云,吴珺
(江苏省泰州市药品检验院,江苏 泰州 225300)
甘露醇(D-甘露糖醇)为良好的脱水利尿药,临床常用于降眼压、降颅内压等,也常用于治疗急性肾功能衰竭的尿闭症。甘露醇也为常用药用辅料,可用作药物制剂的赋形剂,固体、液体的稀释剂,以及冻干粉针剂的载体[1]。2020年版《中国药典(二部)》中采用高效液相色谱(HPLC)法测定其有关物质,但灵敏度低、柱温高、适用性差等;采用容量分析法测定甘露醇含量,操作烦琐,专属性差[2]。目前,甘露醇及其制剂中甘露醇的研究方法主要有HPLC法、离子色谱法、旋光法、紫外-可见分光光度法等[3-5],其中应用较广的是HPLC法,大多采用蒸发光散射检测器(ELSD)或示差检测器(RID)进行测定[6-7]。ELSD大多采用氨基柱,存在柱效下降快、灵敏度低等问题;RID大多采用离子交换柱,存在柱温高、适用性差、基线波动大等问题。电喷雾检测器(CAD)是一种新型通用检测器,具有灵敏度高、重复性好等优势,且检测信号响应不依赖于被测物的化学结构,适用于不挥发性或半挥发性物质的检测,被广泛应用于皂苷类、糖类、生物碱类、脂类化合物等无紫外吸收或弱紫外吸收组分的测定[8]。本研究中采用HPLC-CAD法对甘露醇原料药及其制剂中的甘露醇进行分析,具有简便、快速、灵敏、准确等优势。现报道如下。
1 仪器与试药
1.1 仪器
UltiMate 3000型高效液相色谱仪(美国Thermo Fisher Scientific公司),配有UltiMate 3000型四元泵、UltiMate 3000型自动进样器、Corona Veo RS型电喷雾检测器、ChromeleonTM色谱工作站;KH-400KDE型高功率数控超声波清洗器(昆山禾创超声仪器有限公司,功率为400 W,频率为40 kHz);Mettler XSE205DU型电子天平(瑞士Mettler Toledo公司,精度为十万分之一)。
1.2 试药
甘露醇对照品(中国食品药品检定研究院,批号为100533-201304,含量为99.0%);乙腈(色谱纯,西班牙Scharlau公司);盐酸、氢氧化钠、30%过氧化氢(分析纯,国药集团化学试剂有限公司);试验用水均由Milli-Q纯水系统制备;甘露醇原料药3批;注射用胸腺五肽为胸腺五肽加适量甘露醇经冷冻、干燥制成的无菌冻干品,共3批,拟采用注射用胸腺五肽进行制剂中甘露醇的测定。各样品批号和来源见表1。
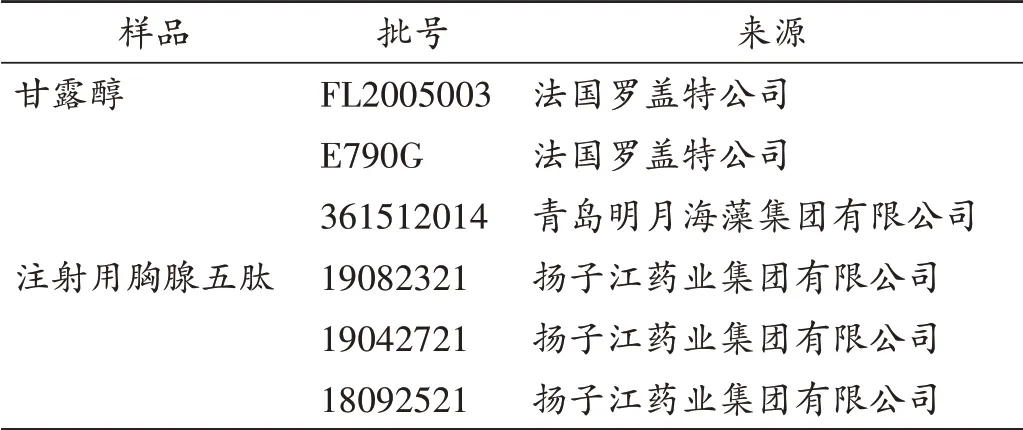
表1 样品批号和来源Tab.1 Batch numbers and sources of samples
2 方法与结果
2.1 色谱条件
色谱柱:Waters XBridge Amide柱(250 mm×4.6 mm,3.5 μm);流动相:乙腈-水(70∶30,V/V);流速:1 mL/min;柱温:35℃;进样量:10 μL;电喷雾检测器参数:雾化温度为55℃,幂率为1.0,采样频率为10 Hz,过滤常数为3.6 s。
2.2 溶液制备
取甘露醇对照品10 mg,精密称定,置100 mL容量瓶中,加水溶解并定容,摇匀,作为对照品溶液。取甘露醇样品10 mg,精密称定,置100 mL容量瓶中,加水溶解并定容,摇匀,作为甘露醇供试品溶液。取注射用胸腺五肽内容物适量,精密称定,加水适量,超声使溶解,用水稀释成每1 mL约含0.1 mg甘露醇的注射用胸腺五肽供试品溶液。取甘露醇样品约50 mg,精密称定,置10 mL容量瓶中,加水溶解并定容,摇匀,作为有关物质测定用供试品溶液;精密量取1 mL,置100 mL容量瓶中,用水稀释并定容,摇匀,作为有关物质测定用对照品溶液。以水作为空白溶液。
2.3 方法学考察
专属性试验:精密吸取空白溶液,2.2项下甘露醇对照品溶液、甘露醇供试品溶液及注射用胸腺五肽供试品溶液各10 μL,分别注入液相色谱仪,按2.1项下色谱条件进样测定,色谱图见图1。结果表明,空白溶剂对主峰无干扰,样品中杂质对测定无干扰,甘露醇色谱峰理论板数大于5 000,拖尾因子小于1.2。
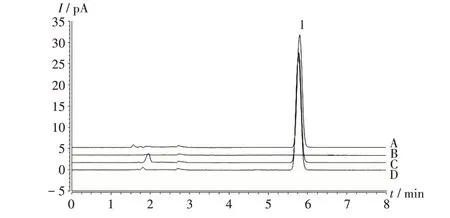
1.甘露醇A.注射用胸腺五肽供试品溶液B.空白溶液C.甘露醇供试品溶液D.甘露醇对照品溶液图1 专属性试验高效液相色谱图1.MannitolA.Test solution of Thymopentin for Injection B.Blank solution C.Test solution of mannitol D.Reference solution of mannitolFig.1 HPLC chromatograms of the specificity test
破坏性试验:取甘露醇对照品10 mg,精密称定,分别置10 mL容量瓶中,加水适量使溶解,分别进行以下破坏性试验。1)碱破坏。加入0.1 mol/mL氢氧化钠溶液1 mL,室温放置4 h,加入0.1 mol/mL盐酸溶液1 mL,用水稀释至刻度,摇匀。2)酸破坏。加入0.1 mol/mL盐酸溶液1 mL,室温放置4 h,加入0.1 mol/mL氢氧化钠溶液1 mL,用水稀释至刻度,摇匀。3)氧化破坏。加入30%过氧化氢溶液1 mL,室温放置4 h,用水稀释至刻度,摇匀。4)高温破坏。水浴加热4 h,放冷至室温,用水稀释至刻度,摇匀。精密量取上述破坏后的试验溶液各10 μL,分别注入液相色谱仪,按2.1项下色谱条件进样测定,色谱图见图2。结果各破坏性试验产生的杂质峰均能与甘露醇主峰达到有效分离,对测定无干扰,表明方法专属性良好。
线性关系考察:取甘露醇对照品20 mg,精密称定,置20 mL容量瓶中,加水溶解并定容,摇匀,作为对照品贮备液;精密量取适量,用水分别稀释成质量浓度为10,20,50,100,200 μg/mL的系列对照品溶液。精密量取上述溶液各10 μL,分别注入液相色谱仪,按2.1项下色谱条件进样测定。以甘露醇的峰面积(Y)为纵坐标、对照品溶液质量浓度(X)为横坐标进行线性回归,得回归方程Y=1.967 5X+25.487 0(r=0.997 8,n=5)。结果表明,甘露醇质量浓度在10~200 μg/mL范围内与峰面积线性关系良好。
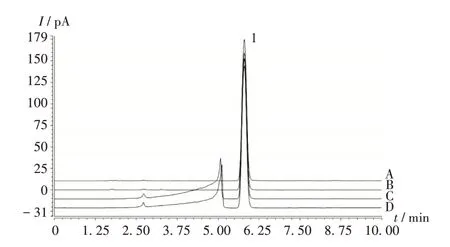
1.甘露醇A.高温破坏B.氧化破坏C.碱破坏D.酸破坏图2 破坏性试验高效液相色谱图1.MannitolA.High-temperature damage B.Oxidative damage C.Alkali damage D.Acid damageFig.2 HPLC chromatograms of damage tests
定量限和检测限确定:取甘露醇对照品适量,精密称定,加水溶解并稀释成系列质量浓度的溶液,并进样测定,以信噪比(S/N)为3时的质量浓度为检测限,以S/N为10时的质量浓度为定量限。结果检测限为0.2 μg/mL,定量限为1.0 μg/mL。
精密度试验:精密吸取质量浓度为0.1 mg/mL的甘露醇对照品溶液适量,按2.1项下色谱条件连续进样测定。结果甘露醇色谱峰保留时间和峰面积的RSD分别为0.07%和0.24%(n=6),表明仪器精密度良好。
重复性试验:取甘露醇原料药(批号为FL2005003)及注射用胸腺五肽(批号为19042721)各6份,按2.2项下方法制备供试品溶液,按2.1项下色谱条件进样测定,记录峰面积,按外标法计算。结果甘露醇及注射用胸腺五肽中甘露醇含量分别为99.21%和0.93 mg/mg,RSD分别为0.34%和0.54%(n=6),表明方法重复性良好。
稳定性试验:取2.2项下甘露醇供试品溶液适量,分别于0,4,8,12 h时按2.1项下色谱条件进样测定,记录色谱图。结果甘露醇色谱峰峰面积的RSD为1.20%(n=4),表明甘露醇供试品溶液在常温下12 h内稳定。
耐用性试验:通过调节流动相比例、流速及柱温,考察甘露醇主峰的拖尾因子及与相邻杂质峰的分离情况。结果甘露醇峰的拖尾因子均小于1.2,杂质对主峰无干扰,表明方法耐用性良好。
加样回收试验:取已知甘露醇含量的注射用胸腺五肽(批号为19042721)9份,精密称定,每组3份,分别按比例精密加入相当于甘露醇含量80%,100%,120%的甘露醇对照品,加水溶解,分别制成高、中、低3个浓度的供试品溶液,平行3次。按2.1项下色谱条件各进样测定,计算加样回收率。结果见表2。
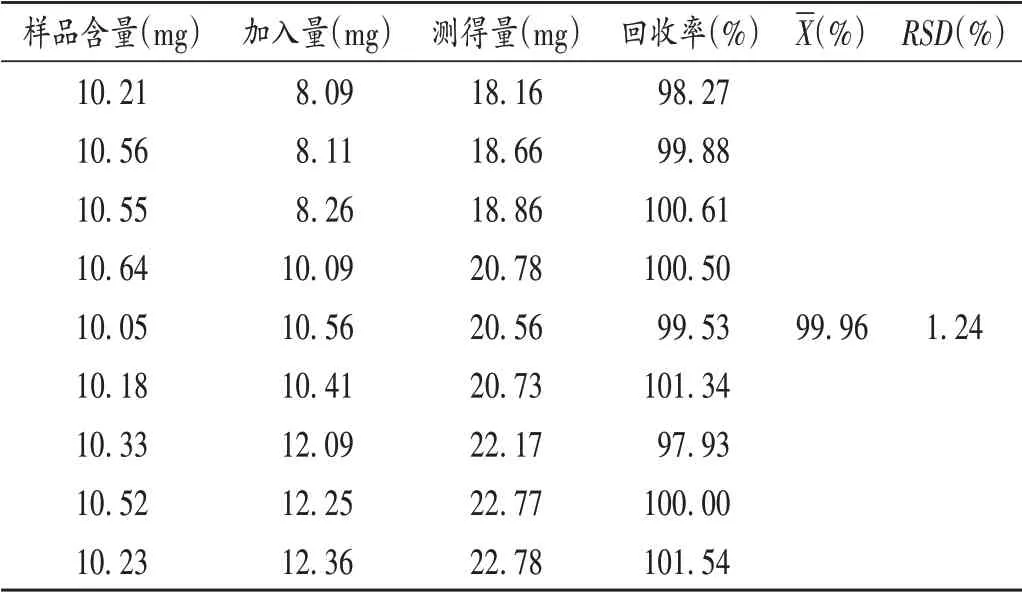
表2 加样回收试验结果(n=9)Tab.2 Results of the recovery test(n=9)
2.4 样品含量测定
分别取甘露醇原料药(批号分别为FL2005003,E790G,361512014),注射用胸腺五肽(批号分别为19082321,19042721,18092521)和甘露醇对照品(批号为100533-201304)各适量,精密称定,按2.2项下方法制备供试品溶液与对照品溶液,平行2份,每份按2.1项下色谱条件进样测定2次,记录峰面积,按外标法计算含量。结果见表3。
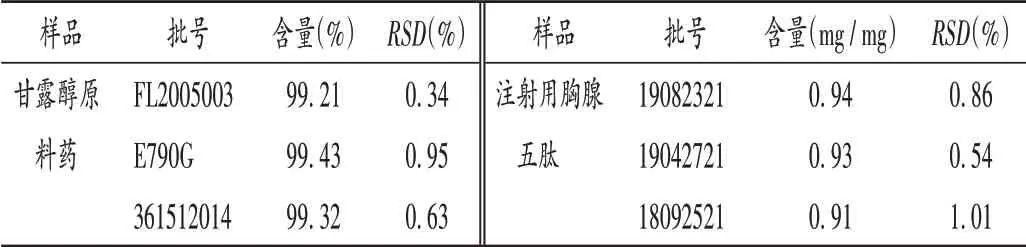
表3 甘露醇含量测定结果(n=4)Tab.3 Results of content determinationin of mannitol(n=4)
2.5 有关物质测定
取甘露醇原料药(批号分别为FL2005003,E970G,361512014)适量,依法制备有关物质测定用供试品溶液和对照品溶液,分别注入液相色谱仪,按2.1项下色谱条件进样测定,记录色谱图至甘露醇主峰保留时间的3倍,按自身对照法计算杂质的含量。结果见表4。
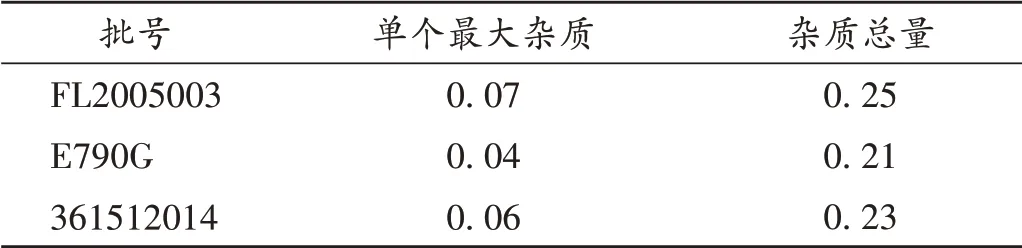
表4 甘露醇原料药中有关物质测定结果(%)Tab.4 Results of determinationin of related substances in mannitol API(%)
3 讨论
3.1 色谱条件选择
常采用氨基柱或强阳离子交换柱对甘露醇进行检测,但氨基柱柱效下降快,强阳离子交换柱使用柱温高、适用性差。本研究中采用XBridge Amide色谱柱,该色谱柱采用了化学稳定、三键键合式的酰胺官能团,为杂化硅胶基质的新型亲水色谱柱,适合分析极性化合物,且稳定性更高,使用寿命更长[9-11]。本研究中分别考察了不同流动相比例对测定结果的影响,结果随着水相比例的增加,甘露醇色谱峰的保留时间不断缩短,理论板数也不断增加。综合考虑分离效果、检测灵敏度及分析时间,最终选择乙腈-水(70∶30,V/V)为流动相。
3.2 CAD参数选择
本研究中分别考察了35℃和55℃两档雾化器温度对检测结果的影响,结果发现,样品检测灵敏度会随着雾化温度的增加而升高,故选择55℃作为雾化器温度。幂率是CAD检测器特有的线性校正参数,不同的化合物具有不同的最优幂率。本研究中分别考察了不同的幂率(0.9,1.0,1.1)对甘露醇线性关系的影响,结果发现,随着幂率的增大,其线性回归的相关系数也不断增大,但甘露醇色谱峰的响应也在不断下降。综合考虑线性关系和响应的影响,幂率最终选定1.0。
3.3 方法评价
本研究中所建立的HPLC-CAD法操作简便、快速、灵敏、准确,可用于甘露醇及其制剂中甘露醇的含量测定及质量控制。
