基于ZIF-8@Ag/MWCNTs的绿原酸电化学传感器的构建及应用
2022-05-30董雷超王红磊陈炫宏南希骏嵇威厉佳怡盛桂华周泉城
董雷超,王红磊,陈炫宏,南希骏,嵇威,厉佳怡,盛桂华,周泉城
(山东理工大学农业工程与食品科学学院,农产品功能化技术山东省高校重点实验室,山东淄博 255049)
绿原酸(CGA)是一种分布广泛,具有显著酚结构的抗氧化物质,是咖啡酸和奎尼酸的结合物[1],分布于各类水果和蔬菜中,尤其是咖啡中富含绿原酸[2]。研究表明,绿原酸具有抗氧化性[3]、抗癌活性[4]、抗炎活性[5]、抗病毒活性[6]等,已被广泛应用于保健、医疗和食品加工等行业[7-9]。由于绿原酸重要的功能特性,近年来对绿原酸的检测分析也越发引起人们的关注。目前对绿原酸的常见检测方法有比色法[10]、高效液相色谱法[11]、联用法[12]、荧光传感器法[13]及电化学分析法[14]等。其中,电化学分析方法操作简便,成本低、准确度高,是一种具有良好前景的检测方法。
金属有机框架材料(MOFs),是一类新型多孔晶体材料,具有众多优势,如大比表面积、高孔隙度、化学稳定性、可调节孔径、结构灵活可调节等[15,16]。基于这些独特的特征,MOF在分离[17]、储气[18]、催化[19]、药物递送[20]、传感器[21]等领域得到了广泛的应用。ZIF-8(沸石咪唑酯骨架-8)是一种由Zn2+和2-甲基咪唑构建的一种MOFs,易于制备,且具有良好的水热稳定性、化学稳定性[22]。ZIF-8也被应用于电化学传感领域,但是由于MOFs的弱导电性,一般将高导电性和催化活性物质引入ZIF-8中,进一步提高改性电极的灵敏度。其中,金属纳米颗粒常用于修饰MOFs,如Au、Ag、Pt等贵金属是常见的修饰用材料,能够使复合材料表现出显著增强的电化学性能,促进电子转移率的增加。
本研究通过ZIF-8与Ag纳米颗粒复合,与羧基化的碳纳米管共同修饰到电化学传感器的工作电极表面,改善其导电性及电催化性能,以获得电化学传感器在检测绿原酸时的灵敏信号。实验结果表明,修饰行为可以有效的提高电化学传感器对绿原酸的检测能力。在优化条件下,可以简单高效的测定绿咖啡豆中的绿原酸含量。
1 材料与方法
1.1 原料
2-甲基咪唑、乙酸锌(纯度≥99%),上海爱纯生物科技有限公司;氧化铝抛光粉,上海辰华仪器有限公司;AgNO3(分析纯),国药集团化学试剂有限公司;MWCNTs(羧基化多壁碳纳米管),江苏先丰纳米材料科技有限公司;壳聚糖,上海爱纯生物科技有限公司;绿原酸(5-CQA),上海源叶生物科技有限公司;其他实验试剂均为分析纯;试验用水为二次蒸馏水;绿咖啡豆购自当地超市。
1.2 主要仪器设备
CHI760E电化学工作站,上海辰华仪器有限公司;玻碳电极,上海辰华仪器有限公司;Ag/AgCl电极,上海辰华仪器有限公司;铂丝电极,上海辰华仪器有限公司;quanta 250场发射扫描电子显微镜,美国FEI,用于查看所制备样品的形态特征,使用配套的X射线能谱仪获得样品的能量色散X射线光谱图;WJGS-009X射线衍射仪,德国BrukerAXS,用于获得粉末X射线衍射图谱;Nicolet 5700傅里叶变化红外光谱仪,美国Thermo Nicolet,用于获得样品的红外光谱图;ASAP 2460比表面积及孔径分析仪,美国Micromeritics,用于获取样品的比表面积。
1.3 实验方法
1.3.1 室温下制备ZIF-8
参考文献[23]制备ZIF-8。准确称量275 mg(1.5 mmol)乙酸锌和985 mg(12 mmol)2-甲基咪唑,分别溶解在90 mL无水乙醇中。在磁力棒搅拌下,将后一种澄清溶液倒入前一种澄清溶液中。合并各组分溶液后搅拌1 h,停止搅拌。静置24 h后,通过离心(4000 r/min)将固体与乳状胶态分散体分离。用无水乙醇洗涤4次后,将产物在60 ℃真空干燥箱中干燥24 h,获得ZIF-8粉末。
1.3.2 制备ZIF-8@Ag
参考文献[24]并做适当调整制备ZIF-8@Ag,取20 mg ZIF-8,超声10 min分散在30 mL乙醇中,滴加0.1 mL AgNO3(5 mg/mL)溶液,继续搅拌6 h。加入1 mL BNaH4(0.076 g/L)碱性水溶液,持续搅拌1 h,将所得乳浊液通过离心(4000 r/min)将沉淀物分离出来,依次用用无水乙醇洗涤4次,将产物在60 ℃真空干燥箱中干燥24 h,获得ZIF-8@Ag粉末。
1.3.3 修饰电极的制备
将裸玻碳电极(GCE)依次用1.0、0.3、0.05 μm的氧化铝粉末精心打磨,并在每种粉末打磨后用无水乙醇和蒸馏水各超声清洗3 min。将打磨好的电极用高纯氮气吹干备用。取0.5 mL 3%壳聚糖溶液加4.5 mL水,溶解5 mg MWCNTs,搅拌后超声10 min,所得溶液用移液器取4 μL用于滴涂电极,获得MWCNTs/GCE电极,在50 ℃烘箱中烘干后备用。取20 mg ZIF-8@Ag粉末用10 mL乙醇溶解,所得乳浊液取1 mL与1 mL 3%壳聚糖溶液混合超声分散后在上述的MWCNTs/GCE修饰电极上滴加2 μL,获得ZIF-8@Ag/MWCNTs/GCE电极,在50 ℃烘箱中烘干后备用。取0.01 g ZIF-8添加到10 mL乙醇中,超声分散10 min后,滴加2 μL到裸玻碳电极,再滴加2 μL 3%的壳聚糖溶液固定,获得ZIF-8/GCE电极,在50 ℃烘箱中烘干后备用,ZIF-8@Ag处理方式同ZIF-8。
1.3.4 电化学测试
电化学测试均在电化学工作站CHI760E上完成,采用三电极系统:工作电极为GCE或修饰GCE,参比电极为Ag/AgCl电极,对电极为铂丝电极。PBS缓冲液由0.1 mol/L的NaH2PO4和0.1 mol/L的Na2HPO4配制而成,调整比例获得不同pH的缓冲液,加入0.1 mol/L的KCl为支持电解质。通过将0.3540 g的绿原酸溶解在100 mL的无水乙醇中来制备0.01 mol/L的绿原酸储备液。工作标准溶液是通过用所需pH的PBS缓冲液逐步稀释绿原酸储备液到相应浓度而获得的,绿原酸储备液配置后放4 ℃冰箱储存备用。所有测量均在室温下进行。
1.3.5 样品处理
将购买的绿咖啡豆样品使用多功能粉碎机粉碎5 min,将其打磨成粉末状。精确称取1 g粉末,将其分散在50 mL的水/乙醇混合液(体积比50:50)中,将样品混合液置于超声浴中5 min,然后在水浴(70 ℃)中萃取20 min,然后通过滤纸过滤,在环境温度下冷却,然后通过0.45 μm PTFE过滤器过滤以除去所有沉淀物。在即将测量之前,将提取液用PBS缓冲液(pH=6)稀释50倍。向10 mL的样品稀释液中依次添加绿原酸标准品溶液,以计算加标回收率。
1.4 数据统计分析
本文中设计的数据统计分析和绘图均采用Origin 2018软件完成。
2 结果与讨论
2.1 修饰材料的表征
图1给出了ZIF-8和ZIF-8@Ag的傅里叶变换红外光谱图。右侧的421 cm-1处的峰可以归因于Zn-N的伸缩振动,而出现在1586 cm-1处的峰则对应于C=N伸缩振动,1422或1458 cm-1处的峰值与环的伸缩振动有关,2930 cm-1处的峰对应环外甲基饱和C-H的伸缩振动,3134 cm-1处的峰对应环内不饱和C-H的伸缩振动,与文献[25]一致。并且,光谱图中ZIF-8@Ag各峰基本与ZIF-8各峰一致,表明ZIF-8@Ag的制备不会破坏ZIF-8的表面基团。
为了进一步探究形成ZIF-8@Ag复合物后,ZIF-8的结构是否被破坏,测定了ZIF-8及ZIF-8@Ag复合物的特征晶体衍射峰,如图2所示,观察到大约在7.5 °、10.5 °、12.5 °和18 °处的几处主衍射峰,分别对应ZIF-8的(110)、(200)、(211)和(222)晶面,与文献基本一致[26]。这些特征衍射峰说明成功获得了ZIF-8晶体,并且ZIF-8具有良好的晶型。所得ZIF-8@Ag复合物的特征晶体衍射峰与ZIF-8的X射线衍射图谱基本一致,各峰没有明显变化。这表明ZIF-8在形成ZIF-8@Ag复合物的过程中仍然保持本身的形态结构,与上述红外光谱表征所得的结果相吻合。
通过氮气吸脱附实验测定修饰前后ZIF-8@Ag的比表面积变化,测定结果为ZIF-8的BET比表面积为1365.44 m²/g,ZIF-8@Ag的BET比表面积为1290.73 m²/g,ZIF-8@Ag复合材料的比表面积接近于纯ZIF-8。这表明Ag纳米粒子在ZIF-8表面成功修饰,且ZIF-8@Ag保持了纯ZIF-8的高比表面积的优良特性。
利用扫描电镜对所制备的ZIF-8及ZIF-8@Ag进行表征,由图3a,b可见,ZIF-8为较为规整的菱形十二面体,粒径为250 nm左右,具有较窄的粒径分布范围。在ZIF-8表面使用BNaH4原位还原Ag+制备ZIF-8@Ag,所得产物如图3c所示,ZIF-8主体结构形态保持稳定,而Ag纳米颗粒较为均匀的分散在ZIF-8表面,图3d为能量色散x射线光谱图中Ag的元素分布,进一步证明Ag纳米颗粒较为均匀的分散在各ZIF-8表面。
如图4a所示,一定粒径范围内的Ag纳米颗粒相对均匀的分布在ZIF-8表面,由图4b可得,所示纳米颗粒的晶格间距为0.236 nm,与Ag(111)的晶格间距很好地吻合,对应所获得的银纳米颗粒。
2.2 修饰材料的电化学表征
以K3[Fe(CN)6]/K4[Fe(CN)6]体系为探针,分别将裸玻碳电极及修饰电极置于 5×10-3mol/L K3[Fe(CN)6]/K4[Fe(CN)6]和0.1 mol/L KCl的混合溶液中测试了不同修饰电极的循环伏安行为(CV)和电化学阻抗(EIS)。如图5所示,在GCE上观察到一对可逆且明确的氧化还原峰,峰电位差(ΔEp)为80 mV左右。修饰ZIF-8后,因为ZIF-8本身的弱导电性,电流信号相对于裸电极变化不大,而GCE修饰ZIF-8@Ag后电信号有一定增强。另一方面,在羧基化多壁碳纳米管的存在下修饰电极获得了较高的峰值电流,因为与裸玻碳电极相比,羧基化多壁碳纳米管的高电导率支持快速的电子转移。ZIF-8@Ag/ MWCNTs/GCE的CV响应呈现最高电流信号,可能是因为Ag纳米粒子在具有高比表面积的ZIF-8表面均匀分布,Ag纳米粒子的优良导电性配合羧基化多壁碳纳米管的高电导率,协同提高了复合材料的电子转移速率。循环伏安测试实验结果表明ZIF-8@Ag/ MWCNTs修饰电极具有良好的导电性,有可能实现更灵敏的检测。
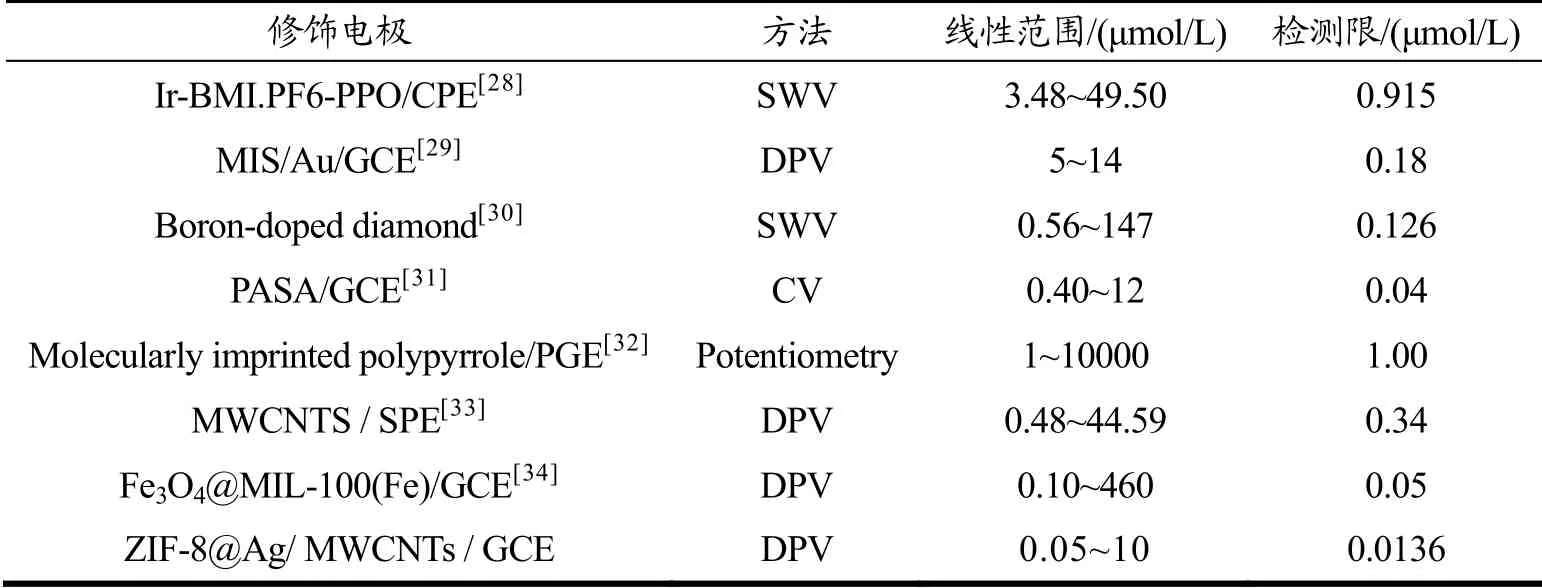
如图6所示,测试了裸GCE电极、ZIF-8/GCE电极、MWCNTs/GCE电极、ZIF-8@Ag/MWCNTs/GCE电极的电阻抗行为。电化学阻抗谱的奈奎斯特图包括在高频观察到的半圆形部分和在低频观察到的线性部分,分别对应于电子转移和物质转移过程,半圆形的直径对应于转移电阻(Rct),在图6的插图中展示了相应的等效电路模型。裸玻碳电极的阻抗值估计为181.4 Ω,修饰了ZIF-8的玻碳电极的抗值估计为446.3 Ω,阻抗值相较于裸玻碳电极明显增大,表明ZIF-8的不良电导率阻碍了电子的转移,ZIF-8@Ag/GCE抗值估计为289.1 Ω,阻抗值GCE 在含5×10-3mol/L K3[Fe(CN)6]/K4[Fe(CN)6]体系、0.1 mol/L的KCl的电解液中使用CV测试裸GCE、ZIF-8/GCE、ZIF-8@Ag/GCE、MWCNTs/GCE和ZIF-8@Ag/MWCNTs/GCE,并据此计算各电极的电活性面积。准可逆反应的电极活性面积采用Randles-Sevcik方程[27]计算,如下所示: 式中: n——参与氧化还原反应的电子数,n=1; A——电极电活性表面积,cm2; D——铁氰化物的扩散系数,cm2/s; C——铁氰化物在本体溶液中的浓度,mol/cm3; v——扫描速,V/s。 计算出的裸GCE、ZIF-8/GCE、MWCNTs/GCE、ZIF-8@Ag/GCE和ZIF-8@Ag/MWCNTs/GCE电活性面积分别估计为0.06、0.08、0.10、0.22、0.36 cm2。上述电化学表征结果表明,ZIF-8@Ag/MWCNTs复合材料可以扩大电活性表面积,加速分析物和电极之间的电子转移,从而ZIF-8@Ag/MWCNTs/GCE可用于绿原酸的灵敏测定。 为测试电极修饰对绿原酸检测的影响,分别用GCE和ZIF-8@Ag/MWCNTs/GCE对1×10-5mol/L浓度的绿原酸缓冲液(pH=7)进行CV扫描,发现相对于裸电极,ZIF-8@Ag/MWCNTs/GCE的CV曲线中电流信号显著增强,修饰的碳纳米管和ZIF-8@Ag使得电极具有较大的活性表面作用于绿原酸的氧化还原过程,复合材料对于这一过程具有良好的电催化作用,最终促使电流响应增强。 2.3.1 pH的影响 在图8中给出了不同pH条件(pH=5.0、6.0、7.0、8.0、9.0)对1.00×10-3mol/L绿原酸在ZIF-8@Ag/ MWCNTs/GCE上CV扫描的影响。可以发现绿原酸的峰电位随溶液pH的变化而变化,随pH增大电位逐渐左移。各pH条件下的CV结果表明在缓冲液pH为6.0时,ZIF-8@Ag/MWCNTs/ GCE测定绿原酸时有最高的峰电流信号,因此在后续的测试中也使用pH为6.0的PBS缓冲液进行测试。 2.3.2 扫描速率的影响 研究了ZIF-8@Ag/MWCNTs/GCE在不同扫描速率(0.01、0.02、0.03、0.04、0.05、0.03、0.07、0.08、0.09、0.10 V/s)下对1.00×10-4mol/L绿原酸CV扫描的影响。如图9a所示,阳极峰值电流随着扫描速率从0.01到0.10 V/s的增加而增加。同时,氧化峰电流(Ipa)与扫描速率的平方根(v1/2)呈良好线性关系。线性回归方程可表示为: 表明绿原酸在ZIF-8@Ag/MWCNTs/GCE上的电化学过程是受扩散控制的过程。 差分脉冲伏安法(DPV)用于测定ZIF-8@Ag/MWCNTs/GCE检测绿原酸的线性范围和检出限(LOD)。ZIF-8@Ag/MWCNTs/GCE修饰电极测定不同浓度绿原酸的DPV曲线在图10a中给出,峰电流强度与CGA的浓度在以下范围内呈线性关系:5×10-8~1×10-5mol/L。线性关系式为: 根据3Sb/S计算检出限(LOD),其中Sb是空白测量的标准偏差(n=11),S是校准图的斜率。发现LOD为1.36×10-8mol/L。本研究中获得的LOD表明,设计的ZIF-8@Ag/MWCNTs/GCE对CGA的测定比较敏感,检测限较低。将本研究方法与其他先前报道的绿原酸电化学传感器方法进行比较,如表1所示。显然,本研究方法具有较宽的检测范围及较低的检测限,表明ZIF-8@Ag/MWCNTs/GCE可以作为灵敏的绿原酸电化学传感器使用。 表1 不同绿原酸电化学传感器的比较Table 1 Comparison of different chlorogenic acid electrochemical sensors 以氧化峰信号强度的±5%范围为允许相对误差,DPV测试结果表明100倍浓度的Na+、Cl-、K+、NO3-、SO42-、Ca2+、肌酸、腺嘌呤、蔗糖、果糖、葡萄糖对200 μmol/L绿原酸的测定几乎没有影响,如图11所示。因此,可以认为该方法具有较好的抗干扰性,可以在实际样品中进一步应用于绿原酸的检测。 为了验证重复性,在制备好ZIF-8@Ag/MWCNTs/ GCE修饰电极后,在含5 μmol/L绿原酸PBS缓冲液中用同一电极连续测试9次DPV,峰值电流的相对标准偏差(RSD%)为2.04%,这一结果表明制备的修饰电极在测定一定浓度的绿原酸时具有良好的重复性,如图12a所示。为了评估再现性,同时用同一流程制备的5根修饰电极进行测试,在含5 μmol/L绿原酸PBS缓冲液中通过DPV测量峰值电流的相对标准偏差(RSD)为4.25%,证明所提出的传感器具有良好的再现性,如图12b所示。 通过标准添加方法进行回收率实验,以绿原酸标准品(5-CQA)的校准曲线作为定量标准,每个浓度水平测试三次。如表2所示,该传感器具有96.34%至103.34%的较优回收率,这表明这项工作中的绿原酸电化学传感器可以应用于实际含绿原酸样品的分析。 表2 真实样品中的绿原酸的测定Table 2 Determination of the chlorogenic acid in real samples 本研究在常温下制备ZIF-8颗粒,并以银纳米粒子修饰,将ZIF-8@Ag与羧基化多壁碳纳米管结合共同修饰玻碳电极,构建了一种新型的用于绿原酸检测的电化学传感器。ZIF-8颗粒具有的大比表面积负载 了均匀分布的银纳米颗粒,使用的多壁碳纳米管则进一步促进了电子转移速率。在最佳实验条件下,该传感器检测绿原酸在5×10-8~1×10-5mol/L范围内表现出良好的线性关系,检出限为1.36×10-8mol/L。此外,该传感器成功地用于实际样品绿咖啡豆中绿原酸的检测。2.3 实验条件的优化
2.4 线性范围及检出限
2.5 修饰电极的抗干扰性、重复性、再现性
2.6 实际样品的检测

3 结论
