时间-空间关联成像联合高分辨率血流显像在胎儿先天性血管环诊断中的应用价值
2022-05-30姚立国李天刚王艺璇彭梅娟
马 斌 姚立国 冉 婕 李天刚 王艺璇 彭梅娟
先天性血管环是指胚胎期的6 对弓动脉血管退化异常,形成包绕气管、食管的环形结构[1],产后少部分血管环会压迫新生儿气管、食管,形成不同程度的呼吸、吞咽等临床症状。产前超声可通过判断主动脉弓、动脉导管与气管的位置关系对其诊断[2]。随着时间-空间关联成像技术(spatio-temporal image correlation,STIC)的快速发展,应用其高分辨率血流显像(high definition flow imaging,HDF)模式对胎儿心脏及大血管进行三维立体重建,可动态显示主动脉弓分支及其与动脉导管、气管的位置关系。本研究旨在探讨HDF-STIC技术对胎儿先天性血管环的产前诊断价值。
资料与方法
一、临床资料
选取2017 年1 月至2020 年5 月在我院经超声心动图初诊的先天性血管环胎儿 89 例,孕妇年龄 19~37 岁,平均(29.32±4.26)岁;超声检查时间孕21~30周,平均孕(24.23±3.14)周。本研究经我院医学伦理委员会批准,所有孕妇或其家属均知情同意。
二、仪器与方法
1.HDF-STIC 检查:使用GE Voluson E 10 彩色多普勒超声诊断仪,RM6C探头,频率2.0~5.0 MHz;配有STIC软件包。首先行产科超声常规检查,参照胎儿心脏超声检查规范性专家共识[3]对常规超声初步诊断为血管环的图像进行HDF-STIC 容积数据采集:以三血管气管切面为初始采集切面,选择四维检查STIC模式,容积扫描角度为20°~40°,正交三平面模式下根据需要旋转X、Y、Z 轴线,以清晰显像主动脉弓、动脉导管及分支血流,启动HDF模式以获得动态血流重建图。按照血管环对气管的包绕程度,将血管环分为完全性和不完全性血管环,完全性包括“U”形和“O”形血管环,不完全性主要为“C”形血管环[1]。
2.随访:对选择引产终止妊娠者,行尸解以明确诊断;对选择继续妊娠者,建议于产后行新生儿超声心动图复查,重点观察主动脉弓位置、分支、走行及血流等;对新生儿气管受压产生临床症状者,行CT 血管三维重建;并与产前HDF-STIC 诊断结果进行对照分析。
结 果
一、胎儿血管环HDF-STIC特征
89 例先天性血管环胎儿中,完全性血管环58 例,不完全性血管环31例;其中77例获得动态三维重建图像容积数据,12例未能取得完整容积数据。二维超声及彩色多普勒超声对主动脉弓及动脉导管弓相对气管位置异常均能显示,显示率为100%,主动脉弓分支显示68 例,显示率为76.4%;HDF-STIC 对主动脉弓及动脉导管弓相对气管位置异常均能显示,显示率为100%,主动脉弓分支显示75 例,显示率为84.3%。形成“U”形血管环的类型包括:右位主动脉弓(RAA)+迷走左锁骨下动脉(ALSA)+左位动脉导管(LDA)36 例、镜像右位主动脉弓(MRAA)+左位动脉导管(LDA,导管连接降主动脉)14 例、左位主动脉弓(LAA)+迷走右锁骨下动脉(ARSA)+右位动脉导管(RDA)1例;形成“O”形血管环的类型包括:双主动脉弓(DAA)+LDA 5 例、RAA+ALSA+DDA 1 例;形成“C”形血管环的类型包括:左位主动脉弓(LAA)+ARSA+LDA 29 例、RAA+ALSA+RDA 2例、肺动脉吊带(PAS)1例。见表1和图1。
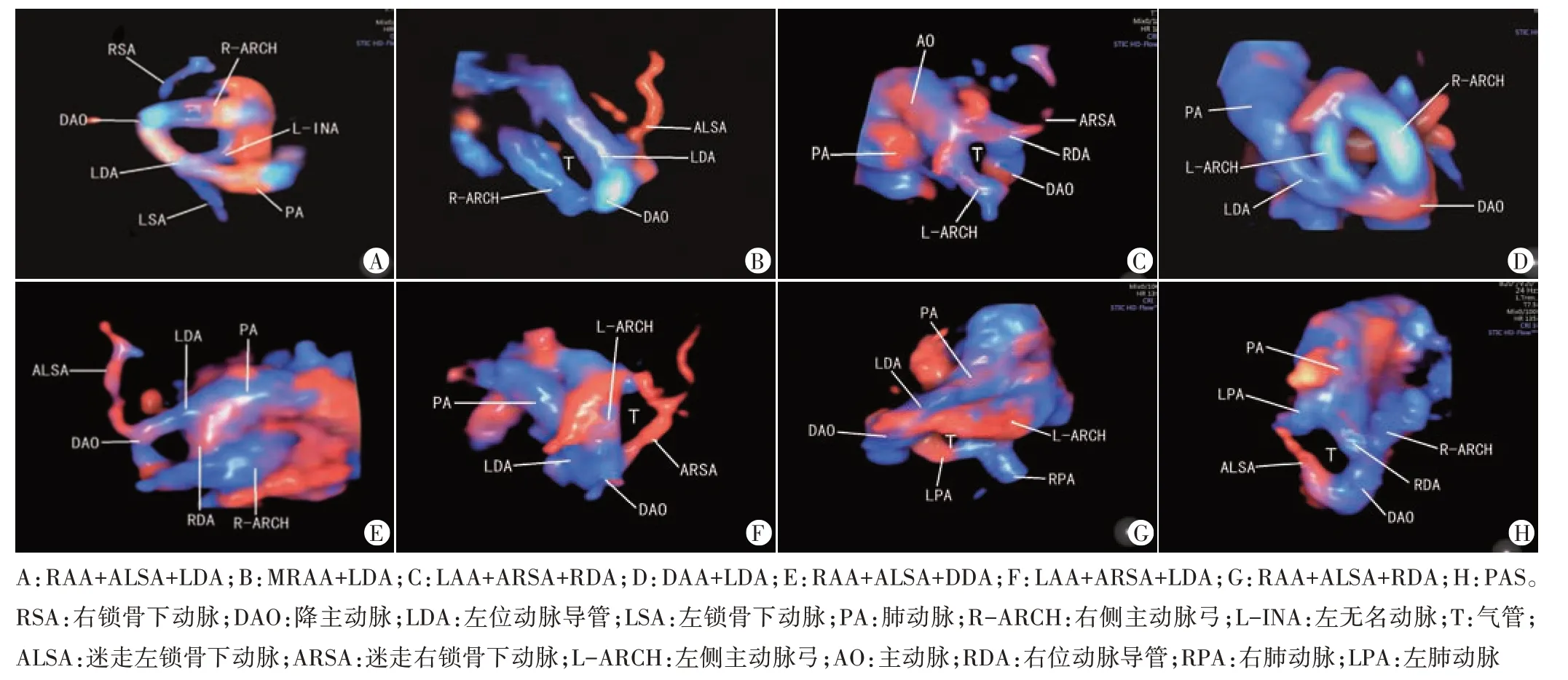
图1 产前超声诊断胎儿不同血管环HDF-STIC图
二、89例先天性血管环具体分型及合并畸形情况
89 例先天性血管环具体分型及合并心内畸形见表1,其中,单纯血管环66 例,合并心内畸形23 例;合并心外畸形11 例,包括无脾综合征2 例、单脐动脉3 例、唇腭裂2 例、肾积水2 例、多囊性发育不良肾和半椎体各1 例。其中行染色体核型及全基因组拷贝数变异分析者36例,包括4例21-三体(血管环合并结构畸形3 例、单纯血管环1 例),2 例22q11 微缺失(单纯血管环、血管环合并结构畸形各1例)。

表1 89例先天性血管环类型及合并心内畸形情况
三、结局及随访情况
66 例单纯先天性血管环胎儿中,仅1 例选择引产;23 例合并其他畸形胎儿中,13 例因合并严重畸形选择引产,包括合并心内膜垫缺损、法洛四联症各3 例,合并右室双出口、右房异构综合征、室间隔缺损各2例,肺动脉狭窄1例。共75例胎儿选择继续妊娠,出生后经超声心动图和(或)CTA 检查证实,1 例MRAA 产前超声误诊为DAA,余74 例产前HDF-STIC 检查结果与之一致,产前诊断准确率为98.7%。见图2。

图2 产后CTA图
讨 论
先天性血管环是一组胚胎期6对弓动脉发育异常引起的先天性结构异常,胚胎早期主动脉囊发出的6 对弓动脉,其中第1、2、5 对弓动脉退化,第3、4、6 对弓动脉继续发育,分别形成主动脉弓及分支、肺动脉、动脉导管[4]。Edward 早在1948 年提出双主动脉弓、双动脉导管的发育模型[4],双侧主动脉弓、双侧动脉导管退化吸收的位置差异,导致各种不同类型血管环的形成。血管环对气管及食管的压迫程度不同,预后也不同,部分血管环产后会造成新生儿出现不同程度呼吸困难、反复肺部感染、吞咽困难等症状,因此产前准确诊断具有重要意义。产前超声对于血管环的评价和描述主要包括:①主动脉弓与气管的相互位置关系;②降主动脉上段相对于脊柱的位置关系;③气管后方是否存在迷走动脉血管;④动脉导管与气管的位置关系及连接位置。既往对以上指标的判断主要依靠二维及彩色多普勒超声,观察切面主要是三血管气管切面,但是对主动脉弓分支的显示欠佳,分型不准确;Bravo 等[5]建议在三血管气管切面的基础上增加锁骨下动脉切面,李文秀等[6]建议增加降主动脉冠状切面,可以更好地显示主动脉弓的数目、分支。但锁骨下动脉切面和降主动脉冠状切面均易受胎儿体位及操作者技术影响,显示较为困难。HDF-STIC 技术是一种四维立体渲染成像模式[4],可同时结合多种成像模式,如彩色多普勒、能量多普勒、玻璃体成像等,从不同角度观察血管环的结构,可更立体、直观地评价先天性血管环的空间位置关系,减少胎儿体位对成像质量的影响[7]。本研究二维联合彩色多普勒超声与HDF-STIC对主动脉弓及动脉导管弓位置的显示准确率均为100%,但对主动脉弓分支的显示,HDF-STIC 的显示率明显高于二维联合彩色多普勒超声(84.3%vs.76.4%),与Wang等[8]研究结果一致。
HDF-STIC 技术以三血管气管切面为初始采集切面,容积扫描角度为20°~40°,向上可以对主动脉弓上分支直观立体呈现,向下则可以对主动脉弓及动脉导管与降主动脉关系,实现对血管环的准确分型。Ito等[9]认为HDF-STIC可提供二维及彩色多普勒超声以外的诊断信息,提高对血管环的诊断准确率;Ma等[10]研究表明,HDF-STIC 技术可对部分罕见血管环可以进行准确诊断。本研究89 例先天性血管环胎儿经HDF-STIC 技术发现,不完全性血管环31 例,主要为“C”形血管环;完全性血管环58 例,主要包括“U”形和“O”形血管环。77 例胎儿均获得满意的血管重建图,对不同血管环进行了准确分型,1例MRAA产前二维超声及HDF-STIC 均误诊为DAA,可能与RAA 发出的左无名动脉与LDA 相邻走行,难以区分是否合并LAA,应在主动脉弓处仔细观察有无主动脉弓左侧分支与降主动脉相连。其余诊断均与产后CTA 诊断结果相符合,证实在二维超声基础上结合HDF-STIC技术产生的三维渲染重建图像可使超声医师更好地理解大血管的空间走行及位置关系,有助于增强超声医师的诊断信心,进一步提高胎儿血管环的产前检出率。
本研究检出的89 例先天性血管环中最常见的血管环类型是RAA+ALSA+LDA,其次是LAA+ARSA+LDA、MRAA+LDA,与徐鹏等[11]研究认为RAA 相关血管环最常见研究结论一致。本研究中 DAA、RDA 及 PAS 相关的血管环少见,而文献[4]报道产后新生儿DAA及PAS发病率较高,可能与产后其他血管环对气管、食管未压迫或临床症状轻,而未进行有针对性的超声心动图检查有关。本研究发现血管环合并心内畸形中最多见的是室间隔缺损,其次是法洛四联症、右房异构综合征及心内膜垫缺损;合并心外畸形主要为无脾综合征、唇腭裂等,其中RAA合并的畸形种类较多,而复杂、少见的血管环中大部分(8/10)为单纯血管环。本研究中仅36例行染色体检查,其中染色体异常者6 例,主要包括21-三体及22q11 微缺失,提示临床发现胎儿血管环时可进一步行染色体微阵列分析排除染色体异常。
综上所述,在二维及彩色多普勒超声的基础上,应用HDFSTIC技术可直观、立体地显示主动脉弓动脉导管与气管的位置关系及主动脉弓分支走行,有助于提高先天性血管环胎儿诊断准确率,并对其进行准确分型,为胎儿先天性血管环的早期诊断及治疗提供参考。
