卵巢-附件报告和数据系统与恶性风险指数鉴别卵巢肿瘤良恶性的对比研究
2022-05-30王荣玲房世保孙咏梅刘岳航唐婉晴杨宗利
王荣玲 房世保 孙咏梅 刘岳航 唐婉晴 杨宗利
卵巢恶性肿瘤是常见女性生殖器恶性肿瘤之一。由于卵巢位置较深且卵巢肿瘤组织类型复杂多样,早期病变无特异性的临床症状,发现时常已处于晚期阶段,治疗效果不佳,预后较差,病死率在妇科肿瘤中占比较高[1]。因此,早期鉴别卵巢肿瘤良恶性尤为重要。超声作为筛查卵巢肿瘤的首选方法,根据卵巢肿瘤超声特征进行分类的诊断模型有很多,如妇科影像学报告和数据系统(gynecology imaging reporting and data system,GI-RADS)、国际卵巢肿瘤分析(ITOA)简单法则[2-3]等,但国内外对GI-RADS 分级系统尚未达成共识[4],IOTA 简单法则不适用于所有的卵巢肿瘤,当判断结果为不确定性肿瘤时,还需联合MRI 等其他方法进行下一步判别[5]。由Jacobs等[6]首次提出的恶性风险指数(risk of malignancy index,RMI)是联合超声检查、血清癌抗原125(CA125)水平及绝经状态对卵巢肿瘤进行综合性评判,研究[7]表明,RMI对鉴别诊断卵巢肿瘤良恶性有较高的特异性和阳性预测值,但对非上皮性肿瘤、交界性肿瘤、卵巢肿瘤早期患者敏感性较低。美国放射协会提出的卵巢-附件报告和数据系统(ovarian-adnexal reporting and data system,O-RADS)[8]为超声鉴别诊断卵巢肿瘤良恶性提供了新的思路和依据。本研究旨在比较O-RADS 与RMI 鉴别卵巢肿瘤良恶性的诊断效能,同时探讨预测卵巢恶性肿瘤的独立危险因素。
资料与方法
一、研究对象
选取2020 年5 月至2021 年8 月我院经手术病理确诊的卵巢肿瘤患者431 例,年龄15~87 岁,平均(50.67±15.23)岁。其中良性258例,包括畸胎瘤63例、黏液性囊腺瘤56 例、子宫内膜异位囊肿46 例、浆液性囊腺瘤43例、单纯卵巢囊肿12例、卵泡膜纤维瘤11例、卵泡膜细胞瘤10 例、卵巢冠囊肿6 例、黄体囊肿3 例、卵巢甲状腺肿 3 例、良性 Brenner 瘤 3 例、纤维瘤 2 例;恶性(含交界性)173例,包括浆液性癌86例、交界性浆液性肿瘤18 例、透明细胞癌16 例、交界性黏液性肿瘤14 例、黏液性癌10 例、粒层细胞瘤6 例、宫内膜样癌5 例、转移癌4 例、无性细胞瘤3 例、卵黄囊瘤和未成熟畸胎瘤各2 例,以及未分化癌、血管肉瘤、小细胞神经内分泌癌、鳞状细胞癌、弥漫性大B 细胞淋巴瘤、交界性透明细胞肿瘤、交界性子宫内膜样癌各1 例。纳入标准:①术前均经妇科超声检查和血清肿瘤标志物检测;②附件区至少有1 个肿块,若具有2 个及以上肿块,将具有最高恶性风险特征的肿块纳入研究,若2 个肿块的特征相似,则选较大的肿块纳入研究;③患者信息资料完整。排除妊娠者、接受过附件区手术及放化疗者、患者信息不完整及超声图像质量不佳者。本研究经我院医学伦理委员会批准,所有患者均签署知情同意书。
二、仪器与方法
1.超声检查:使用GE Voluson E 8、迈瑞Resona 8T等彩色多普勒超声诊断仪。检查前嘱患者排空膀胱,取截石位,常规行经阴道超声检查子宫及双侧附件等盆腔脏器,重点观察肿块大小、内部回声、壁厚、分隔厚度、乳头状凸起物、实性区、有无腹水或腹膜结节、有无血供及血供的丰富程度等。若肿块体积较大,经阴道超声不足以显示其完整轮廓,则需联合经腹超声检查。由2 名具有5 年以上妇科超声诊断经验的医师在双盲的情况下分别应用O-RADS、RMI 对所有卵巢肿瘤进行分类,当分类结果不一致时协商解决。
2.O-RADS:将卵巢肿瘤分为6 类[8],具体:0类,超声不能评估;1类,正常卵巢组织,包括最大径≤3 mm的卵巢和黄体;2 类,几乎可以肯定为良性病变(恶性风险<1%),包括最大径<10 cm 的单纯性囊肿、内壁光滑的非单纯性囊肿、典型良性病变(卵巢出血性囊肿、成熟性畸胎瘤、子宫内膜异位囊肿、卵巢旁囊肿、腹膜包涵囊肿及输卵管积水);3 类,恶性低风险病变(恶性风险1%~<10%),包括最大径≥10 cm 的单房囊肿及典型的良性病变、任意大小的单房囊肿伴有<3 mm 厚的不规则内壁、多房囊肿(最大径<10 cm、内壁光滑、血流评分1~3 分)、实性或实性样肿块(任意大小、外缘光滑、血流评分1 分);4 类,恶性中等风险病变(恶性风险10%~50%),包括多房囊肿(最大径≥10 cm或任意大小且伴不规则内壁或不规则分隔)、单房或多房囊肿(有实性或实性样成分或0~3个乳头状凸起、血流评分1~2 分)、实性肿块(光滑轮廓、血流评分2~3 分);5类,恶性高风险病变(恶性风险≥50%),包括单房囊肿(有实性成分、乳头状凸起≥4 个、血流评分3~4 分)、多房囊肿(有实性成分、任意大小、血流评分3~4 分)、实性肿块(光滑轮廓且血流评分4分,或不规则轮廓且任意血流评分)、腹水和(或)腹膜结节。血流评分1~4分,1 分:无血流信号,2 分:微血流信号,3 分:中等血流信号;4 分:大量血流信号。
3.RMI:计算公式 RMI=U×M×CA125[6]。超声表现包括5 个声像图特征,分别是多房性、有实性区域、双侧肿块、腹水、转移,当这5个特征均不存在时,则U=1,若存在2 个或2 个以上的声像图特征时,则U=3;M 为月经状态,绝经前患者M=1,绝经后患者M=3。当RMI>200 则将肿块归为恶性[6]。
4.实验室检查:采用罗氏诊断公司的Cobas e601全自动化学荧光免疫分析系统检测血清白细胞计数(WBC)、血小板计数(PLT)、人附睾蛋白(HE4)、CA125、癌抗原199(CA199)、癌胚抗原(CEA)、甲胎蛋白(AFP)等,均重复测量3次取其均值。
三、统计学处理
应用SPSS 26.0 统计软件,符合正态分布的计量资料以表示,两组比较行独立样本t检验;不符合正态分布的计量资料以M(QR)表示,两组比较行秩和检验。以病理结果为金标准,绘制受试者工作特征(ROC)曲线分析 O-RADS、RMI鉴别卵巢肿瘤良恶性的诊断效能;两种方法的敏感性、特异性、准确率比较行χ²检验;曲线下面积比较行Z检验。采用多因素Logistic 回归分析筛选预测卵巢恶性肿瘤的独立危险因素。P<0.05 为差异有统计学意义。
结 果
一、O-RADS 与RMI 鉴别卵巢肿瘤良恶性的诊断效能比较
431 例患者中,O-RADS 2 类 79 例、O-RADS 3 类164例、O-RADS 4类89例、O-RADS 5类99例;经ROC曲线分析显示,当O-RADS>3 类时,诊断卵巢肿瘤良恶性的敏感性、特异性、准确率、曲线下面积分别为93.1%、89.5%、91.0%、0.94(图1);RMI诊断良性292例,恶性139 例;诊断卵巢肿瘤良恶性的敏感性、特异性、准确率、曲线下面积分别为68.2%、91.9%、82.4%、0.80(图1);两种方法的敏感性、准确率、曲线下面积比较差异均有统计学意义(均P<0.001);特异性比较差异无统计学意义。见图2~5。

图1 O-RADS、RMI 鉴别卵巢肿瘤良恶性的ROC曲线图

图2 右侧卵巢囊性成熟型畸胎瘤患者(25岁)经阴道超声图像

图3 左侧卵巢子宫内膜异位囊肿患者(30岁)经阴道超声图像

图4 左侧卵巢黏液性囊腺瘤患者(49岁)经阴道超声图像

图5 卵巢高级别浆液性癌患者(56岁)经阴道超声图像
二、分析预测卵巢恶性肿瘤的独立危险因素
1.良、恶性卵巢肿瘤患者临床资料比较:良、恶性卵巢肿瘤患者WBC、CA199、CEA、AFP 比较差异均无统计学意义;良、恶性卵巢肿瘤患者年龄、是否绝经状态,PLT、CA125、HE4比较差异均有统计学意义(均P<0.001)。见表1。

表1 良、恶性卵巢肿瘤患者临床资料比较
2.良恶性卵巢肿瘤患者超声参数比较:将O-RADS及RMI所包含的超声参数进行单因素分析显示,肿块最大径、囊壁或分隔厚度≥3 cm、有实性成分、乳头状凸起≥4个、血流评分3~4分、腹水比较差异均有统计学意义(均P<0.001)。见表2。

表2 良、恶性卵巢肿瘤患者超声参数比较
3.多因素Logistic回归分析筛选预测卵巢恶性肿瘤的独立危险因素:将上述差异有统计学意义的因素进一步行多因素Logistic 回归分析显示,肿块最大径、囊壁或分隔厚度≥3 cm、有实性成分、血流评分3~4 分、腹水是预测卵巢恶性肿瘤的独立危险因素(均P<0.01)。见表3。
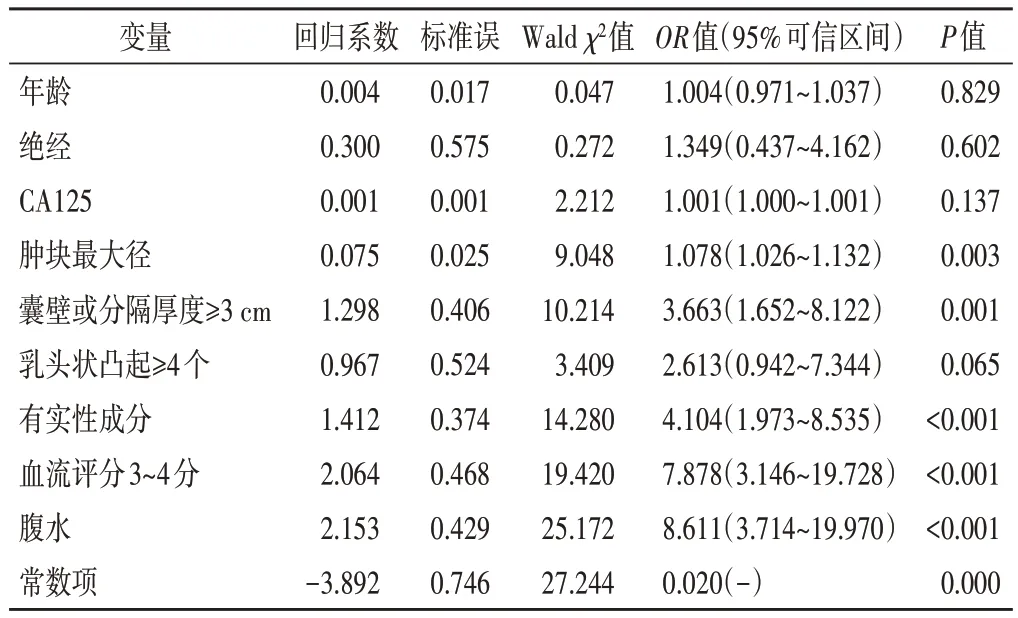
表3 多元素Logistic分析结果
讨 论
术前准确判断卵巢肿瘤的性质对选择最佳治疗方式及预后预测具有重要的临床意义。超声诊断模型可以对卵巢肿瘤进行客观地分类,为患者选择最佳的治疗措施。国内外学者或组织已经提出许多用来鉴别卵巢肿瘤良恶性的超声诊断模型,如Logistic回归模型、IOTA 简单法则、GI-RADS 等,这些模型在我国尚未达成一致共识,未在国内广泛应用。RMI 已经成功地通过了前瞻性和外部验证[9-11],被多个国家和机构认可并广泛使用。O-RADS 对所有正常卵巢及附件病变提供了标准化的超声描述及报告方法,减少或消除了超声医师对卵巢肿瘤超声图像特征描述的不一致性,提高了诊断准确率[8]。本研究通过比较O-RADS 与RMI 鉴别卵巢肿瘤良恶性的诊断效能发现,当O-RADS>3 类时,诊断卵巢肿瘤良恶性的敏感性、特异性、准确率、曲线下面积分别为93.1%、89.5%、91.0%、0.94,RMI诊断卵巢肿瘤良恶性的敏感性、特异性、准确率、曲线下面积分别为68.2%、91.9%、82.4%、0.80;O-RADS 诊断卵巢肿瘤良恶性的敏感性、准确率、曲线下面积均高于RMI(均P<0.001),而特异性比较差异无统计学意义。表明O-RADS 的诊断效能优于RMI。本研究采用O-RADS诊断卵巢肿瘤良恶性的敏感性、特异性与国内外研究[12-14]结果相似,O-RADS的敏感性优于RMI,分析原因为:O-RADS对卵巢肿瘤提供了全面的描述和解释,对一些典型病变如单纯性囊肿、出血性囊肿、成熟性畸胎瘤、子宫内膜异位囊肿等采用规范化的超声术语,使其诊断更加客观、规范,为后期随访或进一步检查或采取手术治疗提供了参考,而RMI 无相应的后续指南。本研究中RMI 的敏感性低于以往研究[15-16]报道,分析原因为:RMI由绝经状态、超声特征及血清CA125 3个因素构成,一方面由于卵巢肿瘤病理组织类型复杂多样,血清CA125 特异性不高,一些恶性肿瘤如透明细胞癌、卵黄囊瘤、黏液性囊腺癌等血清CA125 无明显升高,相反一些良性肿瘤如子宫内膜异位囊肿等血清CA125 有不同程度升高,同样在本研究多因素分析中,CA125 并非预测卵巢恶性肿瘤的独立危险因素;另一方面RMI 中的超声特征未包含彩色多普勒,且多房、实性成分、双侧肿块的声像图特征在卵巢良性肿瘤中也存在。
本研究将O-RADS 与RMI 两种超声诊断方法中包含的多项因素进行分析,探讨预测卵巢恶性肿瘤的独立危险因素。结果发现,良、恶性卵巢肿瘤患者年龄、绝经状态、CA125、PLT、HE4,以及肿块最大径、囊壁或分隔厚度、乳头状凸起、实性成分、血流评分、腹水比较差异均有统计学意义(均P<0.001);经多因素Logistic分析发现,肿块最大径、囊壁或分隔厚度≥3 cm、有实性成分、血流评分3~4分、腹水是预测卵巢恶性肿瘤的独立危险因素(均P<0.01),证实了O-RADS 在鉴别卵巢肿瘤良恶性的重要作用。其中乳头状凸起并非预测卵巢恶性肿瘤的独立危险因素,分析原因可能为:本研究中发现囊腺瘤中存在多个乳头状凸起,在黄体囊肿伴出血及子宫内膜异位囊肿的超声表现中,囊腔及内壁黏附的血块与乳头状凸起相似,有时难以区分,因此,乳头状凸起≥4 个鉴别卵巢肿瘤良恶性的能力相对较弱。吴言等[17]研究中血清CA125 为预测卵巢恶性肿瘤的独立危险因素,本研究结果与之不同,推测原因可能与样本量及病理组织类型不同有关,吴言等[17]研究中卵巢肿瘤291例,交界性肿瘤仅占比2.1%,而本研究中卵巢肿瘤431 例,交界性肿瘤占比7.9%。
综上所述,O-RADS鉴别卵巢肿瘤良恶性的诊断效能优于RMI,具有较高的临床价值;其中肿块最大径、囊壁或分隔厚度≥3 cm、有实性成分、血流评分3~4分、腹水是预测卵巢恶性肿瘤的独立危险因素,具有一定的指导意义及应用价值。
