基于磁性纳米材料修饰的离子液体萃取番茄中的过氧化氢酶
2022-04-12栾鑫鑫王书雅谢云峰
王 涛,翟 晨,栾鑫鑫,王书雅,谢云峰,王 亮*
(1 新疆大学生命科学与技术学院 乌鲁木齐 830017 2 中粮营养健康研究院 营养健康与食品安全北京市重点实验室 北京 102209 3 北京工业大学环境与生命学部 北京 100124)
番茄是世界产量最丰富的常见蔬菜之一,其内富含番茄红素、维生素C 和过氧化氢酶,营养价值极高[1-2],然而易产生劣变。过氧化氢酶是一种典型的抗氧化酶,广泛存在于细胞内,用于代谢乙醇。过氧化氢酶将过氧化氢分解后,产生无毒、无害的水和氧气,可以保护细胞免受来自内源性代谢的过量活性氧(ROS)或外部微环境,减缓果蔬腐败变质[3-5]。
在所有可能的溶剂中,水无疑具有出色的安全性,这是因为水无毒、不易燃,价格便宜且资源丰富。除具有安全和环保优势外,水还表现出优异的物理和化学性质。其独特而牢固的氢键网络可以直接影响反应机理,加速或降低反应速率。离子液体通常由阳离子(有机)和阴离子(无机或有机)组成,组成离子熔点较低(<100 ℃)。其中,阳离子通常由咪唑、季铵盐或磷离子组成,常见的阴离子部分包括氯离子、溴离子、四氟化硼、六氟化磷、双(三氟磺酰)亚胺等。其具有较高的热稳定性,相对较高的黏度,较大的电化学窗口,非常低的挥发性等特性,这些特性吸引研究人员在合成和萃取时应用[6-8]。离子液体对与之混溶液体的极性接受度高,支持有机和无机物质的同步溶解,因而被成功用于从溶液中提取物质的研究。通过选择合适的、烷基链长度不同的阳离子和阴离子,可以调节离子液体的物理性质[9-15]。离子液体在有机合成、催化、液-液萃取、电化学、形态研究、核后处理等方面的应用近年来得到广泛的研究[16-19]。水和离子液体可以相互受益,形成一种新的介质,从而发挥两种成分的优点。借助弱范德瓦尔斯力、库仑力,强共价键等,以化学成键吸附或物理吸附等形式,增大离子液体与纳米材料之间的接触面积,从而提高离子液体的催化、分离性能,同时磁性纳米粒子的引入可以有效避免离子液体的损失[20-23]。不仅拓宽彼此适用范围,还能降低成本。
Zhu 等[24]采用咪唑鎓离子液体-水混合物从小球藻中提取叶黄素,提取率高达98.06%。Mishra等[25]研究用极少量离子液体三辛基硫代水杨酸铵在不同体积、pH 值和铀浓度的水介质中提取铀的效率,结果表明对于杂质含量较低的样品,离子液体提取铀的效率高达85%。Geng 等[26]利用N-烷基碳酸咪唑离子液体分离萃取高酸油中的环烷酸,其再生及回收率高达92%,离子液体也可回收利用。Li 等[27]采用六烷基胍离子液体液-液萃取茶树油中的4-萜烯醇,单次提取率可达90%。Deng等[28]以疏水离子液体为萃取剂,在最佳提取条件下,对生物油水馏分中乙酸、苯酚、愈创木酚和4-甲基愈创木酚的提取率分别为2.71%,95.41%,92.04%和97.98%,表明此种离子液体对生物油水馏分中的酚类物质具有较好的选择性和提取效率。上述研究表明利用离子液体的萃取是可行的。
本研究选用1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体,萃取番茄细胞中的过氧化氢酶。通过测定萃取酶活性,考察1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体加入量、萃取时间和温度等参数对酶活的影响,确定提取过氧化氢酶的最优参数并与缓冲溶液萃取法作比较,旨在为实现高活性过氧化氢酶等蛋白类物质的高效萃取拓展思路。
1 材料与方法
1.1 材料与试剂
由上海士锋生物科技有限公司生产的过氧化氢酶2 000 U/mg,由海默尼化工科技有限公司生产的1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体。
1.2 仪器与设备
Milli-Q Reference 超纯水系统,美国Millipore 公司;11-102-49SH 涡旋混匀器,德国IKA公司;U-3900 紫外可见分光光度计,日本Hitachi公司;THZ-103B 恒温培养摇床,上海一恒科学仪器有限公司;PB-10 pH 计,德国Sartorius 公司;Thermo ST16R 离心机,德国Eppendorf 公司;Multi-mode Synergy Mx 酶标仪,美国Bio-Tek 公司。
1.3 试验方法
1.3.1 1 -羟乙基-3-甲基咪唑基Fe3O4纳米磁流体萃取酶蛋白 准确称取175 mg 纳米磁流体加入离心管中,加入1.5 mL 水溶解,形成双水相体系,再加入预制番茄泥0.1 g,充分振荡后置于35℃恒温培养箱中,于200 r/min 转速下振荡20 min,静置直至两相分离,提取上层清液中的过氧化氢酶,测定活性指标。图1为磁性固相体系萃取酶的原理图。

图1 磁性固相体系萃取酶原理图Fig.1 Schematic diagram of extractase in magnetic solid phase system
1.3.2 缓冲溶液法萃取分离酶蛋白 量取4.5 mL pH=7.8 的PBS 缓冲液置于离心管,再加入0.1 g 番茄泥浆,充分混合后于5 000 r/min 转速下保持40 min,静置后提取上层清液待用,离心和静置保存均于4 ℃恒温下完成。
1.3.3 提取工艺优化 测定不同离子液体添加量 (150,175,200,225,250 mg)、萃取温度(20,25,30,35,40 ℃) 及离心时间(20,25,30,35,40 min)条件下,提取酶活性的变化。
1.3.4 响应面试验设计 以提取酶活性作为响应值,针对3 个变量设计单因素响应面试验,每个变量因素设定3 个水平,各因素具体设定值如表1所示。

表1 响应面试验设计Table 1 Response surface experimental design
1.3.5 酶蛋白活性测定 采用紫外分光光度法测定酶活[29]。
2 结果与分析
2.1 萃取参数优化
2.1.1 1 -羟乙基-3-甲基咪唑基Fe3O4纳米磁流体用量 由图2a 可知,随离子液体加入量的提高酶活逐渐升高,当加入量达到175 mg 时,萃取效果最好,之后随着离子液体加入量升高,酶活性逐渐降低,因此离子液体加入量应控制在175 mg。
2.1.2 萃取温度 如图2b 所示,当其它试验条件固定的前提下,于35 ℃提取的酶活性最理想,即该温度为试验最佳萃取温度参数。
2.1.3 萃取时间 如图2c 所示。随萃取时间增加,过氧化氢酶活性逐渐增加,30 min 时酶活性最高。因此,最优萃取时间为30 min。

图2 单因素酶活试验结果Fig.2 Single factor enzyme activity test results
2.2 响应面结果分析
2.2.1 响应面设计及结果 对表2数据进行分析,得到二次回归拟合方程Y=347.64+0.27A+1.78B-0.031C+2.94AB+1.25AC+8.34BC-28.01A2-26.91B2-30.26C2。

表2 响应面试验设计方案Table 2 Response surface experiment design scheme
模型方程方差小于0.0001,为差异极显著因素;失拟项P 值为0.5090(>0.05),表明该因素差异不显著,即回归方程拟合结果与试验结果相吻合。因此,该模型用于酶活分析获取的结果真实可靠。在A、B、C 3 个因素中,B 对酶活影响最大,A次之,C 相对最小,即萃取温度最显著,1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体加入量次之,萃取时间影响相对较小。
2.2.2 响应面分析 绘制如图3所示的响应曲面图,用于分析对比A、B、C 因素两两组合对酶活影响的强弱。
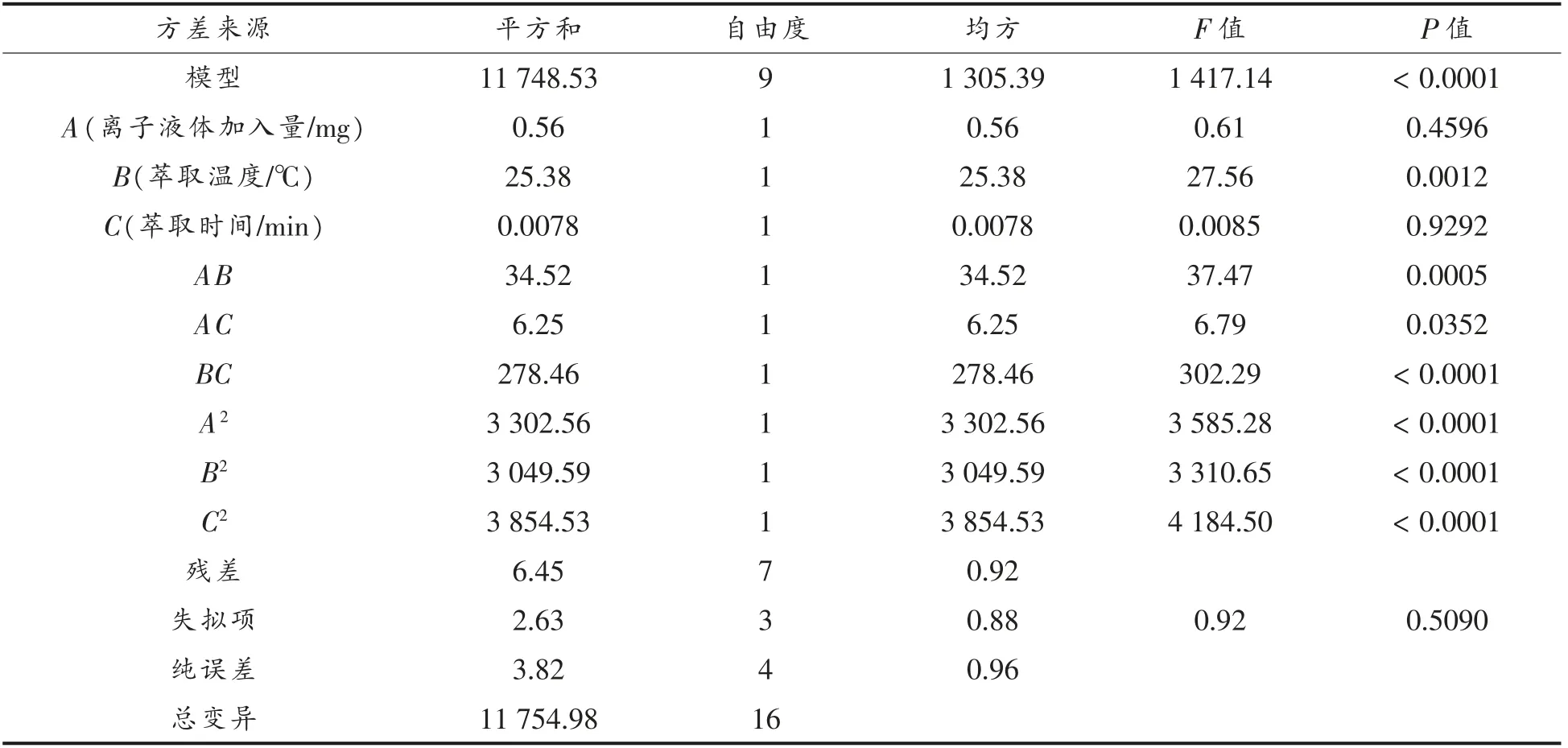
表3 方差分析表Table 3 Anova table


图3 三因素间两两交互的响应面及等高线图Fig.3 The response surface and contour map of the interaction among various factors
由上图三维响应面趋势可知,三因素的两两交互作用对酶活影响显著,由等高线图可确定最高酶活对应的三因素水平范围,分析结果与试验结果相一致,证明响应面模型和等高线模型的可靠性,并由此确定最佳过氧化氢酶萃取试验条件:1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体加入量175.99 mg、萃取温度及时间分别为34.87 ℃、30.14 min。
2.3 验证试验
为兼顾试验操作可行性,将各因素设定为1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体加入量176 mg、萃取温度及时间分别设定为35 ℃、30 min。由酶活测量的3 次平行试验结果可知,酶活平均值(345.68 U/g)与预测值(345.15 U/g)相近,进而再次证明所建立模型的可靠性。
2.4 磁性固相体系与PBS 缓冲溶液萃取番茄中5 种蛋白酶的比较
表4为在最优条件下对番茄中5 种抗氧化酶进行萃取的结果,由表可以看出,通过磁性固相提取的各种酶的活性均明显高于PBS 缓冲溶液法,且大部分标准偏差更小,导致这一现象的主要原因是纳米材料与离子液体对蛋白酶的强有力的吸附萃取效果,实现高活性蛋白酶类物质的高效提取。总而言之,与传统萃取技术相比,由磁性固相体系萃取法抵御外界干扰的效果更优,提取的蛋白酶活性更稳定。

表4 磁性固相体系与PBS 缓冲溶液萃取番茄中5 种蛋白酶的比较Table 4 Comparison of five proteases extracted from tomato with magnetic solid phase system and PBS buffer solution
3 结论
本研究基于新型离子液体1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体,以番茄细胞过氧化氢酶提取为例,优化了蛋白酶类物质萃取试验条件。以酶活为指标对1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体的加入量、萃取温度及时间进行调整,并对以上3 个显著变量分别设计单因素响应面试验,并与试验所得结果进行对比。模型、试验两方面的数据结果显示:1-羟乙基-3-甲基咪唑基Fe3O4纳米磁流体加入量176 mg、萃取温度及时间分别设定为35 ℃、30 min 时,提取酶的活性最高。本试验以番茄细胞过氧化氢酶提取为基础,优化了传统的蛋白酶类物质萃取方法,将萃取周期由原来的40 min 缩短至30 min,在保证酶活的同时提高了萃取效率。
