保定平原南部超采区地下水化学特征研究
2022-04-11李谨丞杨会峰张永波
李谨丞 杨会峰 张永波
(1.中国地质科学院水文地质环境地质研究所,河北 石家庄 050061;2.中国地质大学(北京),北京 100083;3.京津冀平原地下水与地面沉降国家野外科学观测研究站,河北 石家庄 050061;4.中国地质环境监测院,北京 100081)
0 引言
20 世纪70 年代以来, 随着保定地区农业和工业的快速发展, 对地下水进行大规模长期的过度开采,引起了保定平原区地下水水位的持续下降,形成了多处地下水降落漏斗,部分含水层被疏干或枯竭,引发了一系列环境地质问题,如地面沉降、地裂缝、水质恶化等[1]。 这些严重地制约了保定平原区经济社会可持续发展,危及了研究区的生态安全和供水安全。
在地下水运移的过程中,地下水持续与流经的介质相互作用,形成了不同的区域地下水化学组分[2]。 地下水化学特征能够较好地反映区域地下水循环和水化学演化,是地下水资源评价的重要内容[3]。 因此以保定平原区南部为例, 对其地下水水化学组成进行分析,探讨其地下水水化学特征、演变因素及年龄特征,对于了解保定平原区地下水资源的分布、补给流动状况及开采后的变化以及对于科学管理、合理开发地下水资源具有重要实际意义。
1 研究区概况
保定平原区南部位于河北平原与太行山脉的接壤地带,总体地势平坦。 西临太行山区,中部以及东南部为河北平原区。 保定平原区位于北温带,为大陆型半干旱季风气候区,多年平均气温为12.6℃,其中以七月份气温最高,平均26.4℃;一月份气温最低,平均-5℃。研究区多年平均降水量543.5 mm,多年平均蒸发量约为平均降水量的3.2 倍,高达1 728 mm。
2 样品采集与分析
为阐明保定平原南部地下水水文地球化学特征及地下水年龄特征,明确地下水超采对地下水年龄分布规律及水化学特征的影响, 自非漏斗区至漏斗区,沿区域地下水流方向,以A-A′,B-B′两条典型剖面进行研究。 采集水化学样品40 组,并将取样点分为非漏斗区采样点(Ⅰ类采样点)和漏斗区采样点(Ⅱ类采样点),采样点分布如图1 所示。

图1 保定平原南部地下水采样点分布图
研究区所采集水样的pH 值和水温均在野外用便携式测试仪完成, 其他指标数据进行实验室室内测试。 国土资源部地下水科学与工程重点实验室对研究区水样进行室内测试,通过原子吸收分光光度对阳离子进行测定, 采用离子色谱仪对Cl-、SO42-等阴离子进行测定,HCO3-则采用的是滴定法测定得出。
3 地下水水化学特征
3.1 地下水主要组分特征
保定平原区南部地下水水化学主要成分统计结果见表1。由统计结果显示:研究区地下水中阳离子以Ca2+、Na+为主,约占阳离子总量的82.34%,主要阳离子浓度平均值大小依次为 Ca2+>Na+>Mg2+>K+,其中 Na+的变异系数较大,为94.2%,这表明研究区地下水中Na+在空间上变化较大;研究区地下水中阴离子以HCO3-、SO42-为主,约占阴离子总量的87.35%,主要阴离子浓度平均值大小依次为 HCO3->SO42->Cl->NO3-, 其中NO3-、SO42-、Cl-的变异系数较大分别为 151.00%、122.11%、116.4%,说明研究区地下水中的 NO3-、SO42-、Cl-在空间上变化较大。
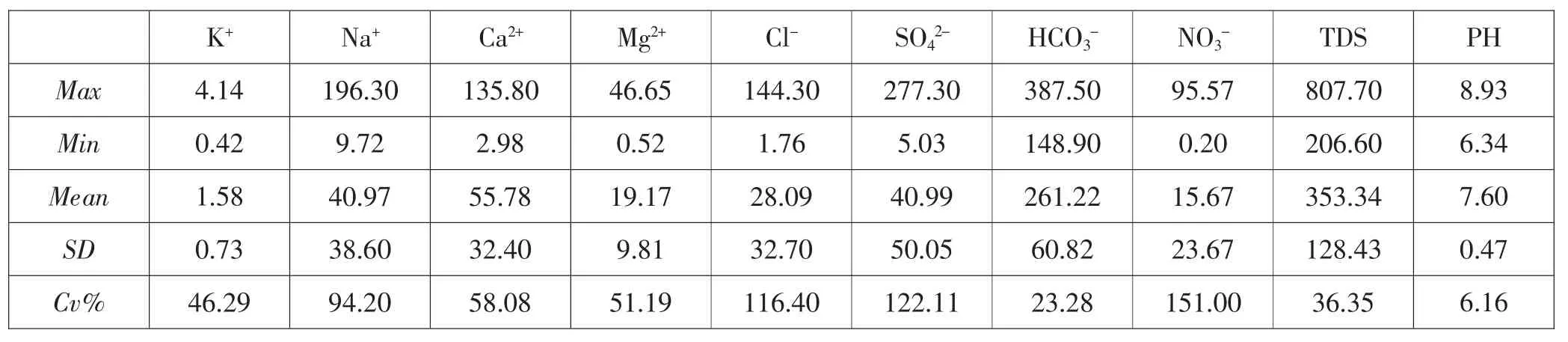
表1 地下水主要化学组分统计特征
研究区地下水水样pH 值范围为6.34~8.93,均值为7.60,整体上呈弱碱性,变异系数为6.16%,说明研究区地下水pH 值在空间上分布较为稳定。 TDS 含量206.60~807.70 mg/L,均值为 353.34 mg/L,变异系数为36.35%,处于中等变异级别。 按照TDS 划分咸淡水的方法[3],研究区所有水样均为淡水,无咸水出现。 各类采样点TDS 值表现为漏斗区采样点>非漏斗区采样点, 由非漏斗区采样点到漏斗区采样点Na+、SO42-和Cl-表现出明显的上升趋势,Ca2+、Mg2+和 HCO3-浓度呈下降趋势。
3.2 地下水水化学类型
通常利用Piper 三线图对地下水水化学的主要离子组成特征进行分析[10]。 由非漏斗区到漏斗区地下水对碳酸盐矿物的溶滤逐渐减弱;研究区地下水阴离子以 HCO3-、SO42-、Cl-为主, 非漏斗区与漏斗区地下水优势阴离子为HCO3-, 但出现部分漏斗区采样点优势阴离子为 SO42-;阳离子以 Ca2+、Na+、Mg2+为主,非漏斗区地下水优势阳离子为Ca2+, 漏斗区地下水优势阳离子为Na+。 按舒卡列夫分类[3],研究区非漏斗区地下水化学类型主要类型为 HCO3-Ca·Mg 型、HCO3-Ca·Na 型、HCO3-Ca 型; 漏斗区采样点主要类型为HCO3-Na 型、HCO3·SO4-Na 型。
4 地下水组分来源
4.1 Gibbs 模型分析
Gibbs 模型[4]可以用来识别自然水体中各种离子的起源。 利用 TDS 与 Na+/(Ca2++Na+)以及 Cl-/(Cl-+HCO3-)浓度比值关系绘制的Gibbs 图, 对研究区地下水水化学过程进行分析, 从图2 可以看出地下水采样点主要落在岩石风化控制区, 说明地下水化学组分的形成受蒸发浓缩和大气降水影响较小,主要受岩石风化作用控制[5-8]。 各区水点 Cl-/(Cl-+HCO3-)没有明显的规律性,比值普遍较低,表明地下水径流路径上地下水化学组分受盐岩矿物溶解影响较小。Na+/(Na++Ca2+)比值分布范围较广, 漏斗区与非漏斗区采样点Na+/(Na++Ca2+)比值有较好的集群性,其中所有非漏斗区采样点Na+/(Na++Ca2+)<0.5; 有 82.35%的漏斗区采样点 Na+/(Na++Ca2+)>0.5,由此可以看出,随着漏斗的形成和发展,漏斗区地下水位大幅下降,水力坡度变大,水交替变强,加剧了水岩作用。

图2 Gibbs 水化学图
4.2 阳离子交替吸附作用
阳离子交替吸附作用是地下水化学形成和演变的一个重要过程[9]。通常氯碱指数(CAI)的变化可以用来分析地下水发生离子交换作用的方向和强度。

若发生正向Ca-Na 交换, 则两个指数均小于0;当发生反向Na-Ca 交换时,则两个指数均大于0。 漏斗区与非漏斗区的氯碱指数有较好的集群性,漏斗区采样点的CAI1 和CAI2 均小于0,而非漏斗区采样点CAI1 和CAI2 值多集中于0 附近或大于0, 表明在漏斗区发生了正向的 Ca-Na 交换; 从CAI1 和CAI2 均值来看非漏斗区CAI1 和CAI2 均值分别为-0.639 和0.0082, 漏斗区则为-5.89 和-0.135, 漏斗区 CAI1 和CAI2 均值低于非漏斗区,表明漏斗区地下水离子交换作用的强度大于非漏斗区。 以上两种现象说明大量开采地下水后导致漏斗区地下水与围岩之间正向Ca-Na 交换作用增强,从而改变了地下水的水化学组分。
5 结语
研究区非漏斗区采样点地下水化学类型主要类型为 HCO3-Ca·Mg 型和 HCO3-Ca·Na 型, 进入漏斗区后主要地下水水化学类型变为HCO3-Na 型和HCO3·SO4-Na 型;由非漏斗区到漏斗区地下水对碳酸盐矿物的溶滤逐渐减弱; 大量非漏斗区采样点发生逆向Ca-Na 交换作用,而所有漏斗区采样点则发生正向Ca-Na交换作用,且强度大于非漏斗区;进入漏斗区后地下水的水流运动加快,水动力条件变好。 地下水超采地下水的过度开采造成地下水水位下降,形成地下水降落漏斗,水力梯度增大,增强了地下水对围岩的溶滤作用以及正向Ca-Na 交换作用,改变了地下水水动力场和水化学场的原始平衡。
