乙肝5项标志物定量诊断试剂的优化及性能评价
2022-04-07黄贞杰张剑清
黄贞杰,张剑清
(1.泉州医学高等专科学校 基础医学部,福建 泉州 362011;2.福建省洪诚生物药业有限公司,福建 莆田 351254)
化学发光免疫分析技术由于灵敏度高、线性范围宽、有效期长、无有害物污染、可实现自动化,兼具放射性免疫学方法和酶免疫方法二者的优点,被广泛应用[1-3].它可满足现代医学对疾病相关因子的精确定量和动态检测的要求,与其他方法相比,在技术上具有明显的优势[4-6].我国是乙型肝炎的高发区,乙肝系列化学发光诊断产品对乙型肝炎的监测、传染源控制及疗效判断等具有重要意义[7].乙型肝炎5 项血清标志物,即乙肝两对半,是检测血液中乙肝病毒的血清学标志,高效定量检测乙肝5 项标志物对乙肝的诊断具有重要临床意义[8].目前,国外产品如Abbott、Roche 的试剂性能相对稳定,检测结果符合率较高,市场占比具有优势;国内也出现了越来越多的乙型肝炎系列体外诊断试剂厂家,但是试剂的性能参差不齐[9-10],而且大多是定性检测为主[11].国产化学发光法诊断试剂的检测灵敏度相对较低,存在漏检情况[12-13].本文对国产化学发光法乙型肝炎5 项标志物诊断试剂进行优化,研制较高质量和稳定性的国产新型化学发光法乙型肝炎血清标志物定量诊断试剂,以缓解国外化学发光诊断试剂独霸国内市场的不利局面,提高我国体外诊断试剂与国外知名企业的竞争力.
1 材料与方法
1.1 材料
1.1.1 主要试剂 微孔板购自深圳市金灿华实业有限公司;各检测试剂盒包被及酶原料分别购自军事医学科学院、北京京达致远生物有限公司、洛阳市佰泰科生物技术有限公司、北京万象宏达生物技术研究所、北京科跃中楷生物技术有限公司;小牛血清、白蛋白购自上海洛神生物技术有限公司;对比用的化学发光定量检测试剂购自Abbott公司;HBeAg国际灵敏度参考品1#、2#和3#5个梯度的浓度(质量浓度,后同)分别为1∶16、1∶32、1∶64、1∶128和1∶256;HBeAb国际灵敏度参考品1#、2#和3#5个梯度的浓度分别为1∶8、1∶16、1∶32、1∶64和1∶128;HBcAb国际灵敏度参考品1#、2#和3#5个梯度的浓度分别为1∶1、1∶2、1∶4、1∶8和1∶16.
1.1.2 仪器设备 自动包被机(A208),北京拓普分析仪器有限公司;自动酶标洗板机(DEM-III),北京拓普分析仪器有限公司;化学发光分析仪(HC-CLIA-Ⅲ),福建省洪诚生物药业有限公司;隔水式培养箱(GHP-9080),上海一恒科技有限公司;旋涡混合器(GL-86B),海门麒麟;ARCHITECT i2000SR 检测系统,Abbott公司;除湿机(DH-830C),川岛.
1.2 研究方法
1.2.1 包被原料活性筛选 按照厂家提供的参考比例进行包被,比较包被原料的活性高低.
1.2.2 最适包被浓度及酶标工作浓度的确定 将包被原料用包被液分别稀释成不同浓度后,包被微孔板.将HRP 标记的酶原料稀释不同浓度后,以校准品或阴阳性对照作为样本,采用方阵滴定法,确定最适的包被比例及酶标浓度.
1.2.3 灵敏度试验 定量检测以原试剂盒校准品S0和S1的发光值比值衡量试剂盒灵敏度;定性检测以测定国标灵敏度参比品,观察是否可以全部检出.
1.2.4 包被板及酶稳定性考核 将包被板及HRP 标记酶置于37 ℃恒温培养箱中3 d,对其进行稳定性考核.
1.2.5 HBsAg强阳性血浆原料筛选及处理 选择1份HBsAg强阳性血浆,体积足够多,采用Abboott化学发光定量检测试剂盒和本研究试剂盒检测,严格按照说明书要求操作,两种试剂盒分别检测2 次.经两种试剂盒筛选好的HBsAg阳性血浆,经101~103 ℃90 s及65 ℃10 h巴氏消毒处理,作为配制质控品的原料.
1.2.6 HBsAg强阳性血浆的标定 以PBS为稀释液,将HBsAg阳性血浆用稀释液稀释一系列梯度,以国家表面抗原定量线性参考品为标准,预实验对HBsAg 阳性血浆的浓度进行初步估算.估算好浓度的HBsAg 阳性血浆先用稀释液按1∶32 稀释后,再按1.5 倍系列稀释8 个点,由国家线性参考品及洪诚试剂经双平行线方法进行标定,并进行t检验.同时,将1∶32 的稀释液按照2 倍系列稀释8 个点,并按照上述方法进行标定.对两次标定结果进行评价.两次标定结果偏差若符合检测试剂的变异范围,则确定HBsAg阳性血浆的初始浓度.将确定浓度值的HBsAg阳性血浆稀释至校准品浓度,配制成校准品.
1.2.7 统计学方法 采用SPSS19.0软件分析处理,计量数据以均数±标准差(x±s)表示,采用t检验,计数数据以率(%)表示.检验水准设为α=0.05.
2 实验结果与分析
2.1 乙肝两对半原料筛选与稳定性试验
2.1.1 包被原料筛选 对于定量检测,以校准品进行对比;定性检测,则以阴阳性对照作为考核对象.实验结果:1)HBsAg 包被原料中军科院和万象的原料活性较高,可以作为下一步试验材料;2)HBsAb 包被原料中万象、科跃及佰泰科的原料较好;3)HBeAg、HBeAb 包被原料除了军科院的外,其他活性均不高;4)HBcAb包被原料中万象原料的活性比京达的稍低,京达的活性最高,可以考虑作为下一步试验材料.
2.1.2 包被浓度及酶标浓度的确定 经过方阵滴定试验,实验结果如下:1)HBsAg检测试剂:军科院包被浓度1∶3 000,酶浓度1∶2 000;万象包被浓度1∶2 500,酶浓度1∶2 000.2)HBsAb检测试剂:万象包被浓度1∶4 000,酶浓度1∶2 500;科跃包被浓度1∶5 000,酶浓度1∶2 000;佰泰科包被浓度1∶7 000,酶浓度1∶3 000.3)HBeAg检测试剂:军科院包被1∶2 000,酶浓度1∶5 000.4)HBeAb检测试剂:军科院包被1∶2 500,酶浓度1∶8 000.5)HBcAb检测试剂:京达包被1∶5 000,酶浓度1∶5 000;万象包被1∶6 000,酶浓度1∶4 000.根据各检测试剂原料的最适包被比例及酶浓度,分别包被一些微孔板,并配置酶溶液,与现有试剂盒进行灵敏度比较试验.
2.1.3 灵敏度试验 试验结果如下.
1)试剂盒定量检测.以试剂盒S0、S1 发光值的比值作为定量检测的衡量指标,HBsAg 检测试剂的灵敏度情况具体如表1所示.
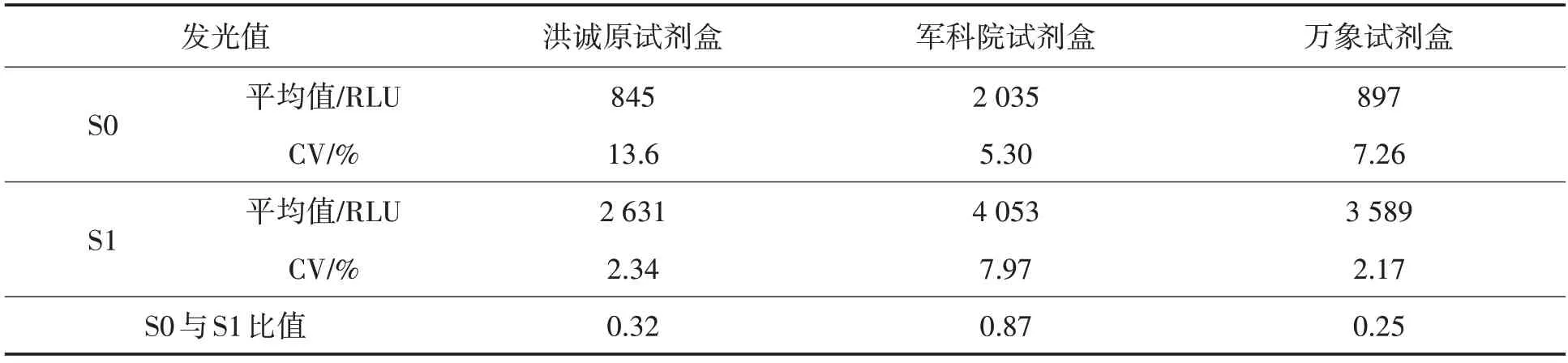
表1 HBsAg 3种试剂灵敏度比较
由表1 可以看出,万象HBsAg 原料的S0 与S1 比值最小,说明S1 与S0 发光值拉得比较开,因此灵敏度最好,军科院的原料活性虽然也比较好,但是灵敏度不够.
2)HBsAb检测试剂的灵敏度比较.HBsAb 4种试剂的灵敏度情况如表2所示.

表2 HBsAb 4种试剂灵敏度比较
由表2可见,只有佰泰科原料的灵敏度比原试剂盒好.
3)乙型肝炎病毒e 抗原国家灵敏度参考品测试.军科院HBeAg 原料制备的试剂盒检测灵敏度参考品的结果如表3所示.
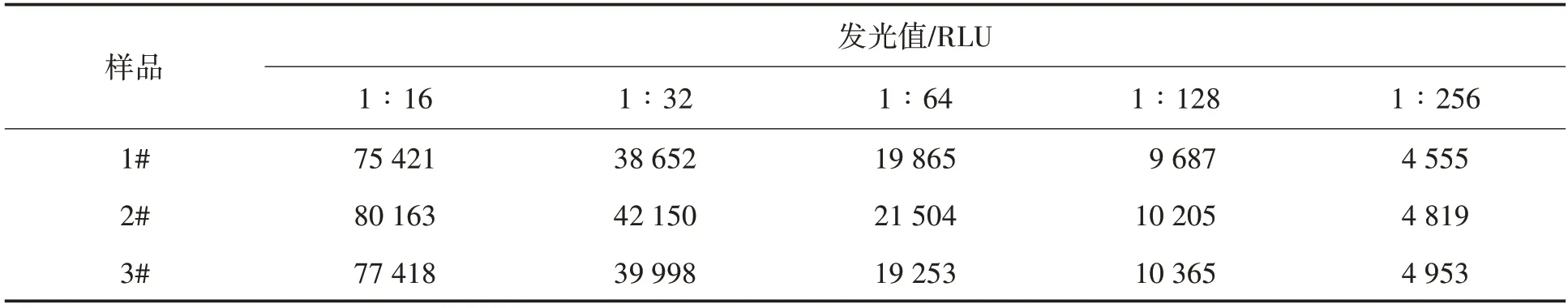
表3 HBeAg试剂灵敏度试验结果
由表3 可知,军科院HBeAg 原料制备的试剂盒均能检测出国家灵敏度的15 个样品,说明符合国家标准规定的最低灵敏度检出标准.
4)乙型肝炎病毒e 抗体国家灵敏度参考品测试.军科院HBeAb 原料制备的试剂盒检测灵敏度参考品的结果如表4所示.
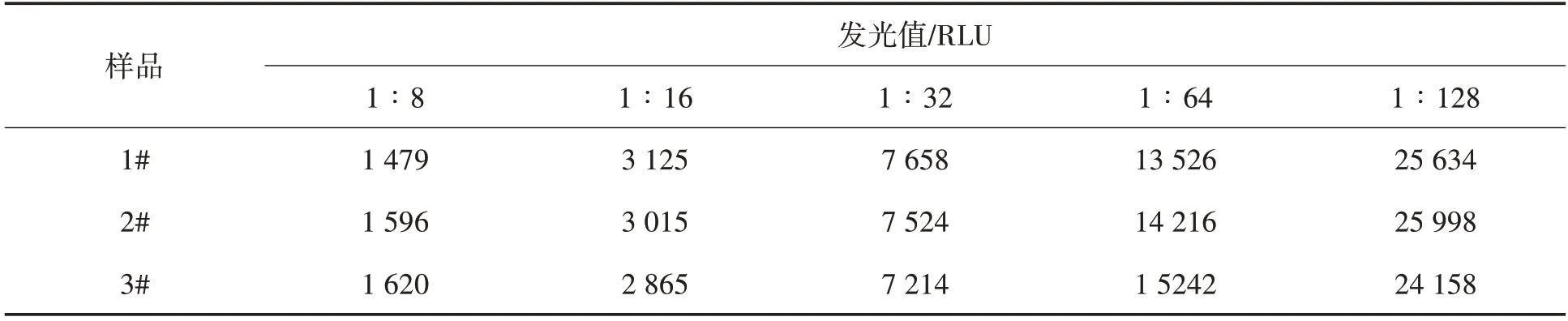
表4 HBeAb试剂灵敏度参考品试验结果
由表4 可知,军科院HBeAb 原料制备的试剂盒均能检测出国家灵敏度15 个样品,说明符合国家标准规定的最低灵敏度检出标准.
5)乙型肝炎核心抗体.京达和万象HBcAb检测试剂国家灵敏度参考品测试结果如表5所示.

表5 京达和万象HBcAb试剂灵敏度试验结果
由表5 数据分析可知,京达HBcAb 原料制备的试剂盒均能检测出国家灵敏度15 个样品,说明该原料的灵敏度最高;万象HBcAb 原料制备的试剂盒只能测出1#和2#灵敏度,无法测出3#,因此,万象原料检测HbcAb的灵敏度不够高,所以,选择京达原料制备HBcAb试剂盒.
2.1.4 稳定性试验 试验结果如下.
1)HBsAg试剂稳定性试验.HBsAg以万象作为原料,进行稳定性试验,结果如表6所示.

表6 HBsAg试剂稳定性试验结果
本研究以成品检定技术指标等随贮存时间的变化来评价试剂盒的稳定性.根据国家对体外诊断试剂的质量要求规范,在37 ℃保温3 d,进行稳定性实验.表6数据表明该试剂盒稳定性符合要求.
2)HBsAb 试剂稳定性试验.经筛选,HBsAb 原料灵敏度最好的原料为佰泰科,故选取由此原料组成的试剂进行稳定性试验,结果如表7所示.

表7 HBsAb试剂稳定性试验结果
表7数据表明,在37 ℃保温3 d,试剂盒各项检定技术指标均符合国家对体外诊断试剂的质量要求,该试剂盒稳定性符合国家要求.
3)HBeAg 试剂稳定性试验.经筛选,确定采用军科院的作为HBeAg 原料,并对此原料组成的试剂进行稳定性试验,结果如表8所示.表中,S/CO表示样品发光值和临界值的比值,下同.

表8 HBeAg试剂稳定性试验结果
本研究以成品检定技术指标等随贮存时间的变化来评价试剂盒的稳定性.根据国家对体外诊断试剂的质量要求规范,在37 ℃保温3 d,进行稳定性实验.表8数据表明该试剂盒稳定性符合要求.
4)HBeAb试剂稳定性试验.经筛选,确定HBeAb原料采用军科院的,并对此原料组成的试剂进行稳定性试验,结果如表9所示.

表9 HBeAb试剂稳定性试验结果
从表9可见,在37 ℃保温3 d下,试剂盒各项检定技术指标均符合国家对体外诊断试剂的质量要求,表明该试剂盒稳定性符合要求.
5)HBcAb试剂稳定性试验.经筛选,HBcAb原料灵敏度最好的原料为京达,对此原料组成的试剂进行稳定性试验,结果如表10所示.

表10 HBcAb试剂稳定性试验结果
本研究以成品检定技术指标等随贮存时间的变化来评价试剂盒的稳定性.根据国家对体外诊断试剂的质量要求规范,在37 ℃保温3 d,进行稳定性实验.从表10可见,该试剂盒稳定性符合相关要求.
2.2 乙肝表面抗原企业二级IU标准品制备
2.2.1 HBsAg 阳性血浆浓度估算 HBsAg 阳性血浆先用稀释液按1∶10 稀释后,按2 倍稀释成1∶20、1∶40、1∶80、1∶160、1∶320、1∶640 和1∶1 280 共8 个梯度.将国家线性参考品(表11)及稀释血浆分别制作曲线,结果如图1 所示.图1 中:x代表血浆浓度;Sn代表不同浓度下的发光值;S0代表浓度为0 时的发光值(下同).由图1 可见,国家线性参考品的相关系数为0.996 5,而稀释血浆线性的相关系数为0.974 4,但是两条线性接近平行,因此,实验结果可靠.由每个稀释血浆的标定结果乘以稀释倍数,可估算出HBsAg阳性血浆的浓度范围为3 000~3 500 IU·mL-1.
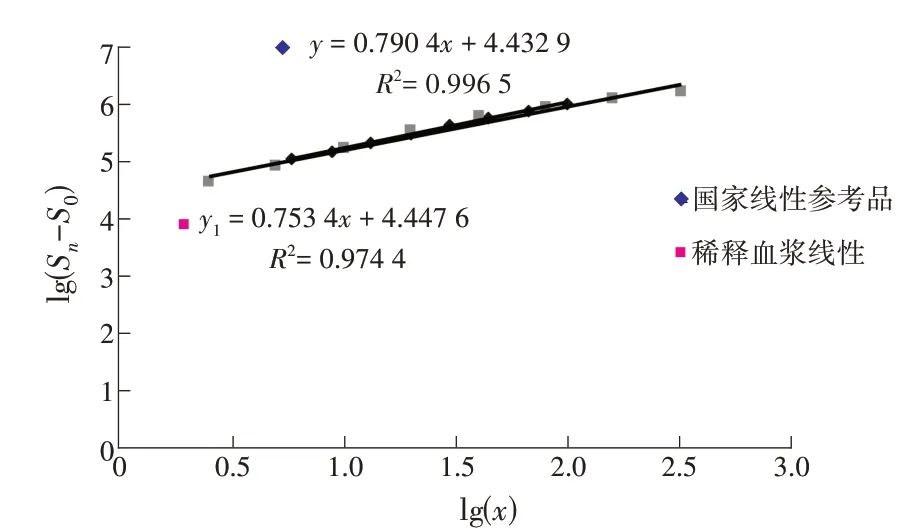
图1 国家线性参考品与稀释血浆线性比较

表11 表面抗原国家线性参考品
2.2.2 HBsAg强阳性血浆标定结果 HBsAg阳性血浆先用稀释液按1∶32稀释后,再按1.5倍和2倍分别系列稀释8个点,由国家线性参考品及优化试剂经双平行线方法进行标定,并进行t检验.结果如图2所示.

图2 HBsAg阳性血浆标定
由1.5倍梯度稀释制得的曲线为y1,2倍梯度稀释制得的曲线为y2.由曲线y1推算HBsAg阳性血浆的浓度值为3 200 IU·mL-1,而由曲线y2推算HBsAg 阳性血浆的浓度值为3 400 IU·mL-1,两者的偏差为4.29%,小于15%,因此符合检测试剂的变异范围.同时,对y1各稀释度的理论浓度及由国家线性参考品计算得出的浓度值进行t检验,检验得出P单尾值为0.024,小于0.05,因此,系统误差的可能性可以排除,说明实验结果可靠.由于曲线y1与国家线性参考品曲线y的重合性较好,且相关系数也较高,因此确定HBsAg阳性血浆的原始浓度值为3 200 IU·mL-1.
2.2.3 校准品配制 将已经确定好浓度值为3 200 IU·mL-1的HBsAg阳性血浆,用稀释液稀释成校准品所需要的浓度,对两条曲线采用双平行线法进行比较,结果如图3所示.
由图3 可以看出,校准品曲线y1与国家线性参考曲线基本上平行,并且重合性很好,同时校准品浓度值与发光值具有较好的相关性.
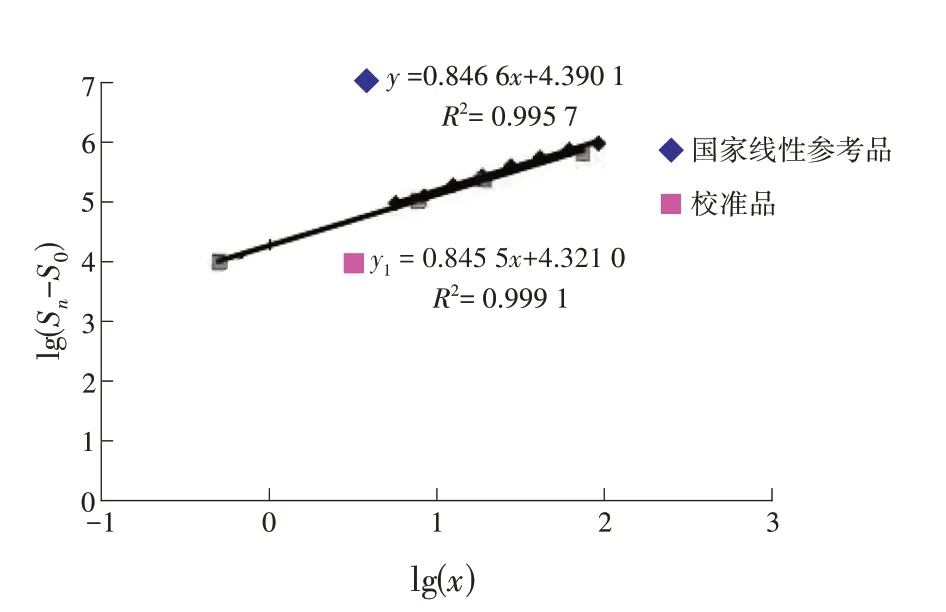
图3 校准品配制
2.3 乙肝两对半化学发光诊断试剂与进口同类产品的对比
以福建省内3 家三甲医院进口乙肝两对半化学发光诊断试剂的临床检测结果进行比对,共比对了280例血清标本,比对检测结果如下.
2.3.1 乙肝表面抗原试剂盒比对 1)表面抗原试剂盒检测结果为:总符合率为98.2%(275/280),特异性(阴性符合率)为100%(175/175),灵敏度(阳性符合率)为95.2%(100/105).2)表面抗原试剂盒定量检测值与进口雅培试剂盒的相关系数为0.97,表明HBsAg 定量诊断试剂盒(化学发光法)与进口雅培试剂盒的检测结果相关性佳.
2.3.2 乙肝表面抗体试剂盒比对1)表面抗体检测结果为:总符合率为98.2%(275/280),特异性(阴性符合率)为100%(149/149),灵敏度(阳性符合率)为96.2% (126/131).2)表面抗体与雅培试剂盒的相关系数为0.978,表明HBsAb定量诊断试剂盒(化学发光法)与雅培试剂盒检测结果的相关性好.
2.3.3 乙肝e 抗原试剂盒比对1)e 抗原的检测结果为:总符合率96.4%(270/280),特异性(阴性符合率)为100%(219/219),灵敏度(阳性符合率)为83.6%(51/61).2)对不符合的e 抗原检测结果分析,发现不符合的样本全都处于临界值范围.
2.3.4 乙肝E抗体试剂盒比对1)总符合率为96.0%(269/280),特异性(阴性符合率)为95.4%(212/222),灵敏度(阳性符合率)为98.2%(57/58).2)对不符合的样本进行分析,发现不符合的样本全部处于临界值范围.
2.3.5 乙肝核心抗体试剂盒比对 总符合率为97.1%(272/280),特异性(阴性符合率)为93.1%(27/29),灵敏度(阳性符合率)为97.6%(245/251).总符合率佳.
2.3.6 原试剂盒与雅培试剂盒的比对HBsAg、HBsAb、HBeAg、HBeAb、HBcAb 比对的总符合率分别为97.1%(272/280)、97.5%(273/280)、96.0%(269/280)、95.3%(267/280)、96.4%(270/280).
3 结论
本研究先筛选了生物活性原材料,从全国各地乙肝诊断试剂所用抗原抗体生物活性原材料生产厂家取得原材料小样,进行小试和比对实验,确定最优化的原材料组合.然后,重新标定乙肝两对半定量校准品,溯源至国家参考品(IU).用乙肝表面抗原的国家IU 标准品为溯源,制备乙肝表面抗原的企业二级IU标准品,并完成企业原纳克单位与IU单位的转换,结果准确.最后,在三甲医院进行临床比对,乙肝两对半诊断产品的符合率达96%以上,其中表面抗原、表面抗体试剂盒总符合率为98.2%;而比对的医院采用的是进口的雅培乙肝两对半化学发光诊断产品试剂.结果表明,本研究乙肝两对半产品的性能和质量指标达到进口产品水平.灵敏度试验表明,优化后的试剂灵敏度要比原试剂好,如HbsAg 和HBsAb 原试剂的S0与S1比值分别是0.32、0.41,而优化后的试剂S0与S1比值分别是0.25、0.27,灵敏度更好.稳定性试验比较结果表明,优化后的试剂批内精密度CV值均比优化前相对应的试剂更小,其他指标更优,说明稳定性更好.与Abbott 试剂检测结果的对比表明,优化后的试剂盒比原试剂盒总符合率更高,检测效果更好.可见,通过优选试剂生产所需的生物活性原材料,使乙肝两对半诊断试剂的产品性能,包括稳定性、重复性、批间和批内差、准确性等指标保持优异,可一定程度上提高我国乙肝体外诊断试剂与国外知名企业的竞争力.
化学发光免疫分析方法把酶标记手段与免疫反应相结合,兼具了放射性免疫学方法和酶免疫方法二者的优点,通过测定酶促反应释放的光子进行定量分析,具有很高的灵敏度,用于乙肝的血清学诊断,相比于酶联免疫吸附法和金标法等具有明显的优势.国产新型化学发光法乙肝系列诊断产品拥有巨大的市场潜力,但也面临着更加激烈的竞争,提高检测的精确度、稳定性必将是化学发光法乙肝血清学诊断产品保持竞争力的核心.乙肝血清学标志物诊断技术从定性到定量的发展,需要解决溯源准确性的问题.相对于乙肝5项标志物的定性检测产品,定量检测可以更好地监测病情、指导治疗、可预测血清学转换、预测乙肝病毒感染变化过程以及评价免疫效果[11,14],等等.因此,需要更科学准确的检测结果,检测结果的溯源性也必然是试剂生产的重要质量指标.
