阿托伐他汀手性中间体(R)-(-)-4-氰基-3-羟基丁酸乙酯制备工艺的研究
2022-03-15周怡孔祥儒胡成楠
周怡,孔祥儒,胡成楠
阿托伐他汀手性中间体(R)-(-)-4-氰基-3-羟基丁酸乙酯制备工艺的研究
周怡1,孔祥儒2,胡成楠1
(1. 抚顺顺能化工有限公司,辽宁 抚顺 113006; 2. 中国石油抚顺石化公司,辽宁 抚顺 113099)
提出了一种绿色环保的阿托伐他汀手性中间体(R)-(-)-4-氰基-3-羟基丁酸乙酯的制备工艺。该工艺采用化学-酶法合成,以(S)-环氧氯丙烷为起始原料,先与液体氢氰酸在碱催化作用下发生亲核加成反应得到(S)-(-)-4-氯-3-羟基丁腈;再用(S)-(-)-4-氯-3-羟基丁腈与氯化氢-乙醇发生Pinner反应得到亚氨酯的盐酸盐中间体,再水解得到(S)-(-)-4-氯-3-羟基丁酸乙酯;最后(S)-(-)-4-氯-3-羟基丁酸乙酯在生物酶的催化下与氢氰酸和氨水反应制得(R)-(-)-4-氰基-3-羟基丁酸乙酯。该制备工艺简单,反应条件温和,原子经济性高,其总收率可达到75%以上。
阿托伐他汀;手性中间体;(R)-(-)-4-氰基-3-羟基丁酸乙酯;化学-酶法合成
阿托伐他汀是由美国华纳-兰伯特公司开发的一种新型高效的他汀类降血脂药物,主要由母核和手性侧链组成,其中手性侧链是药物降血脂功能的关键部分。其调脂作用主要表现为,对胆固醇生物合成过程中的限速酶,3-羟基-3-甲基辅酶A (HMG-CoA)还原酶的抑制作用,减少细胞内的游离胆固醇,加速循环中极低密度脂蛋白(VLDL)残粒(IDL)和低密度脂蛋白(LDL)的清除,最终降低血清中总胆固醇和LDL的水平[1-2]。(R)-(-)-4-氰基-3-羟基丁酸乙酯是降血脂药物阿托伐他汀的关键手性中间体,其品质好坏直接影响着药品最终的质量。因此,开发反应条件更温和、原子经济性更高并且更加经济环保的制备方法和生产路线一直是医药领域的研究方向[3-5]。
目前文献中报道的(R)-(-)-4-氰基-3-羟基丁酸乙酯的合成方法主要为化学合成和化学-酶法合成。其中化学合成路线中最具有代表性的是洪华斌[6]等在2009年提出的以(S)-环氧氯丙烷为起始原料,经五步合成得到(R)-(-)-4-氰基-3-羟基丁酸乙酯,合成路线如图1。
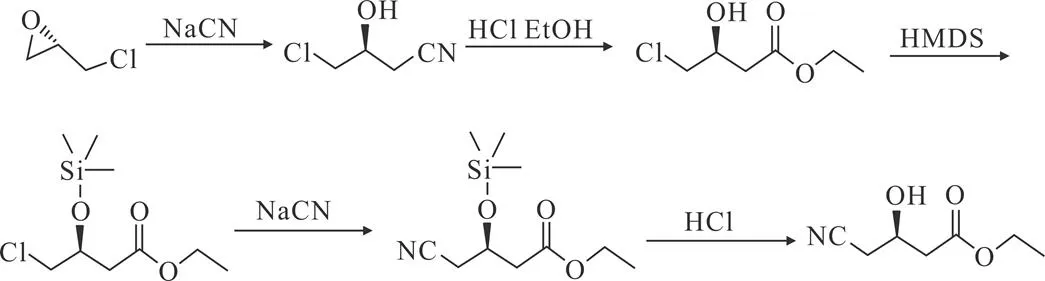
图1 (S)-环氧氯丙烷化学法制备(R)-(-)-4-氰基-3-羟基丁酸乙酯
孙丰来[7]专门针对(S)-4-氯-3-羟基丁酸乙酯化学法合成(R)-(-)-4-氰基-3-羟基丁酸乙酯进行了详细的研究。随后贾荣荣[8]等在此制备方法的基础上进行了一些优化改进,但仍然是以(S)-环氧氯丙烷为起始原料的纯化学制备的方法。化学-酶法合成路线是在纯化学法合成路线的基础上发展而来的,也是目前应用到工业化生产中比较成熟的技术路线,其中主流的工艺路线有两种:①以4-氯-乙酰乙酸乙酯为起始原料的两步合成法(见图2)。先以4-氯-乙酰乙酸乙酯为底物、NADPH为辅因子,用羰基还原酶不对称还原制备得到(S)-4-氯-3-羟基丁酸乙酯[9];或者是将4-氯-乙酰乙酸乙酯与固载Ru2Cl4(R-BINAP或Segphos)2NEt3的催化剂放入高压釜中,醇类溶剂,采用不对称氢化法制备得到(S)-4-氯-3-羟基丁酸乙酯[10]。然后再以(S)-4-氯-3-羟基丁酸乙酯为底物与卤醇脱卤酶,在pH值为6.5~8.0的条件下与氰化钠反应得到产品(R)-(-)-4-氰基-3-羟基丁酸乙酯[11]。②以手性还氧氯丙烷为起始原料的三步合成法(见图3)。先用手性环氧氯丙烷与硫酸和氰化钠反应得到S-4-氯-3-羟基丁腈,再用4-氯-3-羟基丁腈与盐酸乙醇反应得到S-4-氯-3-羟基丁酸乙酯,最后用S-4-氯-3-羟基丁酸乙酯在卤醇脱卤酶催化下与氰化钠和硫酸作用得到(R)-(-)-4-氰基-3-羟基丁酸乙酯[12]。而研究者们又专门针对第三步使用卤醇脱卤酶催化S-4-氯-3-羟基丁酸乙酯制备(R)-(-)-4-氰基-3-羟基丁酸乙酯中生物酶的筛选和固化上进行了大量的研究[13-15]。
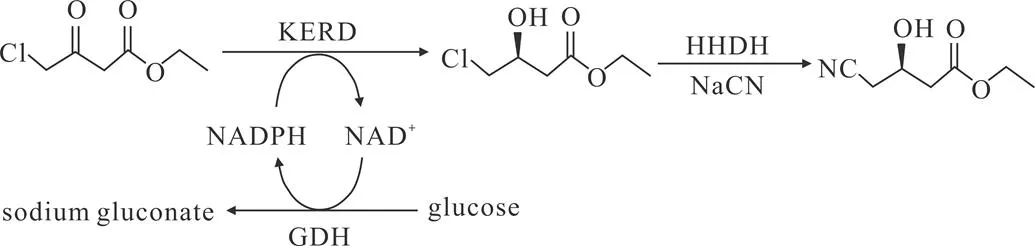
图2 4-氯乙酰乙酸乙酯两步酶法制备(R)-(-)-4-氰基-3-羟基丁酸乙酯
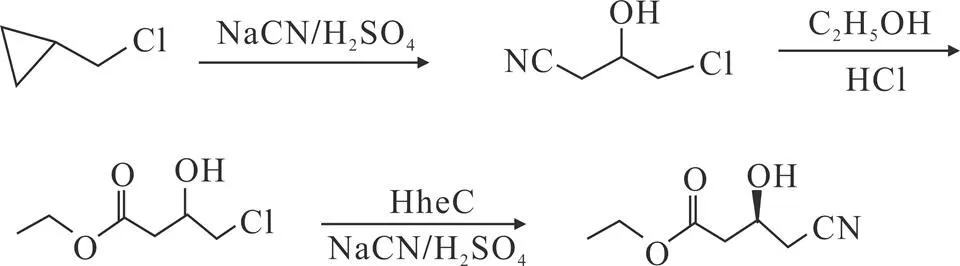
图3 (S)-环氧氯丙烷化学-酶法制备(R)-(-)-4-氰基-3-羟基丁酸乙酯
笔者公司在以手性环氧氯丙烷为起始原料化学-酶法合成(R)-(-)-4-氰基-3-羟基丁酸乙酯工艺路线的基础上进行了优化改良,提出了一种更加绿色环保的制备新工艺[16]。该制备方法是以(S)-环氧氯丙烷和液体氢氰酸为起始原料反应得到(S)-(-)-4-氯-3-羟基丁腈;再将所得的(S)-(-)-4-氯-3-羟基丁腈与氯化氢-乙醇得到(S)-(-)-4-氯-3-羟基丁酸乙酯;之后将(S)-(-)-4-氯-3-羟基丁酸乙酯与氢氰酸和脱卤酶反应得到(R)-(-)-4-氰基-3-羟基丁酸乙酯。本文将对该制备工艺的相关研究进行进一步的论述说明。
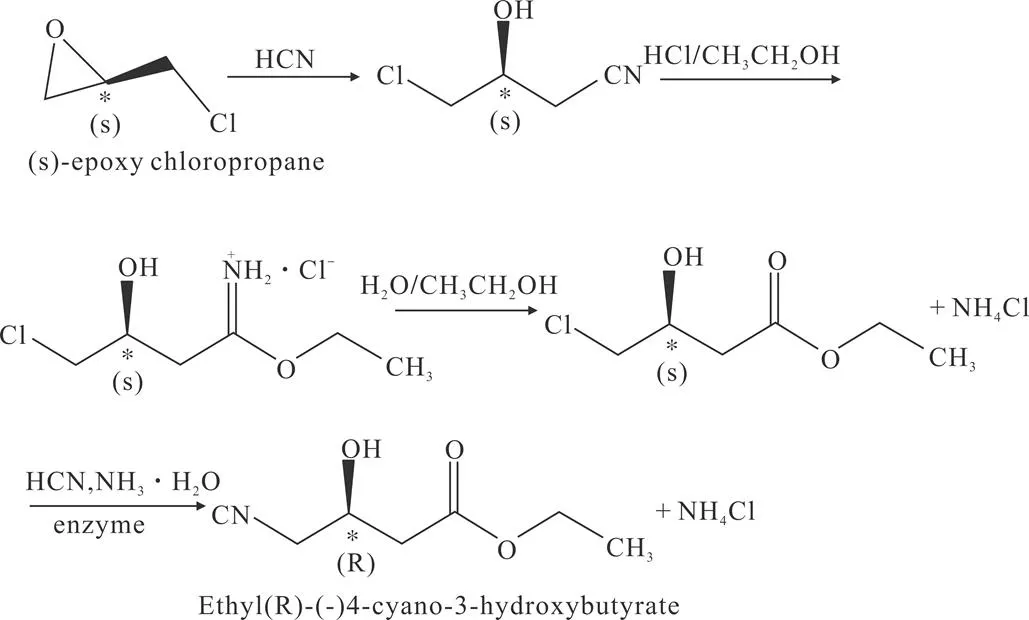
图4 改进后的(S)-环氧氯丙烷化学-酶法制备(R)-(-)-4-氰 基-3-羟基丁酸乙酯
1 实验部分
1.1 样品分析检测条件
气相色谱分析:采用福立GC-9790Plus气相色谱仪带FID检测器,色谱柱类型为SE-54色谱柱,柱长30 m,柱内径0.32 mm,柱填料0.33 μm;色谱条件为柱前压(高纯氮气,>99.99%)0.1 MPa,空气0.1 MPa,氢气0.1 MPa,总压0.3 MPa;柱温为程序升温,初温60 ℃,保持时间1 min;升温速率为20 ℃·min-1,终温250 ℃,保持时间10 min;进样口230 ℃,检测器250 ℃。
旋光度测试:采用WZZ-3旋光仪,按GB/T 613—2007化学试剂比旋度测定通用方法测定。
核磁共振结构鉴定:样品送至中科院化学所分析测试中心进行检测。
1.2 (S)-(-)-4-氯-3-羟基丁腈的制备
将100 g(1.08 mol)(S)-环氧氯丙烷、200 g水和2 g二乙胺一次性加入1 000 mL三口瓶中,搅拌混合5 min得到混合溶液,在25 ℃的条件下以每秒1~2滴的速度在上述混合溶液中加入43.8 g (1.62 mol)液体氢氰酸,25 ℃条件下继续搅拌反应6 h得到反应液,用50%的硫酸调节所述反应液的pH值至5,减压蒸馏除去水,然后高真空精馏得到122.5 g (S)-(-)-4-氯-3-羟基丁腈,摩尔收率为94.96%。分析检测结果:气相含量99.34%(见图5),比旋度[]D25=-17.0°。
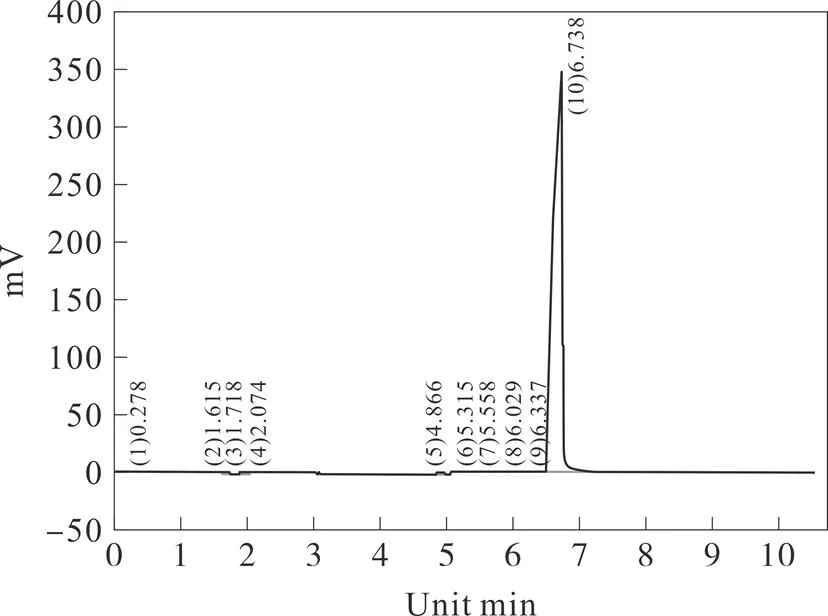
图5 (S)-(-)-4-氯-3-羟基丁腈的气相谱图
1.3 (S)-(-)-4-氯-3-羟基丁酸乙酯的制备
将400 g氯化氢-乙醇溶液(其中HCl质量分数为35.5%,水分为0.40%)加入1 000 mL三口瓶中,取100 g(0.836 mol)(S)-(-)-4-氯-3-羟基丁腈在40 ℃的条件下以每秒1~2滴的速度缓慢加入上述氯化氢-乙醇溶液中,40 ℃条件下继续搅拌反应1 h,减压蒸除未反应的氯化氢-乙醇得到黏稠的反应液。向上述反应液中加入300 g含水乙醇(其中含水22.5 g(1.25 mol)),在80 ℃条件下继续搅拌反应8 h,减压蒸除乙醇,离心过滤除去其中的氯化铵,然后高真空精馏得到124g (S)-(-)-4-氯-3-羟基丁酸乙酯,摩尔收率为89.21%。分析检测结果:气相含量99.36%(见图6),比旋度[α]D25=-17.8°。
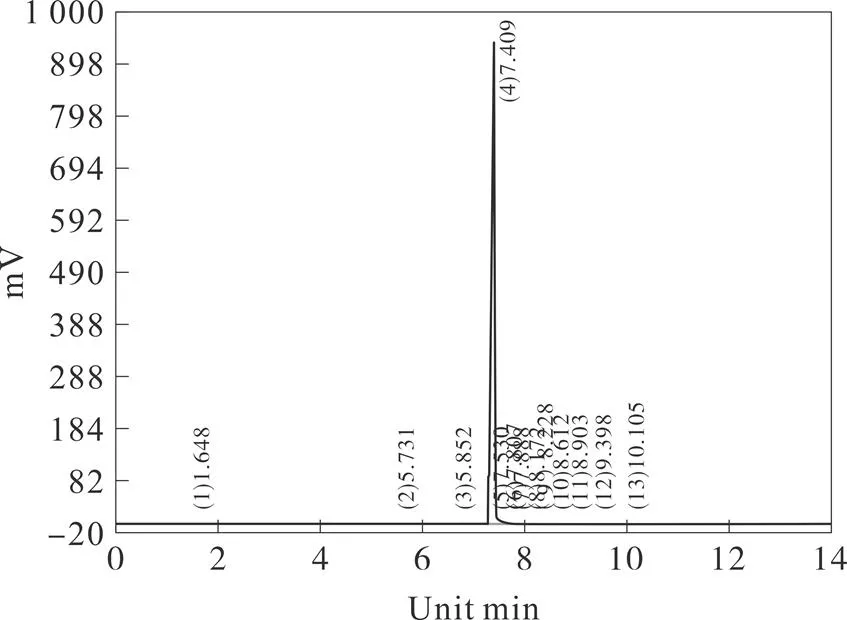
图6 (S)-(-)-4-氯-3-羟基丁酸乙酯的气相谱图
1.4 (R)-(-)-4-氰基-3-羟基丁酸乙酯的制备
取100 g(0.600 mol)(S)-(-)-4-氯-3-羟基丁酸乙酯和500 g氯化铵-氨水缓冲溶液一次性加入 1 000 mL三口瓶中,搅拌混合5 min得到混合溶液,20 ℃的条件下以每秒3~4滴的速度在上述混合溶液中加入48.6 g(1.80 mol)液体氢氰酸,继续搅拌10 min得到混合溶液,向上述反应液中加入8 g 卤醇脱卤酶,根据反应的进行情况向上述混合溶液中滴加质量分数为10%的氨水使反应液的pH值始终维持在6.8~7.0之间,在48~49 ℃条件下搅拌反应6 h,然后减压蒸除水,离心过滤除去其中的氯化铵和脱卤酶,最后高真空精馏得到84.9 g (R)-(-)-4-氰基-3-羟基丁酸乙酯,摩尔收率为90.00%。分析检测结果:气相含量99.46%(见图7),比旋度[α]D25=-33.3°。此外,还对最终产物(R)-(-)-4-氰 基-3-羟基丁酸乙酯进行了结构鉴定,其核磁共振氢谱和碳谱见图8和图9。
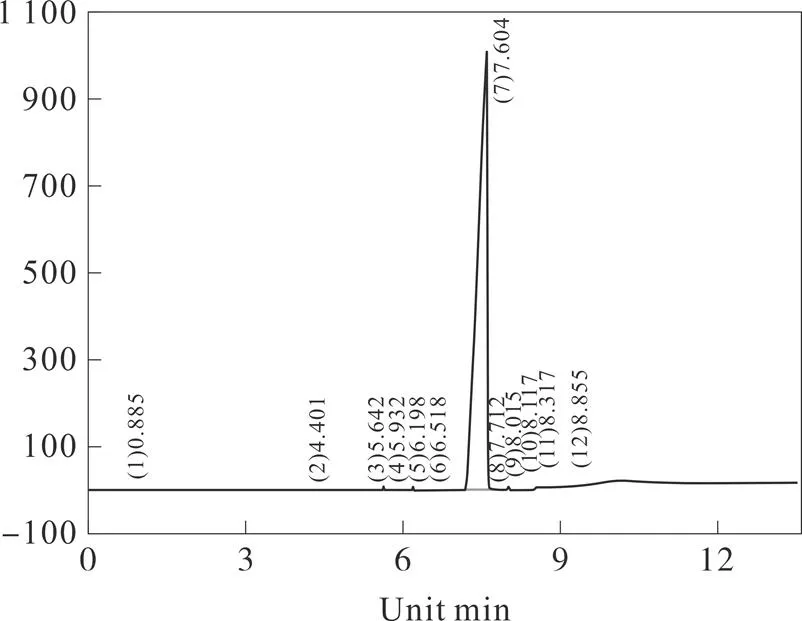
图7 (R)-(-)-4-氰基-3-羟基丁酸乙酯的气相谱图
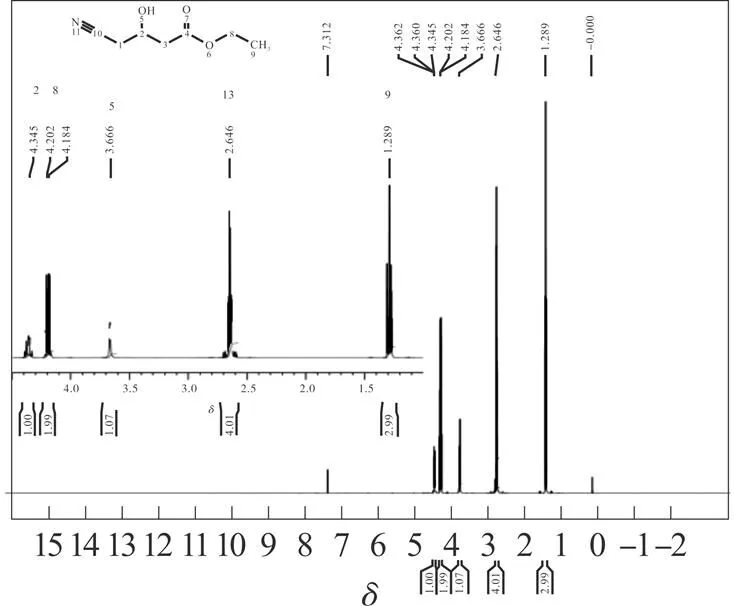
图8 (R)-(-)-4-氰基-3-羟基丁酸乙酯的核磁共振氢谱图
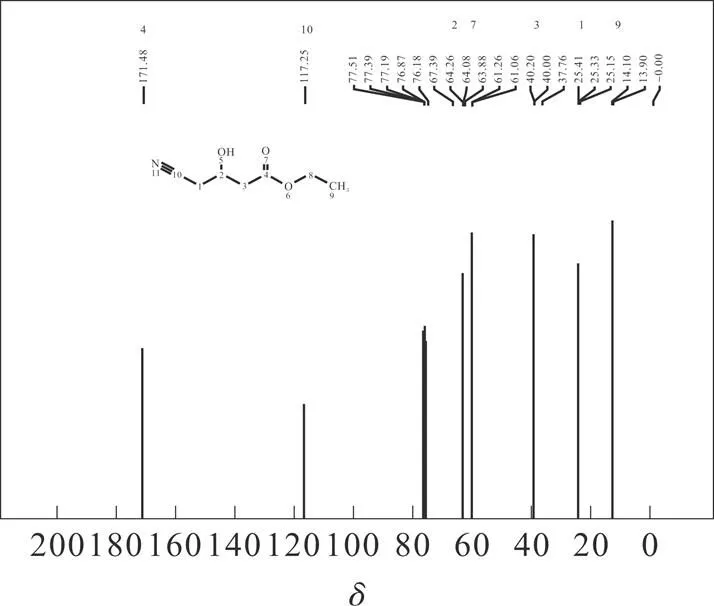
图9 (R)-(-)-4-氰基-3-羟基丁酸乙酯的核磁共振碳谱图
2 结果与讨论
在系统性研究该制备工艺的过程中发现,在(S)-(-)-4-氯-3-羟基丁酸乙酯的制备过程中,若使用的氯化氢-乙醇中氯化氢的浓度太低或含水量太高都将严重影响Pinner反应的反应速度和反应效果;若水解前不将未反应完的氯化氢-乙醇蒸除,氯化氢与水形成盐酸会导致反应液的酸度较高,在水解过程中容易导致生成的(S)-(-)-4-氯-3-羟基丁酸乙酯进一步水解成(S)-(-)-4-氯-3-羟基丁酸,使得收率下降;若Pinner反应完成后不加水进行水解反应,生成的亚氨基酯的盐酸盐中间体则会继续和反应液中过量的乙醇反应进一步生成原酸酯,最后在氯化氢(酸)的催化下脱除一分子乙醇和一分子氯乙烷后也能得到(S)-(-)-4-氯-3-羟基丁酸乙酯,但此过程中产生的废气氯乙烷将额外增加废气的后处理成本。氯乙烷的产生机理如图10。本发明在(S)-(-)-4-氯-3-羟基丁酸乙酯的制备过程中采用了分步处理,在Pinner反应完成后及时进行未反应底物的蒸除。同时,在水解前通过添加含水乙醇,进行水解反应有效地避免废气氯乙烷的产生。
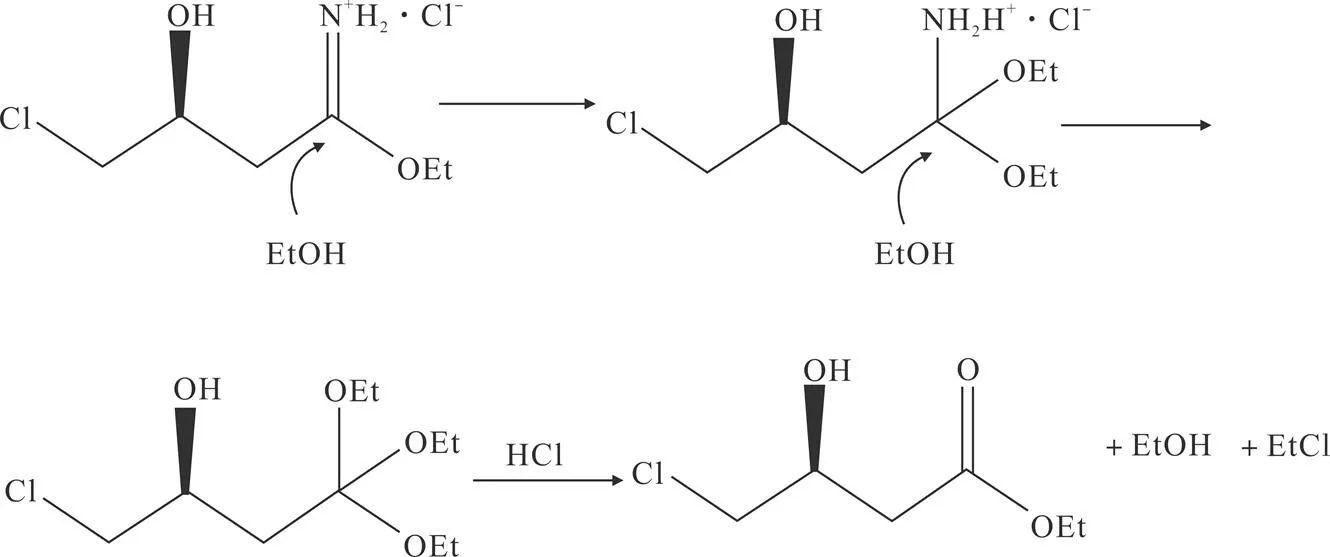
图10 制备(S)-(-)-4-氯-3-羟基丁酸乙酯过程中氯乙烷的产生机理图
本工艺最后一步制备(R)-(-)-4-氰基-3-羟基丁酸乙酯的过程中,现有制备方法中该步骤使用的原料普遍为氰化钠和硫酸,二者相互反应之后可生成氢氰酸和硫酸钠,生成的氢氰酸再与(S)-(-)-4-氯-3-羟基丁酸乙酯反应得到(R)-(-)-4-氰基-3-羟基丁酸乙酯,反应脱下来的Cl-与反应液中的Na+反应又会得到氯化钠盐,使得反应液中含有两种不同的碱金属盐类(硫酸钠和氯化钠),后处理困难[12]。因此,直接选用氢氰酸作为原料不仅可以提高反应效率,而且可以避免含氰废盐的生成。此外,酶促反应因其特殊性,酶对反应的温度和反应液的pH值均较为敏感:温度太低,则酶活性较低,反应速度较慢;而温度太高又会破环酶蛋白的结构导致其变质失活;每种生物酶都有其最佳的反应pH值,pH值的过高和过低都会使其活性降低甚至失活[15]。因此,针对现有制备方法在这方面的不足,一方面,可以采用缓冲溶液的反应体系,避免反应过程中体系的pH值有较大的波动;另一方面,可通过滴加氨水(碱)的方式及时中和掉反应生成的Cl-形成氯化铵盐,从而维持了反应的高效进行,后处理时反应液浓缩析出的氯化铵盐还可以作为副产品处理。最后,在高活性脱卤酶的催化作用下,通过对反应温度和反应液pH值的精细控制,实现了对反应物的高效转化,从而获得了较高的产品收率。
3 结 论
相较于现有的制备工艺,本文提供的(R)-(-)-4-氰基-3-羟基丁酸乙酯的制备工艺具有以下3个方面的有益效果:
1)以廉价易得的(S)-环氧氯丙烷和丙烯腈生产过程中的副产物氢氰酸为原料,生产成本较低,氢氰酸液体产于产物合成,副产物少,原子经济性高。
2)制备工艺简单,工业化生产易实现,产物的化学纯度和光学纯度均较高。
3)整个制备工艺中,不使用有机溶剂,不产生含盐废水、废气等,符合绿色精细化学的设计理念,也更具市场竞争力。
[1]刘伟. 阿托伐他汀中间体合成的研究[D]. 北京:北京化工大学,2006.
[2]梁玉霞. 瑞舒伐他汀和阿托伐他汀侧链的合成[D]. 天津:天津大学,2016.
[3]陈阳,张磊.利伐沙班的合成研究[J].辽宁化工,2021,50(1):9-11.
[4]刘洪杰,周鹏. 氨氯地平分散片的产业化研究[J].辽宁化工,2020,49(12):1484-1485.
[5]李立标,林文龙,郑爱,等. 盐酸利多卡因的合成工艺研究[J]. 辽宁化工,2020,49(9):1078-1080.
[6]洪华斌,蒋成君. (R)-(-)-4-氰基-3-羟基丁酸乙酯的制备[J]. 中国医药工业杂志,2009,40(7):486-487.
[7]孙丰来. 化学酶法制备他汀药物关键手性中间体的研究[D]. 杭州:浙江大学,2007.
[8]贾荣荣,解美仙,周进辉,等. 阿伐他丁中间体4-氰基-3-羟基丁酸乙酯的制备新工艺:CN 102627580A[P]. 2012-08-08.
[9]严明,郝宁,沙风,魏淼. 一种酶法不对称还原制备(S)-4-氯-3-羟基丁酸乙酯的方法[P]. 南京工业大学, CN 103290072,2013.
[10]刘庆彬,李耀峰,李立斌,等. 一种光学纯度的S-4-氯-3-羟基丁酸乙酯的制备方法:CN 103145557A[P].2013-06-12.
[11]汪斌,梁国斌,刘维桥,等. (R)-(-)-4-氰基-3-羟基丁酸乙酯的制备方法:CN105132488A[P].2015-12-09.
[12]付瑞新,王明. (R)-(-)-4-氰基-3-羟基丁酸乙酯的生物耦合制备方法:CN101914582A [P].2010-12-15.
[13]许成兵,鲍烨烨,鲍甜甜,等. 一种树脂固定卤醇脱卤酶催化合成(R)-4-氰基-3-羟基丁酸乙酯的工艺:CN 105368886A[P].2016-03-02.
[14]陈少云. 氧化还原酶-卤代醇脱卤酶多酶法合成手性β-羟基腈[D]. 杭州:浙江大学,2013.
[15]万南微. 卤醇脱卤酶的表达、改造及其在(R)-4-氰基-3-羟基丁酸乙酯合成中的应用[D]. 杭州:浙江工业大学,2015.
[16]周怡,胡成楠,王晓宁,等. 一种(R)-(-)-4-氰基-3-羟基丁酸乙酯的绿色环保制备方法:CN 109628511A[P].2019-04-16.
Study on Synthetic Technology of Atorvastatin’S Chiral Intermediate Ethyl (R)-(-)-4-Cyano-3-hydroxybutanoate
1,2,1
(1. Fushun Shunnun Chemical Co., Ltd., Fushun Liaoning 113006, China;2. PetroChina Fushun Petrochemical Company, Fushun Liaoning 113099, China)
An environmental friendly synthetic technology of atorvastatin’s chiral intermediate ethyl (R)-(-)-4-cyano-3- hydroxybutanoate was put forward. This is a chemoenzymatic synthesis process, which uses (S)-epichlorohydrin as starting material. Firstly,under the action of a basic catalyst, (S)-epichlorohydrin reacts with hydrocyanic acid to form (S)-(-)-4-chloro-3- hydroxybutanenitrile. Secondly, Pinner reaction happens between (S)-(-)-4-chloro-3-hydroxybutanenitrile and hydrogen chloride- ethyl alcohol to get imine ester hydrochloride intermediate, then it hydrolyzes to form ethyl (S)-(-)-4-chloro-3-hydroxybutyrate. Finally, under the catalysis of bio-enzyme, (S)-(-)-4-chloro-3-hydroxybutyrate reacts with hydrocyanic acid and ammonium hydroxide to form the product of (R)-(-)-4-cyano-3-hydroxybutanoate. This synthetic technology is very simple with mild reaction conditions and high atom economy, the total recovery is over 75%.
Atorvastatin; Chiral intermediate; Ethyl (R)-4-cyano-3-hydroxybutanoate; Chemoenzymatic synthesis
TQ073
A
1004-0935(2022)02-0174-05
2021-07-20
周怡(1993-),女,重庆市长人,中级注册安全工程师,理学硕士, 2017年毕业于四川大学物理化学专业,研究方向:医药中间体研发。
