超高效液相色谱串联质谱法测定环境样品中高氯酸盐和氯酸盐的含量
2022-03-13王娟刘阿静王新潮张晓美王波
王娟 刘阿静 王新潮 张晓美 王波
(兰州海关技术中心 甘肃兰州 730030)
1 前言
高氯酸盐和氯酸盐均具有极强的氧化性,在航空航天业的固体推进剂、炸药和烟火制造方面被广泛作为氧化剂使用[1-2]。近年来,随着经济的快速发展,工业生产方面使用的高氯酸盐和氯酸盐越来越多,而高氯酸盐的正四面体结构使其具有高度的化学稳定性和良好的迁移性,加之其极易溶于水,因此极易造成土壤及地下水污染,随着土壤和水被植物吸收,高氯酸盐开始富集进入人体[3]。
氯酸盐是消毒过程中产生的副产物,进入人体后会引起血液学反应,损害红细胞以影响血氧的运输功能。高氯酸盐的分子结构与碘分子相似,因此可以阻止甲状腺对碘的吸收,导致甲状腺激素T3和T4的合成量减少[4],影响甲状腺功能[5-6],干扰人体的新陈代谢。有研究报道,在水果、蔬菜、大米、茶叶、饮用水、饲料、畜禽肉及其副产品等农产品中均有高氯酸盐和氯酸盐的检出[7-13],由此可见氯酸盐、高氯酸盐在农产品中已广泛存在,而这种现象的产生与土壤、灌溉水资源具有密切联系。2020年5月25日,欧盟委员会发布(EU)2020/685号条例,修订高氯酸盐在部分食品中的最大残留限量。而我国对于氯酸盐、高氯酸盐污染的研究尚处在起步阶段,无土壤中氯酸盐和高氯酸盐检测的相关标准,缺乏系统的研究数据。因此,建立环境样品(如水体、土壤)中氯酸盐和高氯酸盐的检测方法刻不容缓。
目前,氯酸盐和高氯酸盐的检测方法主要有拉曼光谱法[14]、分光光度法[15]、离子色谱法[16-18]、离子色谱-质谱法[19]、液相色谱串联质谱法[20]等。其中,拉曼光谱法需使用金、银等作为基底,检测成本极高;分光光度法常需使用有毒试剂,安全隐患大,且操作复杂、重现性差;离子色谱法常会受到其他共存离子的干扰,易出现假阳性,灵敏度较低;离子色谱-质谱法在样品处理过程中常需添加酸、碱及盐,而质谱仪接口对酸、碱及金属盐的耐受性较差,需增加专业抑制器组件或手动去酸、碱及盐,造成检测成本和工作量的增加,易因人为操作不当造成对仪器设备的损害。
本文采用超高效液相色谱串联质谱法同时检测水体和土壤样品中的高氯酸盐和氯酸盐,用内标法定量,并将所建立的方法用于100批环境样品中氯酸盐和高氯酸盐的检测,以期为环境中高氯酸盐和氯酸盐的监测及标准制定提供科学的数据支撑。
2 材料与方法
2.1 仪器与试剂
液相色谱质谱联用仪(美国Agilent 6460C,配有电喷雾离子源ESI);离心机(美国SIGMA,3K30);涡旋仪(逗点生物,BC-1000);分析天平(德国Sartorius,BSA822)。
甲醇、乙腈、二氯甲烷、甲酸(德国默克,色谱纯);乙酸、甲酸铵、乙酸铵(国药集团,分析纯);超纯水(屈臣氏);高氯酸盐标准物质、氯酸盐标准物质(北京北方伟业计量技术研究院,1000μg/mL);高氯酸盐内标标准物质(HCLO4-O4)、氯酸盐内标标准物质(ClO3-18O13)(ANPEL,100μg/mL);HLB固相萃取柱(3cc,60 mg)。
样品来源:100批环境样品,部分按照《HJ/T 166-2004》、《HJ 25.2-2014》和《HJ/T 91-2002》自行采样,部分由陇南市祥宇油橄榄开发有限责任公司提供。其中,水体样品50批,随机在兰州市辖区不同区域、不同河道自行采样30批,陇南市祥宇油橄榄开发有限责任公司提供20批,采样地点包含陇南市及其各乡镇,样品涵盖生活饮用水、农田灌溉水;土壤样品50批,自行采样40批,采样地点遍布大棚蔬菜种植土壤、旱地粮食作物种植土壤、河边泥土,陇南市祥宇油橄榄开发有限责任公司提供10批不同橄榄果树种植基地及附近土壤。
2.2 色谱条件
色谱柱:Thermo Acclaim Trinity P1复合离子交换柱(50 mm×2.1 mm,3μm);柱温:30℃;进样量:2μL;流速:0.3 mL/min;流动相A:20 mmol/L甲酸铵,B相:乙腈;梯度洗脱程序:0~0.5 min,A为65%;0.5~4 min,A从65%下降至40%,4~5 min,A从40%下降至10%;5~6 min,A为10%;6~7 min,A从10%上升至65%;7~10 min,A保持65%不变。
2.3 质谱条件
离子源:电喷雾离子ESI(-);干燥气温度:300℃;干燥气流速:10 I/min;雾化气压力:45psi;毛细管电压:3.5 KV;鞘气温度:250℃;鞘气流量:5 I/min;喷嘴电压:1 000 V;检测方式:多反应监测(MRM)模式采集数据,具体参数见表1。

表1 高氯酸盐和氯酸盐定性、定量离子对和质谱分析参数
2.4 标准溶液的配制
高氯酸盐标准储备液:准确吸取100μL高氯酸盐标准物质(1 000 mg/L),用超纯水定容至100 mL,配制成1.00 mg/L标准储备液,-20℃保存。
氯酸盐标准储备液:准确吸取100μL高氯酸盐标准物质(100 mg/L),用超纯水准确定容至10 mL,配制成1.00 mg/L标准储备液,-20℃保存。
高氯酸盐内标(HClO4-O4)、氯酸盐内标(CLO3-18O13)混合标准储备液:准确吸取100μL高氯酸盐、氯酸盐内标标准物质(100 mg/L),用超纯水定容至10 mL,配制成1.00 mg/L标准储备液,-20℃保存。
高氯酸盐、氯酸盐混标工作曲线:分别配制高氯酸盐浓度为:0.05、0.1、0.2、0.5、1、2、5、10、20、50、100μg/L,氯 酸 盐 浓 度 为0.1、0.2、0.5、1、2、5、10、20、50、100、200μg/L的标准曲线,其中高氯酸盐和氯酸盐内标标准溶液的浓度均为2μg/L,现配现用。
2.5 样品的前处理
2.5.1 水体样品
准确移取980μL试样,加入20μL高氯酸盐内标(HClO4-O4)、氯酸盐内标(CLO3-18O13)混合标准储备液(100μg/L);涡旋混匀,过0.22μm水系滤膜,待测。
2.5.2 土壤样品
称取土壤样品(自然风干,缩分,过0.25 mm筛)2.00 g于50 mL离心管中;加入50μL高氯酸盐内标(HClO4-O4)、氯酸盐内标(CLO3-18O13)混合标准储备液(1.00 mg/L);加入25 mL 0.2%乙酸水,高速涡旋5 min;加入5 mL二氯甲烷,涡旋1 min;10 000 r/min离心5 min;取上清5 mL过HLB固相萃取柱(预先用6 mL的超纯水和6 mL甲醇活化)净化,前2 mL流出液弃去;过0.22μm水系滤膜,待测。
3 结果与分析
3.1 土壤样品前处理优化
3.1.1 提取时间的优化
本试验考察1、2、5、10 min这4个不同的提取时间对提取效率的影响,从图1可以看出,随着提取时间的增加,高氯酸和氯酸盐的回收率呈现先上升后下降的趋势;当提取时间为5 min时,高氯酸盐和氯酸盐的添加回收率最高;当提取时间从5 min增加至10 min时,回收率明显降低。由此可知,提取时间为5 min时,目标化合物已经得到充分提取,本文最终选择高速涡旋5 min作为土壤样品的提取时间。
3.1.2 提取溶剂的优化
本文分别考察0.2%乙酸水溶液、甲醇、1%甲酸乙腈溶液、乙腈和50%乙腈水溶液作为提取溶剂时,高氯酸和氯酸盐回收率的变化。从图2可以看出,乙酸水溶液和乙腈作提取溶剂时,二者的提取率在整体上明显优于甲醇;当用乙腈和0.2%乙酸水溶液提取时,二者的回收率响应值最高;用乙腈提取时二者的回收率分别为90%和91%,0.2%乙酸水提取时二者的回收率分别为88%和93%。由此可见,2种提取溶剂均能满足试验要求,从节约成本及试剂安全性方面考虑,本文最终选择0.2%乙酸水溶液作为提取试剂。
3.1.3 土壤样品中提取试剂加入次序的优化
本文重点考察样品中提取试剂添加次序的影响:一组土壤样品中先加入5 mL二氯甲烷,再加入25 mL 0.2%的乙酸溶液;另一组土壤样品中先加入25 mL 0.2%的乙酸溶液,再加入5 mL二氯甲烷,其它测试条件不变。由检测结果可知,先加入提取试剂二氯甲烷时,土壤样品中目标物的添加回收率仅为30%,后加入二氯甲烷时,样品中目标物的回收率均高于80%。
分析原因可能为:二氯甲烷具有较强的渗透性,能够快速渗透在土壤样品中将目标物包裹;二氯甲烷为非极性化合物,当加入0.2%乙酸溶液时,二者由于极性的不同使得萃取能力瞬间下降,从而导致目标物提取率减少;反之,当先加入0.2%乙酸溶液时,目标化合物迅速溶于水,而二氯甲烷不溶于水,目标化合物能够更好地在样品中保留,而不被二氯甲烷包裹。
3.2 色谱条件的优化
3.2.1 色谱柱的优化
本文分别考察了3款不同固定相的色谱柱Waters ACQUITY UPLC BEH C18(50 mm×2.1 mm,1.7μm)、Waters ACQUITY UPLC HSS T3(50 mm×2.1mm,1.8μm)和Thermo Acclaim Trinity P1(50 mm×2.1mm,3μm)对目标物的分离效果,从图3可以看出,C18和T3色谱柱均对目标化合物不保留,即使调节流动相组成和洗脱梯度,色谱图也无法得到理想的改善,无法将目标化合物与杂质进行有效分离;而Thermo Acclaim Trinity P1能够实现高氯酸盐和氯酸盐的有效分离,峰形规整,尖锐,分离度>1.5,这可能是因为Thermo Acclaim Trinity P1色谱柱是一种混合模式色谱柱,采用独特的多模式表面化学键合相,固定相采用纳米杂化硅聚合物(带电荷纳米高分子微球的高纯多孔球形颗粒),单填料具备反相、阳离子和阴离子交换功能,使得其可以保留离子和可离子化的分析物。因此,本文最终选取Thermo Acclaim Trinity P1色谱柱。
3.2.2 流动相的优化
本文分别考察纯水、0.1%甲酸水溶液、5 mmoL/L乙酸铵溶液和20 mmoL/L甲酸铵溶液作为水相流动相时,目标化合物的分离效果。结果显示,20 mmoL/L甲酸铵溶液作为水相流动相时,分离效果最好,峰形尖锐,目标物响应值最高;纯水为水相流动相时目标化合物分离度低,峰展宽较宽,峰面积响应值低,即纯水不利于目标化合物在Thermo Acclaim Trinity P1色谱柱上的洗脱。
采用ESI(-)扫描时,甲酸对其产生抑制作用,不利于氯酸盐和高氯酸盐的有效分离,进而影响目标物结果的准确性。但在水相流动相中加入盐之后,目标化合物的离子化率开始有明显提升,同一浓度的标准品峰面积响应值增涨了2倍以上,可见20 mmoL/L甲酸铵谱图峰形更好,峰面积响应更高。因此,本文最终选用流动相为乙腈和20 mmoL/L甲酸铵溶液。
4 方法学考察
以内标法定量,采用安捷伦定量分析软件进行分析,以氯酸盐和高氯酸盐与其内标的比值相对响应值为纵坐标,以相对浓度为横坐标,绘制曲线。由表2可知,高氯酸盐在0.05~100μg/L线性范围内线性关系良好,R2=0.999 7;氯酸盐在0.20~100μg/L线性范围内线性关系良好,R2=0.999 2。高氯酸盐、氯酸盐的检出限以3倍的信噪比(S/N=3)计算,分别为0.025μg/L、0.20μg/L;定量限以10倍的信噪比(S/N=10)计算,分别为0.05μg/L、1.0μg/L。
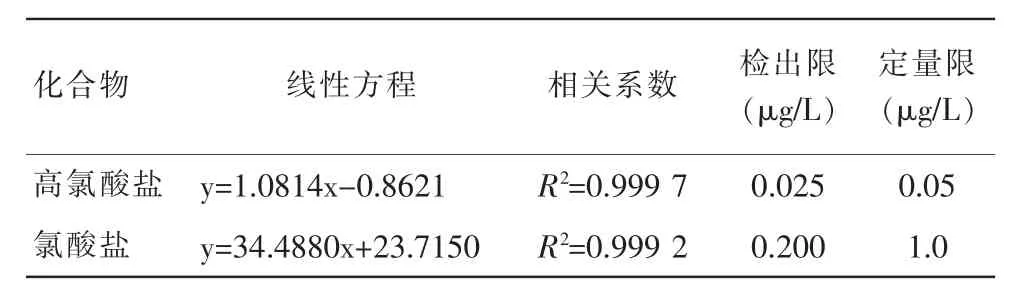
表2 线性范围、相关系数、检出限及定量限表
在水体样品中分别添加低、中、高(1、10、100μg/L)3种浓度的氯酸盐、高氯酸混合标准溶液,考察方法的回收率和日内日间精密度,最终测得回收率在95%~105%之间,RSD<4%,其中10μg/L添加6平行最终测得RSD<3%;在土壤样品分别添加低、中、高(1、10、100μg/L)3种浓度的氯酸盐、高氯酸混合标准溶液,测得回收率在80%~108%之间,RSD<5%,其中10μg/L添加6平行最终测得RSD<5%。试验结果表明,该方法重现性较好,样品加标回收率高,且相对标准偏差较小。
5 实际样品的测定
采用本文的优化方法测定环境样品中的氯酸盐和高氯酸盐的含量,结果见图4和图5。由结果可知,所有土壤样品中均检测出高氯酸盐(>0.025μg/kg),检出率为100%;氯酸盐检出36批(>0.2μg/kg),检出率为72%;水体样品中高氯酸盐的检出8批,检出率为16%,远远低于2017年世界卫生组织发布的高氯酸盐的限值(0.07 mg/L)[21],但高于美国环保局规定的生活饮用水中高氯酸盐的规定限值(1.0μg/L)[22];氯酸盐检出28批,检出率为56%,但所有检出值均低于我国生活饮用水卫生标准(GB 5749-2006)中的规定限值(0.7 mg/L)[23]。由此可见,兰州及陇南辖区的部分地区存在氯酸盐和高氯酸盐污染的情况,农户及规模化种植中药材、蔬菜水果的场地应对高氯酸和氯酸盐予以监测。
6 结论
本文建立了超高效液相色谱串联质谱法测定环境样品(水体、土壤)中高氯酸盐和氯酸盐含量的方法,该方法用同位素内标法定量,一定程度上消除了操作条件等因素变化所引起的误差,定量准确;水体样品直接过膜进样,降低了前处理的成本;土壤样品前处理使用固相萃取净化,有效消除了基质干扰。
该方法灵敏度高、重现性好、准确度高,可用于常规水体、土壤等环境样品中氯酸盐、高氯酸盐的检测,能够为我国生活饮用水等环境样品中高氯酸盐和氯酸盐标准的制定提供可靠的数据支撑。
