虎杖苷十一碳烯酸酯的酶法合成与动力学研究
2022-03-11刁怡涵李明依毕艳红杜文迎杨荣玲王朝宇
刁怡涵 李明依 毕艳红 杜文迎 杨荣玲 王朝宇
(淮阴工学院生命科学与食品工程学院, 江苏 淮安 223003)
黄酮苷类化合物是自然界中普遍存在的一类植物多酚代谢产物,具有独特的化学结构及生物和药理活性[1-2]。在保持该类化合物基本骨架结构的基础上,对某些官能团进行化学修饰是当前天然产物类新药开发的重要手段之一[3]。天然产物化学家David J. Newman分析了34年来FDA(Food and Drug Administration)批准上市的1 562种天然产物类药物,发现46%的药物是携带有天然药效基团的衍生物或者类似物[4]。
虎杖苷(Ploydatin)是中药材虎杖(ReynoutriajaponicaHoutt)的主要药效成分,具有改善心肌损伤、抗动脉硬化、抗癌以及免疫调节等多种药理活性[5-6]。然而,虎杖苷的多羟基结构导致其在脂质体系中存在生物利用度低、溶解度差及结构不稳定等缺陷,限制了其在功能性食品、药品及化妆品中的工业化应用[7]。将黄酮苷类化合物的分子结构进行适当修饰(如引入烷基链),使其成为脂溶性药物是解决上述问题的有效途径[8],如携带有不同结构烷基链的芦丁、芒果苷、樱桃苷和柚皮苷均表现出更优的生物活性[9-11]。此外,研究者还发现,含有双键或苯环等功能性基团的烷基链与活性化合物的结合往往可以合成具有双重功能的前导化合物,这为新药的发现提供了思路[12-13]。
天然产物的化学法酰化修饰一般采用酰氯、酸酐等作为酰化试剂,还需要进行繁琐的保护/去保护步骤,导致副反应多,污染环境[14-15]。与化学法相比,酶法酰化修饰具有选择性高、减少双键异构化及产物组成简单等优势,酶法酰化修饰已逐渐成为天然产物酰化修饰的主流方法[16-17]。本研究拟采用酶催化的方式,将虎杖苷与具有抗真菌抗病毒药效的十一碳烯酸连接以制备具有潜在药用价值的虎杖苷十一烯酸酯双前药(图1),并对酶促合成过程的动力学行为进行详细研究,以期为绿色酶催化合成技术改进传统化学合成过程提供借鉴。

图1 酶促虎杖苷与十一碳烯酸乙烯酯的酰化反应Fig.1 Enzymatic regioselective acylation of polydatin with vinyl undecenoate
1 材料与方法
1.1 材料与试剂
固定化棉状嗜热丝孢菌脂肪酶(Thermomyceslanuginosuslipase,TLL,55 U·g-1)、固定化南极假丝酵母脂肪酶B(CandidaantarcticaB lipase,CAL-B,44 U·g-1)和固定化根霉脂肪酶(Rhizomucormiehelipase,RML,12.6 U·g-1)购于中国Novozymes公司;固定化洋葱布克氏菌脂肪酶(Burkholderiacepacialipase,PSIM,12.4 U·g-1)购于日本Amano公司。虎杖苷(≥98%)和2-甲基四氢呋喃(2-MeTHF)(≥99%)购于中国Aladdin公司;十一碳烯酸乙烯酯(≥98%)购于上海TCI公司。乙腈和甲醇均为色谱纯,购于广东西陇化工公司。反应介质均需经4 Å分子筛脱水48 h后使用。
1.2 主要仪器与设备
Agilent 1260高效液相色谱仪、Zorbax SB-C18色谱柱(4.6 mm×250 mm),美国Agilent Technologies公司;BrukerAVANCE Digital 400 MHz超导核磁共振谱仪,德国Bruker公司;B-491旋转蒸发仪,瑞士BUCHI Labortechnik公司;CT15RE台式高速离心机,日本Hitachi Koki公司;FA2004B电子天平,上海精科天美科学仪器有限公司。
1.3 反应初速度、底物转化率、区域选择性的计算
反应初速度(V0)=(C0-Ct)/t,底物转化率(C)=(C0-Ct)/C0×100%,区域选择性6″-Regioselectivity=Cpi/Ctotal×100%。其中,C0和Ct分别代表反应前后虎杖苷的浓度,Cpi和Ctotal分别代表酰化产物和所有酰化产物的浓度之和。
1.4 不同脂肪酶对酰化反应的影响
取5个10 mL反应瓶,分别加入3 mL 2-MeTHF和0.03 mmol虎杖苷,0.21 mmol十一碳烯酸乙烯酯,置于恒温振荡器中恒温10 min(40℃,200 r·min-1),其中4个反应瓶分别加入2.75 U不同来源的脂肪酶(TLL、CAL-B、PSIM、RML)启动反应,另一反应瓶不加脂肪酶作空白对照,定时取样离心(10 000 r·min-1,4℃)10 min后进行液相色谱分析。
1.5 反应介质对酰化反应的影响
取4个10 mL反应瓶,分别加入3 mL不同溶剂(丙酮、2-甲基四氢呋喃、叔丁醇、四氢呋喃)和0.03 mmol虎杖苷,置于恒温振荡器中恒温10 min(40℃,200 r·min-1),分别加入0.21 mmol十一碳烯酸乙烯酯和2.75 U TLL启动反应,定时取样离心(10 000 r·min-1, 4℃)10 min后进行液相色谱分析。
1.6 底物摩尔比对酰化反应的影响
取6个10 mL反应瓶,分别加入3 mL丙酮和0.03 mmol虎杖苷,置于恒温振荡器中恒温10 min(40℃,200 r·min-1), 分别加入酰基供体(十一碳烯酸乙烯酯与虎杖苷摩尔比为3∶1、5∶1、7∶1、9∶1、11∶1、13∶1)和2.75 U TLL启动反应,定时取样离心(10 000 r·min-1, 4℃)10 min后进行液相色谱分析。
1.7 温度对酰化反应的影响
取6个10 mL反应瓶,分别加入3 mL丙酮和0.03 mmol虎杖苷,分别置于不同反应温度(35、40、45、50、55和60℃,转速200 r·min-1)的恒温振荡器中,加入0.27 mmol十一碳烯酸乙烯酯和2.75 U TLL启动反应,定时取样离心(10 000 r·min-1,4℃)10 min后进行液相色谱分析。
1.8 酶促虎杖苷十一碳烯酰化反应的动力学研究
取24个10 mL反应瓶,分别加入3 mL 2-MeTHF、丙酮、四氢呋喃和叔丁醇和不同浓度虎杖苷(4、6、8、10、12、14和16 mmol·L-1),置于恒温振荡器中恒温10 min(50℃,200 r·min-1),以9∶1的摩尔比加入酰基供体及2.75 U TLL启动反应,定时取样离心(10 000 r·min-1, 4℃)10 min后进行液相色谱分析,测定反应初速度(V0),根据Hans-Woolf 曲线得Km和Vmax。其中,Km为米氏常数,Vmax为最大反应速率。
1.9 高效液相色谱分析与产物结构鉴定
高效液相色谱仪,检测波长为305 nm,流速1.0 mL·min-1。虎杖苷及酯的保留时间分别为2.29和4.65 min。将1.7中的反应放大20倍,过滤除去酶,以石油醚(petroleum ether,PE)/乙酸乙酯(ethyl acetate,EA)作为洗脱剂,进行快速柱层析,旋转蒸发后得到虎杖苷十一碳烯酸酯,并进行核磁共振分析。
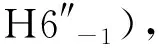
2 结果与分析
2.1 不同来源脂肪酶对虎杖苷十一碳烯酰化反应的影响
以反应初速度、底物转化率和6″-区域选择性为衡量指标,研究了4种不同来源的固定化脂肪酶对酰化反应的影响。由表1可知,不同来源的酶在催化相同的酰化反应时表现出不同的催化特征,以来源于Thermomyceslanuginosus的固定化酶TLL的催化效果最佳,反应初速度和底物转化率分别达13.9 mmol·L-1·h-1和71.6%;其次是CAL-B,但其初速度仅为TLL的50.4%,为7.0 mmol·L-1·h-1。 就PSIM和RML而言,较低的反应初速度和底物转化率均表明二者的催化活性较低,特别是RML的底物转化率仅为16.4%。同时,经核磁共振分析产物结构可知,所用酶的催化位点均为虎杖苷分子结构中的6″-OH,表现出了优异的区域选择性(100%)。

表1 不同来源脂肪酶催化虎杖苷十一碳烯酰化反应Table 1 Regioselective undecenoylation of polydatin catalyzed by various lipases
2.2 反应介质对酶促虎杖苷十一碳烯酰化反应的影响
由表2可知,TLL在4种溶剂中均能催化虎杖苷的酰化反应,尤其以丙酮中最好,反应初速度为17.3 mmol·L-1·h-1,底物转化率亦高达86.0%。其次为2-MeTHF,效果较差的为叔丁醇和THF溶剂,不适宜作为本试验中酰化反应的介质。由表2还可知,酶的催化行为与溶剂的LogP、粘度和溶解度无相关性。如LogP在非水相酶催化中是重要的溶剂参数指标[18],但TLL在LogP值最低的丙酮和最高的2-MeTHF中均表现出了较好的催化活性。此外,TLL在粘度相近的2-MeTHF和THF中表现出较大的催化差异。虽然虎杖苷在THF中溶解度是在其他溶剂中溶解度的数倍,高达72.1 mmol·L-1,但在THF中反应初速度仅为2.3 mmol·L-1·h-1,底物转化率仅为19.3%。由此可见,溶剂的多种性质与酶促反应活性并未呈现直接相关性,其对酶催化活性的影响是多方面的。

表2 反应介质对TLL催化虎杖苷十一碳烯酰化反应的影响Table 2 Effect of medium on enzymatic acylation of polydatin with vinyl undecenoate
2.3 底物摩尔比对酶促虎杖苷十一碳烯酰化反应的影响
TLL介导的酰化反应中酰基供体的量会对反应有一定影响[17]。本研究将虎杖苷的浓度固定为10 mmol·L-1, 通过改变酰基供体的浓度来探究底物摩尔比对反应的影响。如图2所示,当底物摩尔比介于3∶1 到9∶1 之间时,酶促反应初速度及底物转化率随摩尔比的增大而明显提高。当摩尔比升至9∶1时,二者升高至18.8 mmol·L-1·h-1和99.0%,进一步升高底物摩尔比对反应的影响甚微。在所选择的底物浓度范围内,酶促反应的6″-区域选择性始终保持在100%。表明在该酰化反应中存在水解反应,当酰基供体和底物摩尔比达到9∶1时反应初速度和转化率达到峰值。

图2 底物摩尔比对TLL催化虎杖苷十一碳烯酰化反应的影响Fig.2 Effect of the molar ratio on TLL-catalyzed acylation of polydatin
2.4 温度对酶促虎杖苷十一碳烯酰化反应的影响
由图3可知,35℃时酶促反应初速度为16.0 mmol·L-1·h-1, 随着温度上升,反应初速度呈上升趋势并在50℃时达到最大值20.8 mmol·L-1·h-1,因此50℃为反应的最适温度。继续升高温度,反应速度迅速下降。本研究还发现,温度的改变并未改变反应的最大底物转化率和区域选择性,始终保持在100%,显示出TLL较好的温度适应性。

图3 温度对TLL催化虎杖苷十一碳烯酰化反应的影响Fig.3 Effect of the temperature on TLL-catalyzed acylation of polydatin with vinyl undecenoate
2.5 TLL催化虎杖苷十一烯酰化反应的过程曲线
酶促反应的转化率和区域选择性随反应时间变化的规律如图4所示,在20~100 min时,底物转化率从11.5%上升到了80.0%,于200 min时达到98.4%;240~280 min时,底物转化率则始终趋近100%,之后底物转化率逐渐降低,在500 min时降至85.6%。在研究的时间范围内,酶促反应的产物始终是虎杖苷-6″-十一碳烯酸酯,显示出稳定的区域选择性。

图4 TLL催化虎杖苷十一碳烯酰化反应的过程曲线Fig.4 Process curve of TLL-catalyzed acylation of polydatin with vinyl undecenoate
2.6 不同反应介质中的酶促反应的动力学研究
本研究利用米氏方程,并依据Hanes-Woolf曲线对酶促反应的动力学参数进行了研究(图5)。在所考察的介质中,TLL在丙酮中的反应初速度最大,为68.9 mmol·L-1·h-1。而就米氏常数而言,丙酮中的Km值为24.7 mmol·L-1,远低于2-MeTHF(28.9 mmol·L-1)、叔丁醇(29.3 mmol·L-1)及THF(41.9 mmol·L-1)中的相应值。催化效率(Vmax/Km)是衡量酶促反应是否具有工业化应用价值的重要标准,在丙酮中,该反应Vmax/Km值为2.79 h-1,是在2-MeTHF、叔丁醇和THF中的1.3~6.6倍。

图5 在丙酮(A),2-甲基四氢呋喃(B),叔丁醇(C),四氢呋喃(D)中虎杖苷浓度对酶促酰化反应的影响Fig.5 Effect of polydatin concentration on enzymatic acylation in acetone (A), 2-MeTHF (B), t-butanol (C), and THF (D) (Inset of Hanes-Woolf plot)
3 讨论
酶的活性中心是影响酶促反应的核心要素[19-20]。Pleiss等[21]曾将脂肪酶的活性中心划分成裂缝状、烟囱状和隧道状等不同形状;且研究发现不同形状的酶活性中心会影响底物分子中的活性基团与酶活性中心催化基团的结合,进而导致出现不同催化行为[22]。黄酮苷类化合物具有羟基众多、空间结构复杂的特点,不同位点的酰化往往会产生一系列具有不同药理活性的衍生物。虎杖苷结构中糖基上6″-伯羟基相比于其他仲羟基具有更小的空间位阻和更高的催化活性,这可能有助于其进入裂缝状的TLL活性中心,以亲和、攻击酰基-酶过度中间体。进而形成优势产物6″-单酯[23-24]。同时,酰基供体采用乙烯酯能使该反应成为准不可逆反应,其副产物乙醛易与酶蛋白中赖氨酸的末端氨基形成Schiff′s碱,从而使酶失活[25],但这种失活程度由酶中特定赖氨酸残基的亲核性决定,与脂肪酶的来源、分子量等性质有关,这也是不同脂肪酶表现出不同催化活性的原因之一。此外,Kuo等[26]还发现有些脂肪酶可高效催化苷元中的4′-OH以形成相应的酯,但是本研究并未发现4′-OH被酰化,猜想虎杖苷中具有的较大空间位阻的糖基是导致上述现象的原因。
反应介质的性质对酶催化行为有显著影响[27-29]。如Laane等[18]认为酶在LogP>4的溶剂中表现出优异的催化活性,而在LogP<2的溶剂中几乎没有活性。但在本研究中,酶促反应与溶剂的LogP并无直接相关性,粘度和溶解度同样如此。Yang等[30]研究发现,溶剂分子可占据酶的活性中心影响双底物与活性中心的结合,而影响程度则取决于溶剂分子的类型以及空间构型。由此可见,溶剂的多种性质影响酶的催化行为。此外,溶剂的改变并未改变催化反应的区域选择性,这主要归因于底物分子的特殊结构。
TLL酶促虎杖苷酰化反应体系中存在产物酶促水解的副反应,增加底物摩尔比有助于反应向酯合成方向进行,且在摩尔比为9∶1时反应速度和底物转化率达到峰值。温度对酶促反应的影响主要涉及酶蛋白的热失活及溶剂体系的热改变[31]。如升高温度可以赋予酶蛋白中化学键更高的能量,使其运动性增强,继而带来酶活性中心的结构变化,最终导致酶催化行为的改变。此外,升高温度还会导致反应溶剂粘度下降,从而降低酶促反应的传质阻力,提高反应速度。当反应时间超过280 min(图4),底物的最大转化率略有降低,主要是由于随着反应的进行,酶促6″-十一碳烯酸酯的水解逐渐占据优势,导致产物减少。
非水相介质中酶促双底物酰化反应大都符合乒乓反应机制。TLL在丙酮中的Km值最低,Vmax/Km值最大,表明在该溶剂中酶与底物的亲和力更强,催化效率更高,这也与溶剂筛选的结果相一致(图5)。此外,已有研究发现,CAL-B催化虎杖苷与山梨酸乙烯酯酰化时,CAL-B在2-MeTHF中展现出最佳的催化特性,表明相同介质中酶促反应的特征也会因酶源、底物的差异而不同,表明酶与溶剂的生物相容性会因反应的改变而不同[23]。
4 结论
本研究以TLL为催化剂建立了绿色、高效、高选择性合成虎杖苷十一碳烯酸酯双前药的生物催化体系,考察了酶源、反应介质、底物摩尔比及温度等对反应的影响,结果表明,反应介质是影响酶催化活性的重要因素,但其LogP值、粘度以及溶解度等性质参数却与催化反应活性无直接相关性,表明溶剂对酶催化行为的影响是多方面的;进一步的动力学研究也表明酶的催化行为会因酶源、底物的改变而不同。本研究为黄酮苷类化合物的合成提供了新途径,还为绿色生物催化体系改造传统化学合成过程提供了借鉴。
