白蛋白结合型紫杉醇在晚期乳腺癌治疗中的疗效及安全性分析
2022-03-09单海霞
单海霞
(徐州医科大学附属医院肿瘤科,江苏 徐州 221000)
乳腺癌(breast cancer)是一种来源于乳腺组织的恶性肿瘤,其发病率逐年上升,并有年轻化趋势[1,2]。据报道[3],乳腺癌发病率居女性恶性肿瘤的第1 位,死亡率居女性恶性肿瘤的第5 位。晚期乳腺癌患者的预后较差,5 年生存率约为20%,其中3%~8%的乳腺癌患者初诊时即为转移性,而接受规范治疗的早期乳腺癌患者也有30%~40%会发展为晚期乳腺癌[4]。因此,需要不断探索新的治疗方案,缓解临床症状,提高晚期乳腺癌患者的生活质量并延长总生存期。白蛋白结合型紫杉醇是一种新型的紫杉类药物,由美国Celgene 公司研发,是紫杉醇与人血白蛋白的无溶剂胶体悬浮制剂,其以白蛋白为载体,能分散、稳定微粒和运载主药,可以靶向结合到肿瘤组织,提高紫杉醇的用药剂量及组织分布,具有高效低毒的优势。目前FDA 和CFDA 批准白蛋白结合型紫杉醇用于联合化疗无效的转移性乳腺癌以及辅助治疗6 个月内复发的乳腺癌[5,6]。本研究中结合2019 年4 月-2020 年3月我院收治的24 例晚期乳腺癌患者临床资料,分析白蛋白结合型紫杉醇在晚期乳腺癌中的疗效及安全性,现报道如下。
1 资料与方法
1.1 一般资料 选取2019 年4 月-2020 年3 月徐州医科大学附属医院收治的24 例晚期乳腺癌患者,均为女性,年龄33~70 岁,平均年龄(52.32±3.14)岁;浸润性导管癌21 例,浸润性小叶癌3 例;绝经前患者14 例,绝经后患者10 例;肺转移11 例,肝转移5例,骨转移9 例,脑转移3 例,其他3 例;分子分型:三阴性5 例,HR 阳性9 例,HER-2 阳性10 例。本研究经医院伦理委员会审批通过,患者知情同意并签署知情同意书。
1.2 纳入及排除标准 纳入标准:①符合晚期乳腺癌诊断标准,且有明确的组织病理学结果并经影像学资料证实有远处转移;②ECOG 体能状况评分为0~1 分,预计生存时间大于3 个月;③存在可客观评价的靶病灶(≥1 个)。排除标准:①存在化疗禁忌证;②存在精神及认知功能障碍者。
1.3 方法 根据患者年龄、一般状态、既往治疗用药情况及分子分型等选择合适的治疗方案,其中白蛋白结合型紫杉醇联合化疗者14 例,白蛋白结合型紫杉醇非联合化疗者10 例。白蛋白结合型紫杉醇联合化疗:白蛋白结合型紫杉醇(石药集团欧意药业有限公司,国药准字H20183044,规格:100 mg×1 支)200 mg(第1、8 天),若化疗期间发生3 级以上骨髓抑制,则第8 天用量减为100 mg。非联合化疗中白蛋白结合型紫杉醇按照260 mg/m2,第1 天用完。21 d 为1 个周期,患者至少完成2 周期的化疗,除非病情进展或者副反应不可耐受,最长不超过8 个周期。
1.4 观察指标 分析晚期乳腺癌患者近期疗效及安全性。近期疗效依据RECIST 1.1 版[7]进行评价,完全缓解:指所有靶病灶完全消失,无新病灶出现;部分缓解:指靶病灶直径之和比基线水平减少至少30%;疾病进展:指靶病灶直径之和增大大于20%;疾病稳定:指靶病灶的变化介于部分缓解和疾病进展之间。客观缓解率=(完全缓解+部分缓解)/总例数×100%,疾病控制率=(完全缓解+部分缓解+疾病稳定)/总例数×100%。不良反应事件采用术语标准(NCI-CTCAE)5.0 版进行评价,共分为0~4 级,其中中性粒细胞计数在(1.5~1.9)×109/L 为1 级,(1.0~1.4)×109/L 为2 级,(0.5~0.9)×109/L 为3 级,<0.5×109/L 为4 级;血红蛋白在正常~100 g/L 为1 级,80~100 g/L 为2 级,<80 g/L 需输血为3 级,危及生命需住院治疗为4 级;腹泻24 h 内<4 次为1 级,4~6 次为2 级,6~8 次为3 级,>8 次为4 级;分级越高,代表药物毒副作用越大[8]。
1.5 统计学方法 应用统计软件SPSS 19.0 处理数据,计量资料以()表示,采用t检验,计数资料采用(%)表示,采用字2检验;等级资料采用秩和检验,检验水准α=0.05。P<0.05 为差异有统计学意义。
2 结果
2.1 近期疗效评价 24 例晚期乳腺癌患者经治疗后完全缓解0 例,部分缓解14 例,疾病稳定7 例,3 例患者2 周期化疗后疾病进展而停止继续使用,客观有效率为58.33%(14/24),疾病控制率为87.50%(21/24),见表1。进一步分层分析发现,不同转移部位的疾病控制率比较,差异有统计学意义(P<0.05),其中淋巴结或胸壁转移、肺转移和骨转移的疾病控制率高于脑转移、肝转移;而不同月经状态、分子分型、治疗方案的疾病控制率比较,差异无统计学意义(P>0.05),见表2。

表1 晚期乳腺癌患者近期疗效情况(n,%)
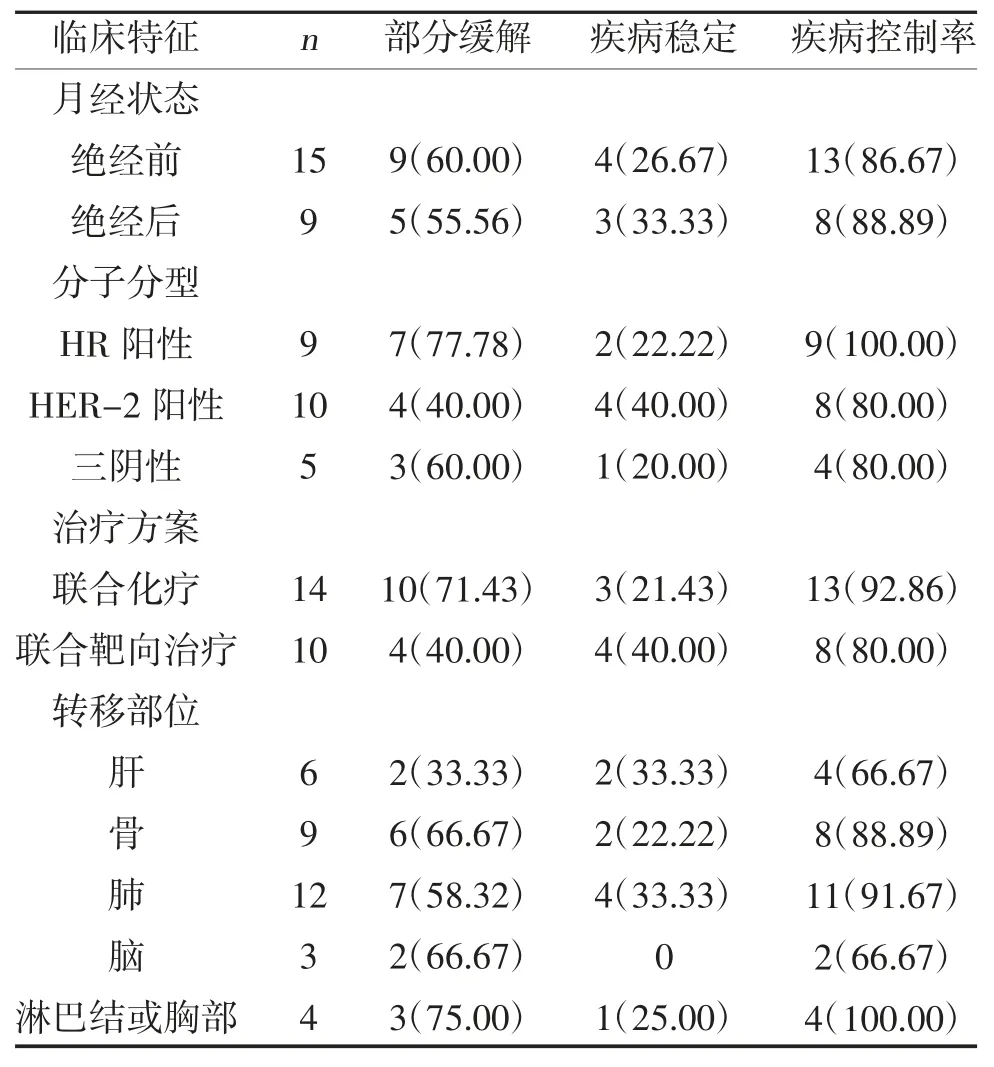
表2 不同临床特征晚期乳腺癌患者近期疗效情况[n(%)]
2.2 安全性评价 治疗过程中最常见的不良反应为中性粒细胞减少、贫血、脱发、肌肉关节酸痛、四肢麻木、恶心呕吐、肝功能异常、腹泻。其中3~4 级中性粒细胞减少、脱发、肌肉关节酸痛发生率较高,其他不良反应多为轻至中度,整体安全性良好,见表3。

表3 晚期乳腺癌患者安全性评价(n)
3 讨论
世界卫生组织将早期乳腺癌定义为可治愈肿瘤[9,10],其治疗后预后较好。而肿瘤一旦发展为晚期,中位生存期约为2 年,尤其是三阴性乳腺癌,其中位生存期仅10 个月左右[11]。因此,及早选择有效的治疗方案至关重要。对于晚期乳腺癌化疗方案的选择要综合考虑既往辅助治疗方案、无瘤生存期、无进展生存期等,才能优选出更合适的治疗方案。
白蛋白结合型紫杉醇是一种新型的紫杉醇类药物,应用纳米技术,以人血白蛋白为载体制成的130 nm 冻干剂[12,13]。传统的紫杉类药物不溶于水,需要助溶剂,容易引起过敏反应,需要预处理抗过敏,而且助溶剂形成的胶束降低了其生物利用度,容易出现骨髓抑制和神经毒性等不良反应,临床应用具有一定局限性[14,15]。而紫杉醇与白蛋白结合后,白蛋白包裹在紫杉醇的外层,进入人体后,可通过与细胞膜上白带白受体Gp60 相集合,从而激活细胞膜上小窝蛋白,利于紫杉醇穿过血管内皮细胞,分布至组织作用于肿瘤细胞,使其局部药物浓度增高;同时,肿瘤组织中高表达半胱氨酸酸性分泌性蛋白会吸引和黏附白蛋白,从而使白蛋白药物复合体靶向聚集在肿瘤细胞周围,最终进入肿瘤细胞,并释放出细胞毒物,促进微管蛋白聚合,阻碍肿瘤细胞纺锤体形成,阻滞细胞分裂进程从而发挥抗肿瘤作用[16,17]。既往研究发现[18,19],白蛋白结合型紫杉醇联合吉西他滨可延长进展期胰腺癌患者的生存期。雷声云等[20]研究发现,白蛋白结合型紫杉醇联合铂类治疗晚期妇科肿瘤的近期疗效较好,不良反应较少。本研究结果显示,24 例晚期乳腺癌患者经治疗后完全缓解0例,部分缓解14 例,疾病稳定7 例,3 例患者2 周期化疗后疾病进展而停止继续使用,客观有效率为58.33%,疾病控制率为87.50%,提示白蛋白结合型紫杉醇可有效控制晚期乳腺癌患者病情进展,与梁旭等[21]研究结果一致。此外,本研究结果发现,24例患者治疗过程中不良反应多为轻至中度,整体安全性良好,提示以白蛋白结合型紫杉醇为主的治疗方案不良反应轻,患者可耐受。但本研究由于研究样本数较少,随访时间短,对患者远期疗效及总生存的影响有待于进一步探索。
综上所述,白蛋白结合型紫杉醇在晚期乳腺癌治疗中近期疗效确切,不良反应可控,应用安全有效。
