氯化钠对水溶液氢键作用的红外光谱组学特征
2022-03-08于宏伟
王 欣, 于宏伟
(石家庄学院 化工学院,河北 石家庄 050035)
水是生命之源,所有的生命过程都是在水环境中发生.尽管水分子是最简单的分子,但却有很多的特殊性质,如高的沸点、大的热容、异常的密度/温度关系等.水的这些特殊性质和水的微观结构有关[1-6].红外光谱法根据波数的大小可以分为近红外光谱(NIR)、中红外光谱(MIR)和远红外光谱(FIR).2005年,Tsenkova首次提出水光谱组学(aquaphotomocs)的概念[7-9].主要利用NIR进行多元分析方法处理,获得大量的水吸收峰,整合成水吸收峰数据库,就是水光谱组学.水光谱组学以水为研究对象,通过NIR分析水氢键的相互作用,更好地理解生物世界.Brubath等[10]开展了液体水的MIR组学研究.液体水的MIR被分解为位于3 295 ,3 490 ,3 590 cm-1处的3个的高斯谱峰,它们分别归属于有4个和3个氢键水分子、2个氢键水分子、1个及0个氢键水分子.Sun[11]使用了5个高斯谱峰分解了水的拉曼光谱,通过归纳具有各种氢键结构的水团簇的—OH伸缩振动频率,这5个从低频到高频的谱峰分别被归属于单供体-双受体(single donor-double acceptor,DAA)、双供体-双受体(double donor-double acceptor,DDAA)、单供体-单受体(single donor-single acceptor,DA)、双供体-单受体(double donor-single acceptor,DDA)和自由—OH水分子.研究发现水分子的平均氢键数对水的微观结构有很大的影响[12-14].由于传统的IR谱图分辨能力不高,2D-IR光谱[15-16]的谱图分辨能力要优于传统的IR光谱,并能提供更多有价值的光谱信息.电解质、温度、有机物等因素会影响水的微观结构.本文中,笔者以常见的电解质(氯化钠)为物理扰动因素,首次采用IR光谱(包括MIR及NIR)及2D-IR光谱(包括2D-MIR和2D-NIR)技术,开展了氯化钠-水溶液的红外光谱组学(包括MIR,NIR,2D-MIR和 2D-NIR)研究,并进一步探索了电解质对水氢键微观作用的影响.
1 材料与方法
1.1 试剂与仪器
氯化钠(分析纯,天津市风船化学试剂科技有限公司),水(二次蒸馏水).
Spectrum100型中外红光谱仪(美国PE公司,测定频率4 000 ~600 cm-1,分辨率4 cm-1);单次反射ATR-IR附件(英国Specac公司);Spectrastar XL型近外红光谱仪(美国Unity公司,测定频率14 000~4 000 cm-1).
1.2 实验方法
1.2.1 配制氯化钠-水溶液
用氯化钠和二次蒸馏水依次配制质量分数为0,5 %,10 %,15 %,20 %和25 %的氯化钠-水溶液.
1.2.2 红外光谱仪操作条件
1.2.2.1 中红外光谱仪操作条件
采用ATR-MIR附件,以空气为背景,依次对不同质量分数的氯化钠-水溶液(0,5 %,10 %,15 %,20 %和25 %)进行中红外光谱数据采集,每个样品扫描24次.采用Spectrum V6.3.5 软件获得一维MIR光谱和二阶导数MIR光谱数据(其中平滑点为13).
1.2.2.2 近红外光谱仪操作条件
采用近红外光透射光谱附件,依次对不同质量分数的氯化钠-水溶液(0,5 %,10 %,15 %,20 %和25 %)进行近红外光谱数据采集,每个样品扫描24次.采用InfoStar软件(版本3.11.3-SP1)获得一维NIR光谱数据,采用Spectrum V6.3.5软件获得二阶导数NIR光谱数据(其中平滑点为13).
1.3 2D-IR光谱数据处理
采用2D shinge(c)软件(Shigeaki Morita,Kwansei-Gakuin University,2004~2005)处理2D-MIR和2D-NIR光谱数据.
2 结果与讨论
2.1 一维IR光谱研究
在4 000~600 cm-1测得氯化钠-水溶液的一维MIR光谱如图1a所示.其中1 640 cm-1处的吸收峰归属于水的弯曲振动(δ),而3 640 cm-1处的吸收峰比较复杂,分别包括水的不对称伸缩振动(νas)、对称伸缩振动(νs)和弯曲振动一级倍频峰(2δ)[17].在14 000 ~4 000 cm-1,进一步研究了氯化钠-水溶液的一维NIR光谱(图1b),其中6 883 cm-1处的吸收峰是水的νas和νs组合频吸收;而5 136 cm-1处的吸收峰对应水的νas和δ组合频吸收.实验发现:随着氯化钠-水溶液体系中氯化钠含量的增加,水的δ,ν(MIR)和ν(H2O-1),ν(H2O-2)的NIR光谱对应的红外吸收频率发生了明显的蓝移.
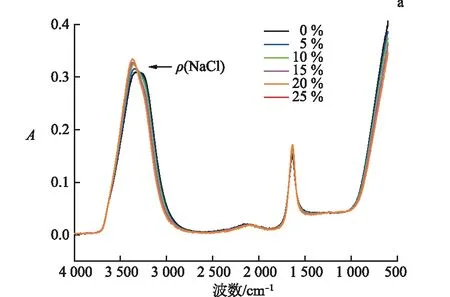
a.一维MIR光谱; b.一维NIR光谱.
2.2 二阶导数IR光谱研究
2.2.1 二阶导数MIR光谱
在4 000~3 000 cm-1测得氯化钠-水溶液二阶导数MIR光谱如图2a所示,由于谱图过于复杂,并没有得到有价值的光谱信息.在1 800 ~1 600 cm-1处继续进行氯化钠-水溶液的二阶导数MIR光谱研究(图2b).结果发现:随着体系中氯化钠含量的增加,氯化钠-水溶液δMIR对应的强度有所降低,而相应的吸收频率没有明显改变.

图2 氯化钠-水溶液的二阶导数MIR光谱
2.2.2 二阶导数NIR光谱
在7 400~6 500 cm-1测得氯化钠-水溶液的二阶导数 NIR 光谱如图3a所示.实验发现:二阶导数NIR谱图的分辨能力要优于相应的一维NIR光谱,其中水的νNIR对应的红外吸收包括:7 307 cm-1处ν(H2O-1-A),7 126 cm-1处ν(H2O-1-B)和6 611 cm-1处ν(H2O-1-C.随着体系中氯化钠含量的增加,水的ν(H2O-1-A)(红移51 cm-1)和ν(H2O-1-B)(红移32 cm-1)对应的吸收峰出现了明显的红移,而水的ν(H2O-1-C)(蓝移106 cm-1)对应的吸收峰出现了明显的蓝移.在5 500~5 000 cm-1处进一步研究氯化钠-水溶液二阶导数NIR光谱(图3b).其中水的ν(H2O-2)对应的红外吸收频率包括:5 389 cm-1ν(H2O-2-A)和5 299 cm-1ν(H2O-2-B).随着体系中氯化钠含量的增加,水的ν(H2O-2-A)(红移17 cm-1)和ν(H2O-2-B)(红移13 cm-1)对应的吸收峰出现了明显的红移现象.研究结果发现:氯化钠-水溶液的一维IR光谱和二阶导数IR光谱存在着一定的差异性,这主要是因为一维IR光谱的谱图分辨能力不高,不能提供更多有价值的光谱信息.

图3 氯化钠-水溶液二阶导数NIR光谱
2.3 氯化钠-水溶液2D-IR光谱研究
2.3.1 2D-MIR光谱
1) 4 000~3 000 cm-1的2D-MIR光谱.在4 000~3 000 cm-1处氯化钠-水溶液的同步2D-MIR光谱见图4a.在3 160,3 160 cm-1和3 440,3 440 cm-1处发现2个相对强度较大的自动峰(相对强度均为正值),而在3 160,3 440 cm-1附近发现1个相对强度较大的交叉峰(相对强度为负值).氯化钠-水溶液的异步2D-MIR光谱见图5b,在3 160,3 440 cm-1附近发现1个相对强度较大的交叉峰(正值).光谱数据说明:水的2D-MIR对应的红外吸收包括ν(H2O-1-A)(3 440 cm-1)和ν(H2O-1-B)(3 160 cm-1).根据NODA原则[18],随着体系中氯化钠含量的增加,水的ν(H2O-1-A)(3 440 cm-1)对应的结构最先改变,而ν(H2O-1-B)(3 160 cm-1)对应的结构相对稳定.

a.同步2D-MIR光谱; b.异步2D-MIR光谱.
2) 1 800~1 600 cm-1处的2D-MIR光谱.1 800~1 600 cm-1处氯化钠-水溶液的同步2D-MIR光谱见图5a.其中在1 630,1 630 cm-1处发现1个相对强度较大的自动峰(正值),而在1 630,1 710 cm-1附近发现1个相对强度较大的交叉峰(负值);氯化钠-水溶液的异步2D-MIR光谱见图6b,在1 630,1 710 cm-1附近发现1个相对强度较大的交叉峰(负值).光谱数据说明:水的2D-MIR对应的吸收频率包括1 710 cm-1的δ(H2O-1-A)和1 630 cm-1的δ(H2O-1-B).根据NODA原则[18],随着氯化钠-水溶液体系中氯化钠含量的增加,水的δ(H2O-1-B)对应的结构最先改变,而水的δ(H2O-1-A)对应的结构相对稳定.

a.同步2D-MIR光谱; b.异步2D-MIR光谱.
2.3.2 2D-NIR光谱
1) 7 500~6 500 cm-1的2D-NIR光谱.在7 500~6 500 cm-1处氯化钠-水溶液的同步2D-NIR光谱见图6a.在6 600,6 600 cm-1和7 140,7 140 cm-1,7 300,7 300 cm-1处分别发现了3个相对强度较大的自动峰(正值);在6 600,7 140 cm-1,6 600,7 300 cm-1和7 140,7 300 cm-1附近发现3个相对强度较大的交叉峰(均为正值).氯化钠-水溶液的异步2D-NIR光谱的研究见图7b.在6 600,7 140 cm-1,6 600,7 300 cm-1和7 140,7 300 cm-1附近发现3个相对强度较大的交叉峰(均为负值).光谱数据说明:水的2D-NIR对应的红外吸收峰包括7 300 cm-1的ν(H2O-1-A),7 140 cm-1的ν(H2O-1-B)和6 600 cm-1的ν(H2O-1-C).根据NODA原则[18],随着体系中氯化钠含量的增加,水的对应吸收峰变化快慢顺序为ν(H2O-1-A)>ν(H2O-1-B)>ν(H2O-1-C),其中ν(H2O-1-A)对应的结构最先改变,而ν(H2O-1-C)对应的结构相对稳定.

a.同步2D-NIR光谱; b.异步2D-NIR光谱.
2) 5 500~5 000 cm-1的2D-NIR光谱.在5 500 ~5 000 cm-1处氯化钠-水溶液的同步2D-NIR光谱见图7a.在5 300,5 300 cm-1和5 360,5 360 cm-1处发现了2个相对强度较大的自动峰(均为正值),而在5 300,5 360 cm-1附近发现1个相对强度较大的交叉峰(正值).氯化钠-水溶液的异步2D-NIR光谱见图8b,在5 300,5 360 cm-1附近发现1个相对强度较大的交叉峰(负值).光谱数据说明:水的2D-NIR对应的红外吸收峰包括5 360 cm-1ν(H2O-2-A)和5 300 cm-1的ν(H2O-2-B).根据NODA原则[18],随着体系中氯化钠含量的增加,对应吸收峰变化快慢顺序为ν(H2O-2-A)>ν(H2O-2-B),其中ν(H2O-2-A)对应的结构最先改变,而ν(H2O-2-B)对应的结构相对稳定.
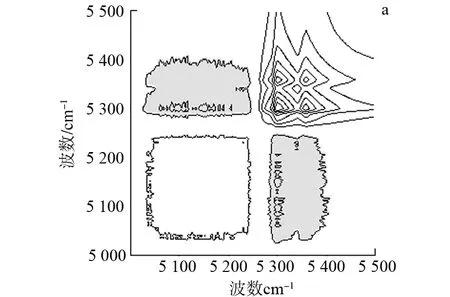
a.同步2D-NIR光谱; b.异步2D-NIR光谱.
Brubath等[10]报道了水的不同氢键对应的中红外频率.其中3 295 cm-1对应的是4个和3个氢键,3 460 cm-1对应的是2个氢键,而3 590 cm-1对应的是1个和0个氢键.Kinoshita等[19]报道了水的不同氢键对应的近红外频率.其中1 482~1 495 nm(6 689~6 748 cm-1)对应的是4个氢键,1 472~1 485 nm对应的是3个氢键(6 793~6 734 cm-1),1 458~1 468 nm对应的是2个氢键(6 859~6 812 cm-1),而1 432~1 433 nm对应的是1个氢键(6 983~6 978 cm-1).根据Buijs和Choppin的理论[20],液态下水分子氢键作用通常可分为3类:①水分子不与任何—OH基团形成氢键结合(对应ν(H2O-1-A));②水分子与1个或2个—OH基团形成氢键结合(对应ν(H2O-1-B)和ν(H2O-1-A));③水分子与3个或4个—OH基团形成氢键结合(对应ν(H2O-1-C)和ν(H2O-1-B)).第1类水分子具有最强的—OH键和最高的伸缩振动频率,而第3类水分子具有最弱的—OH键和最低的伸缩振动频率.而当水溶液中存在离子时,会造成水分子间氢键的断裂,电子云移向—OH键,导致其力常数增加[2].根据分子振动吸收原理,化学键力常数越大,则化学键的振动频率越高,吸收峰将出现在高波数区.这主要是因为Na+与水分子之间的离子势能比水分子之间的氢键之间结合大很多倍,离解的Na+破坏了水分子之间的氢键.随着溶液中Na+浓度的增加,水分子之间的氢键被破坏,从而引起水的吸收峰的频率及强度发生很大改变.
3 结 论
通过研究系列不同质量分数的氯化钠-水溶液的红外光谱组学发现,氯化钠-水溶液中同时存在δ(MIR),ν(NIR)和ν(H2O-1),ν(H2O-2)的NIR等4种红外吸收模式.结果表明:体系中氯化钠的添加会破坏部分水分子的氢键作用,同时增强了部分水分子的氢键作用.本研究为红外光谱组学在氯化钠-水溶液的氢键作用的原理开辟了新领域,具有重要的理论参考价值.
