儿童期生长发育延迟的Andersen-Tawil综合征一例报道并文献复习
2022-02-14蒋宗志魏晓晶王子燚孙慧于雪凡
蒋宗志 魏晓晶 王子燚 孙慧 于雪凡
1 病例报道患者男,16岁。因“发作性四肢无力6年”于2020-08-13入院。患者6年前出现发作性双下肢无力,表现为步态蹒跚,症状持续数分钟后自行缓解;3年前开始累及双上肢,出现发作性抬举费力,及双手精细活动差,每次发作持续1 d至1周不等,可自行恢复,发作期间无其他临床症状。患者发病以来肢体无力逐渐进展,表现为发作程度加重,频率增加,严重时可出现一过性晕厥,缓解期间遗留持续性的四肢近端无力。病程中偶有胸闷心悸,无晨轻暮重、眼睑下垂、肌肉萎缩等。出生时体重较轻,皮肤皱薄,出生身高53 cm,体重3 kg;3个月时头围31 cm。患者发育较正常新生儿迟缓,15个月时几乎不能独立行走;2岁时只能说两三个字,与同龄人相比身材矮小;在校成绩低于平均水平;6岁时体检发现心律不齐;无手术、外伤史,否认家族遗传病史。入院查体:身高175 cm,宽眼距,小下颌,双手第5指轻度弯曲畸形,心脏听诊可闻及早搏音,余心、双肺、腹部检查未见异常。意识清楚,语言流利,脑神经检查未见异常。四肢近端肌力Ⅳ级,远端肌力Ⅴ级;四肢肌张力正常,四肢腱反射(-),双侧Babinski征(-),双侧跟膝胫试验、指鼻试验及轮替试验均正常。实验室检查:发作期间,血钾均在正常水平;血肌酸激酶211 IU/L(正常参考值:24~195 IU/L),肝肾功能、外科综合、风湿三项、免疫五项、甲状腺功能、ANA、ANCA、肿瘤标志物、血尿固定电泳等检测结果均正常。24 h动态心电图检查结果显示频发室性早博,部分呈二、三联律,短阵室性心动过速的表现。肌电图检查显示左上肢正中神经、尺神经,右下肢腓总神经运动传导波幅减低。长时程运动诱发试验显示复合肌肉动作电位幅度(CMAP)下降了56%。骨骼肌病理检查提示部分肌纤维中央和膜下可见点状、团状嗜碱性颗粒状物质沉积,肌纤维内酶活性升高(图1)。简易精神状态评价量表(MMSE)、日常生活能力评定量表(ADL)检测及头部MRI检查结果均显示正常。基因检测:先证者KCNJ2基因4号外显子发生杂合突变,先证者父亲及母亲该位点基因无突变(图2)。结合症状、体征及辅助检查,该患者诊断为Andersen-Twail综合征(ATS)。给予患者口服氟卡尼(50 mg,2次/d)、肌肉注射左卡尼汀(1g,1次/d)治疗。3个月后电话随访,患者心律不齐症状控制良好,肢体无力情况未见改善。
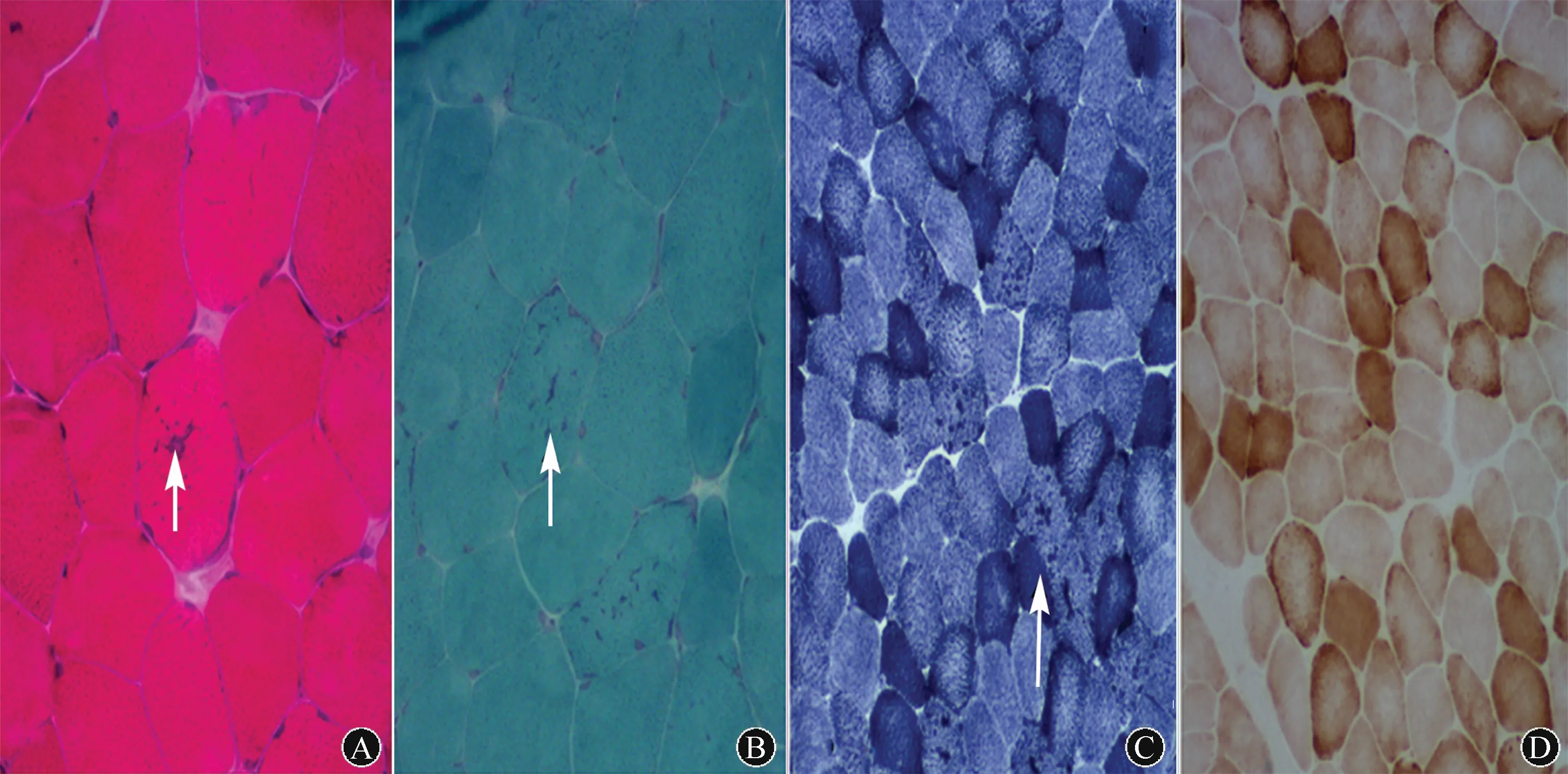
注:A:部分肌纤维中央及膜下可见点状、团状嗜碱性紫蓝色颗粒状物质沉积(箭头所示;HE染色,×100);B:部分肌纤维胞浆中及肌膜下可见紫红色颗粒状物质沉积(箭头所示;GT染色,×100);C:部分肌纤维胞浆内或肌膜下可见氧化酶活性升高,呈蓝黑色深染(箭头所示;NADH染色,×100);D:各型肌纤维未见着色(COX染色,×100)
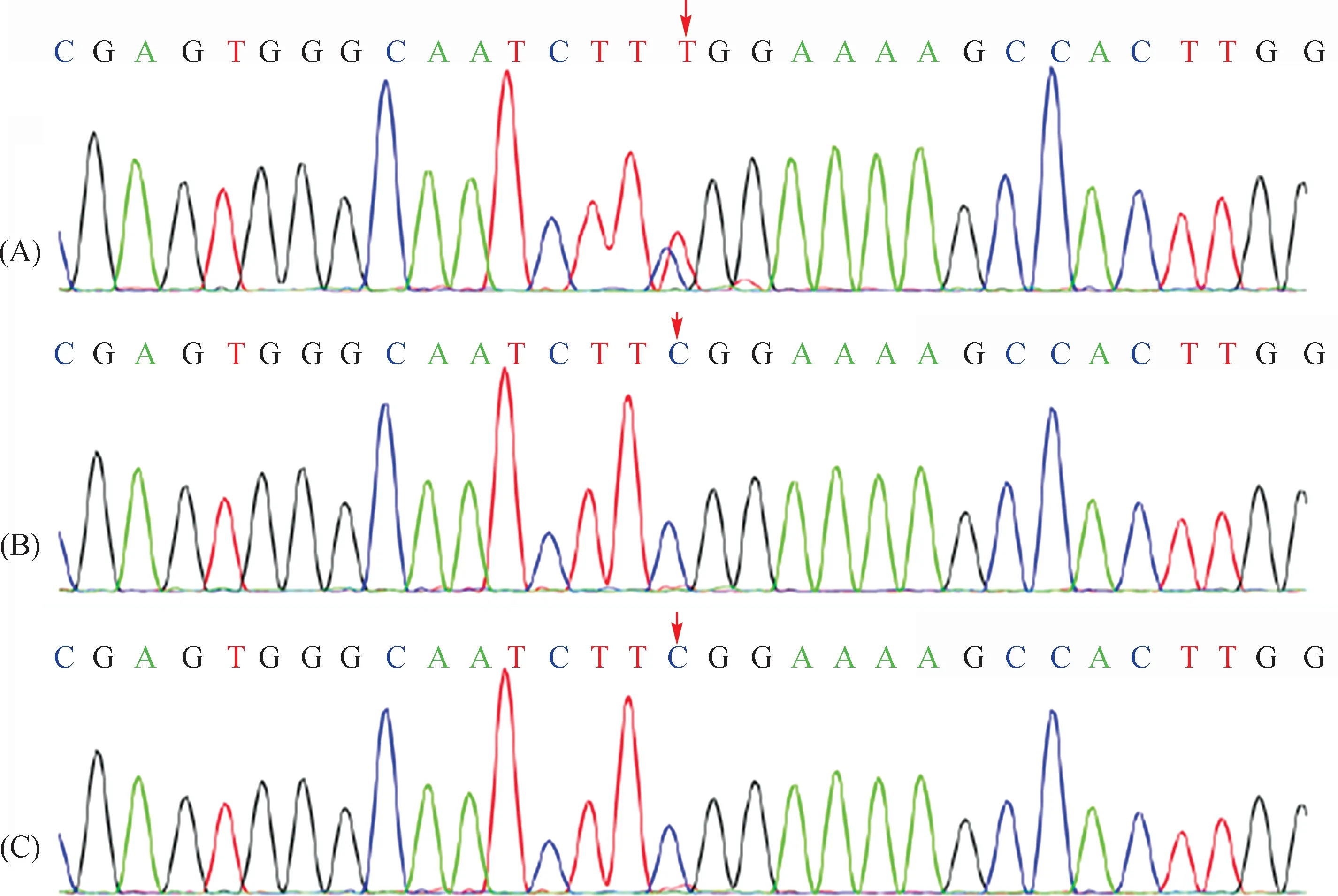
注:A:先证者KCNJ2基因4号外显子发生杂合突变:KCNJ2(NM_000190),chr11:118959812,c.652(exon4)C>T,p.R218W杂合变异(箭头所示);B:先证者父亲该位点基因无突变(箭头所示);C:先证者母亲该位点基因无突变(箭头所示)
2 讨论ATS是一种罕见的常染色体显性遗传的离子通道病变,临床特征为周期性瘫痪、心律失常和畸形三联征[1]。KCNJ2基因是其主要致病基因之一,其突变对钾通道蛋白Kir2.1具有显性负效应,可引起内向整流钾电流减少,从而导致骨骼肌细胞、心肌细胞动作电位时程延长[2]。ATS表型多样,近些年研究发现并非所有ATS患者均表现为典型三联征症状,因此将其分为典型ATS(>2个ATS特征)和非典型ATS(只有1个ATS特征或多形性室性心动过速)[3]。当患者出现两个及两个以上特征或者具有家族史时,即可诊断该病[4]。日本一项纳入57例ATS患者的研究显示,非典型ATS患者基因阳性率高达75%,提示对非典型ATS患者进行KCNJ2基因筛查具有重要临床意义[5]。
与典型离子通道性疾病患者不同,该例患者虽然以发作性肌无力为首发症状,但此患者病程持续时间长且在发作期间检测血钾离子却未见异常,这为临床诊断带来一定困扰。除典型三联征外,ATS患者还会出现生长受限及发育延迟。Kim等报道韩国一个家系中两姐妹存在严重的生长受限、特征性面部异常和发育迟缓,其父亲具有相似的面部特征和矮小的身材,3人均出现G215D变异[6]。本例患者存在生长发育异常史及面部畸形,但与既往报道不同的是,该例患者生长发育延迟仅发生在儿童时期,10岁后其发育与同龄人同步。目前有关KCNJ2基因突变导致Kir2.1通道功能的显性负效应与 “良性”发育迟缓之间的关系尚不清楚,作者推测延迟的生长发育可以通过改善营养、社会生活或其他因素来弥补。此外,该例患者在病程中存在一过性昏厥,结合患者存在频发室性早搏,提示患者是发生心律失常事件(LAE)危及生命的高风险人群。
目前ATS的治疗以对症处理周期性瘫痪和室性心律失常为主[2]。除补钾治疗外还可予以保钾利尿剂或碳酸酐酶抑制剂来缩短发作时间,减轻严重程度,控制发作频率。对于ATS导致的室性心律失常的治疗,常用β受体阻滞剂作为预防性药物,可单独使用,也可与胺碘酮或氟卡因联用,其中对于QT间期延长的患者,须避免应用具有肾上腺素能刺激作用的药物[7]。对于药物治疗无效及LAE高风险人群,可适当降低门槛,予以心脏起搏器或植入式心律转复除颤器(ICD)预防心脏猝死事件[3]。
综上所述,当临床遇到周期性麻痹的患者,要考虑到ATS的可能性,尤其患者存在面部结构畸形伴生长发育受限,须警惕本病,必要时行全外显子测序,以免漏诊。
