Ce-MnOx低温净化氮氧化物和一氧化碳的催化性能研究
2021-12-15韩新宇刘凯杰边梦瑶张一波杨向光
韩新宇,刘凯杰,边梦瑶,张一波,3,杨向光,3
(1.中国科学技术大学,安徽合肥230026;2.中国科学院赣江创新研究院;3.中国科学院长春应用化学研究所)
中国积极推进绿色低碳发展,承诺力争在2030年前实现碳达峰、2060年前实现碳中和[1]。其中,解决工业界排放尾气净化问题并构建现代化的绿色工业体系,是碳达峰与碳中和过程中的重点与难点。钢厂[2]、焦化厂[3]和铝厂[4]等工厂排出的烟气温度通常在200℃以下[5],其中氮氧化物(NOx)和一氧化碳(CO)是烟气中常见的主要污染成分,因此开发低温活性强的双功能协同脱除NOx和CO的催化剂,可实现低温工业烟气的深度净化,对中国完成碳达峰与碳中和的目标具有重要的意义。
烟气中含有大量的氧气(O2),尤其是钢铁行业低温烧结烟气中的O2体积分数达16%,因此本文采用低温CO催化氧化的方式来处理此类低温烟气中的CO[6]。而对于NOx,目前使用最为广泛的净化方法是以氨气(NH3)作为原料,并使用合适的催化剂来进行选择性催化还原反应,简称NH3-SCR反应[7],其反应方程式组如下:
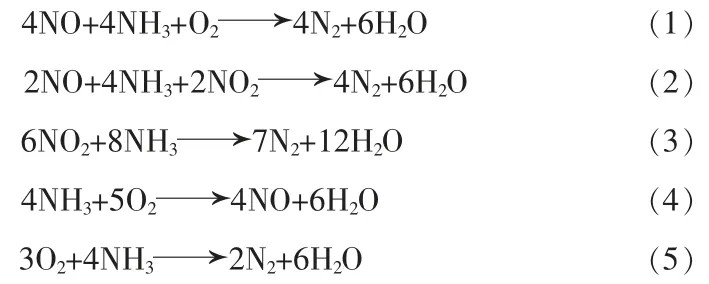
方程式(1)称为标准SCR反应,适用于一氧化氮(NO)含量多、二氧化氮(NO2)含量少的烟气。方程式(2)称为快速SCR反应,反应速率约为标准SCR反应的17倍,其发生率随着NO2含量增加而增加。方程式(3)为NO2的还原反应,此反应不需要借助O2便可进行,在n(NO2)/n(NO)>1的烟气中较易发生,但其反应速率远低于快速SCR反应[8]。方程式(4)为NH3的氧化反应,该反应在高温下发生,反应中NH3被消耗,产生了NO,进而导致高温下催化剂的活性急剧下降。方程式(5)为方程式(4)的后续反应,是方程式(1)与方程式(4)的加和,是NH3-SCR反应中的副反应之一,会导致NOx脱除率降低[9];该反应同时也是工业NH3-SCR脱硝过程中处理NH3逃逸的常用手段,即将泄漏的还原剂NH3处理为无污染气体。
当烟气温度高于300℃时,常用的钒-钨-钛(V2O5-WO3/TiO2)催化剂表现出优异的催化性能,但对于低温烟气而言,V基催化剂在200℃以下无法高效地活化分子氧,进而无法产生更高的催化活性[10]。近年来,研究人员发现锰基氧化物(MnOx)催化剂具有较好的低温SCR活性,目前已成为低温脱硝催化剂的研究热点[11]。
单一的锰氧化物已经具有较好的催化能力,为了进一步优化性能,通常将MnOx与其他元素进行掺杂或修饰。例如,KIM等[12]通过溶胶-凝胶法制备了掺铁(Fe)的MnO2催化剂,并将其负载至TiO2上,提高了NOx转化率;ZHANG等[13]制备了物质的量比为1∶1的CuO-MnO2粉体混合物,并将其负载至SAPO-34分子筛上,其NOx转化率相比掺杂前提高了20%;ZHU等[14]制备了钴(Co)掺杂的锰氧化物催化剂,形成了Mn2Co1Ox结构,在180℃时NOx转化率接近100%;ZHANG等[15]向MnOx中同时掺杂了镁(Mg)和Fe两种金属元素,相较于Mn-Fe体系进一步降低了起活温度。YANG等[16]于1992年发现稀土金属铈(Ce)的氧化物(CeO2)本身对于NOx的还原具有一定的催化能力,且CeO2又具有较好的氧储存性能,有利于O2的吸附活化。因此,本文意图结合两种物质的优点,采用Ce来掺杂Mn基催化剂,通过不同方法制备CeMnOx固溶体和CeO2-MnOx无定型混合物,并用于低温烟气中NOx和CO的协同脱除。
1 实验部分
1.1 样品制备
1.1.1 共沉淀法
正向共沉淀法:将Ce(NO3)3·6H2O固体和质量分数为50%的Mn(NO3)2溶液混合,然后加入48 mL去离子水和12 mL乙醇,此时溶液的离子浓度为0.1 mol/L。随后向上述溶液中滴加6 mL氨水与54 mL去离子水的混合溶液,静置并离心去除上清液后,充分洗涤以去除杂质,随后将沉淀物质在80℃下干燥12 h,并在马弗炉中在500℃下煅烧4 h。此方法制备的n(Ce)∶n(Mn)=x∶y的样品记为FC-x∶y。
反向共沉淀法:将上述金属离子溶液滴加到6 mL氨水与54 mL去离子水的混合溶液中,同上进行后续提纯操作,制备了反向共沉淀样品。此方法制备的n(Ce)∶n(Mn)=x∶y的样品记为RC-x∶y。
1.1.2 球磨法
将CeCl3·7H2O固体与过量NaOH固体混合,加入两倍于所有固体原料质量的磨球,在球磨机中以540 r/min的速度球磨1 h,以创造良好的碱性环境。再向球磨罐中加入KMnO4固体,球磨1 h后,将磨球取出;对产物进行充分洗涤、离心并在80℃下干燥12 h。此方法制备的n(Ce)∶n(Mn)=x∶y的样品记为BM-x∶y。
1.1.3 溶液燃烧法
将Ce(NO3)3·6H2O固体和质量分数为50%的Mn(NO3)2溶液混合,加入聚乙二醇(PEG),再加入10 mL去离子水和5 mL乙醇。搅拌至固体完全溶解后,在70℃下烘干至溶液为胶状,后放入马弗炉中,在500℃下煅烧4 h。此方法制备的n(Ce)∶n(Mn)=x∶y的样品记为SC-x∶y。
1.1.4 溶胶-凝胶法
将Ce(NO3)3·6H2O固体和质量分数为50%的Mn(NO3)2溶液混合,加入60 mL去离子水和0.012 mol一水柠檬酸,然后用氨水将pH调节至8.0。在70℃下水浴并搅拌至凝胶出现,于80℃下干燥12 h后,在马弗炉中在500℃下煅烧4 h。此方法制备的n(Ce)∶n(Mn)=x∶y的样品记为SG-x∶y。
1.2 测试与表征
1.2.1 催化剂性能测试
CO与NOx单独催化性能测试:将制备得到的催化剂分别置于两台固定床反应器中,并采用GC2060气相色谱仪和Hiden HPR-20EGA质谱仪分别对CO和NOx的脱除率进行检测分析。其中,CO催化氧化测试所用的气体中含有体积分数为1%的CO和99%的空气,测试空速为60 000 mL/(g·h);在NH3-SCR测试中使用的气体中含有O2、NH3、NO和氩气(Ar),它们的体积分数分别为5%、0.05%、0.05%和94.9%,测试空速为100 000 mL/(g·h)。
CO与NOx协同催化性能测试:将组成(含量以体积分数计)分别为NO(0.05%)、NH3(0.05%)、CO(0.25%)、O2(5%)、N2(19.5%)和Ar(75.15%)的气体通入固定床反应器,空速为100 000 mL/(g·h),检测CO和NOx的脱除率。
催化剂持续性能测试:将组成(含量以体积分数计)分别为NO(0.05%)、NH3(0.05%)、CO(0.25%)、O2(5%)、N2(19.5%)和Ar(75.15%)的气体通入固定床反应器,空速为100 000 mL/(g·h),在200℃下保持20 h,并持续监测CO和NOx的脱除率。
1.2.2 催化剂的表征
使用D8 Advance X射线衍射仪对所制备的样品进行X射线粉末衍射分析(XRD),以表征其物相组成;使用AutochemⅡ2920化学吸附仪对样品进行氨气程序升温脱附测试(NH3-TPD)和氢气程序升温还原测试(H2-TPR),同时使用ASAP2460物理吸附仪进行氮气吸附-脱附等温线测试,以检测样品的比表面积。
2 结果与讨论
2.1 CO催化氧化性能
图1是采用不同方法制备的CeMn氧化物催化剂的CO催化氧化活性与温度的关系图。其中,图1a是采用共沉淀法制备的3种不同比例的样品的CO脱除率与温度曲线图。由图1a可知,所有催化剂起活温度均低于100℃,且在160℃时都能够达到100%的CO转化率。反向共沉淀法制备的催化剂整体性能优于正向共沉淀法制备的催化剂。反向共沉淀法制备的样品中RC-2∶1活性最高,在120℃时达到了100%的CO转化率,整体趋势为Ce元素占比越高,催化性能越强;而正向共沉淀法所制备的催化剂相反,Ce元素占比越高,催化活性越低,且FC-2∶1样品活性最低,其原因可能是溶液体系中碱性环境的强弱导致催化性能存在差异。金属离子溶液为酸性,其pH约为3,向其中加入氨水,环境由酸性逐渐转变为碱性。由于Ce和Mn的溶度积差异[Mn(OH)2,KSP=1.9×10-13;Ce(OH)3,KSP=1.5×10-20]导致Ce优先沉淀,但由于溶液pH较低,Mn不能和Ce同时沉淀,不利于CeMnOx固溶体的形成。而反向共沉淀法是将pH低的金属离子溶液加入pH高于11的氨水溶液中,Ce和Mn在高碱性环境下能够同时沉淀,CeMnOx一经形成便不再变化,因此结构完整,催化效率较高。
图1b是采用球磨法制备的3种不同比例的样品的CO脱除率与温度的关系曲线图。由图1b可知,在180℃以下时BM-1∶2催化剂性能最好,且在160℃时能达到80%以上的CO转化率;在180℃以上时,3种比例的催化剂性能接近,都能够在200℃时将CO全部转化为CO2。
图1c是采用溶液燃烧法制备的3种不同比例的样品的CO脱除率与温度的关系曲线图。由图1c可知,3种不同比例的催化剂性能差异明显。在相同温度下SC-1∶2具有最高的CO转化效率,在120℃时CO转化率达到了100%;其次为SC-1∶1催化剂,在140℃时将CO完全转化。而SC-2∶1的性能不佳,在180℃时达到100%的CO转化率。由以上结果可知,溶液燃烧法制备的催化剂中Mn元素占比越高,催化性能越强。
图1d是溶胶-凝胶法制备的3种不同比例的样品的CO脱除率与温度的关系曲线图。由图1d可知,与溶液燃烧法不同,SG-1∶1具有最优异的CO催化氧化性能,在140℃时达到了100%的CO脱除率,并在后续的升温过程中保持不变;其次是SG-1∶2和SG-2∶1,分别在160℃和180℃达到了100%的CO转化率。SG-1∶1样品具有最佳的CO转化性能,因为在使用柠檬酸形成溶胶后,再用氨水将柠檬酸-金属离子络合物溶液的pH调节至8.0,随后在pH=8.0的环境和70℃的蒸发温度下,CeMn-柠檬酸络合物胶体粒子长大和胶体体积收缩同时进行[17],最终在形成n(Ce)∶n(Mn)=1∶1的凝胶时可以最大限度地增加固溶体的缺陷空间[18],因此表现出了最优的表面特性,即最优的催化性能。
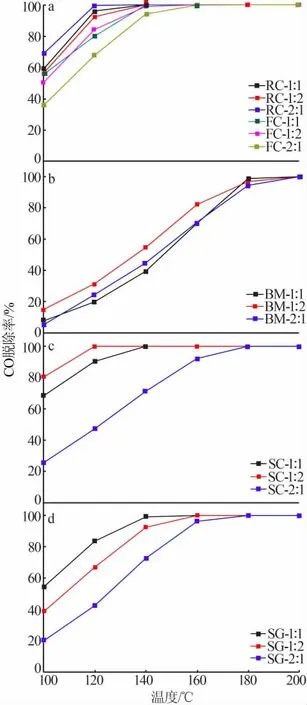
图1 不同方法制备的铈掺杂锰氧化物催化剂的CO脱除率-温度曲线Fig.1 CO removal rate-temperature curves of cerium-doped manganese oxide catalyst prepared by different methods
综合对比以上4种制备方法所得到的样品性能,可见共沉淀法制备的催化剂性能最优,主要表现在起活温度低、低温下转化率高和无高温衰减3个方面;其次是溶液燃烧法所制备的样品,其性能与共沉淀法制备的样品相似,但不同比例的催化剂之间性能相差较大。对于溶胶-凝胶法所制备的样品,其催化能力随温度上升而快速上升,但由于起活温度较高,在160℃以上才能够转化98%以上的CO。最后,球磨法制备的样品催化氧化能力较低,在180℃时尚未完全将CO转化为CO2。
2.2 NOx催化还原性能
在固定床反应器上测试了催化剂的NH3-SCR性能,并用质谱仪进行检测,结果绘制成NOx脱除率-温度曲线,如图2所示。
图2a记录了采用共沉淀法制备样品的性能数据。由图2a可知,通过反向共沉淀法制备的3种催化剂性能相近,在100℃时NOx的转化率已经接近90%,其性能随温度上升而略有上升后保持不变。正向共沉淀法制备的样品性能差异较大,FC-1∶1催化剂性能优于所有反向共沉淀法制备的样品,位于所有参与测试样品的首位;FC-1∶2和FC-2∶1性能在160℃以下与其他样品有较大的差距,其活性随温度上升而大幅上升后保持稳定。这说明在FC-1∶1的催化剂中出现了较为显著的CeMn协同作用。
图2b呈现了由球磨法制备的3种不同比例的样品的NOx脱除率与温度的关系曲线图。由图2b可知,与CO催化氧化性能的测试结果不同,在140℃以上BM-1∶1催化剂性能明显优于其他2份样品,且该催化剂的性能随温度的上升有较大幅度的提升。其余两种催化剂的NOx脱除率随温度变化的趋势一致,整体性能均落后于BM-1∶1。3种催化剂之间出现了非常明显的性能差距,原因是BM-1∶1中出现了Ce与Mn两种元素的协同作用。
图2c是溶液燃烧法制备的3种不同比例的样品的NOx脱除率与温度的关系曲线图。由图2c可知,3种催化剂NOx脱除率随温度变化的趋势一致。在120℃以上SC-1∶1和SC-1∶2的活性十分接近,远高于SC-2∶1催化剂。此现象表明,在测试条件下SC-2∶1无法提供足够的活性位点,导致大量气体无法吸附在催化剂表面,降低了催化性能。
图2d是溶胶-凝胶法制备的3种不同比例的样品的NOx脱除率与温度的曲线关系图。由图2d可知,3种催化剂的起活温度不同,催化能力随温度上升而上升的幅度也不同。SG-2∶1催化剂在100℃时的性能与其他两种比例的样品差距较大,但其催化能力随温度升高迅速增加,在140℃以上时其性能已经与SG-1∶1相同。这种现象可能是由于Mn进入CeO2的晶格后,Ce原子在晶格表面覆盖率高于Mn原子,导致活性组分与气体无法充分地接触,无法使更多NOx参与反应。

图2 不同方法制备的铈掺杂锰氧化物催化剂的NOx脱除率-温度曲线Fig.2 NOx removal rate-temperature curves of cerium-doped manganese oxide catalyst prepared by different methods
对比以上4种制备方法制得的催化剂的性能,可以发现共沉淀法制备的样品起活温度最低,且同温度下性能最强;其次是溶胶-凝胶法制备的催化剂,在140~180℃转化率平稳。溶液燃烧法制备的样品测试所得曲线与溶胶-凝胶法相似,但整体性能均低于溶胶-凝胶法制备的样品。最后,球磨法制备的样品催化效率随温度变化的波动较大,且其效率在低温下不稳定。
2.3 CO与NOx协同催化性能与持续性能测试
由于共沉淀法制备的催化剂在2.1节和2.2节的CO催化氧化性能测试与NOx催化还原性能测试中均位于第一位,且相对于其他3种方法制备的催化剂具有较大幅度的性能优势,因此选择RC-1∶1和FC-1∶1进行CO与NOx协同催化性能测试,将测试结果分别绘制为CO脱除率-温度曲线和NOx脱除率-温度曲线,如图3a所示。
由图3a可知,两种催化剂在180℃以上的性能相同,都能够将98%以上的CO转化为CO2。在低温区段,RC-1∶1性能优于FC-1∶1,在140℃达到了85%的CO转化率,而FC-1∶1在此温度下的CO转化率为80%。对于NH3-SCR反应,FC-1∶1和RC-1∶1催化剂在测试的温度区间内性能较为稳定,且在所测试的温度区间内均能脱除80%以上的NOx。
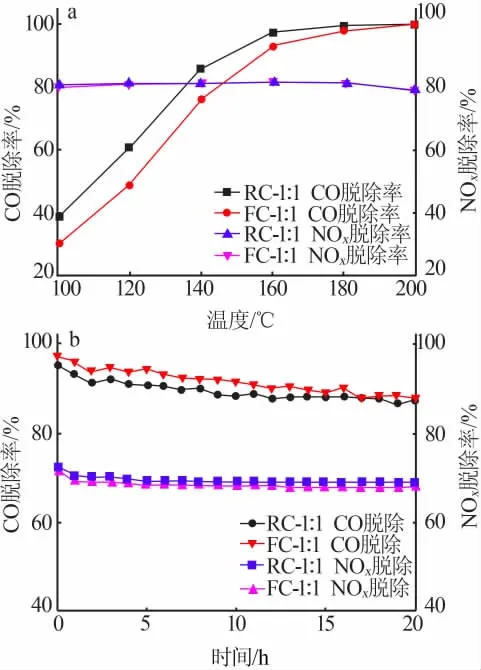
图3 催化剂在协同催化工况下的CO脱除率-温度曲线与NOx脱除率-温度曲线(a);催化剂在协同催化工况下运行20 h的CO脱除率-温度曲线与NOx脱除率-时间曲线(b)Fig.3 CO removal rate-temperature curves and NOx removal rate-temperature curves of catalysts in synergistic catalysis reaction(a);CO removal rate-time curves and NOx removal rate-time curves of catalysts for 20 h in synergistic catalysis reaction(b)
在协同催化反应中,由于活性位点出现了竞争吸附的现象,催化剂有了较为明显的性能下降,以至于FC-1∶1和RC-1∶1均不能在较低的温度达到100%的CO转化率,相比2.1节的CO催化氧化性能测试有较大幅度的性能降低;而NH3-SCR性能相较于2.2节的NOx催化还原性能测试下降约10%,但其性能随温度变化的趋势仍然保持不变。
将两种催化剂在固定床反应器上加热至200℃,并通入混合气,进行时长20 h的协同催化持续性能测试,并将实验实时结果绘制为CO脱除率-时间曲线和NOx脱除率-时间曲线,如图3b所示。实验误差原因导致持续性测试开始时的活性略低于图3a中活性。两种催化剂在持续运行1 h后均出现了小幅度的性能衰减,CO脱除率从接近100%降低至90%,NOx脱除率从75%降低至70%,随后保持不变。该测试证明共沉淀法制备的催化剂不但具有优异的催化性能,且能够在20 h的长时间使用下保持较高活性和稳定性。
为进一步探究催化剂在长时间运行前后的结构变化,使用X射线衍射对两种样品的晶体结构进行了分析,如图4所示。由图4可以看出,RC-1∶1(图4a)和FC-1∶1(图4b)在进行持续测试前与标准CeO2卡片吻合良好,曲线较为平滑,表明结晶度较好;在进行20 h的持续性能测试后,两种催化剂的XRD谱图均出现了低强度杂峰,表明在催化反应的过程中,晶格中的O原子在离开后,混合气中的O2并未完全进入催化剂晶格以填补空位,导致晶体的部分晶面出现缺陷,在X射线衍射中以低强度峰的方式呈现。同时,40~60°衍射角内的峰出现了强度降低的现象,证明(221)面、(311)面和(222)面是参与反应的主要晶面,Ce原子和Mn原子在此晶面分布较多,在长时间测试后结晶度有所下降。

图4 催化剂进行稳定性测试前后的XRD谱图Fig.4 XRD patterns of the catalysts before and after the stability test
2.4 XRD分析
选择RC-1∶1、BM-1∶1、SC-1∶2和SG-1∶2这4种催化剂作为不同方法制备的典型样品进行了X射线衍射分析,结果如图5所示。由图5可知,溶液燃烧法和共沉淀法所制备的样品与标准CeO2晶型卡片吻合良好,同时衍射峰出现右移,证明Mn原子进入CeO2的晶格之中,使其晶格参数发生变化,即生成了CeMnOx固溶体;溶胶-凝胶法和球磨法制备的催化剂则以CeO2和MnOx粉体混合物为主,结晶度较差,故衍射峰不高,且没有明显的晶体结构。
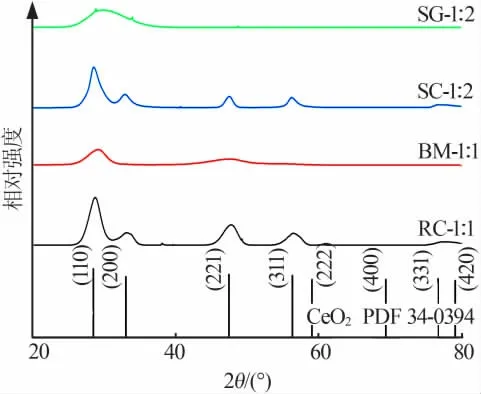
图5 不同制备方法得到的典型样品的XRD谱图Fig.5 XRD patterns of the catalysts obtained by different preparation methods
2.5 NH3-TPD分析
选择2.4节中的4种催化剂进行NH3-TPD测试,结果如图6所示。根据TPD测试的原理,脱附峰出现时间先后与酸性的相对强弱成反比关系[19],由图6可知,当脱附温度在300℃以下时,共沉淀法和球磨法制备的样品吸附的NH3首先解吸,对应温度约为100℃;随后溶胶-凝胶法和溶液燃烧法制备的催化剂在170℃时解吸,表明这4种样品中均含有一定量的弱酸位,结合NH3-TPD实验结果可知弱酸性位点含量并不是影响催化活性的决定性因素。
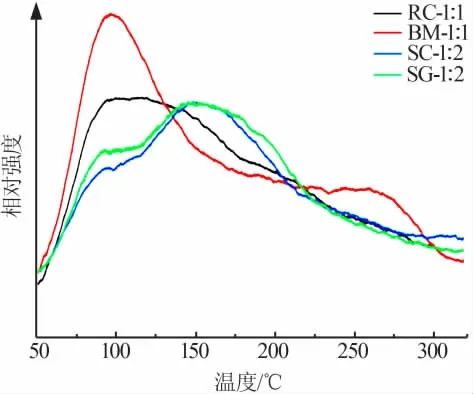
图6 催化剂的NH3-TPD曲线Fig.6 NH3-TPD curves of catalysts
2.6 H2-TPR分析
选择2.4节中的4种催化剂,进行了H2-TPR测试,并将测试结果绘制为相对强度-温度曲线,结果如图7所示。由图7可知,采用共沉淀法、溶液燃烧法和溶胶-凝胶法制备的样品中含有多个还原峰,原因是CeMnOx中MnOx在还原时按照MnO2、Mn2O3、Mn3O4的顺序依次进行,其中MnO2在众多锰氧化物中具有最高的催化活性[20]。RC-1∶1、SC-1∶2和SG-1∶2催化剂中含有较大量的MnO2,因而表现出卓越的NH3-SCR催化能力;球磨法制备的样品中Mn元素并不是单纯以MnO2的形式存在,且具有高催化活性的锰氧化物含量也是四者中最少的,因此在还原过程中400℃以下的峰面积最小,催化性能较差。
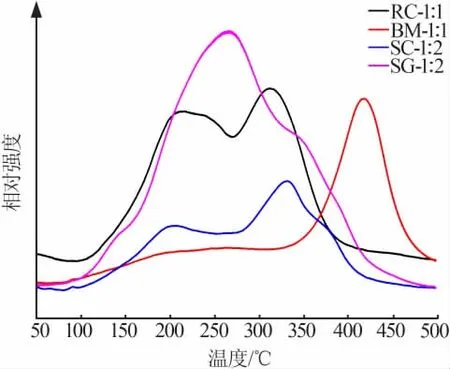
图7 催化剂的H2-TPR曲线Fig.7 H2-TPR curves of catalysts
2.7 氮气吸附-脱附测试
选择2.4节中的4种催化剂,采用氮气吸附-脱附等温线测定样品的BET比表面积,结果如表1所示。由表1可知,共沉淀法制备的样品比表面积最大,其次是溶液燃烧法制备的样品;球磨法和溶胶-凝胶法制备的样品比表面积相近,都小于50 m2/g。在CO氧化性能测试中,催化剂性能的强弱与比表面积大小呈正相关;但在NH3-SCR测试中,由于不同制备方法所得到的氧化物形成机制不同,且NH3-SCR与CO氧化的机理完全不同,溶胶-凝胶法制备的样品虽然比表面积较小,但其性能在NH3-SCR中排在第二位。因此,对于CO催化氧化反应,比表面积大小能够影响催化剂的活性;对于NH3-SCR反应,比表面积的大小与气体吸附位点的多少相关,但由于不同制备方法得到的催化剂所含的活性位点数量不同,且存在CeMn两种元素的相互作用,因此减弱了比表面积对催化剂性能的影响。
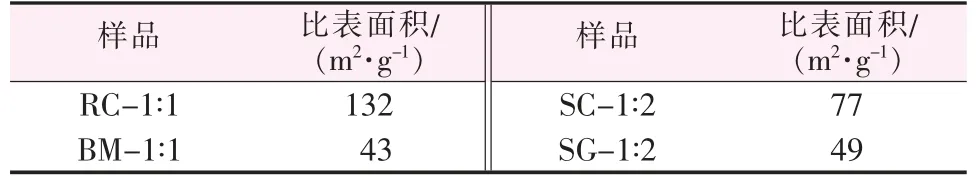
表1 催化剂的比表面积Table 1 Specific surface area of catalysts
3 结论
1)通过不同的制备方法(共沉淀法、球磨法、溶液燃烧法和溶胶-凝胶法)成功合成了4种不同的CeMnOx/CeO2-MnOx催化剂,并对其进行了CO氧化和NOx选择性还原的催化性能测试。活性测试结果显示,不同的制备方法对催化剂的催化性能有很大的影响。其中,共沉淀法制备的催化剂整体表现最为优异,在单独的CO催化氧化性能测试和NOx催化还原性能测试中,140℃时该催化剂的CO转化率大于90%,NOx转化率大于80%,且性能随着温度上升而继续增加;在协同催化测试中,该类催化剂出现了不同程度的性能降低,但仍然能够在200℃时转化全部的CO和80%以上的NOx。经过20 h的持续运行,该类催化剂出现了小幅度的活性衰减,但仍然能够脱除70%以上的NOx和80%以上的CO。
2)通过多种表征技术对催化剂的物化性质和结构组成进行了探讨,结果表明不同的制备方法对催化剂的结构和性质产生了不同程度的影响。不同方法制备的催化剂在XRD测试中结果差异较大,其中共沉淀法制备的样品最符合标准CeO2晶型;在化学吸附测试中,球磨法制备的样品具有最多的弱酸位点,而溶胶-凝胶法制备的样品具有最多的氧化性位点。共沉淀法制备的催化剂具有最高的比表面积,能够暴露更多的活性位点,从而表现出较高的CO催化氧化和NOx选择性还原脱除能力。
