基于HPLC指纹图谱与多成分定量结合化学模式识别法评价不同产地白芍的质量*
2021-11-23张生杰田志梅曹雪芹庞文娟
张生杰,田志梅,曹雪芹,庞文娟,王 丽
(武威市药品检验检测中心,甘肃 武威 733000)
白芍是我国著名的传统中药,始载于《神农本草经》,列为中品,具有平肝止痛、养血调经和敛阴止汗的功效,自古以来既可作观赏花卉又可作药用,目前全国药用白芍主产区为安徽亳州、浙江磐安、四川中江和山东菏泽[1]。中药材作为特殊的农产品,具有严格的道地性和对生态环境的选择性,盲目进行引种,不仅违背了生态适应性和道地性原理,而且很难保证中药材的适宜生长和增产保质[2]。中药材的质量受环境影响较大,同一种植物在不同环境下会产生不同的性状,中药材的主要有效成分基本是次生代谢产物,次生代谢产物的生态作用就是抵御外界不良的生态胁迫,在逆境条件下才大量合成次生代谢产物,药材质量的形成是通过增加次生代谢形成的[3]。现今杭白芍主产于浙江磐安县和缙云县等地区,该地区地处亚热带季风气候,而甘肃走廊的气候属大陆性干旱气候,气候干燥、冷热变化剧烈,风大沙多,因此在不同地域种植的白芍其质量定会存在差异,甘肃地区低温、高海拔、低降水量将影响白芍药材药效物质基础。为保证用药安全性、有效性,系统评价引种白芍与道地产区白芍的质量差异是非常必要的。
中药质量控制与评价是中药现代化研究的关键问题之一,目前化学成分检测是绝大多数中药质量控制的主要手段,但很多成分缺乏专属性、也没有生物活性,这必将大大降低中药质量标准的实际价值,而且也很难真实反映中药的质量[4]。2016年,刘昌孝院士提出中药质量标志物(Q-markers)的创新概念,为规范中药质量的研究和标准的建立奠定了基础,有利于中药全程质量控制和质量溯源体系的建立[5]。同时化学计量学的发展为中药质量研究提供了新的手段,化学模式识别是利用现代化分析技术分析中药复杂化学数据,再用化学计量学方法对数据进行特征提取和处理分析[6-7]。本研究收集了白芍四大主产区和甘肃地区引种白芍,通过建立指纹图谱,确认指标成分并同时测定其含量,利用化学模式识别分析不同产地白芍质量,为全面评价白芍质量提供参考和依据。
1 仪器与试药
1.1 试药共收集了50批白芍样品,其中包括来自安徽亳州、浙江磐安、四川中江和山东菏泽四大主产地40批,10批甘肃地区引种白芍样品,均经武威市药品检验检测中心中药鉴定师张生杰鉴定为白芍饮片。
1.2 试剂没食子酸对照品(批号:110831-201906,含量以91.5%计)、儿茶素对照品(批号:110877-201604,含量以99.2%计)、芍药苷内酯对照品(批号:190027-201902,含量以98.0%计)、芍药苷对照品(批号:110736-201943,含量以95.1%计)(中国食品药品检定研究院);1,2,3,4,6-五没食子酰基葡萄糖对照品(批号:230031-201909,含量以98.0%计)、苯甲酰芍药苷对照品(批号:02003-201902,含量以98.0%计)(北京更新生物科技有限公司);乙腈(色谱纯,默克Merck公司,批号:10945730812);其他试剂均为分析纯。
1.3 主要仪器LC-20AD高效液相色谱配有DAD检测器(日本岛津公司);MS105DU十万分之一电子分析天平(梅特勒托利多);UA10MFD超声波清洗器(德国wiggens)。
2 方法与结果
2.1 色谱条件色谱柱:Shim-pack GIST-HP C18色谱柱(250 mm×4.6 mm,5.0 μm);流动相:乙腈(A)-0.1%磷酸溶液(B),梯度洗脱:0~10.0 min,95%~90%B;10.0~20.0 min,90%~80%B;20.0~30.0 min,80%~70%B;30.0~35.0 min,70%B;35.0~37.0 min,70%~50%B;37.0~50.0 min,50%B;检测波长:232 nm;体积流量:1.0 mL/min;柱温:30℃;进样量:20 μL。
2.2 对照品溶液的制备取没食子酸、儿茶素、芍药苷内酯、芍药苷、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷对照品适量,用甲醇配成含没食子酸105.31 mg/L、儿茶素115.43 mg/L、芍药苷内酯403.12 mg/L、芍药苷997.35 mg/L、1,2,3,4,6-五没食子酰基葡萄糖303.54 mg/L、苯甲酰芍药苷107.35 mg/L的混合对照品溶液,作为对照品储备液备用。
2.3 供试品溶液的制备取白芍细粉约1.0 g,精密称定,置150 mL三角瓶中,加入70%乙醇约50 mL,称定,超声(300 W,50 kHz)处理30 min,放冷,70%乙醇补足,摇匀,0.22 μm微孔滤膜滤过,即得。
2.4 方法学考察
2.4.1 线性关系考察 精密量取“2.2”项下混合对照品储备液,依次用甲醇溶液稀释20、10、5、2倍与对照品储备液组成一系列混合对照品溶液,按照“2.1”项下色谱条件分别进样测定,以峰面积(y)为纵坐标,质量浓度(x)为横坐标进行线性回归,得回归方程。(见表1)
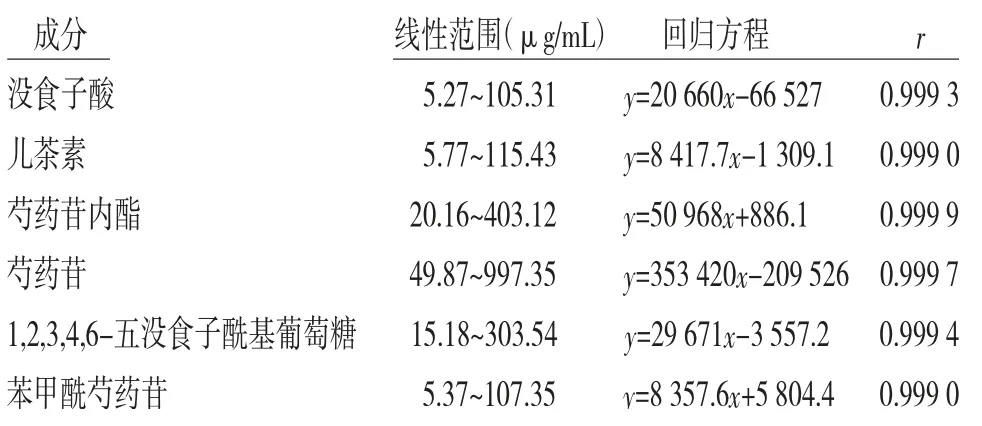
表1 6个化合物峰面积与浓度线性关系
2.4.2 精密度试验 称取甘肃省金昌朱王堡引种栽培白芍样品(S41)约1.0 g,按照“2.3”项下方法制备供试品溶液,以“2.1”项下色谱条件,连续进样5次,测定峰面积值。结果表明没食子酸、儿茶素、芍药苷内酯、芍药苷、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷峰面积的RSD分别为0.69%、0.29%、0.70%、0.16%、0.36%、0.81%,表明仪器精密度良好。
2.4.3 稳定性试验 称取甘肃省金昌朱王堡引种栽培白芍样品(S41)约1.0 g,按照“2.3”项下方法制备供试品溶液,分别于2、4、8、10、12、24 h,按“2.1”项下色谱条件测定峰面积。结果供试品溶液在24 h内色谱峰面积无明显变化,没食子酸、儿茶素、芍药苷内酯、芍药苷、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷的RSD分别为0.59%、0.26%、0.11%、0.25%、0.97%、0.27%,表明供试品溶液在制备后24 h内稳定性良好。
2.4.4 重复性试验 称取甘肃省金昌朱王堡引种栽培白芍样品(S41)6份,按“2.3”项下方法制备供试品溶液,测定各成分含量。结果没食子酸、儿茶素、芍药苷内酯、芍药苷、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷含量平均值分别为0.80、0.85、4.71、29.89、2.38、0.94 mg/g,RSD分别为1.47%、1.27%、1.02%、0.85%、0.74%、0.92%,表明该方法重复性较好。
2.4.5 加样回收率试验 取已知含量的甘肃省金昌朱王堡引种栽培白芍样品(S41)9份,每份约0.50 g,精密称定,分别精密加入约供试品中待测成分含量70%、100%、130%的对照品各3份,按“2.3”项下方法制备供试品溶液,在“2.1”项色谱条件下进样,记录色谱峰峰面积,计算没食子酸、儿茶素、芍药苷内酯、芍药苷、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷的平均加样回收率分别为98.17%、99.21%、98.76%、99.08%、99.72%、99.29%,RSD分别为1.82%、1.39%、0.80%、0.40%、0.49%、1.24%。(见表2)

表2 加样回收率试验结果(n=3)
2.5 指纹图谱的建立与相似度评价
2.5.1 指纹图谱的建立 中药指纹图谱是通过对各样本色谱图进行比较,以反映其所含化学成分的差异,可全面反映中药复杂的化学成分及其相对比例[8]。取不同产地50批白芍粉末,分别按“2.3”项下方法制备供试品溶液,按“2.1”项下的色谱条件进行测定,采集50批白芍色谱图,将HPLC采集到的50批不同样品的色谱图导入《中药色谱指纹图谱相似度评价系统(2012.1版本)》软件,以S1为参照指纹图谱,采用多点校正后进行全谱峰自动匹配,并叠加指纹图谱和对照指纹图谱,见图1。从50批白芍样品的指纹图谱中,共标记出9个共有峰,见图2。通过与对照品图谱比对,确认6个色谱峰,分别是1.没食子酸、2.儿茶素、3.芍药苷内酯、4.芍药苷、7.1,2,3,4,6-五没食子酰基葡萄糖、8.苯甲酰芍药苷,其峰面积和占共有峰面积的98%,6个指标成分基本可以代表白芍共有化合物信息。计算共有峰与对照指纹图谱的相对保留时间和相对峰面积,结果发现,9个共有峰的相对保留时间RSD值小于0.5%,表明方法的重复性较好;相对峰面积RSD值的范围为14.9%~39.4%,说明不同产地白芍饮片的化学成分含量存在差异。
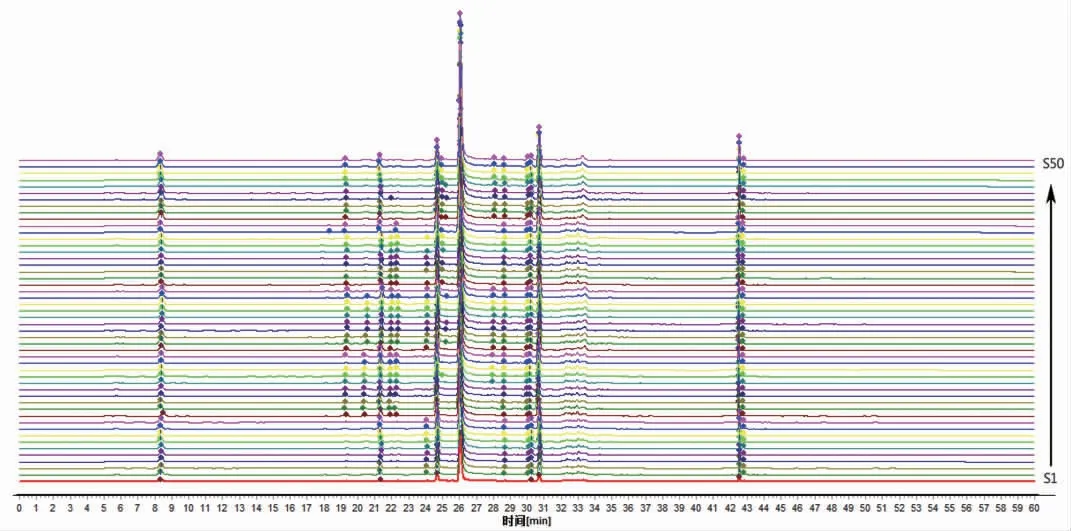
图1 50批白芍饮片色谱峰匹配图

图2 白芍饮片的共有模式图谱
2.5.2 相似度评价 将50批白芍样品指纹图谱的数据文件,导入《中药色谱指纹图谱相似度评价系统(2012.1版本)》软件,计算各样品指纹图谱与生成对照图谱的相似度,结果见表3,50批样品与生成对照图谱的相似度均大于0.996,表明不同产地的白芍饮片质量一致性较好,质量稳定。

表3 50批白芍饮片相似度分析结果
2.6 多指标成分的测定取50批白芍样品,按“2.3”项下方法制备供试品溶液,在“2.1”项色谱条件下同时测定样品中没食子酸、儿茶素、芍药苷内酯、芍药苷、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷峰面积,采用外标法计算各组分百分含量,结果见表4。
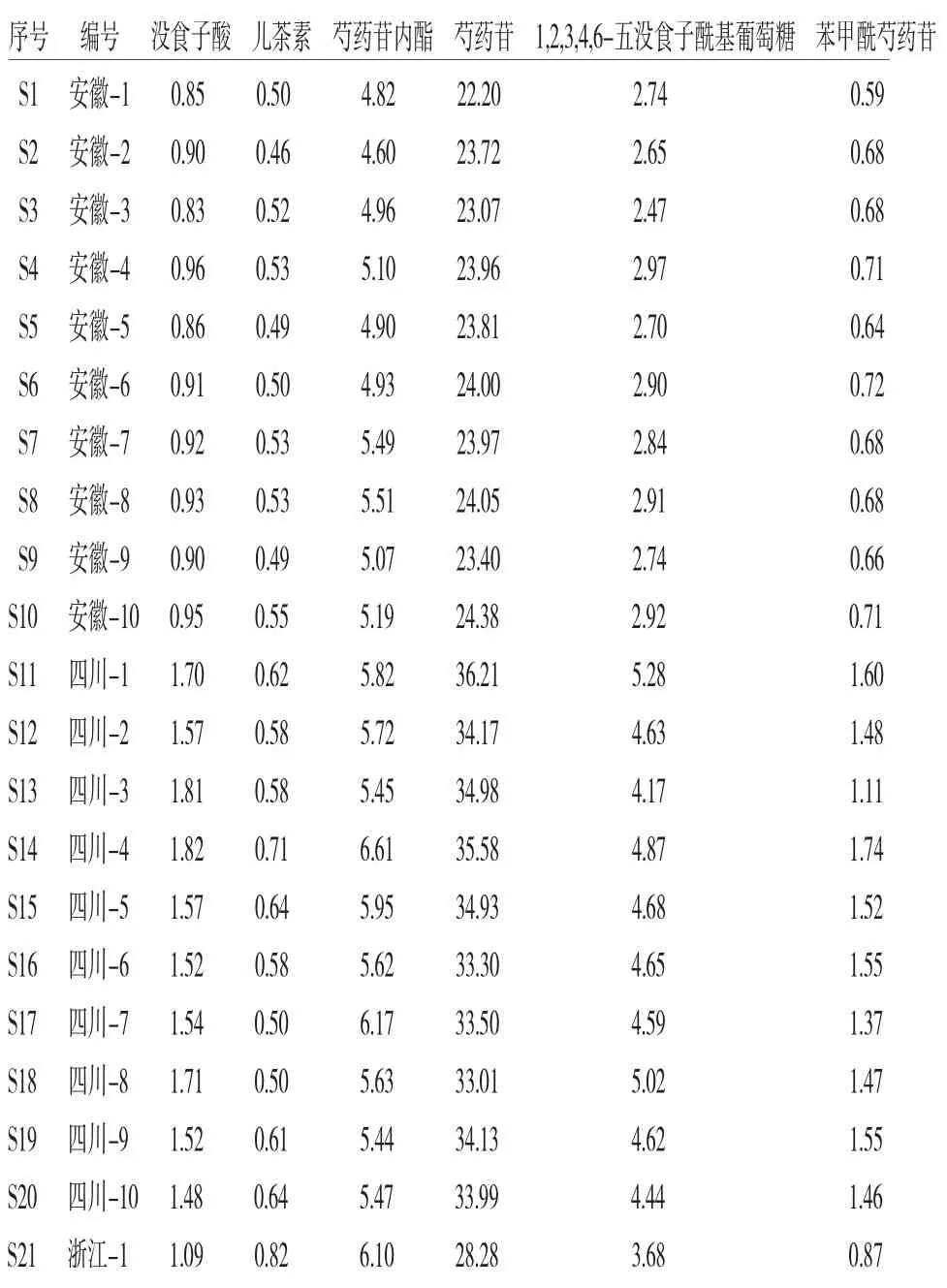
表4 样品测定平均结果(mg/g,n=3)

续表4:
2.7 化学模式识别分析
2.7.1 聚类分析 以不同产地白芍样品6个指标成分含量为变量,Z标准化,得到50×6阶原始数据矩阵,运用SPSS20.0统计分析软件对其进行聚类分析,以欧式平方距离为区间,采用组间连接法,对50批白芍样品进行聚类分析,结果表明,当分类距离为10~15之间时,50批白芍样品被分成3类,S1~S10安徽产白芍、S31~S40山东产白芍与S41~S50甘肃引种白芍为1类,S11~S20四川产白芍为1类,S21~S30浙江产白芍为1类,说明安徽、山东和甘肃引种白芍质量较为相似,与四川白芍与浙江白芍质量差异较大。当分类距离为5时,50批白芍样品将按照5个不同产地S1~S10安徽、S11~S20四川、S21~S30浙江、S31~S40山东、S41~S50甘肃分成5类,说明不同产地白药质量存在差异,同一产地的白芍质量保持稳定。(见图3)

图3 50批白芍聚类分析树状图
2.7.2 主成分分析(PCA)Principal components analysis(PCA)法是中药质量评价中最常用的方法之一,且较为成熟,通过建立PCA模型分析能够发现不同批次之间药物质量存在的微小差异[9]。将50批次白芍6个指标成分含量导入SPSS软件,以主成分因子特征值、方差贡献率为选择主成分的依据进行主成分分析,得到特征值和方差贡献率,特征值大于1的主成分有2个,累积方差贡献率76.8%,见表5。提取主成分进行主成分载荷矩阵分析,主成分载荷矩阵反映了各变量对主成分贡献大小和作用方向[10],没食子酸、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷对第一个主成分贡献较大,儿茶素、芍药苷内酯对第二个主成分贡献较大,都与其呈正相关性。利用模式识别统计分析软件SIMCA 14.1对50批白芍样品6个成分含量进行PCA分析,以主成分矢量为坐标轴作图(二维,称为scores图),得到50批白芍的PCA图,见图4,可以反映类别间的差异。由图4可直观地反映出,50批样品分布在不同象限,各样品之间的距离反映了样品间的相似程度,距离越近相似性越近,50批次白芍饮片主要分成3类,山东、安徽、甘肃为1类,说明山东、安徽、甘肃产白芍质量较为接近;浙江产白芍为1类,四川产白芍为1类,说明浙江和四川产白芍具明显的地域特点,这与聚类分析结果相一致。

表5 特征值和方差贡献率

图4 50批次白芍的PCA图
2.7.3 不同产地白芍的综合评价 综合得分可判别样品质量优劣,综合得分越高说明质量越好[11],用2个主成分对白芍进行质量评价,将主成分得分系数(见表6)与标准化后的化合物变量相乘求和得到主成分得分F1、F2,F1=0.286X1+0.039X2+0.084X3+0.222X4+0.282X5+0.280X6;F2=-0.096X1+0.648X2+0.585X3+0.113X4-0.020X5-0.097X6,并计算综合得分F(F=0.558 6F1+0.209 7F2),F1、F2分别为主成分一、主成分二得分,0.558 6、0.209 7分别为主成分一、主成分二方差贡献率[12],根据主成分综合得分模型计算样品综合得分,并对样品指标成分含量进行打分,以6个指标成分总量乘以0.1为含量得分,以样品编号为横坐标,得分为纵坐标绘制折线图,见图5,可以发现样品含量与主成分综合得分有明显的相关性,经统计分析相关性显著(r=0.860,P<0.01)。说明主成分综合得分能够真实地反映饮片质量,从主成分综合得分分析,浙江(S21~S30)和四川(S11~S20)产白芍质量较安徽(S1~S10)、山东(S31~S40)、甘肃甘肃(S41~S50)产白芍质量好,体现了白芍药材的道地性。

表6 主成分矩阵

图5 S1~S50主成分综合得分及6种成分含量测定结果比较
3 讨 论
3.1 色谱条件的选择为了保证白芍化学成分尽可能多地在一张色谱图上体现出来,且指标成分具有较好的分离度以便用于定量分析,通过HPLC二极管阵列检测器全波长扫描,综合考虑选择232 nm作最佳检测波长;用白芍主要成分混合对照品溶液考察在不同洗脱体系下梯度洗脱,发现以乙腈-0.1%磷酸溶液梯度洗脱6种混合对照品的分离度较好,基线稳定,色谱峰理论塔板数高,同时也适用于供试品溶液。在文献研究的基础上[13-15],比较了50%、70%、90%乙醇提取溶剂,结果表明70%乙醇提取时峰面积和最大;考察了超声、回流不同提取方法,从全面、快捷、绿色环保等因素考虑选择超声(300 W,50 kHz)处理30 min制备供试品溶液。
3.2 指纹图谱的建立与相似度评价本研究建立了不同产地白芍饮片的HPLC指纹图谱,方法简单、重复性好,色谱峰的相对保留时间RSD小于0.5%,主要特征峰的分离度均大于1.2,其他峰也达到了一定的分离,共标记出9个共有峰,通过与图谱比对确认了6种指标成分的色谱峰,其峰面积占共有峰面积98%,基本能够代表白芍化合物信息,不同产地的白芍指纹图谱相似度较高,表明不同产地白芍饮片的化学组成一致性较好,质量稳定。目前色谱指纹图谱相似度只能从整体上表达指纹图的平均相似程度,难以分辨指纹图谱间的细微差异,这些细微差异可能是质量评价的关键[16],所以本实验通过不同方法计算的相似度均大于0.996很难通过相似度来区分不同产地白芍质量,需要结合化学模式识别等方法从化学成分的角度控制其质量。
3.3 化学模式识别分析聚类分析法可将不同产地、品质较接近的药材进行聚类,从而可直观地表现药材间的亲缘关系,聚类分析包括成分含量的信息,还直观地包含了批次和产地信息,并对它们进行归类是一种很好的评价中药饮片质量的统计方法[17]。当类间距离在10~15之间时,安徽产白芍与山东产白芍、甘肃引种白芍因亲缘关系较近先聚为一类,这与安徽、山东环境条件相似,居群多样性分化相对较小,据调查甘肃引种白芍种苗均来自安徽,说明它们遗传物质相似有关;浙江与四川产白芍各聚为一类,这与浙江、四川独特的生长环境有关;在类间距为5时,50批白芍按照不同的产地分为5类,说明聚类分析法能够反映不同产地白芍之间的多样性分化,不同生长环境对白芍的质量具有一定的影响,也证明了中药品质是由植物遗传和生态环境双重因素决定的。主成分分析确定了2个主成分,累计方差贡献率76.8%,其中没食子酸、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷对第一个主成分贡献较大,儿茶素、芍药苷内酯对第二个主成分贡献较大,应考虑将没食子酸、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷、儿茶素、芍药苷内酯含量作为评价白芍质量重要指标。利用SIMCA软件可将样品主成分载荷值快速进行可视化处理,并直观地将样品分类,与聚类分析结果相一致。采用HPLC的指纹图谱结合化学模式识别通过SPSS、SIMCA软件,能够快速地进行聚类分析,建立不同产白芍质量控制模式。
3.4 不同产地白芍质量评价利用主成分分析建立的模型,可利用样品主成分综合得分评价药材质量[18]。本研究所建立的主成分分析模型,主成分综合得分与含量得分有显著相关性(r=0.860,P<0.01),能够真实反映白芍饮片的化学信息特征。从主成分综合得分来看,浙江、四川产白芍质量明显比其他3个地区产白芍质量好,这可能与浙江、四川独特的生态环境相关,也体现了白芍药材的道地性,可对白芍资源跟踪调查研究,探讨有效成分与生境之间的关系,对提高白芍药材质量具有一定的实际意义。甘肃引种白芍质量与安徽、山东产白芍质量相似,本研究通过对甘肃引种白芍和四大主产区(安徽亳州、浙江磐安、四川中江、山东菏泽)白芍饮片6种指标成分的测定,结果表明,不同产地白芍芍药苷含量差异最小,平均百分含量2.9%,高于《中华人民共和国药典》标准规定的1.2%,符合《中华人民共和国药典》将芍药苷作为白芍含量控制标准[19],但仅通过芍药苷一个成分很难真实反映白芍的质量,起不到白芍质量控制的目的,按照Q-markers的概念,需要进一步考察其他相对含量低且具有生物活性的成分。本实验确定的其他5个指标成分没食子酸、儿茶素、芍药苷内酯、1,2,3,4,6-五没食子酰基葡萄糖、苯甲酰芍药苷符合中药质量标志物(Q-markers)的特征。甘肃引种白芍6个指标成分含量均高于平均值且质量稳定,说明该地区适合引种白芍,多成分含量测定的方法可用于白芍质量控制,较单一成分控制更加全面、准确。
