基于改进天线阵列共焦成像算法的脑瘤检测应用∗
2021-11-08周楚霖陈敬东王新余
周楚霖 陈敬东 王新余 曾 真
(中国船舶集团有限公司第七〇九研究所 武汉 430205)
1 引言
我国脑癌发病率和死亡率位居全国癌症发病榜前10位。就目前而言,传统的诊疗手段对肿瘤针对性不强,放射性高且医疗费用昂贵使很多家庭无法承担。现在主流的临床检测手段有:核磁共振成像核磁共振成像(MIR),脑血管造影,神经核医学检查,立体定向活检术等[1]。但是这些手段都有其局限性,例如MIR由于检测机理的局限性,不适用于由于手术等原因植入有磁金属或起搏器的特殊患者。
本文利用正常组织和癌变组织间较大的电磁参数差异检测肿瘤的存在。通过天线阵列发射和接收脉冲信号,计算散射参数并结合本文目标定位算法确定脑瘤位置。这种方法相对安全,无有害辐射,不进入人体内部,没有压迫感,不会伤害正常组织,对小直径的早期肿瘤有着相当可观的检测效果,资源耗费相对较小,更加适合轻量化、可移动化临床检测,并且利用电磁学理论进行肿瘤检测具有重要研究意义,为复杂组织结构的三维立体肿瘤检测提供了具有参考价值的思路和方法。
2 检测机理与数学模型
在特定电磁环境下,每种组织材料有其对应的介电常数和电导率,脉冲在穿过不同有耗组织材料时会产生一定的相移量,这一相移量不仅仅体现在脉冲穿过组织内部,也体现在穿过不同组织边界[2]。并且这个相移不仅与组织材料的电导率和介电常数有关,也与所处的外部辐射源的频率有关。如表1所示为有、无肿瘤时各频率下XFDTD计算出的散射参数相位特性[13~14]。
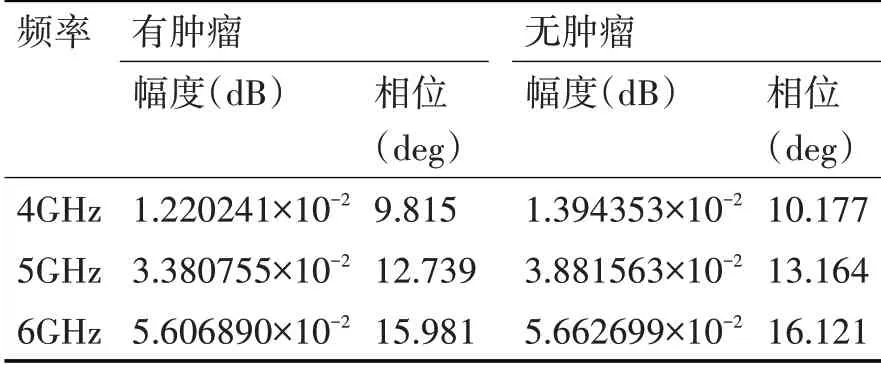
表1 有无肿瘤时各频率的散射参数相位特性
脉冲在有耗媒质内部的相移β根据式(1)计算得出[3]。
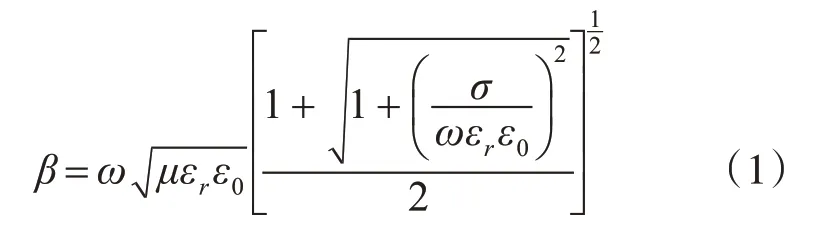
其中,β为脉冲穿过单位长度的相移量,ω为脉冲频率,μ为磁导率,数值为4π×107,εrε0为实际的介电常数,其中εr为相对介电常数,ε0为真空中的介电常数,数值为8.85×1012,σ为各组织材料的电导率,单位为S/m。
脉冲穿过两个不同组织材料边界的相移根据式(2)~(4)计算得出[4]。
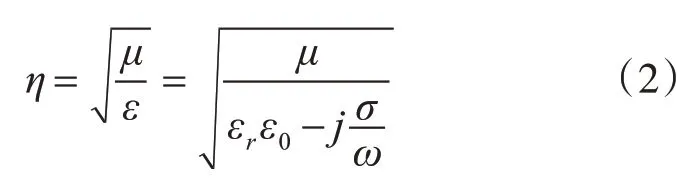
式(2)表示每个有耗媒质组织的波阻抗,μ为磁导率,数值为4π×107,εrε0为实际的介电常数,εr为相对介电常数,ε0为真空中的介电常数,数值为8.85×1012,σ为各组织材料的电导率,单位为S/m,ω为脉冲频率,j为虚数单位。
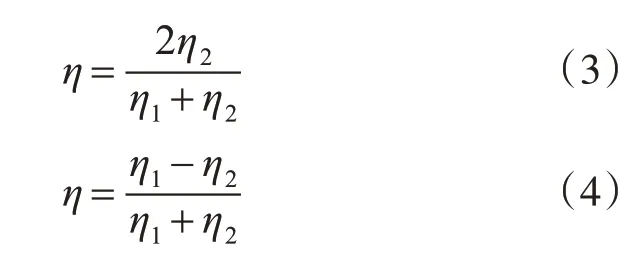
其中,式(3)表示穿过两个不同组织(非肿瘤组织)的透射系数[5],该复数的幅角即为相移量。若脉冲由一般组织边界到肿瘤组织边界或由肿瘤组织反射回一般组织边界,透射系数根据式(4)计算得出[6~7]。
3 基于改进的天线阵列共焦成像算法的脑瘤检测应用
3.1 系统流程及方法
本文在共焦成像算法[8]的基础上,建立人体头部组织模型,进行肿瘤早期检测。利用XFDTD和Matlab实现了人脑的建模工作,建模流程大致为:头部三维模型建立(S1)-网格化处理(S2)-二维组织切面层截取(S3)-添加肿瘤组织(S4)-设置天线阵列和辐射源(S5),建模主要流程如图1所示。
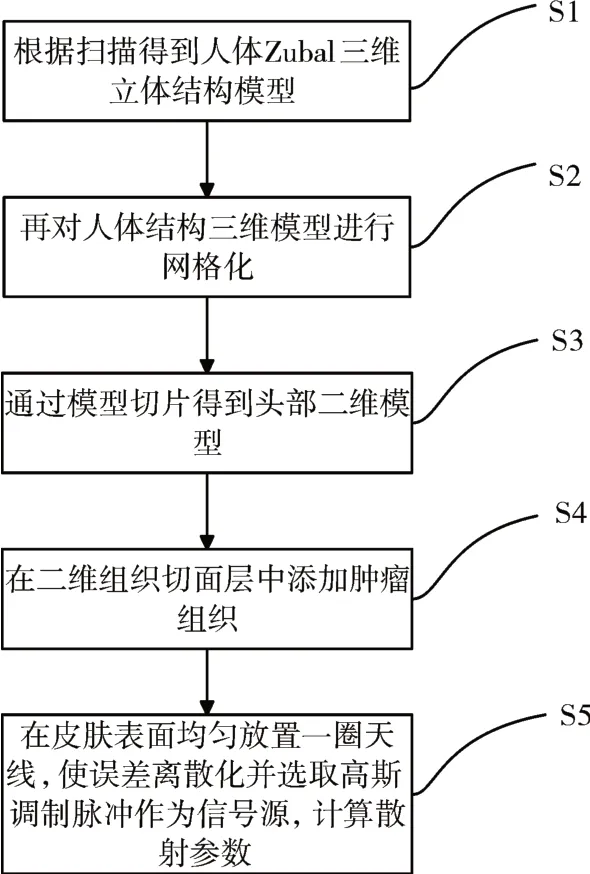
图1 模型建立流程图
本文设计了一套合理可行的算法,在二维组织切面上根据收发天线连线上组织的种类和数量,根据相关公式以及各个组织材料在特定频率下的电磁特性计算出散射参数及其相移。分别按照单发单收,单发多收的方法计算各个天线组,各个频率下组织材料的散射参数相移,并与由XFDTD计算出的有肿瘤和无肿瘤情况下实际散射参数的相移差作对比,得到置信度矩阵。最后,完成矩阵信息可视化,对各组得到的置信度矩阵叠加取平均,使周围组织和肿瘤组织的相似度差距增大到0.5以上,在网格图中颜色差距明显,可以较容易地找到肿瘤的位置。
3.2 头部切片模型建立与肿瘤添加
本文从头部三维立体结构入手,用分层切片的方式提取脑部二维组织切片模型。根据已有技术相对成熟的核磁共振模型[9](The MRI-Head Phan⁃tom)建立人体头部三维模型,每种组织有相应的编号,根据编号可以确定不同的组织类型。例如本文所用的MRI头部影像文件有256*256*128字节的体积。MRI头部影像材料和标号,如表2所示(篇幅有限,列出主要组织)表中数字为The MRI-Head Phantom所用到的主要的ID标号。所有组织结构均采用了基于结构的三维中值滤波,使每个结构的表面具有更真实的“光滑”曲率。利用Matlab可以对每个组织的编码和命名写入,形成人体的三维结构模型。

表2 头部主要组织的电导率和介电常数
对三维模型进行网格化处理,方便直观分辨每种组织的结构与特性,使每种组织由类似于“细胞”的小块构成。实际上,网格化即矩阵特性排列,矩阵中每个元素的数值代表其对应的组织编号,为了兼顾分辨率我们将每个小块的边长设置为3.6mm[10]。人体头部结构复杂,组织众多,相互干扰较为严重,为简化模型和降低仿真难度、优化数据结构、方便数据处理,我们在二维切片截面上进行仿真计算。
首先选取合适的切片层数,依据脑部主要组织(脑灰质和脑白质)材料较多,腔体较大,便于后期仿真实验和数据处理工作的特点,在Matlab中进行分层切片,每种组织以不同颜色显示。此时,最优的人体头部特定切片的二维模型建立已基本完成。
在上一步的基础上,我们在XFDTD仿真软件上加入肿瘤组织,由于正常脑部组织和肿瘤组织的差别较为明显,故依此设置肿瘤的参数。经测试,在4GHz环境下肿瘤的电导率为4(S/m),相对介电常数为60[11]。肿瘤的大小方面,若设置太大不符合肿瘤生长的实际情况,但设置太小,由于mesh网格分辨率不高,肿瘤组织将不会在网格中清楚显示其边界,不易于后续仿真与观察;经反复测试,决定设置小球的球心在一个网格中心,半径为1.8mm,使其刚好占据一个小块大小。如图2所示为添加了肿瘤组织脑部meshXY视图。

图2 添加了肿瘤组织脑部meshXY视图
3.3 天线阵列建立与激励源设置
最后加入天线和设置合适的激励源,由于人脑结构非中心对称结构,为方便起见,我们建立8根线天线,长度各为5cm,平行于Z轴,均匀排列在脑部一周。采用收发天线分离的配置方式,即一个发射天线一根接收天线,即实现单发单收/自发自收,如此做,只需计算S11参数即可;及一根发射天线(T1)配有多个接收天线(R1-R7),即实现单发多收,计算S21,S31,S41等。这样可以降低对天线设计的苛刻要求,同时采用共焦成像算法避免了复杂的散射场计算。各个天线的位置如图3所示,如图4为三维空间当中的实际效果图。
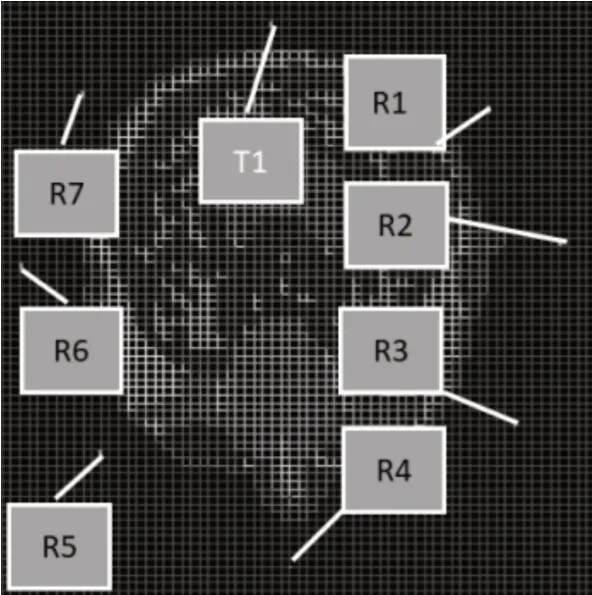
图3 各收发天线位置图

图4 三维空间天线效果图
激励源的选择直接影响着成像的效果,不同的激励源的回波信号之间存在较大的差异。经测试,我们选取高斯调制脉冲[12](Modulated Guassian)作为信号源较其它信号源能够更好地得到散射参数和相移信息,高斯调制脉冲的时域表达式根据式(5)计算。
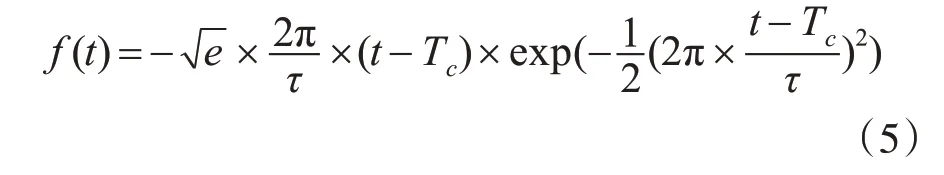
其中Tc为时移单位,τ是脉冲宽度参量。
3.4 改进的共焦成像算法
本文共焦成像算法在不同收发位置、不同辐射环境下、使用单发单收和单发多收策略分别进行肿瘤检测。
首先假设当前检测位置(记为aij)为肿瘤位置,将选定的肿瘤假想点aij与发射、接收天线(分别记为T、Rk)连线并找到连线路径上的组织小块,统计各类组织小块的种类(1、2、3、4……)与数量,记为n,用连线上两两相邻组织的种类编号做差(λ)判断组织小块间类型是否相同,如式(6)所示。

类似的,根据式(1)~(4)遍历并计算所有小块的散射参数总相移β,与电磁数值仿真软件XFDTD计算出的散射参数β*相移相做差比较,得到该点为实际肿瘤位置的置信度值[13],记为θ;重新选择不同辐射环境和不同天线收发位置,直到遍历所有情况,得到该点的置信度平均值,记为θˉ;再对二维组织切面上每一个点做相同的计算,得到整个切面层的置信度矩阵,进行归一化处理,其中置信度较大的位置即为实际肿瘤位置,算法流程如图5所示。
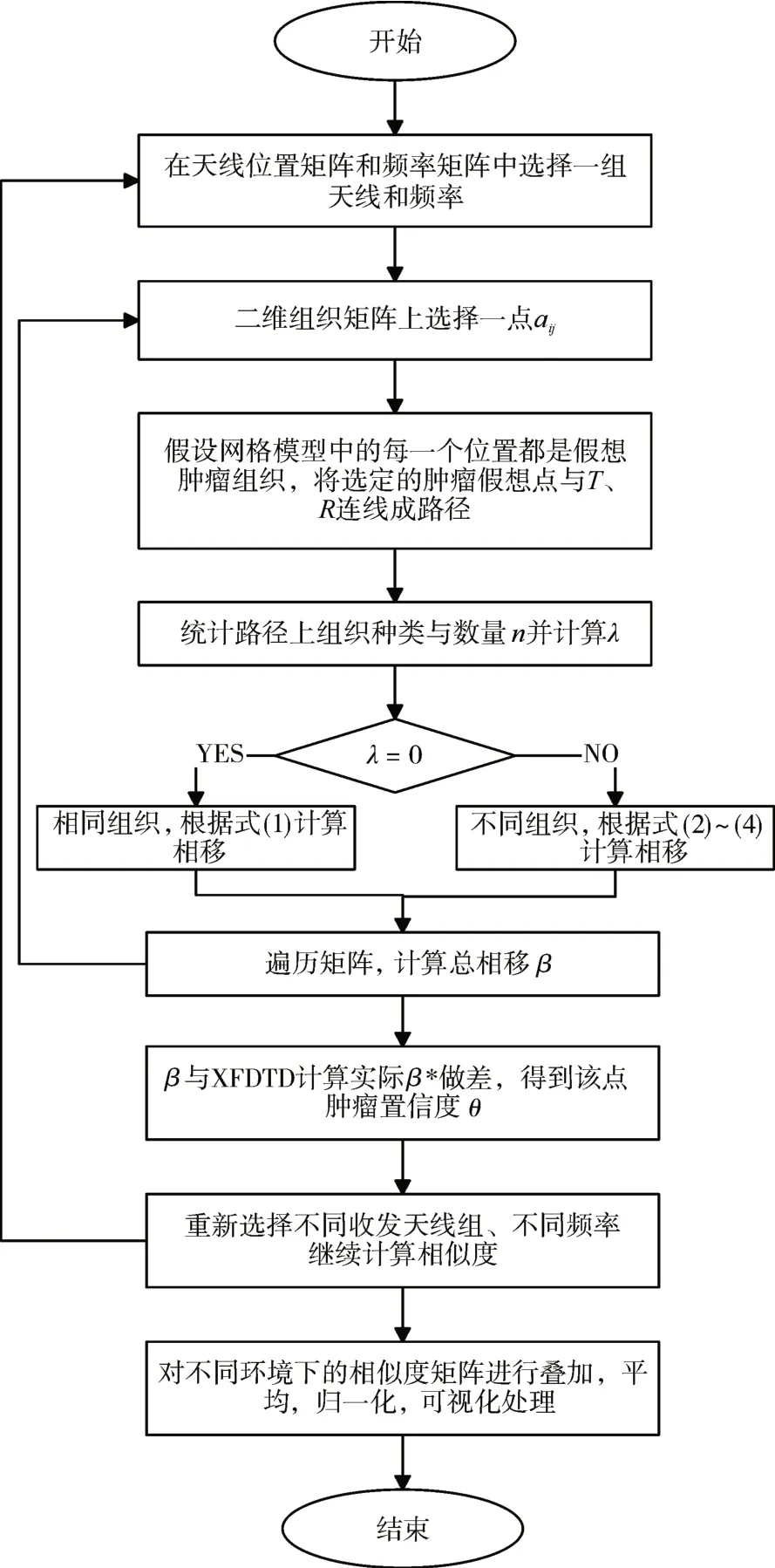
图5 共焦成像算法流程
为提高计算精度、降低复杂度,我们对算法进行了优化。在散射参数处理方面,我们在有肿瘤和无肿瘤两种情况下,对XFDTD计算出的对应频率下的散射参数复数值做差取相移,如此做,可以有效减少其他组织回波干扰和空气层的散射干扰。在肿瘤假设点选取方面,我们没有对二维组织切面上的所有位置进行遍历,而是预先排除了一些不可能的位置,如空气层、皮肤、头骨等组织;如此做,将原先需要遍历的整个二维组织矩阵缩小到了特定的矩阵区域,极大减少了计算量,缩短了检测时间,提高了检测效率[14]。
4 实验结果及分析
经计算,得到二维组织切面的相似度矩阵,利用Matlab绘图即可较明显地观察到肿瘤位置。单发单收模式下,选取一根天线作为发射天线,一根作为接收天线,对4GHz、5GHz、6GHz频率下计算得到的置信度矩阵叠加,归一化,可视化。单发多收模式下,采用8根天线阵列进行仿真;其中设定一根作为发射天线(记为T),其余7根作为接收天线(记为R1-R7),每组分别在4GHz、5GHz、6GHz环境下进行,并对所有收发天线组的计算结果结果进行叠加,归一化,可视化后,得到平均置信度矩阵仿真结果,如图6(a)、(b)所示分别为单发单收,单发多收模式下仿真结果。

图6 单发单收,单发多收模式下仿真结果
由以上的仿真结果可以比较直观地根据颜色分辨出肿瘤的可能位置(置信度越高,颜色越深),肿瘤位置更加清晰可辨,理论上,可以选取任意两个天线位置为发射天线或者接收天线,不仅仅局限于本例中的发射天线T。对比单发单收模式可见,单发多收模式下仿真结果更加理想[15~16],其主要原因在于往返路径上所穿过的组织不同,更加适合脑内的复杂环境,利用7组不同位置的天线源作为接收天线,将围绕脑部360°的组织充分考虑进去,增加数据的多样和仿真结果的可靠性,并且有效地避免了“伪肿瘤”的出现,大大增加了早期肿瘤检测的精准度[17~18]。
为验证优化效果,我们在“单发多收”模式下对未优化的算法在准确度、检测时间和计算资源消耗方面进行对比,如图7(a)、(b)分别为采用未优化、优化算法后的仿真结果,如表3所示为检测时间和资源消耗对比。从中可以看出未优化算法仿真结果并不理想,不但检测时间长、资源占用大,且一定程度上影响检测准确率,使可视化程度降低,肿瘤位置难以清楚分辨,甚至造成漏检、误检。
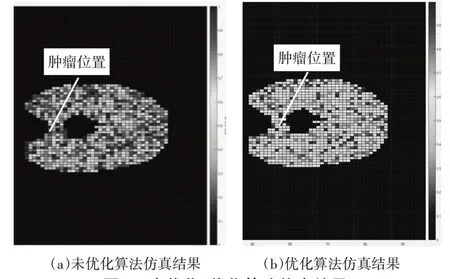
图7 未优化、优化算法仿真结果

表3 未优化、优化算法检测时间与资源消耗对比
5 结语
本文按照建模、仿真、数据处理的顺序逐步实现了人脑肿瘤的检测和定位,一定程度上克服了先前利用超宽带微波成像实现在复杂环境中(如人脑内部)无法成像的缺点[19],并在检测效率和资源消耗方面有所优化。然而本方法仍有待继续改进与深化,例如算法环境设置为肿瘤所在的二维平面,而在现代医学实际检测中,应面向整个头部组织,然而三维结构中的组织复杂,计算量大,对天线阵列,所选激励和算法的要求都更为严苛,实现难度更大。
利用电磁学理论进行肿瘤检测的方法目前仍然处于开发和尝试阶段,而如何突破此方法的局限和难题,使其适用性更广,可实现性更强,可操作性更佳仍然是未来研究的方向。
