脲酶驱动不同晶型碳酸钙微纳米颗粒的制备
2021-10-31周惠田志锋唐小微修志龙
周惠,田志锋,唐小微,修志龙
(1大连理工大学生物工程学院,辽宁大连 116024;2大连理工大学土木工程学院,辽宁大连 116024)
引 言
碳酸钙(CaCO3)的微纳米颗粒具备尺寸小、比表面积大、高空隙率等优良特性,不仅作为填充材料广泛应用于涂料、塑料、油墨、造纸等领域[1-5],而且因其良好的生物相容性和无毒性而用作催化剂载体、药物输送载体、功能材料模板、生物传感器等,在食品工业[6-7]、生物医学[8-10]、环境工业[11-13]等领域有潜在的应用前景,因此碳酸钙微纳米颗粒的制备成为当前学者们研究的热点课题。CaCO3晶体可分为方解石、文石和球霰石三种不同的结晶形态,分属三方、正交和立方晶系,其中球霰石的热力学性质最不稳定,在一定条件下易转化为方解石或文石,所以要想获得亚稳定的球霰石具有一定的挑战性。
制备微纳米CaCO3的方法有机械粉碎法、石灰乳通CO2法、可溶性碳酸盐和钙盐反应法以及微生物诱导沉淀法(microbially induced precipitation,MIP)。机械粉碎法是通过机械压力加工粉碎获得CaCO3粉末,但是这种方法难以获得粒径较小的CaCO3。石灰乳通CO2法与可溶性碳酸盐和钙盐反应法均可获得粒径较小的CaCO3,但是获得的CaCO3颗粒分散性较差,晶型难以调控。MIP法主要应用于岩土工程领域,如地基加固、裂缝修复等[14]。已有研究结果显示,MIP法形成的CaCO3晶型主要有方解石和球霰石,粒径在10~50μm之间[15-16]。
用可溶性碳酸盐和钙盐反应法制备微纳米CaCO3时,影响CaCO3晶型、外形和尺寸的主要因素包括温度、pH、反应物浓度、添加剂种类等。通过改变反应温度可以合成不同晶型的CaCO3,温度为2~3℃时可合成菱形方解石,25℃时合成球形球霰石,40℃时合成星形球霰石[17]。反应体系中的碳酸根与钙离子反应会使溶液pH升高。随着pH的升高CaCO3晶型会发生变化,如pH=8.0时,球霰石是CaCO3的主要晶型;而pH=13时,方解石是CaCO3的主要晶型[18]。反应物浓度对CaCO3沉淀也有一定的影响,如温度为30℃时,2 mmol/L的等浓度Na2CO3和CaCl2反应可获得空心球霰石;当二者浓度增加至5.0 mmol/L,则可获得纯度较高的方解石聚集体;继续增大浓度至12.5 mmol/L,获得纳米球霰石组成的实心球形CaCO3[19]。此方法为了获得不同的CaCO3晶体,通常需要额外在反应体系中加入氨基酸[20-21]、蛋白质[22-23]、可溶性淀粉[19]、聚合物[24]、表面活性剂[6,25-26]等添加剂。
MIP法是利用微生物生长代谢过程中产生的CO32-,在碱性条件下与Ca2+反应形成CaCO3沉淀。菌体种类、培养基组分或代谢物的组成等都会对晶体形态产生重要的影响。如用不同的细菌物种可以从同一合成培养基中诱导生成不同数量、形状和类型的碳酸盐晶体[27]。目前,脲酶分解尿素形成CaCO3沉淀是应用最广泛的MIP方法之一[28]。脲酶催化尿素水解为1分子氨和1分子氨基甲酸[式(1)],氨基甲酸自发水解成氨和碳酸[式(2)],氨和碳酸在水中进一步离解平衡,分别形成NH4+、OH-和HCO3-、H+[式(3)和式(4)]。OH-导致pH增加,从而形成CO32-[式(5)]与溶液中Ca2+反应形成CaCO3[式(6)],反应方程式如下:
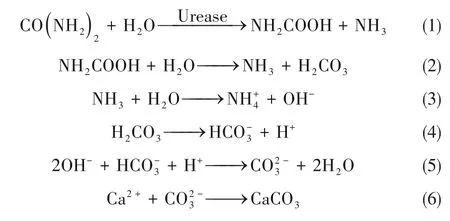
其中,S.pasteurii作为产脲酶能力较强的细菌被广泛研究,多数研究认为S.pasteurii细胞表面带有负电荷,可以提供成核位点,可在细胞表面形成稳定和连续的CaCO3沉淀[29]。但是,活菌液和灭活菌液诱导生成的CaCO3晶型不同,活菌条件下得到直径大于10μm的球型CaCO3,在S.pasteurii细胞表面的微环境中有纳米级的碳酸钙形成,而灭活菌液中得到的CaCO3晶体为典型的方解石[30]。单细胞水平MIP研究显示,细胞与沉淀物共存时产生方解石和球霰石沉淀物[31]。更有研究显示MIP过程中晶体形成分为三个阶段,初始阶段为无定形碳酸钙和球霰石沉淀,第二阶段是方解石成核以及第一阶段晶体的溶解,最后阶段主要是方解石的生长[32]。方解石种子的存在使得形成的方解石晶体更具有不规则形状[33]。此外,不同的钙源对CaCO3晶体的影响更为复杂,如氯化钙诱导的CaCO3多为稳定的方解石,乙酸钙多为片层状的球霰石,乳酸钙和葡萄糖酸钙则为更复杂的堆积状球霰石[34]。
有关细菌诱导CaCO3多晶型沉淀的研究不少,但是利用脲酶水解尿素制备微纳米CaCO3的研究鲜有报道,无细胞的脲酶溶液诱导CaCO3沉淀也难以用细胞成核的观点解释。本研究利用S.pasteurii细胞生长代谢的产物制备不同形式的脲酶溶液,考察CaCO3晶型和尺寸的影响因素,为制备空心球霰石微纳米CaCO3提供了一种新的方法。
1 实验材料和方法
1.1 微生物和试剂
菌种:S.pasteuriiBNCC136654,购自北京北纳创联生物公司。
试剂:酪蛋白胨、大豆蛋白胨、牛血清白蛋白、考马斯亮蓝G250、氯化钠、尿素、无水氯化钙、氢氧化钠、琼脂粉、盐酸、Tris,以上试剂无特殊说明均为分析纯。
1.2 实验方法
1.2.1 微生物的培养 将含15 g/L酪蛋白胨、5 g/L大豆蛋白胨、5 g/L氯化钠的培养基在121℃高温条件下灭菌15 min,20 g/L尿素采用过膜灭菌。接种量为1%,温度为30℃,转速200 r/min,在发酵罐中培养24 h。
平板活菌计数法:将OD600=4的菌液,稀释成不同梯度1、10-1、10-2、10-3、10-4、10-5、10-6、10-7、10-8、10-9、10-10,分别取不同稀释菌液100μl用无菌涂布棒均匀涂在固体培养基中,每个稀释梯度涂3个平板,30℃培养24 h,选择合适的稀释倍数进行计数。
1.2.2 不同脲酶处理液 以细菌浓度OD600=4为标准,取体积相同的发酵液(fermentation broth),离心后得上清液脲酶溶液(supernatant);同时将菌体重悬于pH相同的Tris-HCl缓冲液中,得到菌体溶液(bacterial cell);粗酶溶液(crude enzyme solution)是通过细胞破碎获得的,将装有菌体悬浮液的50 ml离心管置于冰中,在超声破碎仪中进行破碎(300 W,超声4 s,间隔4 s,超声15 min),超声结束后,12000 r/min离心10 min,收集上清液备用。
1.2.3 CaCO3沉淀的制备 在20℃条件下,将一定浓度和体积的尿素溶液与富含脲酶的溶液先反应30 min,之后在1200 r/min条件下边搅拌边加入同等浓度和体积的氯化钙溶液,反应一定时间后取样,离心(12000 r/min,5 min)后用纯净水洗涤2次,去掉CaCO3表面大部分的菌体和细胞分泌物,自然干燥后进行晶体测定及成分分析。
1.2.4 脲酶活性的测定 取1 ml菌液与9 ml 1.1 mol/L的尿素溶液混合,在30℃、pH=9的条件下反应,用电导率仪测量5 min内溶液的电导率变化,将电导率的平均变化值按式(7)计算脲酶单位时间内水解尿素的能力(mmol/(L·min)),即可表示为单位脲酶活性(U/L)。如果脲酶活性较高,可以稀释后测量[35]。
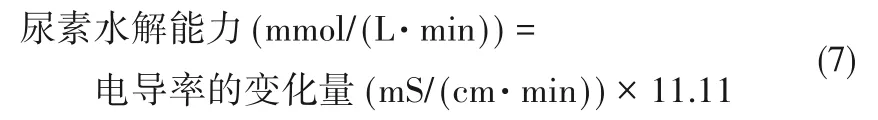
1.2.5 蛋白含量的测定 采用考马斯亮蓝法测定蛋白质的含量,取0.2 ml的待测溶液于试管中,加缓冲液至1 ml,再加入4 ml的考马斯亮蓝G-250溶液,静止10 min后,在595 nm波长下测量吸光度,再与标准曲线对比得出蛋白质含量[36]。牛血清白蛋白(BSA)作为标准蛋白。

1.2.6 扫描电镜(SEM)分析 采用钨灯丝和场发射扫描电镜对制备好的微纳米CaCO3的形貌进行观察分析,取少量CaCO3样品置于导电胶带上,用氮吹仪吹去表面多余样品,对其进行喷金处理后测试样品,加速电压为20 kV,分辨率为3.0。用ImageJ软件对CaCO3颗粒的大小进行分析,每个样品组取3张不同图像,每幅图像测量50个不同颗粒[18]。
1.2.7 X射线衍射仪(XRD)分析X射线用Cu Kα源产生,发射电流75 mA,电压为12 kV,扫描范围为2θ=3°~80°,扫描速度为10(°)/min,步长0.01°,将1~3 mg的样品放入仪器进行测试。
根据以下公式计算不同体系中方解石和球霰石的摩尔分数[25]:
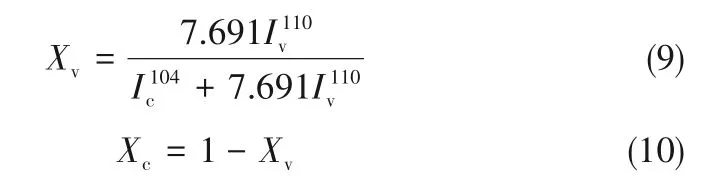
1.2.8 傅里叶红外光谱(FTIR)分析 将少量CaCO3粉末与KBr颗粒混合充分研磨,之后在4000~500 cm-1波数范围内以0.2 cm/s的速度收集光谱。
2 结果与讨论
2.1 不同脲酶催化体系中脲酶活性和反应过程中pH的变化
细菌浓度OD600=4时,平板活菌计数法得到细胞数为1.3×108CFU/ml。对不同脲酶催化体系中的脲酶活性和蛋白浓度进行测定,计算出脲酶的比活性,结果如表1所示。在发酵液中,脲酶比活性较低,为(4.06±0.12)U/g;而在细胞破碎后获得的粗酶液中,脲酶比活性较高,为(6.63±0.21)U/g。这是因为脲酶是一种胞内酶,细胞破碎后会释放较多的脲酶到环境中。上清液和菌体溶液中脲酶比活性分别为(4.28±0.12)U/g和(6.05±0.01)U/g。

表1 不同溶液的脲酶活性测定结果Table 1 The results of urease activity in different solutions
对不同体系脲酶催化制备碳酸钙(加入氯化钙后)过程中30 min内pH的变化进行监测,结果如图1所示。在加入氯化钙的瞬间,溶液中的碳酸根与钙离子迅速反应,pH快速降低。发酵液和上清液催化反应的pH变化范围接近,在8.09~8.36之间;菌体和粗酶溶液催化反应的pH变化范围在8.41~8.65之间。pH的变化主要是由溶液中离子的变化引起的,菌体和粗脲酶溶液中的脲酶比活性较高,相同时间内水解尿素产生的NH4+、HCO3-、OH-较多,所以导致反应过程中pH偏高。
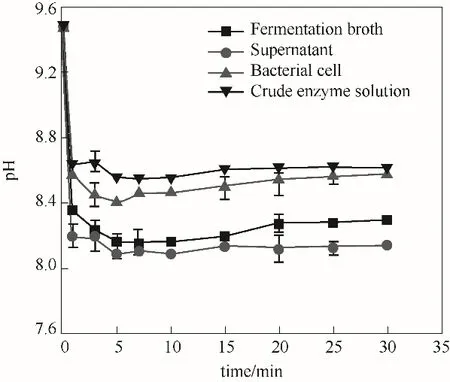
图1 不同脲酶溶液催化反应30 min内的pH变化Fig.1 pH changes within 30 min during reaction catalyzed by urease in different solutions
2.2 不同脲酶溶液对CaCO3形貌和尺寸的影响
不同脲酶体系催化制备的CaCO3扫描电镜图(图2)显示,不同催化体系可以得到不同晶型的CaCO3颗粒,包括球形、方形和椭圆形。发酵液脲酶催化获得大小不均一的球形CaCO3[图2(a)],粒径均值为(3.32±0.87)μm[图2(c)];上清液脲酶催化获得粒径较为均一的球形CaCO3[图2(b)],粒径均值为(1.36±0.27)μm[图2(d)]。菌体脲酶催化获得的CaCO3外貌表现为大小不一的立方体[图2(e)],而粗酶液催化获得的CaCO3外貌有椭圆形和球形[图2(f)]。CO2-3的含量会影响碳酸钙的成核生长[37],脲酶水解尿素产生的CO2-3在不同时间浓度不同,与Ca2+反应成核生长时间不同,造成碳酸钙粒径大小不均一。
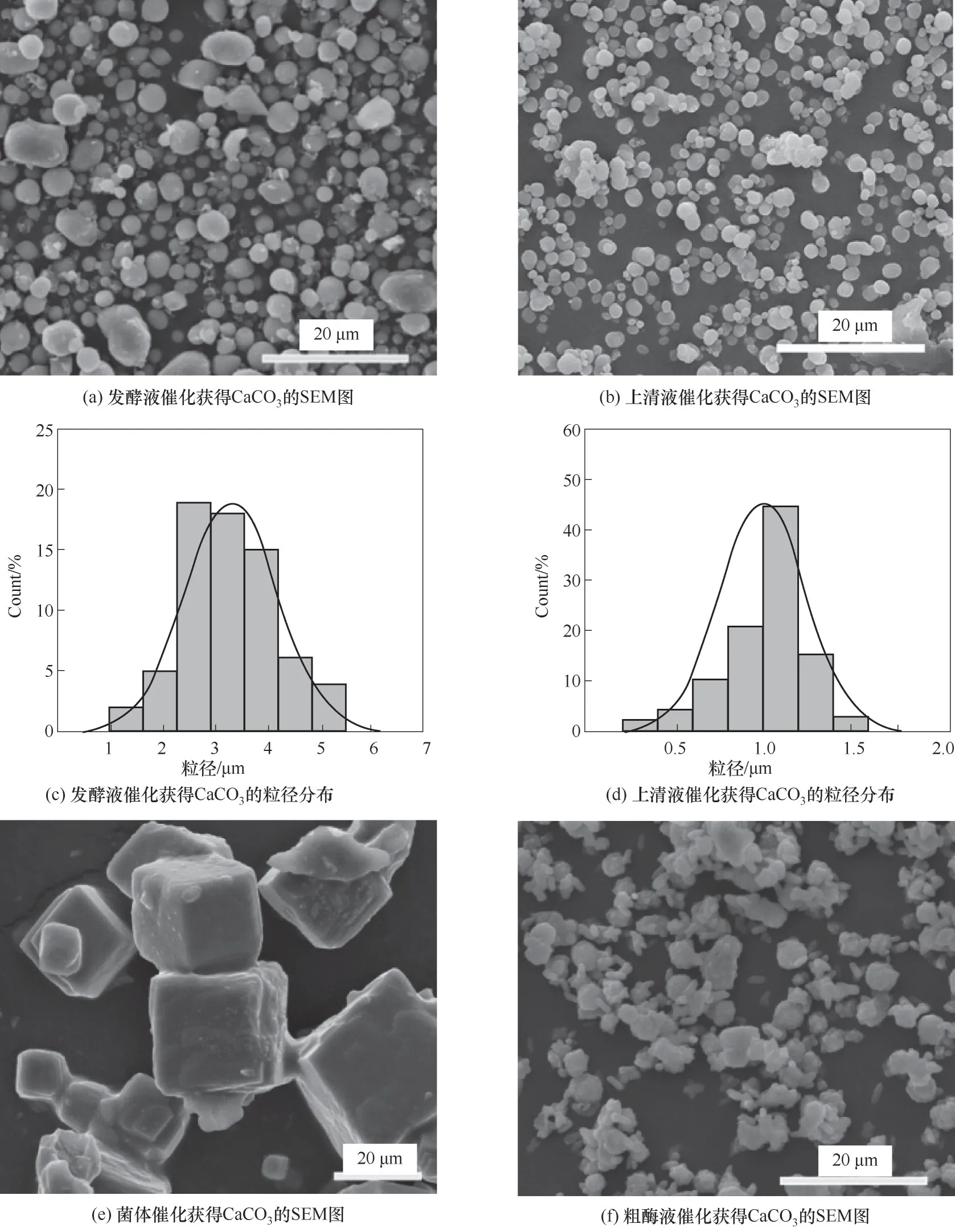
图2 不同脲酶溶液催化获得CaCO3沉淀的SEM图像和粒径分布Fig.2 SEM images and particle size distribution of CaCO3 precipitates prepared by urease in different solutions
进一步用XRD表征不同催化体系中形成的CaCO3晶型。XRD中球霰石的特征峰在21.004°、24.972°、27.124°、32.861°、43.945°、50.269°,对应于(004)、(110)、(112)、(114)、(300)、(118)晶面。方解石的特征峰在23.016°、29.406°、35.925°、39.381°、47.075°,对应于(012)、(104)、(110)、(113)、(024)晶面。从图3的XRD图中发现,发酵液和粗酶液催化获得的CaCO3中既有方解石,又有球霰石,而上清液催化获得的CaCO3为纯球霰石,菌体催化获得的CaCO3晶型主要为方解石。
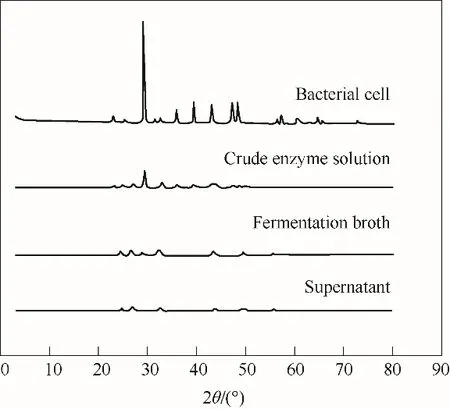
图3 不同脲酶溶液催化获得CaCO3沉淀的XRD图像(Bacterial cells/Crude enzyme solution/Fermentation broth/Supernatant分别代表菌体/粗酶液/发酵液/上清液Fig.3 XRD images of CaCO3 precipitation obtained by urease in different solutions
不同脲酶体系催化获得的球霰石和方解石比例如表2所示,发酵液催化获得的球霰石占比为88.10%,方解石占比为11.90%;上清液催化获得的CaCO3均为球霰石,占比为100.00%;菌体催化获得的方解石占比为100.00%;粗酶液催化获得的球霰石占比为53.26%,方解石占比为46.74%。

表2 不同脲酶溶液中球霰石和方解石的占比Table 2 Proportion of vaterite and calcite by urease in different solutions
用场发射扫描电镜对上清液催化获得的纯球霰石进一步观察,发现微米级球霰石表面是由粒径更小的纳米球霰石组成的[图4(a)],这些纳米球霰石的平均粒径为(25.12±4.76)nm[图4(d)]。微米级球霰石表面为有缝隙的多孔结构[图4(b)];同时也发现由纳米级球霰石组成的微米级球霰石内部是一种中空结构[图4(c)]。这与Wei等[19]以淀粉为模板,在碳酸钠和氯化钙的浓度为2 mmol/L时形成的球霰石结构类似。细胞的某些分泌物可能具有与淀粉类似的模板作用。此外,在粗酶液催化获得的CaCO3中,发现椭圆形CaCO3表面同样由纳米球霰石组成[图4(e)],但尚不清楚其内部结构;在粗酶液和发酵液催化获得的CaCO3中观察到的球体包括由球形 和 层 状CaCO3构 成 的 球 体[图4(f)、(g)]。S.pasteurii培养基中含有丰富的蛋白质,在赋形剂对CaCO3晶体转化的影响研究中发现添加酪蛋白会增加球霰石含量,其次是方解石[25]。研究显示Ca2+浓度在0.5 mol/L时不会抑制脲酶活性,且S.pasteurii水解尿素速率的提高可诱导足够量的方解石沉淀[38]。

图4 球霰石和粗脲酶溶液催化获得CaCO3晶体的形态Fig.4 Morphology of vaterite and CaCO3crystal prepared by crude enzyme solution
对不同脲酶体系催化制备的CaCO3进行红外光谱分析,结果如图5所示,方解石的特征吸收峰为1421、1082、876、713 cm-1,分别对应C—O反对称伸缩振动、C—O对称伸缩振动、O—C—O面外变形振动和O—C—O的面内变形振动。球霰石的特征吸收峰为1421、1082、870、750 cm-1,分别对应C—O反对称伸缩振动、C—O对称伸缩振动、O—C—O面外变形振动和O—C—O的面内变形振动。明显观察到粗酶液催化获得的CaCO3晶体在1140 cm-1处含有羟基的一个强特征峰,可能是细胞内富含带有羟基的物质。在CaCO3成核过程中,羟基对CaCO3形态的影响可以用自组装分子外部顺序的不确定性来解释[39]。羟基自由地围绕Cn-X键旋转,但是由于氢键的作用,使得围绕C键的羟基表面的外部顺序是固定的,所以CaCO3成核朝两个相反的方向进行,形成椭圆型CaCO3[40]。

图5 不同脲酶溶液催化形成的CaCO3晶体红外谱图Fig.5 Infrared spectra of CaCO3 precipitates
2.3 脲酶活性和反应物浓度对球霰石的影响
脲酶活性不仅影响尿素的水解速率,而且脲酶作为一种蛋白质对CaCO3晶体也有一定的影响。在温度为20℃,转速为1200 r/min,反应物(尿素和氯化钙)浓度为0.5 mol/L条件下,用活性分别为2、4、8、16 mmol/(L·min)的脲酶液催化制备CaCO3,分别在反应时间<1 min内和30 min时取样观察,结果如图6所示。随着脲酶活性的增强,CaCO3形态越来越规则,呈现为球形,而且在反应1 min内获得的CaCO3形态明显比30 min后形态更加规则,说明脲酶活性高有利于球形球霰石晶体的形成。较低的脲酶活性可能不足以支撑CaCO3成核后保持球体的形态。

图6 脲酶活性对球霰石的影响[(a)~(d)的反应时间<1 min;(e)~(h)的反应时间是30 min]Fig.6 Effect of urease activity on vaterite urease activity/(mmol/(L·min)):(a),(e)2;(b),(f)4;(c),(g)8;(d),(h)16
球霰石的粒径与反应物浓度有关,浓度越大,粒径越大。为了获得粒径更小的球霰石,探索了反应物浓度对粒径的影响。在温度为20℃、转速为1200 r/min、脲酶活性为8 mmol/(L·min)时,反应物(尿素和氯化钙)浓度设为0.05、0.1、0.3、0.5 mol/L情况下制备球霰石,分别在反应时间<1 min内和30 min时取样观察,结果如图7和图8所示。在不同反应物浓度中,极短时间(<1 min)内形成的球霰石粒径较大,30 min时球霰石粒径较小。说明CaCO3发生了二次成核,可能是CaCO3的自组装或溶解和再沉淀所致[41-42]。反应时间<1 min时,随着反应物浓度的增大,球霰石粒径减小。反应物浓度为0.05 mol/L时,球霰石平均粒径为(11.21±1.63)μm;反应物浓度为0.5 mol/L时,球霰石平均粒径为(2.9±0.42)μm。而在30 min时,随着反应物浓度的增大,球霰石粒径的变化较小,均在1μm左右。

图7 反应物浓度对球霰石的影响[(a)~(d)的反应时间<1 min;(e)~(h)的反应时间是30 min]Fig.7 Effect of reactant concentration on vaterite reactant concentration:(a),(e)0.05 mol/L;(b),(f)0.1 mol/L;(c),(g)0.3 mol/L;(d),(h)0.5 mol/L
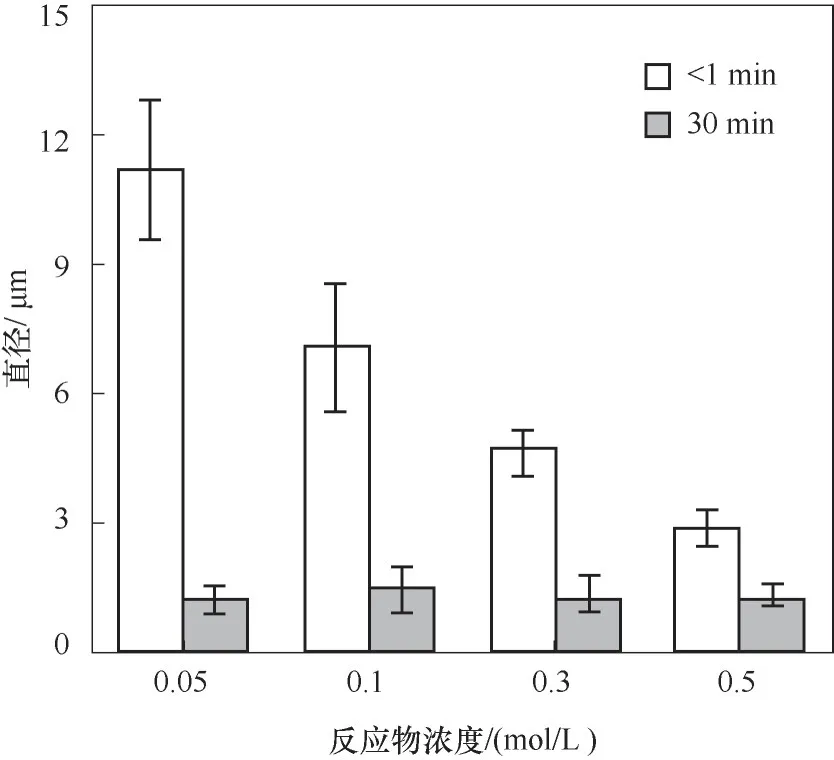
图8 不同反应物浓度和时间对球霰石平均粒径的影响Fig.8 Average particle size of vaterite under different reactant concentrations at<1 min and 30 min
2.4 球霰石稳定性的探究
球霰石是一种亚稳态晶体,并且比CaCO3其他晶型具有更高的溶解度。在水溶液中,亚稳态的球霰石很容易在3 min内通过溶解再结晶的方式向方解石转化[9]。为了延长球霰石的存在时间,获得较稳定的球霰石,往往通过加入添加剂来实现。事实证明,无论是有机添加剂还是无机添加剂,都会对晶体的生长速率起重要作用,并且可以抑制球霰石转变为方解石[43]。
以0.5 mol/L碳酸钠和0.5 mol/L氯化钙化学反应作为对照组,对脲酶溶液催化获得的纯球霰石稳定性进行探究。结果发现在水溶液中,对照组在极短时间(<1 min)内获得的CaCO3有方形和球形两种形态[图9(a)],而在30 min时获得的CaCO3只有方形[图9(b)],在第7天和第14天获得的CaCO3为方形聚集体[图9(c)、(d)]。脲酶催化制备的纯球霰石组中,在极短时间(<1 min)和30 min时获得的CaCO3只有球形[图9(e)、(f)],直到第7天才观察到球形CaCO3的变形体,出现菱形CaCO3[图9(g)],到第14天时球霰石全部变为方形的聚集体[图9(h)]。
XRD图显示了对照组和球霰石组在不同时间的存在状态(图10),从上到下的XRD谱图分别代表图9(a)~(h)的CaCO3晶体。在对照组中,极短时间(<1 min)内存在少量球霰石,大部分是方解石;30 min时球霰石特征峰消失,显示均为方解石;第7天和第14天均为方解石特征峰。纯球霰石组中,极短时间(<1 min)内和30 min时,均为球霰石特征峰,无方解石特征峰存在;在第7天出现方解石特征峰,证明球霰石转变为方解石;第14天球霰石的特征峰消失,溶液中均为方解石。表3显示了对照组和纯球霰石组不同时间方解石和球霰石的含量。

表3 对照组和纯球霰石组在不同时间球霰石和方解石的占比Table 3 Proportion of vaterite and calcite in control group and pure vaterite group at different time

图9 方解石和球霰石在不同时间的SEM图(a)~(d)分别是对照组在<1 min、30 min、7 d、14 d时的晶体形态;(e)~(h)分别是纯球霰石组在<1 min、30 min、7 d、14 d时的晶体形态Fig.9 SEM of calcite and vaterite at different time(a)—(d)were the crystal morphology of the control group at<1 min,30 min,7 d and 14 d,respectively;(e)—(h)were the crystal morphology of the pure vaterite group at<1 min,30 min,7 d and 14 d,respectively
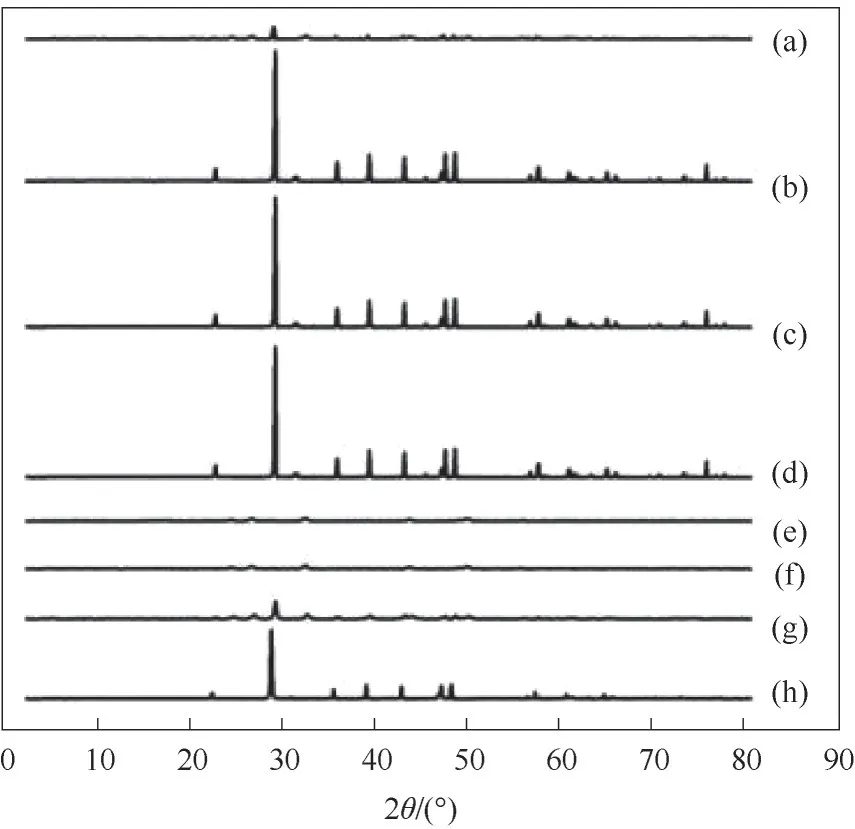
图10 对照组和纯球霰石组在不同时间的XRD谱图(a)对照组,<1 min;(b)对照组,30 min;(c)对照组,7 d;(d)对照组,14 d;(e)球霰石组,<1 min;(f)球霰石组,30 min;(g)球霰石组,7 d;(h)球霰石组,14 dFig.10 XRD of control group and pure vaterite group at different time(a)control group,<1 min;(b)control group,30 min;(c)control group,7 d;(d)control group,14 d;(e)vaterite group,<1 min;(f)vaterite group,30 min;(g)vaterite group,7 d;(h)vaterite group,14 d
有研究提出CaCO3结晶的过程是由无定形CaCO3转化为球霰石再转化为方解石[44]。通过对球霰石稳定性的探究,未观察到球霰石之前的CaCO3存在形态,脲酶催化获得的纯球霰石在水溶液中存在较长时间可能是细胞代谢产物延长了球霰石向方解石转变的时间。
3 结 论
不同脲酶溶液催化获得的CaCO3晶体具有不同的形态。上清液和菌体酶液催化获得的CaCO3分别为纯球霰石和纯方解石;发酵液催化获得球霰石含量较多,方解石含量较少;粗酶液催化获得球霰石和方解石含量约为1∶1。脲酶催化获得的微米级球霰石是由纳米球霰石组成,且纳米球霰石之间存在孔隙。在反应物浓度为0.5 mol/L时,脲酶活性越高越有利于球霰石的形成。脲酶活性为8 mmol/(L·min)时,极短时间(<1 min)内球霰石粒径随着反应物浓度增大而减小;30 min时不同反应物浓度获得的球霰石的粒径均为1μm左右。与化学法(碳酸钠和氯化钙反应)获得的CaCO3相比较,脲酶催化获得的纯球霰石在水溶液中可保存较长时间(7 d),有利于药物载体的开发利用。
球霰石在药物载体中有巨大的应用潜力。脲酶催化可获得由纳米级球霰石组成的多孔微米球霰石,比化学法制备的球霰石更有潜力,但相比磁性复合球霰石[45]的可控性要差,具有磁性的物质(如Fe3O4和α-Fe2O3)可通过外部磁场控制,实现磁性复合球霰石的定向移动,而本实验中脲酶催化获得的球霰石中不含磁性物质,缺乏这种定向操控。可以借鉴硫酸铁和氨水反应制备磁性α-Fe2O3纳米颗粒[46]加以改进,因为尿素酶解会产生氨水,这部分工作将在后续研究报告中进一步探讨。
