燃煤烟气中Cr2O3生成及其在CaO的吸附研究
2021-10-12汤吉昀张肖阳
汤吉昀,陈 娟,张肖阳,崔 琳,董 勇
(1.山东大学 燃煤污染物减排国家工程实验室,山东 济南 260061;2.昌吉学院 物理系,新疆 昌吉 831100)
0 引 言
铬等痕量元素主要来源于燃煤电站等固定源[1-4],具有很高的毒性[5-10]。随着燃煤电站烟气的排放,铬容易进入人体对肝、肾等内脏器官造成损伤,也会对生态系统造成影响[11]。2011年,国务院批复实施的《重金属污染综合防治“十二五”规划》明确指出,铬为重点的重金属污染物[12];2017年,广东省发布的《广东省重金属污染综合防治“十三五”规划》,进一步提出减少重点防控的铬等5种元素的重金属污染物[13];2019年,铬及其化合物被列入《有毒有害大气污染物名录(2018年)》[14]。 “十四五”期间,政府部门为保障国家能源安全和电力科学发展,对三氧化硫、氨、重金属等进一步减排控制[15]。因此,研究铬在烟气中的转化及控制具有重要意义。
煤中Cr主要以无机和有机的形式存在,无机态Cr以铬铁矿的形式或替代晶体中原子的形式存在于晶体中,有机态Cr易与有机基团或金属形成络合物[16]。一般,Cr在煤中主要以Cr3+的形式存在,传统燃煤电站中Cr6+的含量占总Cr含量的5%左右[17-18],另外也有测量发现为8.7%[19]。铬在煤粉燃烧过程中由内挥发到烟气,但伴随炉膛温度、气氛的改变,烟气中铬的存在形式也发生转化[20]。有学者[21]测量发现燃煤电站飞灰中Cr的含量达到0.00 μg/L~82.83 μg/L,其中Cr6+要明显高于Cr3+,Cr的毒性主要依赖于价态,在燃烧过程中Cr3+易被氧化为剧毒的Cr6+。由于Cr6+对环境和人体健康影响尤为突出,因此研究铬在煤燃烧过程中的迁移转化具有重要意义。

研究发现,烟气中存在的O2、HCl、SO2和H2O易对Cr的氧化还原反应造成一定的影响[27]。O2分子的电负性较大,易与烟气中的Cr发生反应,故O2对于Cr3+向Cr6+的转化不容忽视。目前,O2对Cr在迁移转化中的作用机理尚不明朗,且Cr含量较少,反应迅速,很难通过实验对其进行精确研究。
笔者利用分子模拟方法[28-30],采用密度泛函理论(Density Functional Theory,DFT)对烟气Cr和CrO与O2反应生成Cr2O3的反应过程进行模拟并分析其反应机理,同时研究了 Cr2O3被CaO吸附固化的特性。
1 计算方法
以下全部结构和反应路径均在Materials Studio软件的DMol3模块计算完成。其中,采用GGA(Generalized Gradient Approximations)-PBE(Perdew Burke and Ernzerhof)[28]泛函,在DNP基组水平上进行计算,自洽场(SCF)收敛标准为1.0×10-5Ha。对分子结构优化后,分析其振动频率,若无虚频,则该结构为最低能量结构;若有且只有1个虚频,则为1个过渡态。铬的氧化物在CaO表面的吸附能由下列方程计算得来:E(reaction)=E(Cr2O3/CaO)-E(Cr2O3)-E(CaO)。其中,涉及的反应见表1。同时,在500 K、800 K、1 100 K、1 400 K、1 700 K和2 000 K时,对烟气中生成Cr2O3的过程进行热力学计算。

表1 Cr的基元反应Table 1 The elementary reaction of Cr
2 结果与讨论
2.1 铬在烟气中存在形态的密度泛函分析
笔者利用密度泛函分析了Cr2O3的生成。对反应中相关的分子结构进行优化,所得稳定构型如图1所示。

图1 各分子结构示意图Fig.1 Structure diagram of molecules
优化得到的分子结构参数见表2,其键长、键角参数均与相关文献吻合较好,说明计算方法合理,结果较为准确。

表2 分子结构参数Table 2 Molecular structure parameter
2.1.1 Cr的氧化过程
在Cr被氧化为CrO的(Cr+O2→IM1→TS1→IM2→CrO+O)反应过程中(如图2所示),O2与Cr单质吸附后成键,此时Cr-O长度为1.845 Å;O—O键从1.227Å被拉伸为1.443 Å,表明O2分子被激活。此时,形成中间体IM1(Intermediate,IM)。随后O—O键断裂,经过渡态TS1(Transition State,TS)之后,形成更加稳定的中间体IM2。最后,1个O解离,反应生成CrO。

图2 Cr+O2→CrO+O的反应过程示意Fig.2 Reaction process analysis of Cr+O2→CrO+O
在Cr被氧化为CrO的过程中,终态能量比初始能量低43.06 kcal/mol,反应为放热反应。对该过程振动频率分析后,其唯一虚频为-902.82 cm-1,振动强度为2.86 km/mol,步骤能垒为12.048 kcal/mol,反应热为-70.884 kcal/mol。
烟气中O2浓度增大后,单质Cr可被直接氧化为CrO2。Cr氧化为CrO2的过程(Cr+O2→IM1→TS1→FS→CrO2)如图3所示。

图3 Cr+O2→CrO2的反应过程示意Fig.3 Reaction process analysis of Cr+O2→CrO2
由图3可知,反应开始后,Cr与O2吸附后成键,O—O键长由1.227 Å拉伸到1.443 Å,Cr—O键为1.845 Å/1.845 Å。随后,在TS1之后,O—O键被Cr拉断,形成CrO2。该反应过程,终态能量比初始能量低223.82 kcal/mol,为放热反应,需克服12.046 kcal/mol的能垒,释放-70.886 kcal/mol的反应热。经频率计算后,存在的唯一虚频为-904.42 cm-1,对应强度为3.12 km/mol。
2.1.2 CrO的氧化过程

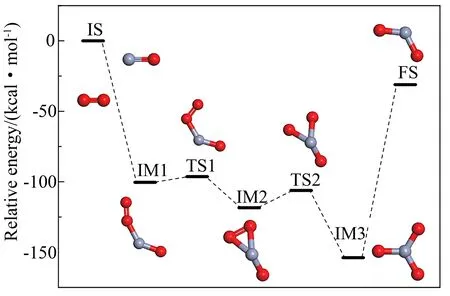
图4 CrO+O2→CrO2+O的反应过程示意Fig.4 Reaction process analysis of CrO+O2→CrO2+O
2.1.3 Cr2O3生成的过程
CrO和CrO2反应生成Cr2O3的过程(CrO+CrO2→IM1→Cr2O3)如图5所示。反应过程中,CrO和CrO2逐渐接近生成IM1,且频率计算均为正值,说明IM1为稳定构型。该过程无反应能垒,为物理吸附过程,释放出50.44 kcal/mol的热量。随着结构进一步优化,得到终态FS,释放了14 kcal/mol的热量。由CrO和CrO2反应生成Cr2O3的过程为物理吸附,该过程无能垒,过程较易发生。

图5 CrO+CrO2→Cr2O3的反应过程示意Fig.5 Reaction process analysis of CrO+CrO2→Cr2O3
2.2 烟气中Cr2O3生成的热力学分析
通过对文中可逆反应的分析,可以计算出不同温度下各反应的平衡常数,对其进一步研究具有重要意义,结果见表3。

表3 不同温度下各反应的平衡常数Table 3 Equilibrium constants for each reaction at different temperatures
由表3可知,各可逆反应的平衡常数随温度的升高而降低,该规律与放热反应的变化相一致。其中,反应(1)、(2)和(4)平衡常数受温度影响较大,但均大于105,可认为该过程为单向反应。反应(3)的平衡常数K也明显受到温度的影响。温度较低时,具有较大的平衡常数,此时反应物转化率高;当温度超过1 700 K,平衡常数开始减小,反应进行不完全,转化率偏低。因此,燃煤烟气中Cr向Cr2O3转化的路径容易进行,是Cr2O3生成的主要途径。
2.3 烟气中Cr2O3生成的动力学分析
经过动力学分析,可调控化学反应向有益的方向进行,促进主反应速率。反应的正、逆反应速率常数kf、kr随温度的变化如图6、7所示,图中纵坐标为kf、kr的对数。

图6 各反应lg kf随反应温度的变化Fig.6 Changes of lg kf with reaction temperature

图7 各反应lgkr随反应温度的变化Fig.7 Changes of lgkr with reaction temperature
从图6、7中可看到,正、逆反应速率常数曲线随温度升高而降低,不符合范特霍夫规律,且受温度影响较大。Cr→CrO/CrO2过程的反应速率曲线表明,正反应速率较高,正向反应进行完全。然而,从CrO到CrO2需经过TS1、TS2,其中TS1的正、逆反应速率常数较高,且保持相对稳定的水平;TS2受温度的影响较大,正、逆反应速率缓慢。因此,该反应的关键步骤是TS2。然而,CrO+CrO2→Cr2O3是物理吸附过程,不需要克服能垒即可自发进行。因此,Cr2O3是燃煤烟气中主要的存在形式。
2.4 Cr2O3分子在CaO表面的吸附特性分析
由上述内容可知Cr2O3是烟气中Cr的主要形式,对氧化钙吸附Cr2O3的吸附机理进行研究具有重要意义。选取CaO(001)表面的3个吸附位点,分别是相邻Ca原子正上方的空位(H)、Ca-Ca键的桥位(B)和Ca正上方的顶位(T)。Cr2O3分子在CaO(001)表面吸附后构型如图8所示,对比发现Cr2O3分子距CaO(001)表面的距离分别缩短至1.796 Å、1.798 Å和1.797 Å。此时,均趋于1种吸附构型。由此表明,CaO(001)对不同吸附位点的Cr2O3分子均具有一定的吸附作用。

图8 Cr2O3分子吸附于CaO(001)面H位的优化结构示意Fig.8 Optimized configurations of hollow (H) sites adsorbed by Cr2O3 on CaO(001) face
为进一步研究氧化钙表面结构对Cr2O3分子吸附行为的影响,又计算了不同吸附位点下Cr2O3分子与CaO(001)面间的吸附能和电荷转移情况,结果见表4。

表4 不同吸附点位吸附能、电荷和键长的值Table 4 Value of adsorption energy,charge and bond length at different sites
从表4中可以看出:
(1)吸附在H、B和T位点的Cr2O3分子与CaO(001)面间的吸附能均为负值(-3.662 6 eV~-3.658 3 eV),表明CaO(001)面的不同位点对Cr2O3分子均具有吸附能力;
(2)Cr2O3分子吸附在CaO(001)面的吸附能近似相等,最终吸附后均趋于H位吸附构型(如图8所示),且此时的吸附属于化学吸附;
(3)Cr2O3分子所带负电荷数(-0.381/-0.382e)、Cr2O3分子中Cr原子与CaO(001)面的H位O原子的键长1.796 Å(H位)、1.798 Å(T位)和1.797 Å(B位)均趋于一致,进一步说明吸附后的结构稳定于H位。
吸附构型(H位)中Cr2O3的Cr与CaO(001)中O原子的态密度变化情况如图9所示,其中吸附底物CaO中的O原子记为Osorb。

图9 Cr2O3 吸附于 CaO(001)面前后的Osorb、Cr的态密度Fig.9 The DOS of Osorb、Cr after Cr2O3 adsorption on CaO(001) surface according to adsorption structure
由图9可知,Cr与Osorb的态密度峰较为尖锐,表现出较强的离域性,说明二者成键的能力增强。在CaO(001)表面吸附Cr2O3后,底物中的O与Cr2O3中Cr的态密度峰均出现向左移动的趋势,此时体系能量整体降低,构型愈加稳定。在吸附后,CaO(001)面O原子s轨道与Cr2O3分子中Cr原子的d和s轨道在-0.659 Ha出处的峰具有很好的重合度,说明二者之间存在强烈的相互作用,容易成键。同时,吸附后CaO(001)表面O原子p轨道在0.0 Ha~0.2 Ha形成新的态密度峰,与Cr2O3分子中Cr原子的d和s轨道在0.0 Ha~0.2 Ha处的态密度形成很好的重合。因此,Cr2O3在CaO(001)表面的O空位吸附后,Cr与表面O形成了Cr-O共价键,其为化学吸附,且Cr的d和s轨道均对Cr-O键的杂化产生贡献。
3 结 论
(1)从Cr→Cr2O3需经过2个反应能垒,发生在Cr+O2→CrO+O的能垒较大,其值为12.048 Kcal/mol,反应较易发生。反应CrO→Cr2O3经过能垒TS1和TS2,最大能垒为12.270 Kcal/mol,发生在TS2,是该反应的关键步骤,但能垒并不高。
(2)在研究的温度范围内,Cr与O2反应生成CrO、CrO2过程,具有较高的正反应速率,正向反应进行完全。在CrO生成CrO2的过程中,TS1的正、逆反应速率常数较高,但随温度的升高变化缓慢,保持相对稳定的水平。TS2的正反应速率常数最低,为该反应的关键步骤。CrO+CrO2→Cr2O3是物理吸附过程,不需要克服能垒即可自发进行,所以Cr2O3是燃煤烟气中主要的存在形式。
(3)步骤(1)、(2)和(4)的平衡常数K易受温度影响,但始终大于105,为单向反应。反应(3)的K也明显受到温度影响,在低温阶段K较大,反应物转化率高;温度超过1 700 K,K很小,反应不完全,反应物的转化率较低。因此,燃煤烟气中Cr向Cr2O3的转化率较高,是Cr2O3生成的主要途径。
(4)从态密度分析可知,Cr2O3化学吸附于CaO(001)表面的O空位后,Cr与CaO(001)表面O形成了Cr-O共价键,且Cr的d和s轨道均对Cr-O键的杂化产生贡献。因此。可采用CaO对Cr2O3进行吸附。
