主动脉球囊反搏泵在A型主动脉夹层术后循环衰竭患者中的应用
2021-10-09郭驹李颖王正凯艾尔肯斯依提邢强宋云林谢志毅于湘友
郭驹,李颖,王正凯,艾尔肯·斯依提,邢强,宋云林,谢志毅,于湘友
主动脉夹层(AD)是各种原因导致的主动脉壁内膜撕裂,循环中的血液通过内膜破口进入主动脉壁中层,导致中层大范围撕裂并形成夹层,属心胸外科急症之一。根据Stanford分型将AD分为A、B两型,A型指内膜破口在升主动脉,如升主动脉未累及,则为B型[1,2]。治疗A型AD的方法包括传统开放手术、杂交手术和介入治疗,目前A型AD的主要疗法是传统外科开放治疗[3]。随着技术进步,A型AD传统开放手术术后病死率仍较高,文献报道从7%~30%[4-6]不等。导致术后死亡的主要原因为心源性休克、出血和脑缺血[7,8],其中心源性休克占A型AD术后死亡的50%[9]。主动脉球囊反搏(IABP)是目前心脏术后低心排血量综合征最常用心脏机械辅助装置,具有使用简单,并发症低并能快速置入使用等优点。IABP作为辅助治疗已被推荐用于心脏手术围手术期缺血性心肌功能障碍或低心排血量综合征患者[10,11]。目前认为AD是IABP的禁忌症,主要担心夹层进展和主动脉破裂, 但目前陆续有在夹层术后患者中成功应用的个案报道[9],我们在9例A型夹层术后,药物治疗无效危及生命的循环衰竭患者中应用IABP进行抢救,现报道如下。
1 材料与方法
1.1 研究对象回顾性分析自2018年6月至2020年10月于新疆医科大学第一附医院收治的A型患者128例,其中9例在围术期接受IABP治疗,收集患者病例资料进行分析。9例患者均为男性,平均年龄51.3±9.7岁。术前由CTA明确诊断为A型,1例于外院手术治疗,术后因严重循环衰竭转入我院,8例于我院接受手术治疗,一般资料见表1。本研究经患者及家属知情同意,并通过我院伦理委员会批准。
1.2 手术资料所有患者均接受外科手术治疗,其中2例先行主动脉造影检查,1例因双侧髂总动脉闭塞给予双侧髂总动脉支架植入。8例采用胸骨正中切口,经左右冠状动脉窦灌注心脏停搏液,中心体温降至25~26℃,深低温停循环,手术方式见表1。
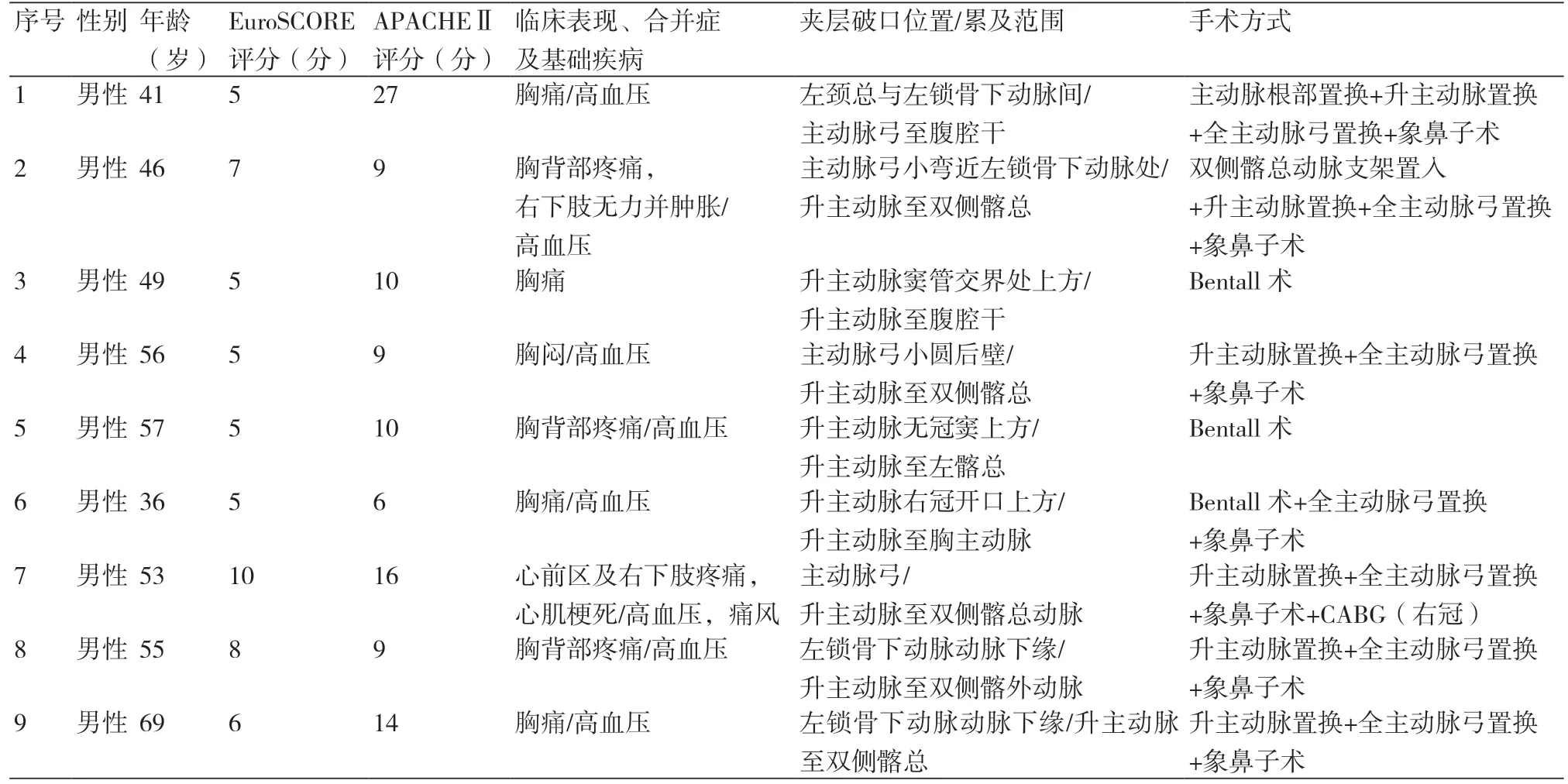
表1 患者的一般资料及手术方式
1.3 IABP治疗患者是否给予IABP治疗,取决于给予血管活性药物及液体治疗后血流动力学是否稳定。当血管活性药物评分VIS=多巴胺(μg·kg/min)+多巴酚丁胺(μg·kg/min)+10×米力农(μg·kg/min)+100×肾上腺素(μg·kg/min)+100×去甲肾上腺素(μg·kg/min)+10 000×垂体后叶素(U·kg/min)大于10分,同时应用两种药物血压进行性下降,休克表现明显,乳酸持续上升,除外低容量时可考虑给予IABP置入。根据患者身高,应用8F,40 ml球囊导管(Datascope Corporation,Fairfield,NJ,USA)。根据心率、动脉血压、血乳酸水平的变化,正性肌力药物及缩血管药物剂量,心脏超声显示心肌收缩状态来评估应用IABP后血流动力学反应。当血流动力学明显改善并稳定及血管活性药物评分(VIS)低于10分时考虑撤离IABP。在应用IABP期间给予低分子肝素进行抗凝治疗。其中8例为术后采用超声引导,经皮穿刺置入,1例于术中切开直视下置入,置入后通过胸部X线片调整导管深度,具体IABP应用见表2。
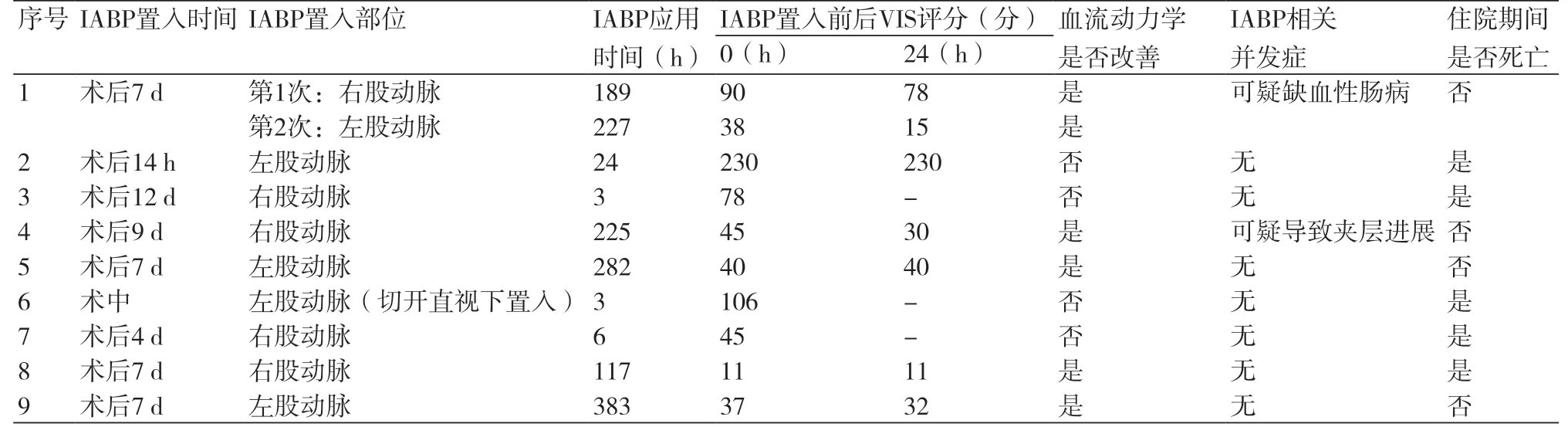
表2 IABP应用情况
1.4 统计学方法采用SPSS 25.0软件进行统计分析。计量资料以(±s)表示,组间比较采用t检验,以P<0.05时,为差异有统计学意义。
1.4 随访出院患者经电话及网络进行随访。
2 结果
9例患者接受了总计10次IABP治疗,其中1例撤离IABP后循环功能恶化再次于对侧股动脉穿刺置入,共接受2次IABP治疗。9次采用超声定位引导经皮股动脉穿刺置入,1次为术中切开股动脉直视下置入。1例因术中心源性休克无法脱离体外循环,于手术室给予置入,其余均为术后因循环衰竭在ICU内穿刺置入完成。其中5例接受6次IABP治疗,应用时间>24 h,数据完整,24 h后血流动力学明显改善,VIS评分(43.5±25.7)分降至(34.3±24)分,心率由(124.8±33)次/min降至(98.3±11.1)次/min,乳酸(2.6±1.3) mmol/L降至(2.2±0.5) mmol/L,平均动脉压由(68.5±17.2) mmHg升至(76±20.6) mmHg,肌钙蛋白-I由(1.6±1.2) μg/L降至(0.8±0.3) μg/L,其中1例因家属放弃治疗死亡;4例接受IABP治疗后血流动力学改善不明显患者,在接受IABP治疗室VIS评分(107.3±86.5)分,最终死亡。所有患者平均接受IABP治疗时间162 h(3 h~17 d),单次最长383 h,累计最长416 h。 随访4例存活出院患者,1例于当地医院因夹层破裂死亡;1例出院2周尚未复查,电话随访表其生存状况良好;1例随访半年、1例随访2年,复查CTA检查,无夹层进展及IABP相关并发症发生。5例于院内死亡,其中1例为家属放弃治疗,住院病死率55.6%。
3 讨论
AD是一种高死亡风险疾病,文献报道未经治疗的AD1周内病死率可达50%[12]。根据临床最常用的Stanford分型,Standford A型AD由于累及升主动脉及主动脉弓,发病尤为凶险、死亡率极高,即使手术治疗,术后并发症发病率及病死率仍居高不下[13,14]。
国内文献报道,术后30 d病死率高达9.1%~19.2%,术后50%的病死率与心脏和循环有关[12]。IABP在1967年由Kantrowitz首次报道成功应用于临床治疗心源性休克,之后迅速广泛应用,从最初的心肌梗死后心脏功能支持到心脏术后的心源性休克,甚至在小儿以左心功能衰竭导致的低心排的治疗中也有效[15-17]。IABP最主要的生理作用是改善冠状动脉循环及降低左心室压力和降低心脏工作负荷,决定了IABP的适应症:①左心室功能支持;②改善心肌氧供需平衡,减轻心肌缺血性损害[8,11,17]。
既往认为IABP属于主动脉夹层的禁忌症,术前夹层破口未经修补,禁用IABP,但术后AD破口经外科修补是否可以应用尚处未知。AD术后发生循环衰竭的患者在传统药物治疗无效时,结局只有死亡。在这种极端情况下,尝试循环机械支持装置治疗,取得了较好疗效。Jaussaud等在8年间给予10例A型AD术后患者应用IABP,仅2例发生IABP相关并发症,1例发生胆固醇栓塞综合征,在撤离IABP后病情迅速好转,1例为股动脉穿刺处发生假性动脉瘤需外科修复动脉,8例血流动力学改善,6例成功救治,是目前文献报道例数最多,但也仅为10例,住院病死率40%,因此对夹层术后药物治疗不佳的循环衰竭患者应用IABP认为是合理的。Weaver等[9]在2例A型夹层术后患者应用IABP,1例成功救治,1例因全心衰竭死亡,未有IABP相关并发症发生。均提供了夹层术后循环衰竭给予IABP循环机械支持的可行性证据。
AD的主要病理改变是主动脉内膜的撕裂导致主动脉壁各层分离并形成假腔,即使术后,仍可有夹层突发破裂的发生。 IABP的使用需将球囊导管放置在主动脉左锁骨下动脉开口远端,IABP工作时,通过球囊在不同时相的充盈和排空,增加舒张期冠状动脉灌注,减轻左室后负荷,达到降低心肌做功、减少心肌氧耗量的目的,改善血流动力学及左心功能。IABP最主要并发症为血管相关并发症包括:肢体、肠系膜缺血,主动脉穿孔,出血等。
在主动脉A型夹层术后出现循环衰竭、心源性休克时,当药物治疗无效,患者即将面临死亡的情况下,可谨慎考虑IABP治疗。本研究中9例患者均为A型AD,夹层累及降主动脉,并行手术治疗,术中及术后出现了循环衰竭,心源性休克。在传统药物治疗无效情况下,被动选择应用IABP。1例为术中无法撤离体外循环,选择股动脉切开,直视下置入IABP,其余均常规在超声引导下选择股动脉穿刺,植入IABP导管,通过经胸心脏超声结合胸部X线片确定并调整导管位置,其中1例经历了双侧股动脉穿刺,2次应用IABP。文献报道采用食道超声引导,避免穿刺过程中导管置入夹层假腔,因条件限制,无法行食道超声检查,采用常规超声定位引导穿刺置入,由于患者夹层未累及双侧股动脉,术前CTA未发现有降主动脉内膜存在撕裂破口。9次穿刺无1例刺入夹层假腔,可见在股动脉未受累及降主动脉无撕裂内膜出现破口情况下,常规穿刺是可行的。紧急情况下在降主动脉受累的A型夹层患者中,抢救性应用IABP相对安全可行,但尚需更多病例进行验证。
IABP在应用中对心脏功能的评价及血流动力学的监测极为重要,不仅对IABP的应用时机具有重要意义,可更好地指导血流动力学治疗,评估效果。因条件限制,未行食道超声检查,通过血流动力学监测及实验室检查,在IABP应用有效患者中发现,应用24 h后,血管活性药物剂量、心率、乳酸及肌钙蛋白水平下降,平均动脉压升高,血管活性药物指数及心率变化更为明显。
9例患者中4例存活出院,5例院内死亡,与应用IABP无关。4例存活患者5次应用IABP治疗,24 h后血流动力学明显改善,心率下降,乳酸下降,平均动脉压升高,不再加用血管活性药物剂量,并最终成功撤离IABP,平均应用IABP时间为326.5 h。5例死亡患者中4例应用后血流动力学改善不明显,治疗24 h内死亡,1例应用后血流动力学改善有效,但家属放弃治疗后死亡,平均应用IABP时间30.6 h。患者应用IABP时,VIS评分(72±62.4)分,最高1例达230分,乳酸(5.23±5) mmol/L,在应用无效患者中VIS评分及乳酸水平更高,提示应用时机过晚,如更早应用或许效果更佳。4例死亡患者应用时间不足24 h,2例仅应用3 h后死亡,患者可能已错过最佳抢救时机,不适合应用IABP救治,如更早使用,或选择动静脉体外膜肺氧合(V-A ECMO)治疗或许可改善预后。VIS评分可作为决定是否应用IABP救治的重要参考依据。
第1例患者在使用IABP后循环迅速得以稳定,在应用IABP后第3 d发生严重的腹泻、消化道出血但无消化道穿孔发生。腹泻量最大时可达4000 ml/d,持续腹泻近70 d才渐好转。除外感染及其他原因导致腹泻后,考虑原因为肠道缺血导致,除夹层本身和休克导致的肠道缺血,可能与IABP导致的肠系膜缺血存在一定关系,IABP本身可导致肠系膜缺血,但发生率较低[20]。推测在胸腹主动脉存在夹层病变时,可能增加了肠系膜缺血的发生,但未能给予完善肠系膜血管CTA检查明确,患者最终痊愈出院,随访2年,健康状况良好。第2例患者在术后应用IABP前双下肢已有缺血改变,应用中可能会加重缺血症状,并非IABP直接导致的肢体缺血。第4例患者在出院后于当地医院继续治疗期间,突然术区纵膈大量出血死亡,虽此时IABP已停用16 d,不能完全除外与IABP应用导致夹层进展并最终破的裂可能,其余未见IABP相关并发症发生。随访4例存活出院患者,1例在当地医院因夹层破裂死亡;1例出院2周尚未复查,电话随访生存状况良好;1例随访半年、1例随访2年,复查CTA检均查,无夹层进展及IABP相关并发症发生。
明确何时在夹层患者围术期循环衰竭时中应用IABP,目前尚处于探索阶段。考虑到IABP是最常用的循环机械辅助装置,尤其在发展中国家的特定人群中,花费及效能高于ECMO[17]。通过9例患者的分析,认为在药物治疗无效的夹层术后循环衰竭患者中,作为一种抢救治疗措施,应用IABP是可行的,应用前对心功能评估及时机的把握至关重要,其安全性尚需更大样本的研究进行验证,同时需警惕IABP相关并发症及夹层进展的可能性,在作出决定时需依据病情权衡患者风险及收益。
