血清ApoA1/B、Hcy、脂蛋白a在T2DM合并微血管并发症患者中的变化及预测价值
2021-09-30王志敏
王志敏
(北京市顺义区医院检验科,北京 101300)
糖尿病(diabetes mellitus,DM)是由多种病因引起的以慢性高血糖为主要特征的代谢性疾病,其中约90%为2型糖尿病(type 2 diabetes mellitus,T2DM)[1-2]。微血管病变为DM特异性并发症,可累及全身各器官组织,引起非创伤性截肢、失明、慢性肾脏病等,巨大疾病负担已构成我国公共卫生问题,阻止及延缓T2DM并发症发生、发展为临床医师共同努力目标[3-4]。血清中同型半胱氨酸(homocysteine,Hcy)含量升高,可促进血小板聚集,增加大血管、微血管并发症危险性[5];谭锦玲[6]研究指出,T2DM患者因胰岛素抵抗,长期慢性高血糖基础上易发生脂质代谢紊乱。近期研究报道,载脂蛋白A1/载脂蛋白B(apolipoprotein A1/apolipoprotein B,ApoA1/B)、脂蛋白a[lipoprotein(a),Lp(a)]在预测血管并发症发生方面优于低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)[7]。现有文献对DM微血管并发症的研究多为单一分析上述指标,较少三者综合分析探究。本研究旨在探究血清ApoA1/B、Hcy、Lp(a)在T2DM合并微血管并发症患者中的变化及预测价值,以期为临床诊治、预防T2DM患者微血管并发症提供指导。报告如下。
1 资 料 与 方 法
1.1一般资料 选取2018年1月—2020年7月我院收治的T2DM患者134例,根据是否合并微血管并发症分为合并微血管并发症组(56例)与无微血管并发症组(78例)。纳入标准:①符合《中国T2DM防治指南(2017年版)》诊断标准[8];②合并微血管并发症组符合《基层糖尿病微血管病变筛查与防治专家共识》诊断标准[9];③无家族性高胆固醇血症者;④患者及家属均自愿签署知情同意书;⑤无意识障碍。排除标准:①妊娠期糖尿病、1型糖尿病或其他特殊类型DM;②严重肝肾功能不全者;③伴有DM酮症酸中毒或高血糖高渗状态等急性并发症;④合并内分泌系统疾病,如多囊卵巢综合征、甲状腺功能异常等;⑤近1个月应用阿托伐他汀等降脂药物者;⑥妊娠试验阳性;⑦自身免疫系统疾病;⑧合并良恶性肿瘤。
本研究经医院医学伦理委员会审批通过。
1.2方法
1.2.1资料收集 收集所有患者性别、年龄、吸烟、病程、饮酒比例、合并高血压、体重指数(body mass index,BMI)、注射胰岛素及实验室指标等临床资料。
1.2.2样本采集与处理 采血前1 d患者禁食高脂饮食、停服相关药物,采集所有患者空腹12 h以上(通常8~12 h)外周静脉血2份,一份为EDTA-K3抗凝血,一份为普通真空采血管,于室温条件下,4 000 r/min离心10 min,待测。
1.2.3实验室指标检测 选用糖化血红蛋白分析仪(东曹-G8)及配套试剂,利用高效液相色谱法测定糖化血红蛋白(glycosylated hemoglobin,HbA1c)水平;选用全自动生化仪(贝克曼AU5800)及其配套试剂,利用葡萄糖氧化酶法测定空腹血糖(fasting blood-glucose,FBG)、餐后2 h血糖(2 h postprandial plasma glucose,2 hPG)水平,测定血清总胆固醇(total cholesterol,TC)、丙氨酸转氨酶(alanine aminotransferase,ALT)、高密度脂蛋白胆固醇(high density lipoprotein-cholesterol,HDL-C)、三酰甘油(triglyceride,TG)、天冬氨酸转氨酶(aspartateaminotransferase,AST)、LDL-C、尿素氮(blood usea nitrogen,BUN)、肌酐(serum creatinine,Scr)水平。FBG、2 hPG、TC、HDL-C、TG、LDL-C、BUN、Scr试剂盒购自中生北控生物科技股份有限公司,ALT、AST采用贝克曼试剂盒。
1.2.4血清ApoA1/B、Hcy、Lp(a)检测 选用全自动生化分析仪(贝克曼AU5800)进行测定,采用免疫比浊法测定ApoA1/B水平;采用循环酶法测定Hcy水平;采用胶乳免疫比浊法测定血清Lp(a)水平,试剂盒均购自中生北控生物科技股份有限公司。
1.3观察指标 ①比较2组血清ApoA1/B、Hcy、Lp(a)水平。②分析血清ApoA1/B、Hcy、Lp(a)与实验室指标(FBG、2 hPG、HbA1c、TC、TG)的相关性。③采用多因素Logistic回归方程分析T2DM合并微血管并发症的影响因素。④分析血清ApoA1/B、Hcy、Lp(a)对T2DM合并微血管并发症的预测价值。⑤分析血清ApoA1/B、Hcy、Lp(a)联合对T2DM合并微血管并发症的预测价值。
1.4统计学方法 应用SPSS19.0统计软件处理数据。计数资料比较采用χ2检验,计量资料比较采用独立样本t检验;相关性分析采用 Pearson 相关系数模型;预测效能分析采用受试者工作特征(receiver operator characteristic curve,ROC)曲线,获取曲线下面积、95%可信区间、敏感度、特异度及cut-off值,不同预测方案间曲线下面积比较采用DeLong 检验,联合诊断实施Logistic二元回归拟合,返回预测概率logit(p),将其作为独立检验变量。P<0.05为差异有统计学意义。
2 结 果
2.12组临床资料比较 2组性别、年龄、吸烟、饮酒比例、注射胰岛素、AST、ALT、Scr、BUN、HDL-C、LDL-C差异无统计学意义(P>0.05);合并微血管并发症组病程、BMI、合并高血压、FBG、2 hPG、HbA1c、TC、TG水平高于无微血管并发症组,差异有统计学意义(P<0.05)。见表1。
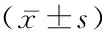
表1 2组临床资料比较Table 1 Comparison of clinical data between two groups
2.22组血清ApoA1/B、Hcy、Lp(a)水平比较 合并微血管并发症组血清ApoA1/B水平低于无微血管并发症组,Hcy、Lp(a) 水平高于无微血管并发症组,差异有统计学意义(P<0.05)。见表2。
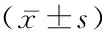
表2 2组血清ApoA1/B、Hcy、Lp(a)水平比较Table 2 Comparison of serum ApoA1/B, Hcy and Lp(a) levels between two groups
2.3血清ApoA1/B、Hcy、Lp(a)与实验室指标的相关性 Pearson相关性分析结果显示,血清ApoA1/B与FBG、2 hPG、HbA1c、TC、TG呈负相关,Hcy、Lp(a)与FBG、2 hPG、HbA1c、TC、TG呈正相关(P<0.05)。见表3。

表3 血清ApoA1/B、Hcy、Lp(a)与实验室指标相关性Table 3 Correlation between serum ApoA1/B, Hcy, Lp(a) and laboratory indicators
2.4T2DM合并微血管并发症的影响因素分析 将T2DM是否合并微血管并发症作为因变量(否=0,是=1),以病程(<5.99年=0,≥5.99年=1)、BMI(<25.28=0,≥25.28=1)、合并高血压(否=0,是=1)、血清ApoA1/B(<1.04=0,≥1.04=1)、Hcy(<15.41 μmol/L=0,≥15.41 μmol/L=1)、Lp(a)(<164.75 mg/L=0,≥164.75 mg/L=1)作为自变量,纳入Logistic回归方程,结果显示,病程、BMI、合并高血压、血清ApoA1/B、Hcy、Lp(a)是T2DM合并微血管并发症的影响因素(P<0.05)。见表4。

表4 T2DM合并微血管并发症的影响因素分析Table 4 Influencing factors of T2DM with microvascular complications
2.5血清ApoA1/B、Hcy、Lp(a)对T2DM合并微血管并发症的预测价值 绘制ROC曲线,结果显示,ApoA1/B预测T2DM合并微血管并发症的AUC为0.771,敏感度为71.79%,特异度为75.00%;Hcy预测T2DM合并微血管并发症的AUC为0.824,敏感度为66.07%,特异度为89.74%;Lp(a) 预测T2DM合并微血管并发症的AUC为0.788,敏感度为55.36%,特异度为93.59%。见表5,图1。
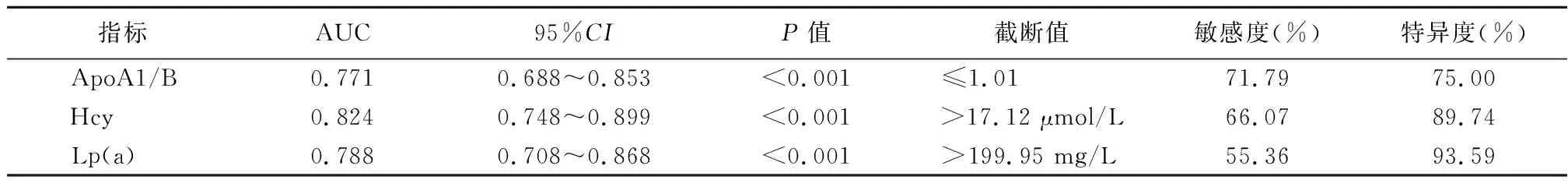
表5 血清ApoA1/B、Hcy、Lp(a)对T2DM合并微血管并发症的预测价值Table 5 The predictive value of serum ApoA1/B, Hcy, and Lp(a) in T2DM with microvascular complications

图1 血清ApoA1/B、Hcy、Lp(a)对T2DM合并微血管并发症的预测价值Figure 1 The predictive value of serum ApoA1/B, Hcy, and Lp(a) in T2DM with microvascular complications
2.6联合预测价值 将血清ApoA1/B、Hcy、Lp(a)进行Logistic二元回归拟合,返回预测概率Logit(P)作为独立检验变量,获取联合预测的AUC为0.878,95%CI:0.814~0.941,P<0.001,敏感度为73.21%,特异度为88.46%,优于各指标单独预测(P<0.05),见图2。

图2 联合预测价值Figure 2 Combined forecast value
3 讨 论
T2DM患者体内存在多种代谢紊乱,其微血管并发症发生发展机制较为复杂,目前尚未完全明确,可能是由多种病理机制共同作用、相互联系所致的结果。近来T2DM与载脂蛋白在机体脂代谢过程中的研究备受广大学者重视,ApoA1为载脂蛋白主要成分,主要负责血浆中大部分胆固醇酯转化,ApoB为LDL主要载脂蛋白,可打开细胞导入胆固醇,ApoA1/B反映血液中促动脉粥样硬化与抗动脉粥样硬化脂蛋白的平衡状态[10]。本研究结果显示,合并微血管并发症组血清ApoA1/B水平低于无微血管并发症组,分析其机制在于,T2DM患者因发生胰岛素抵抗,对脂肪分解抑制作用减弱,致使TG生成增多,HDL-C水平降低;国内外研究指出[11-12],ApoA1、ApoB分别为HDL-C和LDL-C主要结构蛋白,LDL-C水平升高具有较强致动脉粥样硬化作用,HDL-C水平升高代表抗动脉粥样硬化能力增强,故血清ApoA1/B降低,可加速动脉粥样硬化,致使微血管并发症发生。Lp(a)是在肝脏中合成的大分子复合物,为临床评价炎症所致内皮损伤重要指标,在DM合并高血压患者并发DM周围神经病变中呈高表达[13-14];既往研究显示,Hcy与心血管疾病密切相关,Hcy水平升高为微血管病变独立危险因素[15-16]。本研究结果显示,合并微血管并发症组血清Hcy、Lp(a) 水平高于无微血管并发症组(P<0.05),与上述研究结果一致。推测其原因可能为,Lp(a)主要抑制纤维蛋白溶解酶原活性,Lp(a)水平升高干扰机体纤溶系统正常运转,间接引起血管内皮细胞损伤,造成机体微循环障碍和微血管阻塞;Hcy为蛋氨酸代谢过程中重要中间产物,正常情况下其含量极低,T2DM患者Hcy无法代谢转化时,呈现异常高表达,引起血液中氧自由基生成增加,对血管内皮细胞一氧化氮活性产生抑制,造成血管内皮损害,机体凝血-纤溶平衡被打破,进而引起微血管病变发生[17-18]。
国内外研究显示,血糖水平升高可致使一氧化氮合成减少、糖化反应亢进、多元醇代谢异常等,进而引起相应损害,通过控制FBG、2 hPG、HbA1c水平,可降低相应并发症发生率[19-20]。脂肪组织除贮存能量外,还具有重要内分泌功能,可分泌多种生物活性肽,即脂肪细胞因子。脂肪细胞因子可参与调节能量代谢、免疫应答及胰岛素敏感性,TC、TG通过调节糖脂代谢、细胞分化,参与T2DM患者微血管并发症发生过程。本研究结果显示,血清ApoA1/B与FBG、2 hPG、HbA1c、TC、TG呈负相关,Hcy、Lp(a)与FBG、2 hPG、HbA1c、TC、TG呈正相关(P<0.05),提示ApoA1/B、Hcy、Lp(a)是反映T2DM患者微血管并发症发生的敏感指标。绘制ROC曲线发现,血清ApoA1/B、Hcy、Lp(a)联合预测的AUC为0.878,敏感度为73.21%,特异度为88.46%,优于各指标单独预测(P<0.05),可在一定程度上提高预测效能,为临床预测T2DM患者微血管并发症发生提供更准确数据参考,对T2DM患者微血管并发症预防、控制与治疗具有重要临床意义。此外,对于病程较长、BMI较高、合并高血压患者,微血管病变发生风险较高,需作为重点观察对象,进一步加强相关治疗或干预措施,以降低微血管病变发生率。
综上可知,T2DM合并微血管并发症患者血清ApoA1/B表达水平较低、Hcy、Lp(a)表达水平较高,三者联合检测在预测T2DM患者微血管并发症发生方面具有较高临床应用价值,可为T2DM患者微血管并发症发生诊断、预防及治疗提供新的线索与思路。但本研究选取样本量较少,可能造成数据偏移,需扩大样本量做进一步探究,以获取更为可靠的数据支持。
