基于离子交换的乙二醇富液脱盐实验研究
2021-09-22贺三张泽周雪邓志强
贺三,张泽 ,周雪 ,邓志强,3
(1.西南石油大学 石油与天然气工程学院,四川 成都 610500;2.中国石油西南油气田公司输气管理处,四川 成都 610213; 3.华南蓝天航空油料有限公司广东分公司,广东 广州 510470)
海上油气田的勘探与开发正在由浅水向深水方向发展[1-2]。在深水气田开发过程中,常常采用乙二醇再生回收工艺(MRU)防止天然气水合物生成[3]。深水气田中采出水中常含有大量的盐,会对MRU系统的设备造成腐蚀与结垢,因此需要增加乙二醇脱盐工艺。常规乙二醇脱盐工艺存在着工艺复杂、空间占用大等问题[4]。离子交换技术因其工艺简单、脱盐效果好,在水处理、海水淡化等领域广泛应用[5-7],离子交换脱盐工艺能克服常规乙二醇脱盐工艺的缺陷,成为乙二醇脱盐工艺研究与应用的新方向。本文以离子交换树脂为吸附剂,开展乙二醇富液吸附脱盐实验研究。乙二醇富液接近中性,且无腐蚀性,其中阳离子主要是 Na+、Ca2+,阴离子主要为 Cl-,因此选择工业上通用、低价的D001、D201、D113和D301树脂,探讨其吸附热力学模型。
1 实验部分
1.1 试剂与仪器
盐酸、乙二醇、氯化钠、氯化钙、硝酸银、氢氧化钠、乙二胺四乙酸二钠均为分析纯;D001阳树脂、D113阳树脂、D201阴树脂、D301阴树脂均为工业级,其主要物化特性见表1。
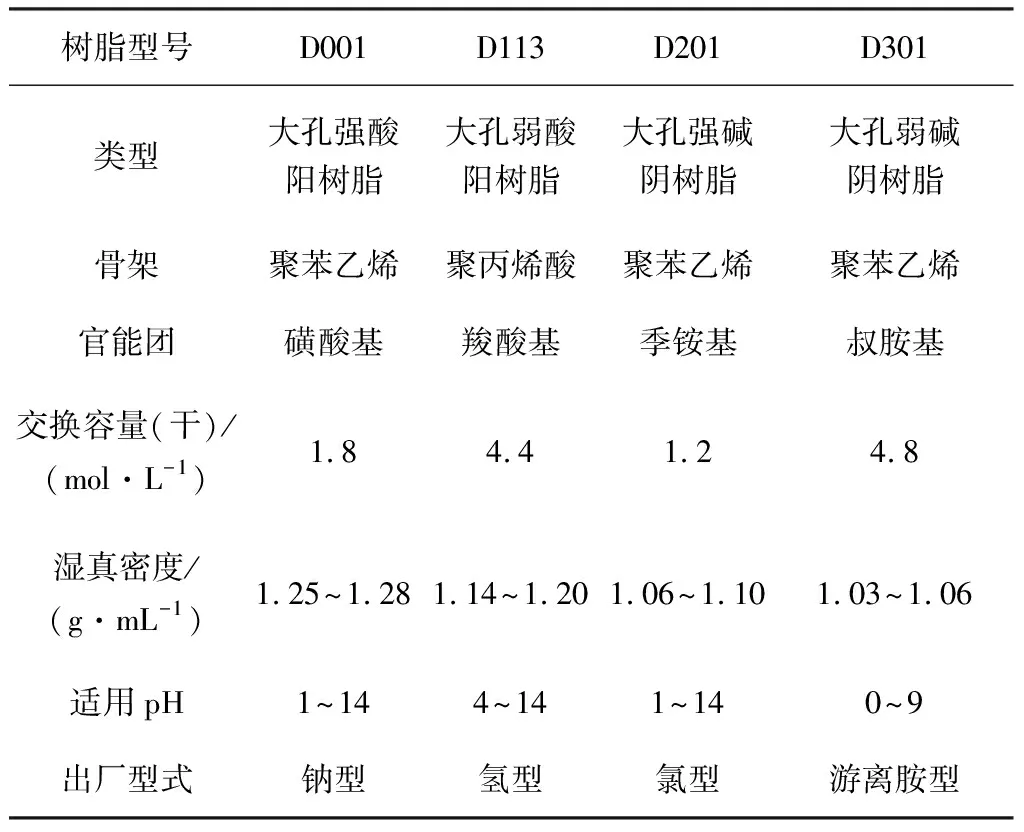
表1 离子交换树脂的主要特性Table 1 Main characteristics of ion exchange resins
85-2A恒温磁力搅拌器;HH-4数显恒温水浴锅;202型电热恒温干燥箱;PHS-3C雷磁酸度计;ESJ210-4A分析天平;MP10010D直流电场。
1.2 实验方法
1.2.1 乙二醇富液 乙二醇富液含盐量参照番禺34-1CEP平台MRU入口地层水进行设计,选取Cl-、Na+、Ca2+三个离子浓度最高的离子为研究对象[6]。另外,乙二醇富液浓度常见于60%~80%[7],本文以70%乙二醇富液为研究体系,Na+、Ca2+和Cl-的质量浓度分别为993.32,149.24,1 797.99 mg/L。
1.2.2 静态吸附实验 250 mL锥形瓶中加入200 mL 浓度70%乙二醇富液,加入200 mL树脂,将烧杯放在恒温磁力搅拌器上搅拌,温度25 ℃,记录上清液pH值变化情况,吸附结束后,测定上清液的离子浓度。按式(1)计算平衡吸附量。
(1)
式中qe——树脂平衡吸附量,mg/mL;
C0——吸附前溶液中的离子浓度,mg/L;
Ce——吸附平衡后溶液中的离子浓度,mg/L;
V——溶液体积,L;
W——树脂体积,mL。
1.2.3 吸附热力学实验 在浓度70%的乙二醇富液中,配制Cl-浓度为900~2 400 mg/L的NaCl溶液200 mL,在25~40 ℃下,加入20 mL的D201树脂,加入恒温磁力搅拌器搅拌,吸附平衡后,取上层清液测定Cl-浓度。
在浓度70%的乙二醇富液中,配制Ca2+浓度为200~1 200 mg/L的CaCl2溶液200 mL,在25~40 ℃下,用20 mL D113树脂,用恒温磁力搅拌器搅拌,吸附平衡后,取上层清液测定Ca2+浓度。
1.3 分析方法
Cl-测定采用硝酸银容量法,Ca2+测定采用乙二胺四乙酸二钠滴定法,测量方法参见GB 8538—2016《食品安全国家标准 饮用水天然矿泉水检验方法》,Na+的测定采用标准曲线法。
2 结果与讨论
2.1 树脂筛选
分别取20 mL经预处理后的4种树脂(D001、D113、D201、D301)加入到250 mL烧杯中,加入200 mL浓度70%乙二醇含盐富液,放入恒温磁力搅拌器中搅拌,温度25 ℃,记录上清液pH值变化情况,吸附结束后,测定上清液的离子浓度。阴离子交换树脂吸附后上清液pH变化情况见图1,吸附情况见表2。

图1 阴离子交换树脂吸附后上清液pH变化情况Fig.1 Changes of pH value after adsorption of supernatant by anion exchange resin
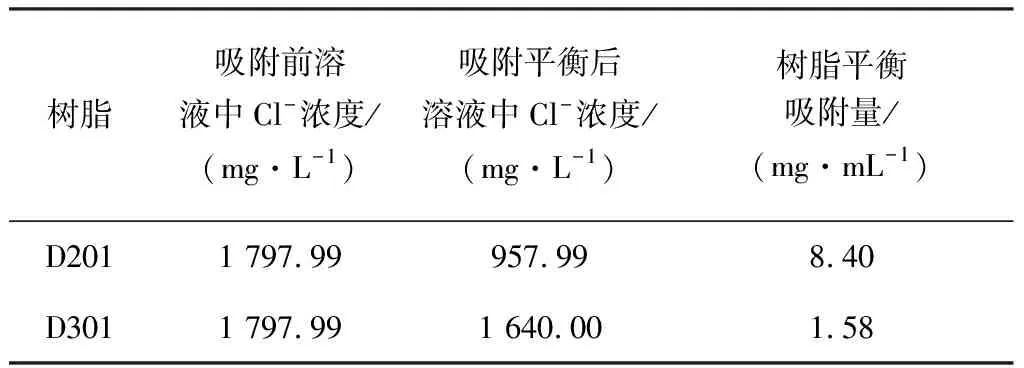
表2 阴离子交换树脂吸附情况Table 2 Adsorption of anion exchange resin
由图1可知,两种树脂吸附后,上清液的pH都呈上升趋势,D201树脂吸附后,上清液pH值高于D301树脂。阴离子交换树脂中的交换基团与溶液中的Cl-发生交换,产生大量OH-,导致上清液的pH值升高,D201树脂属于强碱型树脂,树脂的吸附效果优于弱碱型树脂D301,D201树脂的平衡吸附量为8.4 mg/mL,D301树脂的平衡吸附量为1.58 mg/mL,D201树脂的平衡吸附量远大于D301树脂,故阴离子交换树脂选择D201树脂。
阳离子交换树脂吸附后上清液pH变化情况见图2,吸附情况见表3。
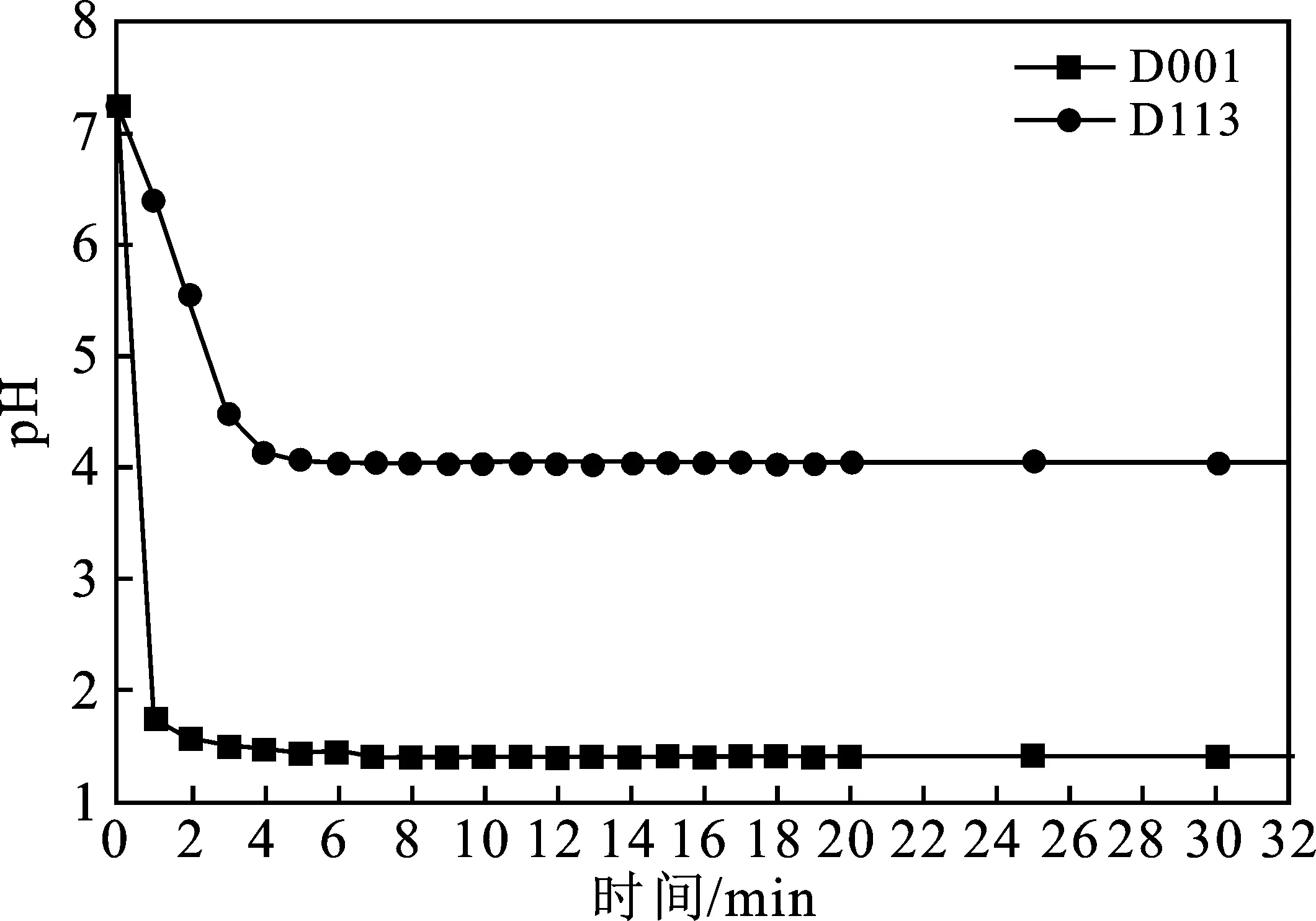
图2 阳离子交换树脂吸附后上清液pH变化情况Fig.2 Changes of pH value after adsorption of supernatant by cation exchange resin
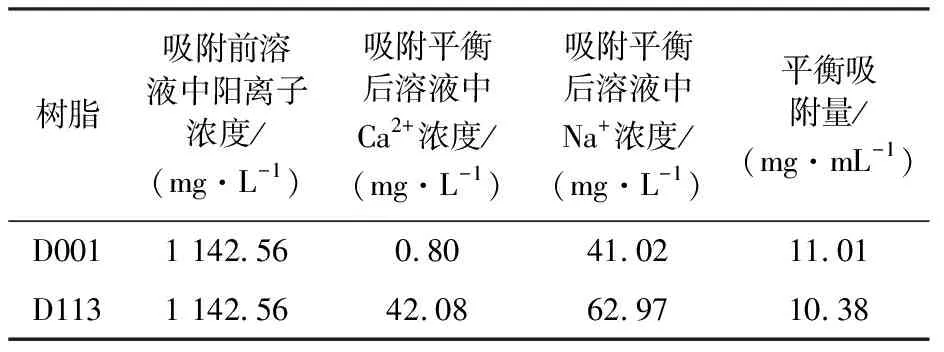
表3 阳离子交换树脂吸附情况Table 3 Adsorption of cation exchange resin
由图2可知,两种树脂吸附后,上清液的pH都呈下降趋势, D001树脂吸附后上清液的pH值低于D113树脂。阳离子交换树脂中的交换基团与溶液中的Na+、Ca2+发生交换,产生大量H+,导致上清液的pH值降低。由于D113树脂为弱酸型树脂,可交换离子解离程度较低,吸附效果小于强酸型树脂。由表3可知,D113树脂与D001树脂的平衡吸附量相差不大,且在乙二醇脱盐体系中,脱除阳离子的含量要求较低。此外,本实验中树脂拟采用电再生工艺,有研究指出D001树脂电再生过程困难,D113树脂电再生过程较容易[8],故阳离子交换树脂选用D113树脂。
2.2 树脂混合比例对吸附效果的影响
D201树脂的体积全交换容量≥1.2 mmol/mL,D113树脂的体积全交换容量≥4.4 mmol/mL,所以理论上在混合床中D201树脂的体积应该大于D113树脂,才能使流出液的pH为中性。将D201树脂与D113树脂的体积比例按1∶1,1.5∶1,2∶1,2.5∶1,3∶1,3.5∶1进行混合,混合树脂总体积为50 mL,将混合树脂倒入250 mL锥形瓶中,加入浓度70%乙二醇含盐富液,放置在25 ℃恒温水浴中,不断摇匀,待树脂吸附结束后测定上清液的pH与离子浓度,结果见表4。
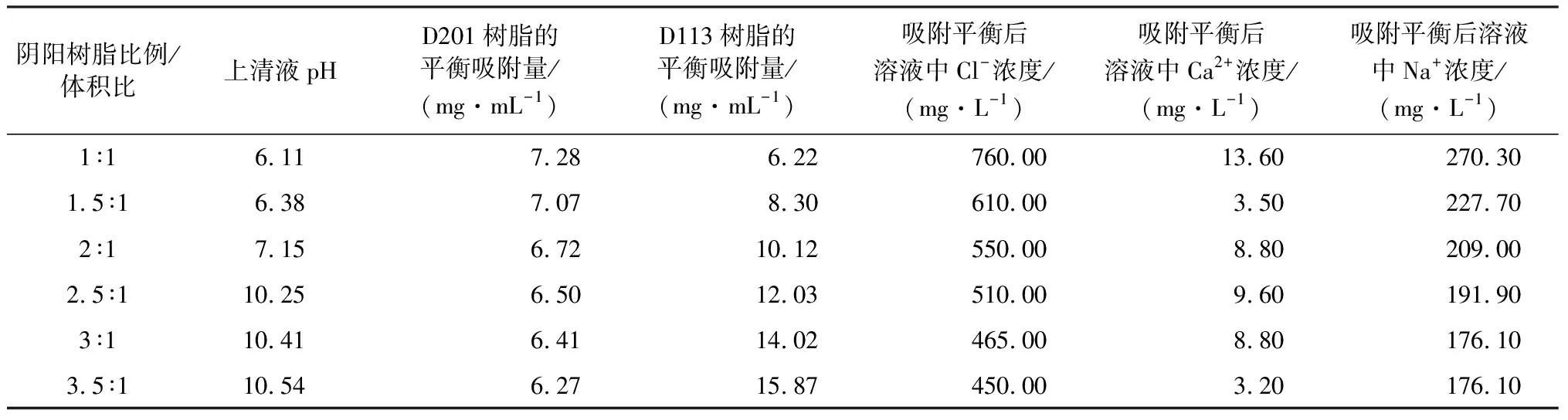
表4 树脂混合比例实验结果Table 4 Experimental results of different resin mixing ratios
由表4可知,阴阳树脂比例越高,D201树脂的平衡吸附量越小,D113的平衡吸附量越大。这是因为当阴阳树脂体积比小于2∶1时,上清液呈酸性,上清液中的H+可与D201树脂交换出来的OH-中和,有利于D201树脂吸附Cl-。当阴阳树脂体积比大于2∶1时,上清液pH呈碱性,上清液中的OH-可与D113树脂交换出来的H+中和,有利于D113树脂吸附阳离子。阴阳树脂体积比例为2∶1时, 经过静态树脂吸附后,溶液中Ca2+、Na+、Cl-质量浓度都大幅降低,其中Ca2+降低94.10%、Na+降低78.96%、Cl-降低69.41%。可根据工艺中乙二醇富液的离子浓度,调节所需的树脂用量与树脂床层来去除大部分离子。
在管道与设备中,为了避免pH值过低或过高而腐蚀金属材料,上清液的pH值应接近7,综合考虑混合树脂的吸附效果与上清液的pH值,阴阳树脂比例选择2∶1较为合适。
2.3 温度对吸附效果的影响
分别取20 mL经预处理后的D113树脂、D201树脂,加入到250 mL烧杯中,分别加入200 mL浓度70%乙二醇富液,将烧杯放在磁力搅拌器上搅拌,温度20~40 ℃,吸附平衡后测定上清液离子浓度。两种树脂平衡吸附量见图3。
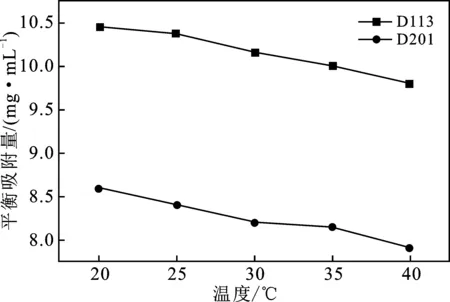
图3 不同温度下的平衡吸附量Fig.3 Equilibrium adsorption capacity at different temperatures
由图3可知,在相同树脂体积条件下,D113树脂吸附阳离子的平衡吸附量大于D201树脂吸附阴离子的平衡吸附量,这是因为D113树脂的体积全交换容量大于D201树脂。温度升高,D113树脂、D201树脂的平衡吸附量均逐渐降低,可能是由于树脂的吸附过程是放热反应,温度升高,不利于吸附的进行。
2.4 D201吸附热力学模型与参数
将实验数据用Langmuir模型[9]进行拟合,结果见表5和图4。

图4 D201树脂吸附乙二醇富液中Cl-的Langmuir模型Fig.4 Langmuir model of D201 resin adsorption of Cl- in ethylene glycol rich solution
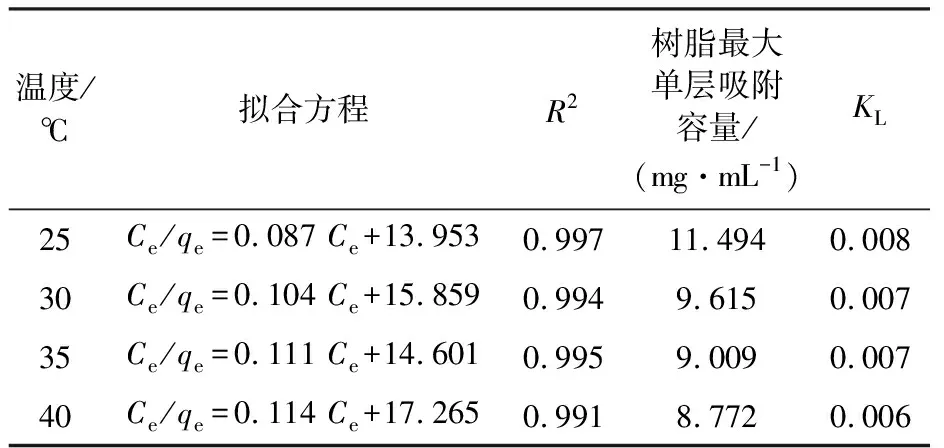
表5 D201树脂吸附Cl-的Langmuir模型拟合结果Table 5 Results of Langmuir model for D201 resin adsorption of Cl-
(2)
式中qmax——被吸附离子在树脂上的最大单层吸附容量,mg/mL;
KL——Langmuir常数,和吸附自由能有关。
由表5可知,Langmuir模型拟合的R2在0.99以上,Langmuir模型能够很好地描述D201树脂吸附乙二醇富液中Cl-的热力学过程,表明D201树脂吸附乙二醇富液中Cl-属于单层吸附。随着温度升高,树脂最大单层吸附容量降低,升高温度不利于提高树脂的吸附。
Langmuir模型能够很好地描述D201树脂吸附Cl-过程,故吸附平衡时离子在树脂和溶液中的平衡常数取Langmuir常数。根据式(3)、(4)计算得到ΔS和ΔH的值,最终求得ΔG,结果见表6。

表6 D201树脂吸附热力学参数Table 6 Results of Langmuir model for D201 resin adsorption of Cl-
(3)
ΔG=ΔH-TΔS
(4)
式中KL——吸附平衡时离子在树脂和溶液中的平衡常数;
R——通用气体常数,8.314 J/(mol·K);
ΔS——吸附熵变,kJ/(mol·K);
ΔH——吸附焓变,kJ/mol;
ΔG——吉布斯自由能变,kJ/mol。
由表6可知,熵变ΔS为-26.605 J/(mol·K),说明D201树脂吸附Cl-过程是一个混乱度减小的过程;焓变ΔH为-13.386 kJ/mol,说明该吸附过程为放热反应,升高温度不利于离子交换树脂的吸附,吉布斯自由能变ΔG在4个温度下的值都小于零,说明吸附反应能够自发进行。
2.5 D113吸附热力学模型与参数
D113树脂吸附乙二醇富液中Ca2+的Langmuir模型见图5,拟合结果见表7。

图5 D113树脂吸附乙二醇富液中Ca2+的Langmuir模型Fig.5 Langmuir model of D113 resin adsorption of Ca2+in ethylene glycol rich solution
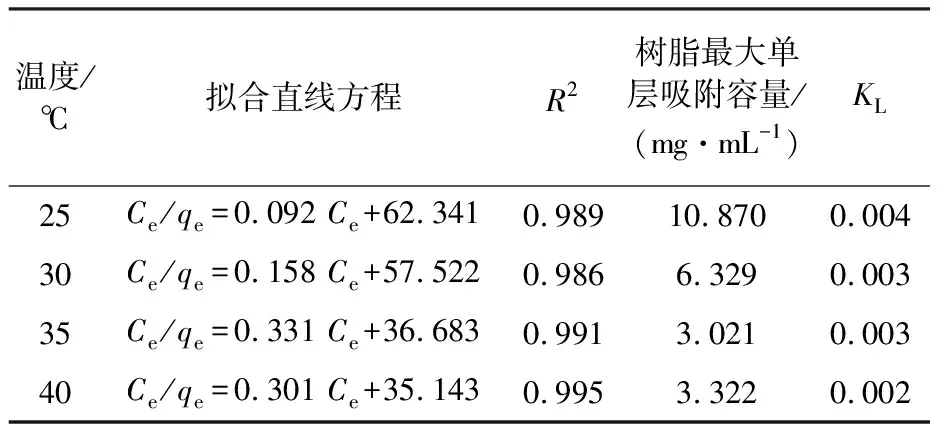
表7 D113树脂吸附Ca2+的 Langmuir模型拟合结果Table 7 Results of Langmuir model for D113 resin adsorption of Ca2+
由图5可知,Langmuir模型能够很好地描述D113树脂吸附乙二醇富液中Ca2+的热力学吸附过程。由表7可知,拟合直线的R2在0.98以上,随着温度升高,树脂的Langmuir平衡常数减小。D113树脂吸附热力学参数求解结果见表8。
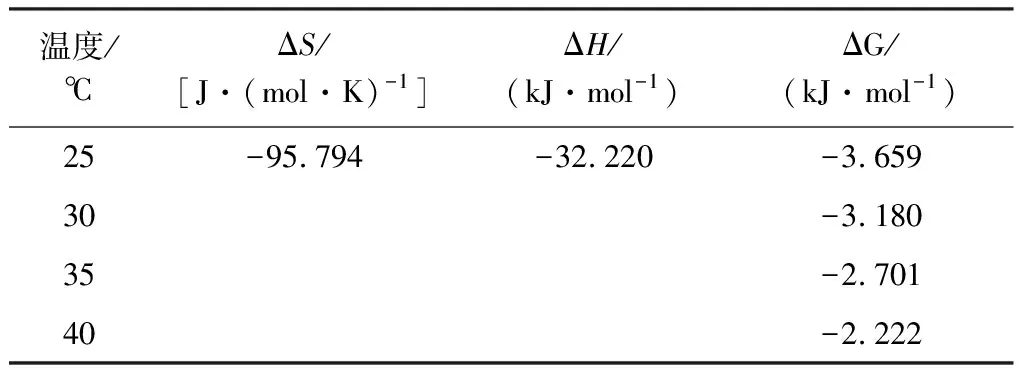
表8 D113树脂吸附热力学参数Table 8 Thermodynamic parameters of D113 resin
由表8可知,在D113树脂吸附Ca2+过程中,熵变ΔS为-95.794 J/(mol·K),说明D113树脂吸附Ca2+过程是一个混乱度减小的过程;焓变ΔH为-32.220 kJ/mol,说明该吸附过程为放热反应,升高温度不利于离子交换树脂的吸附,吉布斯自由能变ΔG在4个温度下的值都小于零,说明吸附反应能够自发进行。
3 结论
(1)在含盐乙二醇富液体系中,根据吸附能力,筛选出D113树脂和D201树脂,阴阳树脂体积比例为2∶1时,脱盐效果好,且上清液呈中性,温度为25 ℃, 阴阳混合树脂剂量为200 mL/L时,阳离子脱除率80.72%,阴离子脱除率69.41%。随着温度升高,树脂平衡吸附量减小。
(2)乙二醇富液体系中,D201树脂吸附Cl-与D113树脂吸附Ca2+的吸附等温线符合Langmuir模型,随着温度的升高,树脂的理论最大饱和吸附量与Langmuir平衡常数都随之减小,D201树脂吸附Cl-过程和D113树脂吸附Ca2+过程的吉布斯自由能变ΔG<0、焓变ΔH<0,因此树脂在乙二醇富液中的吸附过程属于可自发进行的放热反应。
(3)通过对离子交换乙二醇富液脱盐工艺的实验研究表明,D201树脂和D113树脂用于脱除乙二醇富液中的盐是可行的。
