枝晶状纳米铜修饰激光诱导石墨烯电化学传感器的制备及其在葡萄糖检测中的应用
2021-09-11梅正方姚梦婷陈荣生胡成国
梅正方, 姚梦婷, 陈荣生*, 胡成国
(1.武汉科技大学化学与化工学院,湖北武汉 430081;2.武汉大学化学与分子科学学院,湖北武汉 430072)
糖尿病是一种由代谢紊乱引起的、难以治愈的疾病,近年来成为世界上导致病人死亡和残疾的重要原因之一[1 - 4],因此,准确检测和实时监控人体中葡萄糖浓度就显得至关重要。迄今为止,已经报道了许多用于葡萄糖含量分析的技术,如液相色谱、表面等离振子共振、荧光光谱、化学发光等[5 - 8]。尽管这些技术具有许多优点,但存在成本高昂、纯化步骤多、检测时间长和需要经常维护等不足。电化学分析由于其高灵敏度和出色的选择性,已成为一种快速、实时检测葡萄糖浓度的有效方法[9 - 12]。此外,与传统的分析技术相比,它们更便宜、更简单、分析时间更短,因此电化学葡萄糖传感器自开发以来便获得了巨大成功[13]。酶具有专一性,目前普遍采用酶修饰的电极用于测定葡萄糖含量。但是酶对环境条件非常苛刻,极易失活[14 - 18],因此稳定性高、成本低、灵敏度高和重复性强的非酶葡萄糖传感器受到人们广泛的关注。
基于Cu纳米材料的修饰电极对葡萄糖的氧化具有催化作用,可以用来代替葡萄糖氧化酶,因此被人们广泛研究[19]。在本文中,我们采用激光雕刻技术,在柔性聚酰亚胺(PI)薄膜表面构筑激光诱导石墨烯(LIG)三电极阵列,然后通过电沉积方法,分别制备Ag/AgCl参比电极和枝晶状纳米铜修饰的工作电极,发展出低成本、高性能的柔性非酶型葡萄糖电化学传感器。该传感器工作电极上高比表面的LIG不但为Cu的生长提供了大量附着位点,还可以加快电荷传输速度。同时,以LIG作为对电极,所构建的三电极体系,三个电极均在同一基底上制备,无需额外引入电极,为检测过程提供了极大的方便。并且,整个器件都具备柔性,因此有望应用于可穿戴式葡萄糖传感器。
1 实验部分
1.1 仪器及试剂
Y7WDKJ激光雕刻机(上海雕途实业有限公司);CHI660E电化学工作站(上海辰华有限公司);FEI Nova 400 Nano场发射扫描电子显微镜(SEM)(美国,FEI有限公司);Thermo DXR拉曼光谱仪(美国,Thermo Fisher公司);Thermo Scientific K-Alpha+ X射线光电子能谱仪(美国,Thermo Fisher公司);Philips X’Pert Pro X射线衍射仪(荷兰,Philips公司)。
聚酰亚胺(PI)薄膜(昌达盛电子有限公司);AgNO3(上海凌峰化学试剂有限公司);盐酸多巴胺(阿拉丁试剂有限公司);尿酸、5-羟基色胺盐酸盐(萨恩化学技术有限公司);丙酮、无水乙醇、NaNO3、K3[Fe(CN)6]、HCl、CuCl2·2H2O、葡萄糖、NaOH、KCl和抗坏血酸,均购于国药集团化学试剂有限公司。水为蒸馏水。
1.2 LIG的制备
将厚度为125 μm的PI薄膜用剪刀剪成6 cm×6 cm的小片,置于超声波清洗器中依次用丙酮、乙醇和蒸馏水各超声清洗3 min,以除去薄膜表面的杂质,并用氮气吹干。然后将处理好的PI薄膜平放在激光焦点下,并固定四周,设计图案,调整激光参数为:功率5 W,扫描速度230 mm/s。完成后的样品依次用乙醇和蒸馏水冲洗数秒,以除去碳化后样品表面杂质,然后用氮气吹干。随后在LIG相应区域涂抹银胶增强导电性,并用环氧树脂绝缘胶封装,将传感区域和导电区域分隔开。其中,工作电极面积为0.26 cm2,参比电极面积为0.29 cm2,对电极面积为0.61 cm2。
1.3 Ag/AgCl修饰参比电极的制备
称取0.4247 g的AgNO3和0.425 g的NaNO3,加入50 mL的蒸馏水搅拌溶解,配制成0.05 mol/L的AgNO3和0.1 mol/L的NaNO3混合溶液。随后用电极夹夹住LIG的参比电极导电区域,将传感区域在上述溶液中浸泡30 min,使LIG的多孔结构与电解液充分接触。以LIG作为工作电极,Ag/AgCl作为参比电极,铂片作为对电极,在搅拌下以电流密度为5 mA/cm2的阴极电流下电沉积2 400 s,然后用蒸馏水冲洗30 s并用氮气吹干,即得到Ag/LIG。将上述制备的Ag/LIG作为工作电极,保持参比电极和对电极不变,以50 mL 2 mol/L HCl作为电解液,在电流密度为5 mA/cm2的阳极电流下电沉积2 400 s,然后用蒸馏水冲洗30 s,并用氮气吹干,在60 ℃的干燥箱中干燥12 h,即得到Ag/AgCl修饰LIG参比电极(Ag/AgCl/LIG)。
1.4 枝晶状纳米铜修饰工作电极的制备
称取0.0341 g的CuCl2,加入50 mL的蒸馏水超声溶解,配制成4 mmol/L的CuCl2溶液,同时取2 mol/L的HCl 50 μL,加入到配制好的CuCl2溶液中并搅拌混合均匀。用电极夹夹住LIG的工作电极导电区域,将传感区域在上述溶液中浸泡30 min,以LIG作为工作电极,饱和甘汞电极(SCE)作为参比电极,铂片作为对电极,在-1.5 V的电位下进行恒电位电沉积600 s,然后用蒸馏水冲洗30 s并用氮气吹干,在60 ℃的干燥箱中干燥12 h,即得到枝晶状纳米铜修饰LIG工作电极(Cu/LIG)。
电沉积时间优化:保持其他条件不变,选择电沉积时间分别为300 s、600 s、900 s、1 200 s、1 500 s。在0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中进行恒电位阶跃曲线(i-t)测试,通过比较电流响应确定最优电沉积时间。
电沉积电位优化:保持其他条件不变,选择电沉积电位分别为-0.75 V、-1.0 V、-1.25 V、-1.50 V、-1.75 V。在0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中进行恒电位阶跃曲线(i-t)测试,通过比较电流响应确定最优电沉积电位。
整个制备过程的图案设计与实验流程如图1所示。
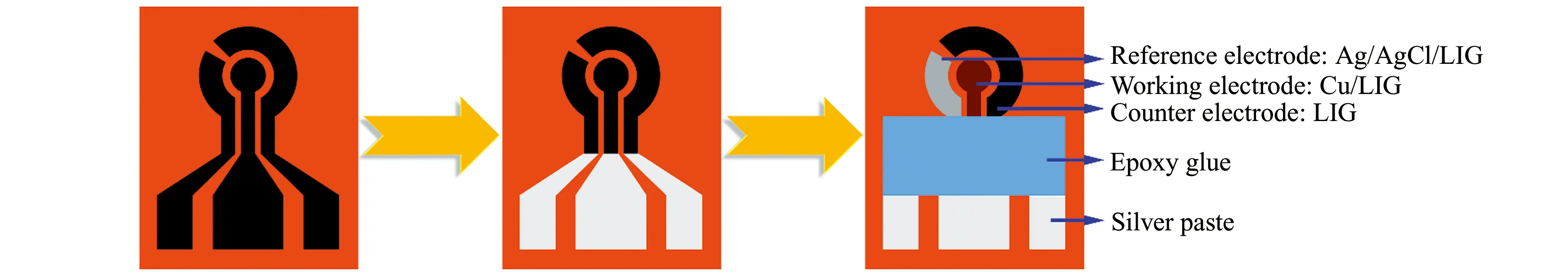
图1 柔性自支撑葡萄糖传感器的制备示意图Fig.1 Schematic diagram of preparation of flexible free-standing glucose sensor
2 结果与讨论
2.1 枝晶状Cu/LIG的形貌和结构表征
图2(a)~2(f)分别是LIG、Cu/LIG -300 s、Cu/LIG -600 s、Cu/LIG -900 s、Cu/LIG -1 200 s和Cu/LIG -1 500 s的扫描电镜(SEM)图。由图2(a)可以看出,LIG表面由许多孔洞和褶皱组成,这种结构具有较大比表面积,可以为Cu的生长提供大量附着位点。当沉积时间为300 s时,如图2(b)所示,LIG表面有许多针状的Cu,随着电沉积时间延长到600 s,从图2(c)中可以看出Cu呈现出明显的枝晶状,这种结构在各个方向均有生长,形成三维结构,比表面积较大。当沉积时间进一步增加到900 s,如图2(d)中所示,枝晶结构变粗,类似于米粒,从而导致比表面积有所下降。当继续延长沉积时间,如图2(e)和2(f),枝晶状结构继续变粗,呈现出叶片状。

图2 LIG(a)、Cu/LIG -300 s(b)、Cu/LIG -600 s(c)、Cu/LIG -900 s(d)、Cu/LIG -1 200 s(e)和Cu/LIG -1 500 s(f)的扫描电镜(SEM)图Fig.2 SEM images of LIG(a),Cu/LIG -300 s(b),Cu/LIG -600 s(c),Cu/LIG -900 s(d),Cu/LIG -1 200 s(e) and Cu/LIG -1 500 s(f)
图3是Cu/LIG -600 s的X射线衍射(XRD)图,在2θ为43.4°和50.4°处的衍射峰对应着Cu的(111)和(200)晶面(JCPDF 89-2838)。在电沉积过程中,生成的Cu结晶性较差,因此衍射峰的强度较低。
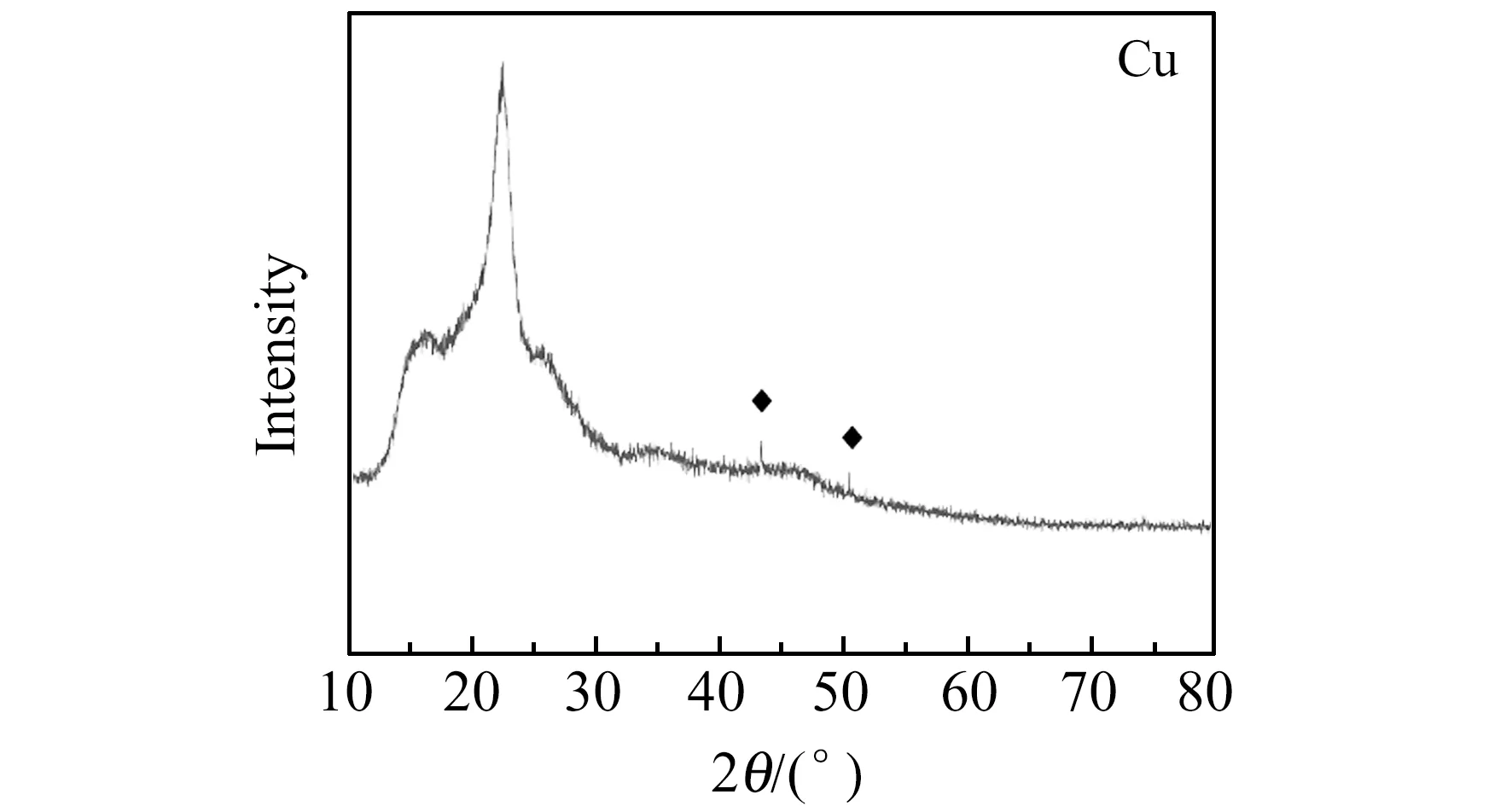
图3 Cu/LIG -600 s的X射线衍射(XRD)图Fig.3 XRD pattern of Cu/LIG -600
X射线光电子能谱(XPS)测试可以用来分析复合材料Cu/LIG -600 s的元素种类和化学价态。图4(a)是该复合材料的全谱图,显示出样品主要包含C、O、Cu三种元素。图4(b)为C 1s的高分辨XPS谱图,在284.7 eV的特征峰对应着C-C键,它来自于基底LIG。O 1s的高分辨XPS谱图如图4(c)所示,530.7、532.7 eV两个特征峰分别归因于Cu-O键和表面吸附的羟基。在图4(d)中,933.4、953.6 eV两个峰分别对应着Cu 2p3/2和Cu 2p1/2,后者证明了Cu2+的存在,而前者无法确定是Cu+还是单质Cu[20,21]。结合XRD分析结果可得,此处应该对应着Cu。综合相关材料表征可知,该枝晶状物质由Cu和少量的CuO组成。
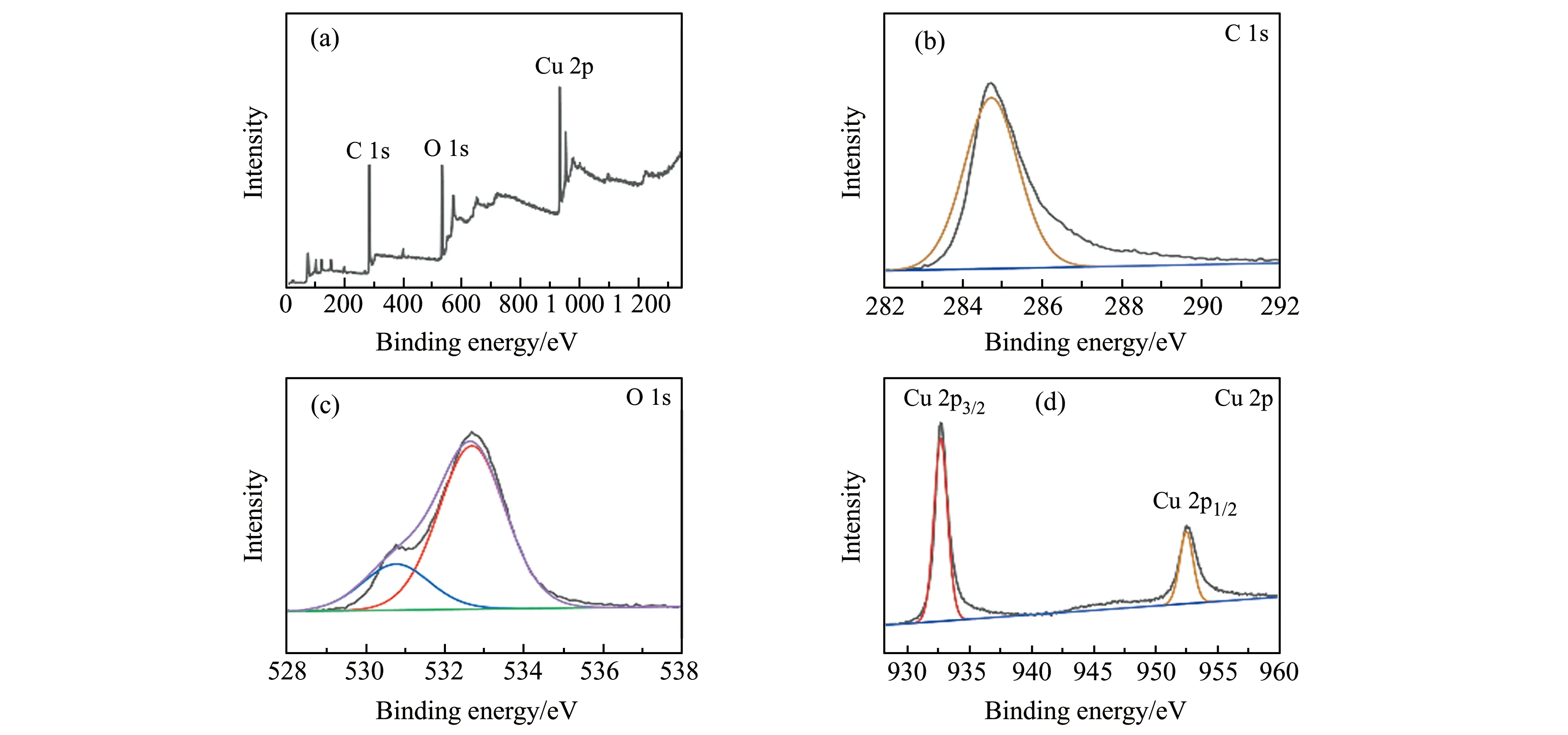
图4 Cu/LIG -600 s的X射线光电子能谱(XPS)全谱图(a)以及C 1s(b)、O 1s(c)和Cu 2p(d)的高分辨谱图Fig.4 XPS spectra of Cu/LIG -600 s(a) and core -level spectra of C 1s(b),O 1s(c),Cu 2p(d)
2.2 枝晶状Cu/LIG的电化学测试
图5(a)是以LIG为工作电极,铂片为对电极,分别以自制Ag/AgCl(参比电极1)和商用Ag/AgCl(参比电极2)(3 mol/L KCl)为参比电极,在5 mmol/L K3[Fe(CN)6]和0.1 mol/L KCl混合溶液中,于扫描速率为20 mV/s时得到的循环伏安(CV)曲线。图中显示不同参比电极的CV曲线形状一致,两个参比电极的氧化峰和还原峰电位差值相等,说明自制的Ag/AgCl可以作为参比电极使用。0.1 mol/L NaOH溶液为Cu基葡萄糖传感器测试提供了碱性环境,而0.1 mol/L KCl则为自制Ag/AgCl参比电极的稳定运行提供了保障。葡萄糖传感器后续的电化学测试均在0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中进行。图5(b)的CV曲线显示,LIG在有无2 mmol/L的葡萄糖的溶液中曲线几乎重合,说明LIG对葡萄糖没有响应,而Cu/LIG在含2 mmol/L葡萄糖溶液中出现明显的氧化峰,说明复合电极对葡萄糖的响应来源于负载的Cu。图5(c)表明Cu/LIG对葡萄糖的响应随着其浓度增加而增加。
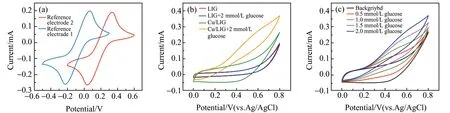
图5 (a)5 mmol/L K3[Fe(CN)6] 和0.1 mol/L KCl混合溶液中在不同参比电极上得到的循环伏安(CV)曲线(扫描速率为20 mV/s);(b)LIG和Cu/LIG在有、无2 mmol/L葡萄糖的CV曲线;(c)Cu/LIG在含有0、0.5、1.0、1.5、2.0 mmol/L葡萄糖溶液中的CV曲线(扫描速度均为50 mV/s)Fig.5 (a) CV curves recorded with different reference electrodes in 5 mmol/L K3[Fe(CN)6] and 0.1 mol/L KCl(Scan rate:20 mV/s);(b) CV curves of LIG and Cu/LIG in the absence and presence of 2.0 mmol/L glucose;(c) CV curves of Cu/LIG in the presence of 0,0.5,1.0,1.5 and 2.0 mmol/L glucose in 0.1 mol/L NaOH and 0.1 mol/L KCl(Scan rate:50 mV/s)
图6(a)~6(c)显示了不同条件制备的传感器对葡萄糖的安培响应。分别在-0.75、-1.0、-1.25、-1.5 和-1.75 V的电位下电沉积600 s制备的电极,在0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中,施加0.5 V测试电位时,连续5次加入100 μmol/L葡萄糖的i-t曲线,该曲线呈现明显阶梯状递增。图6(d)为安培响应和信噪比(S/N)随制备电位的变化关系图。如图所示,在电沉积电位为-1.5 V时两者均达到最大值,说明该条件为最优制备电位。图6(e)显示了以上述最优沉积电位电沉积600 s制备的样品,在0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中,施加测试电位分别为0.3、0.4、0.5、0.6和0.7 V时,连续加入5次100 μmol/L葡萄糖的i-t曲线和响应电流、信噪比与检测电位的关系。由图6(e)可知,在施加0.5 V时具有最高的响应电流和信噪比值,因此后续电化学测试均在此电位下进行。为了优化电沉积时间,在上述最优沉积电位下分别电沉积300、600、900、1 200和1 500 s,同时施加上述最优测试电位,在0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中连续五次加入100 μmol/L葡萄糖。图6(f)显示当沉积时间为600 s时,具有最高的电流响应以及信噪比,因此此条件为最优电沉积时间,在最优条件下制备的复合电极记作Cu/LIG-600 s。综上所述,枝晶状Cu/LIG复合电极的最优制备条件为在-1.5 V的电位下电沉积600 s,最优的安培检测电位为0.5 V。
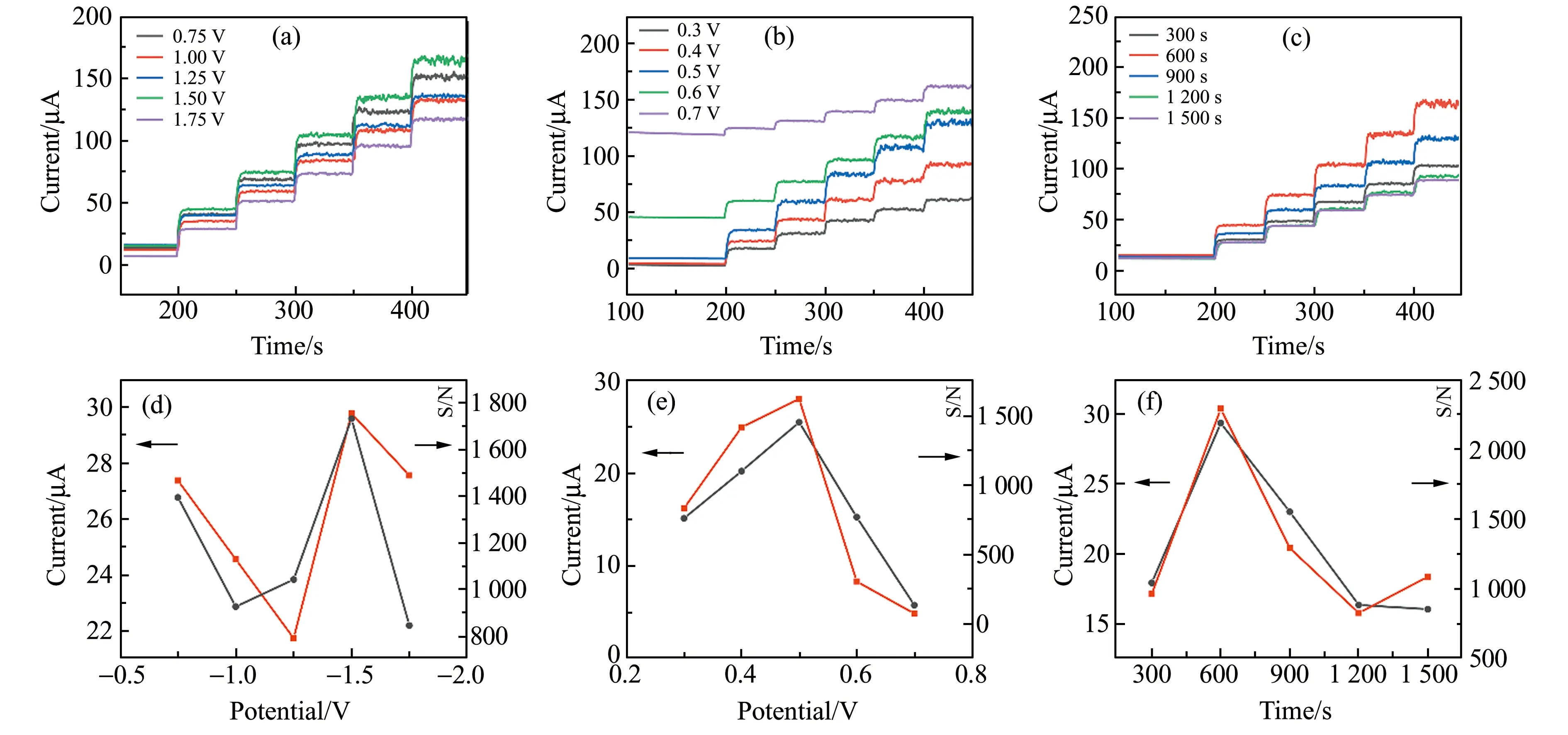
图6 连续向0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中注入5次100 μmol/L葡萄糖,(a)、(b)、(c)是不同条件的i -t曲线和(d)、(e)、(f)与之对应的安培响应(黑色)和信噪比(红色):(a)、(d)不同电位下沉积600 s制备的Cu/LIG,施加0.5 V测试电位。(b)、(e)以-1.5 V电位电沉积600 s制备的Cu/LIG,施加不同的测试电位。(c)、(f)以-1.5 V电位不同沉积时间制备的Cu/LIG,施加0.5 V测试电位。Fig.6 Successive injection of 100 μmol/L glucose five times into a mixed solution of 0.1 mol/L NaOH and 0.1 mol/L KCl with continuous stirring:different electrodeposition voltages for 600 s at an applied potential of 0.5 V(a),(d);different applied test potentials with an electrodeposition voltage of -1.5 V for 600 s,(b),(e);different electrodeposition times with an electrodeposition voltage of -1.5 V and an applied potential of 0.5 V(c),(f).
图7(a)显示了Cu/LIG -600 s在连续加入10次20 μmol/L葡萄糖溶液时的i-t曲线,其电流响应呈现出明显的阶梯状增加,每个阶梯之间的高度近似相等,这一点在图7(b)的响应电流柱形图中得到印证。同时计算可得,10次添加对应的电流响应相对标准偏差(RSD)为2.96%,该结果表明制备的Cu/LIG -600 s电极具有较高的稳定性和良好的重现性。在图7(c)的插图中,当加入葡萄糖浓度低至0.5 μmol/L时,依然有明显的阶梯电流响应,表明该电极具有高灵敏度。不同浓度葡萄糖对应的响应电流如图7(d)所示,其线性拟合图表明制备的柔性非酶葡萄糖传感器线性范围为0.5~365.5 μmol/L,且具有较高的灵敏度(1 554.5 μA/(mmol/L·cm2))和较低的检测限(0.098 μmol/L,S/N=3)。
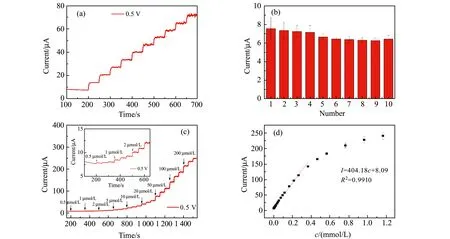
图7 向0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中连续加入10次20 μmol/L葡萄糖的i -t曲线(a)及其对应的响应电流柱形图(b)(测试电位为0.5 V),连续加入不同浓度葡萄糖(0.5、1、2、5、10、20、50、100、200 μmol/L,每组3次)的i -t曲线(c)(插图为前9次加入的放大图),响应电流与葡萄糖浓度的线性拟合曲线(d)。图中误差棒表示3次平行实验的标准偏差。Fig.7 (a) Amperometric responses of successive injection of 20 μmol/L glucose for ten times into a mixed solution of 0.1 mol/L NaOH and 0.1 mol/L KCl with continuous stirring at an applied potential of 0.5 V,(b) response currents for each addition,(c) amperometric responses in a mixed solution of 0.1 mol/L NaOH and 0.1 mol/L KCl at an applied potential of 0.5 V with successive injection of different concentrations of glucose (0.5,1,2,5,10,20,50,100,200 μmol/L,three times per group).The inset shows the injection of glucose for the first nine times,(d) calibration plot of the responses to concentrations.The error bars represent the standard deviation from three parallel experiments.
与具有良好选择性的酶基葡萄糖传感器相比,非酶型葡萄糖传感器在有共存物质的体系中面临着重大挑战。人体血液中除了葡萄糖外,还有多巴胺、抗坏血酸、尿酸、5-羟色胺和组胺等生物分子,但是葡萄糖的浓度远高于这些干扰物质。因此,往0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中连续加入100 μmol/L葡萄糖和20 μmol/L上述物质的i-t曲线见图8(a)。图8(b)显示出共存物质的电流响应与葡萄糖相比非常小,说明制备的Cu/LIG -600 s电极在葡萄糖检测中具有良好的抗干扰性能。
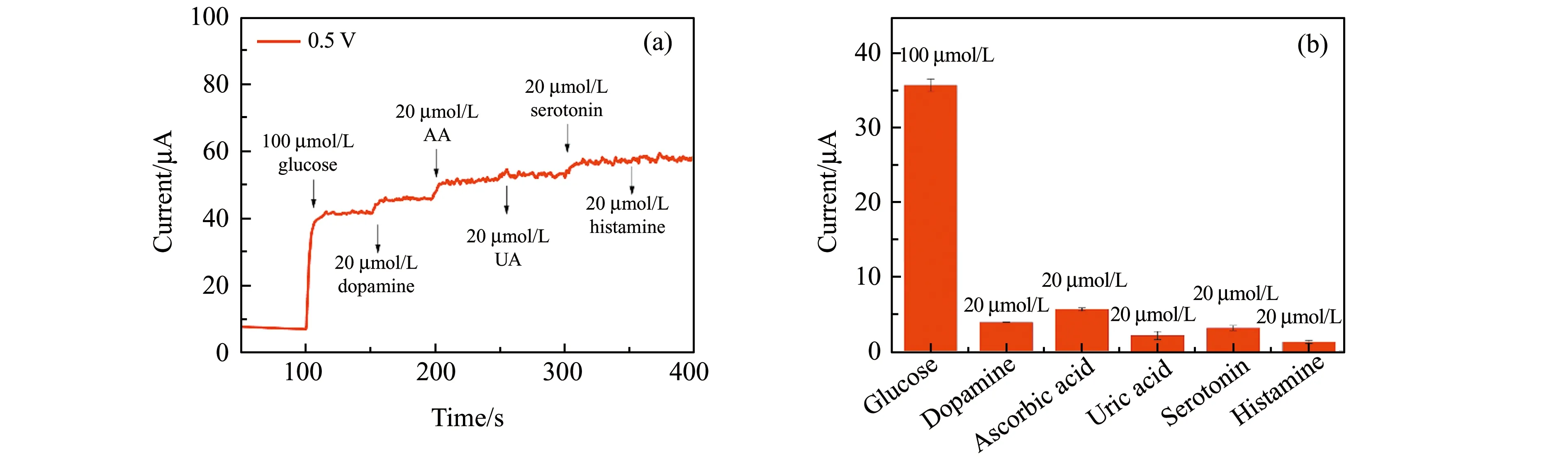
图8 (a)向0.1 mol/L NaOH和0.1 mol/L KCl的混合溶液中连续加入100 μmol/L葡萄糖、20 μmol/L多巴胺、20 μmol/L抗坏血酸、20 μmol/L尿酸、20 μmol/L 5-羟色胺和20 μmol/L组胺的i -t曲线。(b)对应物质的响应电流柱形图(测试电位为0.5 V)。图中误差棒表示3次平行实验的标准偏差。Fig.8 (a) Amperometric responses of successive injection of 100 μmol/L glucose,20 μmol/L dopamine,20 μmol/L AA,20 μmol/L UA,20 μmol/L serotonin and 20 μmol/L histamine in a mixed solution of 0.1 mol/L NaOH and 0.1 mol/L KCl with continuous stirring at an applied potential of 0.5 V.(b) current responses of 20 μmol/L interfering species and 100 μmol/L glucose.The error bars represent the standard deviation from three parallel experiments.
3 结论
本文以柔性材料LIG为基底,采用电沉积方法制备了参比电极Ag/AgCl/LIG和工作电极Cu/LIG,构建了一种柔性非酶型葡萄糖电化学传感器。在最优的条件下,传感器具有优异的灵敏度1 554.5 μA/(mmol/L·cm2)以及较低的检测限0.098 μmol/L。此外,该传感器对葡萄糖的响应具有良好的重现性,连续10次测量20 μmol/L葡萄糖时响应电流的RSD仅为2.96%。同时,对多巴胺、抗坏血酸、尿酸、5-羟色胺和组胺具有良好的抗干扰性能。
