NC-PC锚定微量Fe活化PMS降解水中2,4-二氯苯氧乙酸
2021-08-09郭枭杰方志勇罗豪鹏东华大学环境工程系上海201620
郭枭杰,方志勇,周 鑫,罗豪鹏,周 娟 (东华大学环境工程系,上海 201620)
2,4-二氯苯氧乙酸(2,4-D)是一种能够去除阔叶杂草的苯氧羧酸类农药,低浓度下可作为植物的生长剂,因其廉价易得而广泛应用于农业生产中[1].但其稳定的结构和较高的水溶性使其在经过一系列变化后依旧滞留在环境水体中,对生态环境和人类健康造成了巨大的威胁;毒性研究表明,2,4-D对人体的眼睛和皮肤具有一定的刺激作用,长期接触会损害肝、心脏等,对哺乳类动物存在较强的致癌作用[2],世界卫生组织(WHO)将饮用水中2,4-D浓度标准定为了30μg/L[3].
高级氧化技术(AOPs)因其较强的氧化能力被应用于复杂的实际废水处理中[4],常见的氧化剂有过一硫酸盐(PMS),过二硫酸盐(PDS),过氧化氢(H2O2),过氧乙酸(PAA)等,其中,PMS因分子结构的不对称性,更易活化产生自由基[2],其活性成分主要为 HSO5−,通常通过热、紫外线(UV)[5]、超声波[6]和过渡金属[7]等技术手段来活化 HSO5−产生具有强氧化性的 SO4-⋅,SO4-⋅具有较高的氧化还原电位和较长的半衰期,能够增加与目标污染物的接触时间,从而更大程度地降解水中的有机污染物.
目前能够活化过硫酸盐的方法主要有热活化、紫外光活化[8]、过渡金属活化[9]、电化学活化、超声活化等.其中,利用廉价的过渡金属(Fe、Co、Cu等)活化PMS是一种应用较为广泛的催化方式[10].传统的均相类方法存在适用范围有限、回收较困难、容易造成环境的二次污染等缺陷,使得其发展受到了很大的限制[11];近年来,非均相固体催化剂的研究很好的解决了均相体系中遇到的难题,Fe系固体催化剂因其廉价易得,对环境友好引起了人们的关注[12].固体催化剂常用的载体有金属氧化物、分子筛、碳材料(碳纳米管、石墨烯、中孔碳等)等[13],其中,碳材料因其较高的比表面积和丰富的表面含氧官能团使其成为了催化氧化体系中常用的金属载体[14].PC是一种柠檬酸钾类盐经高温碳化后形成的三维多孔碳材料,表面含有丰富的含氧官能团,有研究表明,利用 N元素锚定Fe产生的Fe-Nx活性中心在ORR过程中表现出较高活性,各项性能均高于最先进的商用Pt/C催化剂[15].但是,该类型材料在催化氧化领域应用颇少.
本研究探讨Fe-NC-PC活化PMS对水体中难降解的 2,4-D的去除效果.通过分步热分解法制备具有三维多孔结构的 PC载体和较低 Fe负载量的Fe-NC-PC催化剂,并对其结构进行表征;研究负载金属、制备方法、催化剂投加量、PMS投加量、初始pH值和水中不同阴离子对Fe-NC-PC/PMS体系降解2,4-D的影响,通过淬灭反应以及EPR测试对其反应机理进行分析,旨在为含有 2,4-D的实际废水处理提供科学依据.
1 材料与方法
1.1 实验材料及仪器
2,4-二氯苯氧乙酸(2,4-D)、C6H4O2购于梯希爱(上海)化成工业发展有限公司;柠檬酸钾盐(C6H5K3O7)购于上海麦克林生化科技有限公司;Fe(NO3)3·9H2O 购于阿法埃莎(中国)化学有限公司;CH3OH 购于德国科技公司;L-组氨酸(C6H9N3O2)购于上海百研生物科技有限公司;α-D 葡萄糖(C6H12O6)、Co(NO3)2·6H2O、过硫酸氢钾盐(KHSO5·0.5KHSO4·0.5K2SO4)、腐殖酸(HA)、叔丁醇(C4H10O)均购于上海阿拉丁生化科技股份有限公司;H2SO4、NaOH、三聚氰胺(C3H6N6)、NaCl、NaNO3、NaHCO3、Cu(NO3)2·3H2O均购于国药集团化学试剂有限公司;以上药品均为分析纯,实验用水为去离子水(DI).管式炉(OTF−1200X,购于合肥科晶材料技术有限公司).
1.2 催化剂制备
PC载体的制备:在N2气氛下,将8mmol柠檬酸钾盐(C6H5K3O7)经管式炉800℃热解1h(升温速率5℃/min),所得的黑色固体加入到 0.5mol/L硫酸(H2SO4)溶液中,搅拌 30min后过滤并用水冲洗至中性,经60℃真空干燥12h得PC载体.
Fe-NC-PC的制备:将0.06gPC载体分散在5mL去离子水中,分别加入 0.3mmol硝酸铁(Fe(NO3)3·9H2O)和 6.7mmolα-D 葡萄糖(C6H12O6),超声处理30min后,用水冲洗过滤,60℃真空干燥12h获黑色固体;按照1:5质量比加入三聚氰胺(C3H6N6),研磨均匀,在N2气氛下,经管式炉800℃热解2h(升温速率5℃/min)获Fe-NC-PC催化剂.
1.3 催化剂表征
通过透射电子显微镜(TEM,JEM-2100,日本JEOL公司)对PC载体以及Fe-NC-PC催化剂的微观形貌进行表征;高精度比表面积仪(BET,Autosorb-iQ,美国康塔仪器公司)对 PC载体的孔隙结构进行分析.通过X射线光电子能谱(XPS,Thermo Scientific K-Alpha,美国 Thermo Fisher Scientific)对Fe-NC-PC催化剂的组成及元素价态进行分析;电感耦合等离子体发射光谱仪(ICP,Agilent 5110,美国Agilent Technologies Inc)对催化剂中的金属含量进行测量.通过电子自旋共振波谱仪(EPR,布鲁克a300,美国布鲁克公司)对其自由基进行检测.
1.4 2,4-D降解实验及分析方法
在室温(25℃)条件下,取0.1mmol/L的2,4-D(初始pH=3.4)于100mL烧杯中,加入一定量的Fe-NCPC催化剂,磁力搅拌作用30min,然后添加一定量的PMS启动反应,按照一定的时间间隔取样,并加入等量甲醇淬灭样品中剩余的自由基.通过 0.1mol/L的H2SO4和0.1mol/L的NaOH调节溶液的初始pH,在淬灭反应中,提前在 100mL烧杯中加入一定量的淬灭剂以淬灭反应过程中产生的目标自由基.
通过配备有 285nm紫外检测器的高效液相色谱仪(Thermofisher,Ultimate 3000)测定2,4-D的浓度,流速和柱温分别设置为1mL/min和30℃,流动相由60%甲醇和40%水组成.
2 结果与讨论
2.1 催化剂的表征
2.1.1 TEM分析 由图1(a)可以看出,PC载体具有较为明显的三维多孔结构,多孔状的结构能够为氧化剂提供更多的活性位点,与污染物充分接触达到更好的降解效果;由图1(b)可见,较低负载量的金属Fe均匀的分散在PC载体的表面,由于N的包裹保护作用,使其并没有出现较为明显的团聚现象.

图1 载体和催化剂的TEM图Fig.1 TEM diagram of support and catalyst
2.1.2 BET分析和ICP分析 BET测试表明,PC载体的比表面积高达851.317m2/g,孔体积为0.51cm3/g,平均孔径0.8nm.ICP测试表明Fe-NC-PC中Fe的含量约为 0.005g/g,间接的证实了 Fe-NC-PC中 Fe的较低负载量.
2.1.3 XPS谱图分析 由图 2(a)的总谱图可以看到,Fe-NC-PC表面主要含有C、O、N、Fe元素;图2(c)O1s谱图可拟合为 3个峰,分别对应于 532.5,533,533.7eV处的C-OH键、C-O键和C=O键,表明Fe-NC-PC表面存在着大量的含氧官能团,这些官能团能够起到活化 PMS活性位点的作用[16].图2(d)N1s谱图可拟合为 5个峰,分别对应于 398.3,399.1,400,400.6,401.7eV处的吡啶-N、Fe-Nx、吡咯-N、石墨-N和氧化-N,从N1s谱图中发现了Fe-Nx物种的存在,有研究表明,Fe-Nx配位体中的 N一方面能够避免Fe在制备过程中发生大规模团聚,另一方面 Fe-Nx作为活性中心能够有效地活化 PMS产生大量的自由基,从而提高污染物的降解速率[14];图2(e)中 Fe2p谱图表明,Fe以+2价的形式存在.同时,对不含前驱体N的 Fe-C-PC进行XPS表征,如图2(b)所示,Fe-C-PC表面仅含有C、O、Fe3种元素,并没有出现较为明显的N峰,图2(f)Fe2p谱图中也没有发现相应的Fe-Nx峰,且Fe-C-PC中Fe同样以+2价形式存在.

图2 Fe-NC-PC/Fe-C-PC的XPS光谱图Fig.2 XPS spectra of Fe-NC-PC/Fe-C-PC
2.2 催化剂及其制备方法的选择
如图3(a)所示,在相同的条件下,Fe-NC-PC对2,4-D的去除率可达 91%,而 Co-NC-PC和 Cu-NC-PC对2,4-D的去除率仅为48%和29%.因此,选择Fe-NC-PC作为催化剂,探讨其催化活性和反应机理.
分别采用浸渍法和热解法制备方法合成 Fe-NC-PC,如图 3(b)所示,在相同的条件下,相比于Fe- NC-PC(热解),Fe-NC-PC(IMP)对 2,4-D的去除率仅为 30%,这是因为相比于浸渍法,三聚氰胺在高温热解的情况下能够产生 CNx物种(如 C3N4等),这些 CNx物种提供的 N源能够包裹金属避免其大规模的团聚并且具有调控金属价态的作用,因此,选取热解法制备 Fe-NC-PC 催化剂,探讨其催化活性和机理.
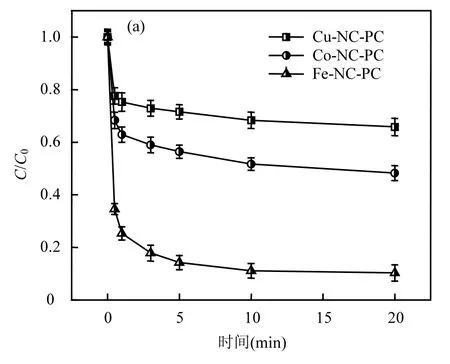

图3 不同负载金属及不同制备方法下2,4-D去除效果Fig.3 Removal efficiency of 2,4-D under different loading metals and different preparation methods
2.3 不同体系对2,4-D降解效果影响
在 2,4-D=0.1mmol/L,初始 pH=3.4,催化剂投加量0.15g/L,PMS浓度0.7mmol/L的条件下,如图4所示,单独的PMS和单独的Fe-NC-PC反应20min后2,4-D去除率分别为10%和18%,这可以归因于PMS在污染物中的自分解以及Fe-NC-PC催化剂的少量吸附.单独的Fe-NC-PC对2,4-D的吸附作用较小,当反应体系达到吸附饱和后加入PMS启动反应,反应20min后2,4-D去除率达到91%,表明反应主要依赖于催化剂表面活性中心活化 PMS产生活性物种进行降解,吸附作用对反应过程的影响较小.单独的Fe(Ⅲ)/PMS体系和单独的 PC/PMS体系,经 20min反应后 2,4-D的去除率仅为 10%和 15%,而在Fe-NC-PC/PMS体系中,2,4-D的去除率可高达91%,这是由于Fe-NC-PC上的活性中心Fe-Nx能够有效地活化 PMS产生强氧化性的自由基,从而促进了2,4-D的降解转化.

图4 不同体系下2,4-D去除效果Fig.4 Removal efficiency of 2,4-D in different systemss
2.4 催化剂投加量对2,4-D降解的影响
在 2,4-D=0.1mmol/L,初始 pH=3.4,PMS浓度0.7mmol/L的条件下,如图5所示,在催化剂投加量为0.05g/L和0.10g/L的条件下,由于催化剂可提供的活性位点有限,并不能够完全活化溶液中的PMS产生足量的自由基,从而导致在反应 20min内2,4-D的去除率仅为40%和75%.随着催化剂投加量的增多,反应体系中的活性位点逐渐增多,当催化剂的投加量为0.15g/L时,反应20min内2,4-D的去除率达到 91%.当催化剂投加量继续增大到0.20g/L时,其 2,4-D去除率基本保持不变,这归因于 0.15g/L的催化剂已经能够提供足量的活性位点来活化体系中的 PMS,反应达到饱和,从而降低了2,4-D的降解转化.因此,本研究选择Fe-NC-PC催化剂投加量为 0.15g/L,探讨其催化活性和反应机理.

图5 不同催化剂投加量下2,4-D去除效果Fig.5 Removal efficiency of 2,4-D under different catalyst dosages
2.5 PMS投加量对2,4-D降解的影响
在 2,4-D=0.1mmol/L,初始 pH=3.4,催化剂投加量0.15g/L的条件下,如图6所示,当PMS投加量为0.3mmol/L和0.5mmol/L时,反应20min内2,4-D的去除率为65%和79%.随着PMS投加量的增加,催化剂活化PMS产生的自由基增多,促进了反应的进行.当PMS投加量为0.7mmol/L时,反应20min内2,4-D的去除率达到91%,继续增大PMS的投加量,发现其去除率基本维持在 91%左右不再降低,这是因为过量的PMS会加快自由基的产生速率,这些自由基之间会发生自我淬灭,同时产生的 SO4-⋅也会与溶液中的HSO5-发生反应生产氧化性较弱的 SO5-⋅(式(1)~式(2)),从而降低了 2,4-D 的降解转化.因此,本研究选择 PMS投加量为 0.7mmol/L,探讨其催化活性和反应机理.

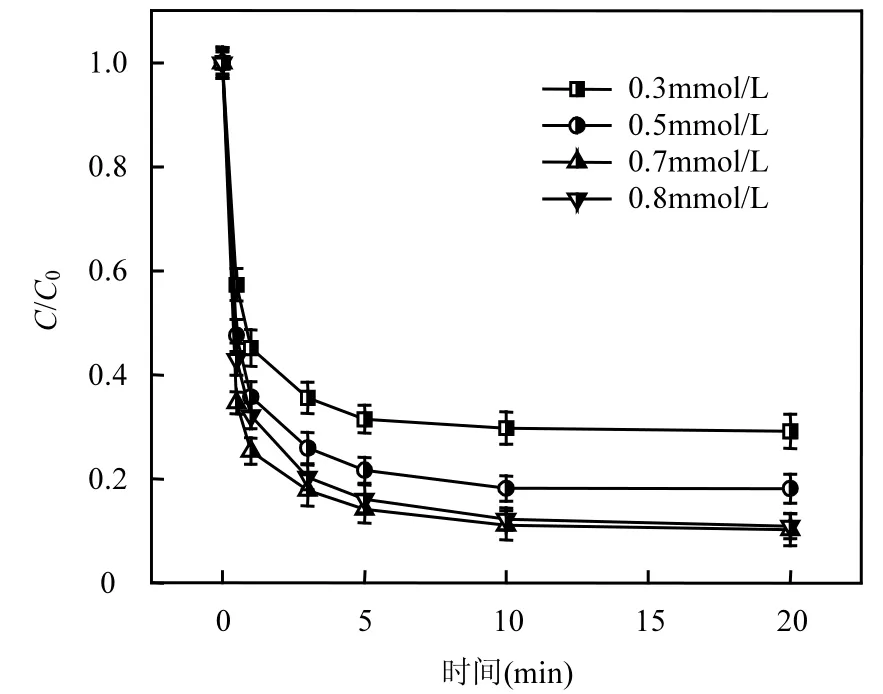
图6 不同PMS投加量下2,4-D去除效果Fig.6 Removal efficiency of 2,4-D under different PMS dosages
2.6 初始pH值对2,4-D降解的影响
在 2,4-D=0.1mmol/L,催化剂投加量 0.15g/L,PMS浓度 0.7mmol/L的条件下,如图 7所示,2,4-D的初始pH=3.4,其在反应20min内的去除率为91%,随着pH值逐渐增大,20min内2,4-D的去除效果逐渐变差,从91%降为了20%,这是因为当pH值增大时,催化剂表面所带负电荷逐渐增多[17],静电斥力的作用抑制了电子的转移,使得难以活化PMS产生自由基,从而降低了2,4-D的降解转化.

图7 不同初始pH值条件下2,4-D去除效果Fig.7 Removal efficiency of 2,4-D under different initial pH conditions
2.7 水体中阴离子和腐殖酸对2,4-D降解的影响
在 2,4-D=0.1mmol/L,初始 pH=3.4,催化剂投加量 0.15g/L,PMS浓度 0.7mmol/L的条件下,考察了0.5mmol/L的不同阴离子(Cl-、NO3-、HCO3-)和0.5mg/L的HA对2,4-D的降解效率的影响.如图8所示,在反应 20min内,0.5mmol/L的 Cl-和 NO3-对2,4-D 的去除率略微下降,约为 85%,这是因为低浓度的Cl-能够与溶液中的⋅OH和SO4-⋅发生弱反应生成氧化性较低的氯自由基(式(3)~式(5))[18].而0.5mmol/L的HCO3-使得20min内2,4-D的去除率从 91%降为了 61%,其归因于碳酸氢盐的淬灭效应,其能够与溶液中存在的⋅OH 和 SO4-⋅反应生成碳酸盐自由基(式(6)~式(8)),生成的 CO3-⋅氧化有机物的能力较弱,从而降低了2,4-D的降解转化.0.5mg/L的HA在反应20min内对2,4-D的去除下降为85%,这是因为HA作为一种有机物,其与2,4-D存在着竞争⋅OH 和 SO4-⋅的关系,从而导致了 2,4-D 降解率的降低[27].

图8 不同阴离子和HA条件下2,4-D去除效果Fig.8 Removal efficiency of 2,4-D under different anions and HA

2.8 催化机理分析
在 2,4-D=0.1mmol/L,初始 pH=3.4,催化剂投加量0.15g/L,PMS浓度0.7mmol/L的条件下,如图9所示,5组对照组分别为Fe-PC(不添加三聚氰胺和α-D葡萄糖)、NC-PC(不添加硝酸铁)、Fe-C-PC(不添加三聚氰胺)、Fe-NC(不添加PC)以及Fe-N-PC(不添加α-D葡萄糖),在Fe-PC/PMS体系和NC-PC/PMS体系中,反应20min内2,4-D的降解速率常数分别为0.039,0.074min-1,降解效率仅为 18%和 33%,这是因为 Fe-Nx活性中心的部分缺失导致无法活化 PMS产生自由基以降解污染物,材料的少量吸附使得污染物浓度略有降低;在 Fe-C-PC/PMS体系中,反应20min内2,4-D的降解速率常数为0.129min-1,降解效率为55%,这可能是因为 α-D葡萄糖的弱还原性以及PC载体表面的含氧官能团和离域π电子[4]可以将Fe(Ⅲ)部分还原为Fe(Ⅱ),在没有N源的情况下,部分Fe颗粒容易团聚,使得催化剂表面的活性位点减少,从而降低了污染物的降解;在完整的 Fe-NC-PC/PMS体系中,反应20min内2,4-D的降解速率常数为 0.164min-1,降解效率高达 91%,这是因为完整的 Fe-Nx活性中心能够充分活化 PMS产生利于污染物降解的自由基[19],加快反应的进程;在Fe-NC/PMS体系中,α-D 葡萄糖高温碳化会为Fe-Nx提供部分C载体,三聚氰胺提供的N源能够有效调控Fe的价态以形成具有活性中心的Fe(Ⅱ)-NC,使得20min内2,4-D的降解速率常数为0.132min-1,降解速率达到 75%;在 Fe-N-PC/PMS体系中,因为PC载体表面的含氧官能团和离域π电子以及N源的价态调控,使得能够形成较好的 Fe-Nx活性中心从而使其20min内2,4-D污染物降解速率达到80%,其降解速率常数为0.139min-1.

图9 不同对照催化剂对2,4-D去除效果和降解动力学的影响Fig.9 Effect of different reference catalyst on removal and degradation kinetics of 2,4-D
研究表明,过渡金属/PMS体系中主要存在SO4-⋅、SO5-⋅和⋅OH3 种主要自由基,SO5-⋅因其较低的氧化能力常常不参与有机物的降解.为验证反应体系的主要活性物种,分别选用甲醇、叔丁醇、L-组氨酸和对苯醌作为自由基淬灭剂进行了实验,其中,甲醇能够同时淬灭反应体系中的 SO4-⋅和⋅OH,叔丁醇对于SO4-⋅的抑制性较差,因此常用于捕获和淬灭体系中的⋅OH,L-组氨酸和对苯醌能够有效的淬灭反应体系中的1O2和 O2-⋅.在 2,4-D=0.1mmol/L,初始pH=3.4,催化剂投加量0.15g/L,PMS浓度0.7mmol/L的条件下,如图 10所示,甲醇和叔丁醇的加入使得20min内 2,4-D的去除率分别降低为 80%和85%,表明反应体系中同时存在SO4-⋅和⋅OH,且 SO4-⋅占主导作用;对苯醌的加入使得20min内2,4-D去除率降低为 82%,表明反应体系中存在 O2-⋅,甲醇的加入并没有完全抑制 2,4-D的降解,说明体系中还存在非自由基参与反应,L-组氨酸的加入使得 20min内2,4-D去除率降低为50%,说明参与反应的非自由基物种为1O2.

图10 不同淬灭剂对2,4-D去除效果的影响Fig.10 Effect of different quenchants on removal of 2,4-D
为验证SO4-⋅和1O2是体系中参与反应的自由基和非自由基物种,分别以DMPO作为SO4-⋅、⋅OH 和O2-⋅的捕获剂,以 TEMPO 作为1O2的捕获剂进行EPR测试.如图 11所示,检测到了典型的峰强比为1:2:2:1的四重峰以及微弱的DMPO-SO4-⋅加合物的六重峰[20],其分别对应于体系中存在的 SO4-⋅以及少量的⋅OH,同时,也检测到了典型的 1:1:1:1的DMPO-O2-⋅四重峰,表明体系中存在 O2-⋅;另外,检测到了TEMPO的典型三重峰,强度比为1:1:1[21],证明了反应中确实存在1O2.
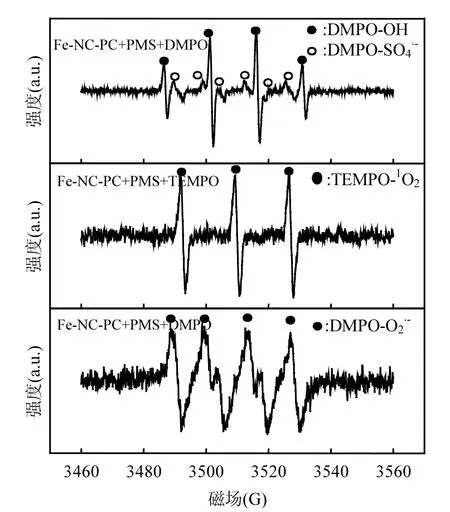
图11 电子顺磁共振波谱图Fig.11 Electron paramagnetic resonance spectroscopy
基于上述的实验结果和相关文献报道,提出了以下反应机理,PC作为催化剂的载体,其表面含有丰富的含氧官能团和离域π电子,通过与α-D葡萄糖的协同作用共同调控前驱体 Fe的价态,N源的存在不仅能够有效的防止 Fe团聚,而且能够直接通过电子的转移调控 Fe的价态,将其从+3价还原为+2价,XPS分析表明(如图2(e)),Fe-NC-PC中的Fe以+2价的形式存在,Fe2+与PMS反应生成具有强氧化性的 SO4-⋅,进一步与产生的 OH-以及 H2O反应生成⋅OH(式(9)~式(11));同时,PMS 在 Fe-NC-PC的催化作用下产生了大量的1O2以及少量的O2-⋅(式(12- 14))[22].最终,2,4-D 在多种氧化物的共同作用下氧化分解.由于2,4-D的酸性性质,需要考虑反应过程中溶出Fe的影响,如图12所示,随着反应的进行,溶液中的Fe2+先增后减,溶液中的Fe3+逐渐增多,表明反应过程中溶出的 Fe2+同样参与了活化PMS的过程,并且随着反应的进行溶出Fe趋于稳定,约为 0.002g/L,在初始的较低 Fe负载量的条件下,溶出的微量Fe可以忽略不计.如图13所示,对反应过程中的 PMS浓度变化进行探究,发现其消耗趋势同2,4- D的降解趋势高度吻合,这也间接证明了 Fe-NC- PC/PMS体系能够最大化的发挥金属催化剂同PMS之间的作用来达到去除污染物的目的.

图12 溶出Fe价态变化示意Fig.12 Schematic diagram of valence state change of dissolved Fe


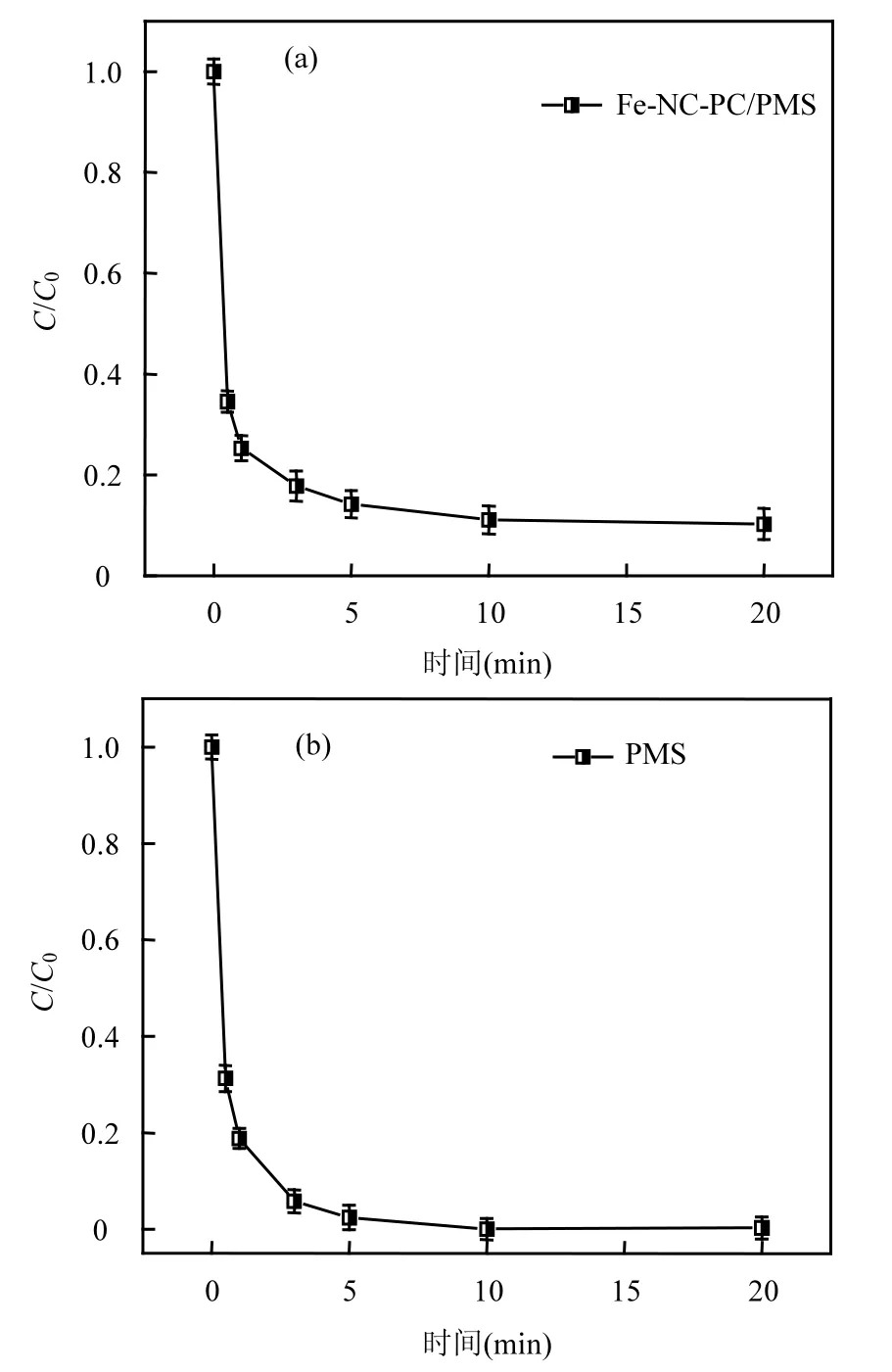
图13 Fe-NC-PC/PMS体系2,4-D去除效果及反应过程PMS浓度变化Fig.13 2,4-D removal efficiency of Fe-NC-PC / PMS system and change of PMS concentration during reaction process
3 结论
3.1 通过分步热分解法制备了较低 Fe负载量的Fe-NC-PC催化剂,能够有效的活化PMS去除水中的 2,4-D污染物,相比浸渍法和同等条件下制备的M-NC-PC(M=Co、Cu)具有更好的降解效果.
3.2 在 pH=3.4,催化剂投加量 0.15g/L,PMS浓度0.7mM/L的条件下,20min内对0.1mmol/L的2,4-D去除率可以达到91%;随着pH的升高,2,4-D的去除率会逐渐降低;水体中低浓度的Cl-、NO3-和HA对2,4-D的降解有轻微抑制作用,低浓度的 HCO3-对2,4-D降解有明显的抑制作用.
3.3 通过制备过程中的还原与包裹保护形成了以Fe(Ⅱ)为主的Fe-Nx活性中心,能够高效的活化PMS以降解水中的 2,4-D,经淬灭实验和 EPR测试可知,1O2在2,4-D的降解过程中起到主要作用.
