羊毛亲水改性及其在活性染料轧染中的应用
2021-08-04李游亚赵强强何瑾馨
李游亚,胡 蝶,赵强强,何瑾馨,2
(1.东华大学 化学化工与生物工程学院,上海 201620;2.东华大学 纺织面料技术教育部重点实验室,上海 201620)
羊毛织物因其丰满的手感、优异的保暖性、独特的悬垂性以及良好的弹性而备受消费者的青睐。由于纤维表面共价结合的脂质以及高交联(异肽键和二硫键)的致密鳞片层的存在,使得本该亲水的蛋白质纤维变得疏水,不仅影响羊毛织物穿着过程中的吸湿排汗性,而且严重影响染料在纤维表面的吸附与扩散[1]。目前对羊毛纤维的改性手段主要分为物理刻蚀、化学修饰和生物酶消蚀。其中物理刻蚀如等离子体处理、超声波处理等可以将鳞片层部分或全部剥落[2-3];化学改性剂如二氯异氰尿酸钠、过氧化氢和功能性大分子等可以将二硫键氧化成磺酸基,或者赋予纤维表面极性基团进而产生新的表面特性[4-5];生物酶可使羊毛角蛋白肽键发生部分降解,提高纤维表面极性基团的数量来提高亲水性[6-7]。但由于有机卤化物的排放及损伤可控性差、生产成本高等原因,以上改性手段并未得到广泛应用。集环保、高效和低损伤于一体的改性手段引起了广泛的关注。高浓度的羟胺可以打断羊毛纤维表面共价结合脂质的硫酯键、氧酯键,表面疏水脂质被去除后而提升羊毛织物的亲水性。但是仍有部分脂质嵌入于二硫键充分交联的多肽链中,亲水效果提升有限并且会引起羊毛织物严重发黄[8]。因此,本文通过低浓度羟胺首先去除羊毛纤维表面共价结合的脂质,降低纤维的疏水性。然后利用L-半胱氨酸打开角蛋白内部的二硫键,同时形成新的二硫键,将L-半胱氨酸结合到羊毛纤维上,进而提高纤维的亲水性,并改善羊毛的轧染性能。
1 实 验
1.1 试剂与仪器
试剂:盐酸羟胺、L-半胱氨酸、氢氧化钠(上海阿拉丁生化科技股份有限公司),氨水(国药集团化学试剂有限公司)、Tween-20(上海西格玛奥德里奇贸易有限公司)、洗涤剂(上海白猫专用化学品有限公司)。
染料:安诺菲克斯C-BS(上海安诺其集团股份有限公司)。
羊毛织物:100% 羊毛平纹机织物(面密度195 g/m2,宁波雅戈尔纺织有限公司)。
仪器:DSA30接触角测试仪(德国Kruss公司),DLS-1000A常温振荡染色试验机(苏州starlet有限公司),DHE型高温汽蒸箱(瑞士Mathis公司),NEXUS-670傅里叶红外光谱仪(美国Nicolet公司),TM-1000型扫描电子显微镜(日本Hitachi公司),VHX-6000超景深三维显微镜(基恩士有限公司),Datacolor SF650型电脑测色配色仪(美国Datacolor公司),Y571B型摩擦牢度测试仪(宁波大禾仪器有限公司)。
1.2 羊毛织物的处理
1.2.1 羟胺预处理工艺
配制用量为11%(owf)的盐酸羟胺溶液,用5 mol/L氢氧化钠溶液调节盐酸羟胺溶液pH值至7,并加入4 g/L Tween-20。将20 g羊毛织物浸入羟胺处理液中(浴比1∶10),在50 ℃下水浴处理2 h后,水洗烘干。
1.2.2 L-半胱氨酸处理工艺
配制用量为20%(owf)L-半胱氨酸溶液,用氨水调节溶液pH值至8,并加入2 g/L Tween-20。将20 g羊毛织物浸入L-半胱氨酸处理液中(浴比1∶30),在50 ℃下处理2 h后,水洗烘干。
1.2.3 羟胺/L-半胱氨酸复合处理工艺
配制用量为11%(owf)的盐酸羟胺溶液,用5 mol/L氢氧化钠溶液调节盐酸羟胺溶液至pH值至7,并加入4 g/L的Tween-20。将20 g羊毛织物浸入羟胺处理液中(浴比1∶10),在50 ℃下水浴处理2 h后,水洗烘干。
配制用量为20%(owf)的L-半胱氨酸溶液,用氨水调节溶液pH值至8,并加入2 g/L Tween-20。将羟胺处理后的羊毛织物浸入L-半胱氨酸处理液中(浴比1∶30),在50 ℃下处理2 h后,水洗烘干。
1.2.4 羊毛织物染色工艺
染液处方:安诺菲克斯C-BS 50 g/L。
固色液处方:氨水6×10-4mol/L。
轧染工艺:经过不同处理工艺的羊毛织物→浸轧染液(二浸二轧,压强为0.25 MPa)→饱和蒸汽汽蒸(100 ℃,5 min)→浸轧碱液(二浸二轧)→饱和蒸汽汽蒸(100 ℃,5 min)→皂洗(皂片2 g/L,95 ℃,10 min,浴比1∶20)→水洗烘干。
1.3 性能测试
1.3.1 织物润湿性
通过水滴的铺展时间来表征羊毛织物的润湿性,采用DSA30接触角测试仪滴加2 μL去离子水,记录从液滴接触织物开始至铺展过程镜面反射完全消失所需的时间。同一织物在不同位置测试20次,取平均值。
1.3.2 纤维的表观结构
将羊毛织物样品喷涂金后,通过TM-1000型扫描电子显微镜在10 kV的加速电压下观察羊毛织物样品的表面形态。
1.3.3 纤维的分子结构
采用NEXUS-670傅里叶红外光谱仪测试经过不同整理工艺的羊毛纤维的大分子结构变化,测试光谱范围为4 000~450 cm-1。
1.3.4 织物的染色性能
采用Datacolor SF650型电脑测色配色仪测量染色织物的L*、a*、b*值以及表观颜色深度K/S值,每个样品上任意测4个点,并取平均值。耐摩擦色牢度参照GB/T 3920—2008《纺织品 色牢度试验 耐摩擦色牢度》进行测试,并通过GB/T 250—2008《纺织品 色牢度试验 评定变色用灰色样卡》进行评级。固色率F计算式为:
式中:(K/S)0和(K/S)1分别对应羊毛织物固色皂洗前后的表观颜色深度。
1.3.5 单纤维活性染料透染性能测试
从羊毛织物样品中分离出纱线,通过哈氏切片器将其切成10~20 μm厚的切片,使用VHX-6000超景深三维显微镜观察纤维切片。
2 实验结果与讨论
2.1 羟胺处理条件对织物润湿性的影响
羊毛纤维表面结合的脂质主要是以硫酯键、氧酯键形式共价交联存在的,羟胺可以通过亲核取代使全部的硫脂键及部分的氧酯键发生断裂,反应过程如图1所示,生成相应的羟肟酸以及羟基或者巯基[9]。羟胺处理温度及时间对织物润湿性的影响如图2所示,在同一温度下随着羟胺处理时间的延长,水滴的铺展时间逐渐减小,羊毛织物表面逐渐变得亲水,水滴最快可在2 s内完成铺展。此外,温度对处理织物达到最佳亲水状态时间有显著影响。在50 ℃下达到最佳亲水效果需要处理90 min,60 ℃下为50 min,而在70 ℃下仅仅需要40 min,说明高温有助于加快羟胺与硫脂键、氧酯键的反应速率。为避免高温对羊毛纤维造成不必要的损伤,羟胺处理温度以60 ℃为宜,处理时间为50 min。
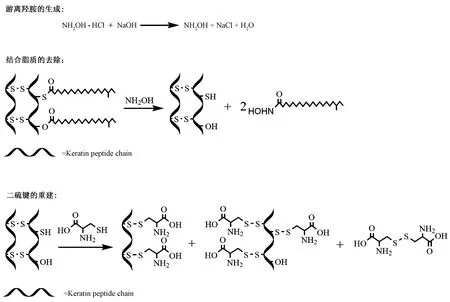
图1 羟胺与羊毛的作用机制
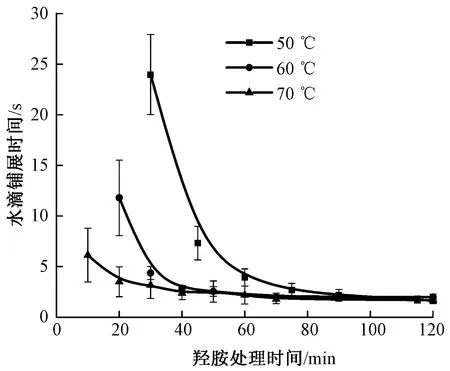
图2 羟胺处理温度及时间对织物润湿性的影响
盐酸羟胺的用量以及处理液pH值也会对织物的亲水性产生影响,盐酸羟胺用量对织物润湿性的影响见图3。可知,随着盐酸羟胺用量的增加,织物的亲水性逐渐增加,并且在7%(owf)的用量下达到最大,说明羊毛表面硫脂键、氧酯键恰好完全断裂所需要的盐酸羟胺用量大约是7%(owf)。

图3 盐酸羟胺浓度对织物润湿性的影响
羟胺处理液pH值对织物润湿性的影响如图4所示。随着pH值的升高,羟胺的有效浓度增加,羊毛织物的亲水性也随之不断提升。当氢氧化钠浓度为16.7×10-2mol/L(pH 值7.51)时,羊毛织物表面的亲水性达到最大,继续增大pH值,水滴铺展时间不再改变。为避免碱性对羊毛织物的损伤,pH值控制在7.5为宜。
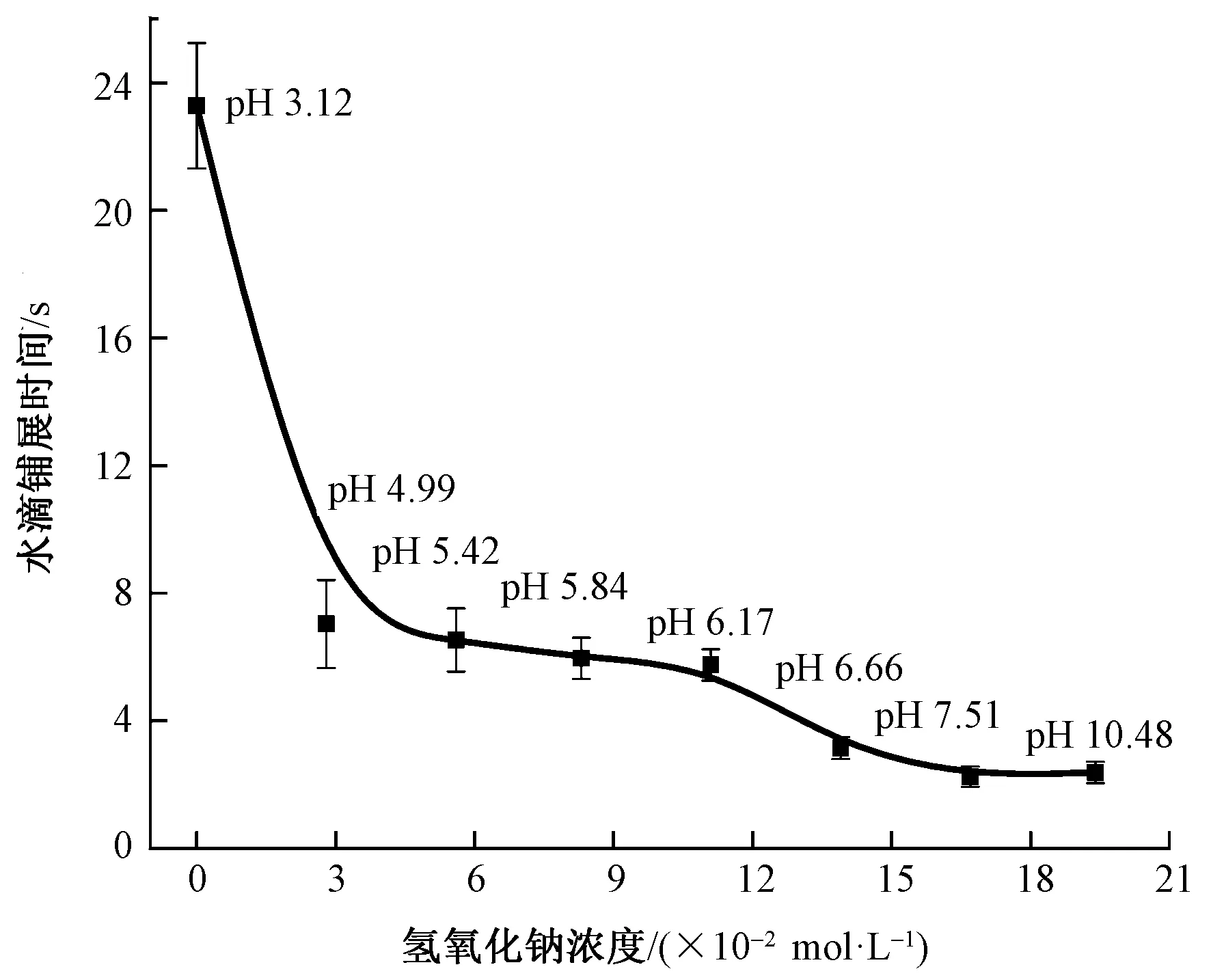
图4 羟胺处理液pH值对织物润湿性的影响
2.2 L-半胱氨酸对织物润湿性的影响
L-半胱氨酸可打开羊毛纤维上二硫键,并生成新的二硫键,L-半胱氨酸与羊毛纤维的反应机制如图5所示,L-半胱氨酸处理温度及时间对织物润湿性的影响如图6所示。在相同温度下,随着L-半胱氨酸处理时间的延长,织物的水滴铺展时间不断减小,亲水性不断提高。此外,随着处理温度的升高,织物达到最佳亲水效果的时间也不断减小。40 ℃下对织物进行L-半胱氨酸处理,达到最佳亲水效果(水滴铺展时间大约2 s)的时间大于120 min,50 ℃下为60 min,而在60 ℃下仅需要30 min,说明较高的温度可以加快L-半胱氨酸的反应速率。为避免高温对羊毛的损伤,60 ℃下处理30 min为最宜。
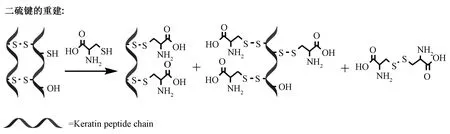
图5 L-半胱氨酸与羊毛纤维的反应机制
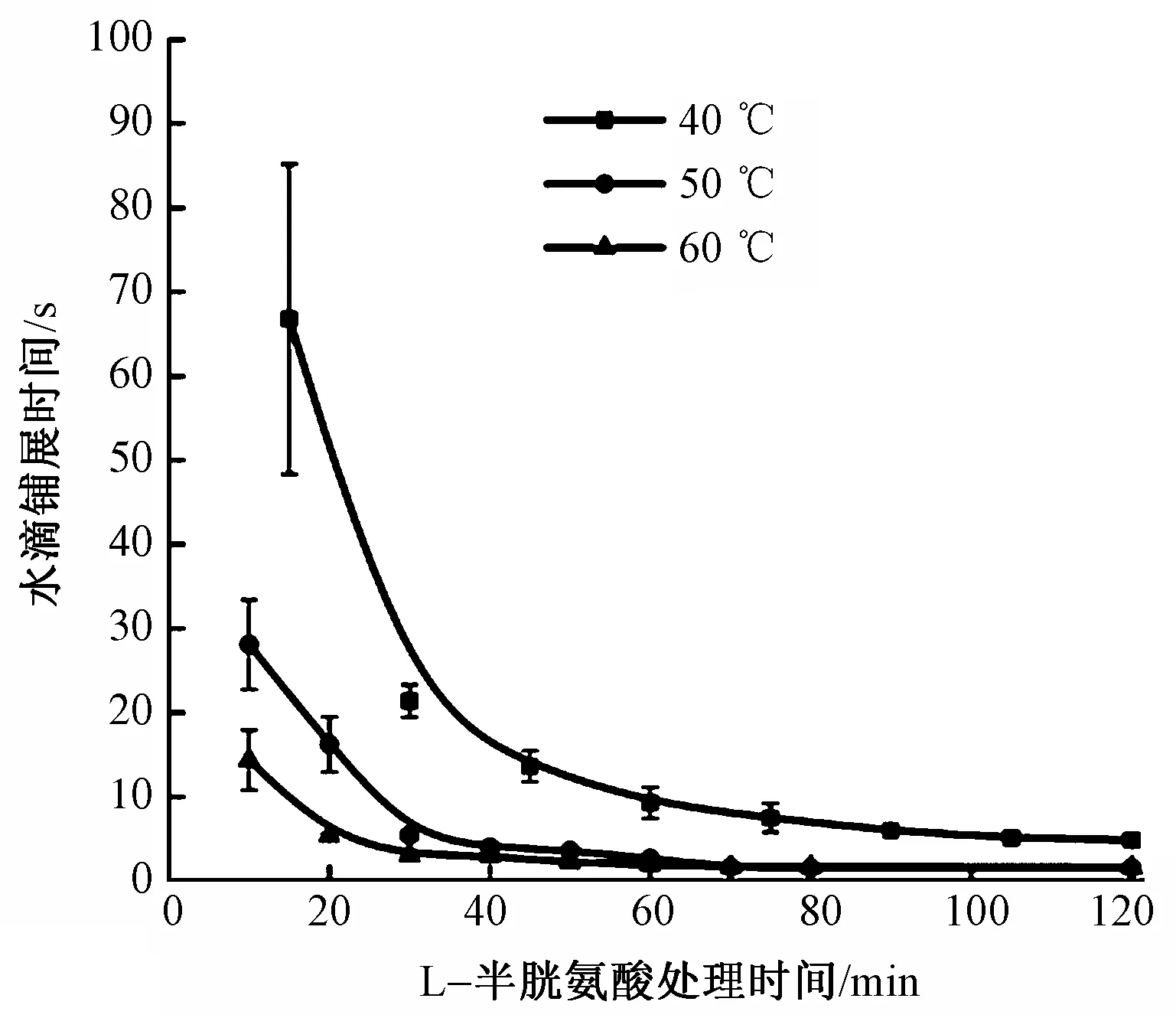
图6 L-半胱氨酸处理温度及时间对织物润湿性的影响
L-半胱氨酸用量以及处理液pH值也会影响织物的亲水性。L-半胱氨酸用量对织物润湿性能的影响如图7所示。随着L-半胱氨酸用量的增加,羊毛织物水滴铺展时间逐渐减小。当L-半胱氨酸用量大于20%(owf)时,亲水性达到最佳(水滴铺展时间大约2 s),此后不再随着L-半胱氨酸用量的增加而增加,因此L-半胱氨酸的最佳用量为20%(owf)。氨水浓度对织物亲水性的影响如图8所示,当氨水浓度从0(pH值为6.27)升高至4.7×10-2mol/L(pH值为8.26)时,织物的水滴铺展时间从33 s迅速下降至2 s左右,此后水滴的铺展时间并不再随着氨水浓度的增加而继续减小。原因是随着氨水浓度的增加,L-半胱氨酸生成的—S—反应性位点也更多[10],有利于纤维内部二硫键的打开。但是为了避免较强的碱性在此温度下对羊毛造成的损伤,氨水浓度以4.7×10-2mol/L为宜。
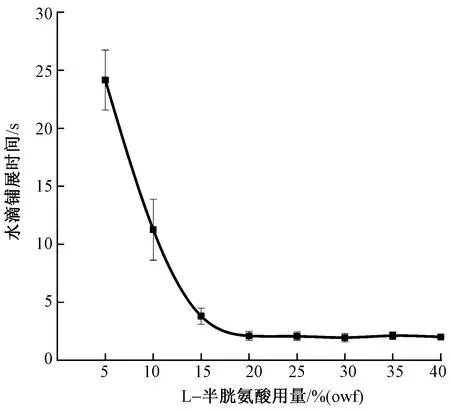
图7 L-半胱氨酸浓度对织物润湿性能的影响
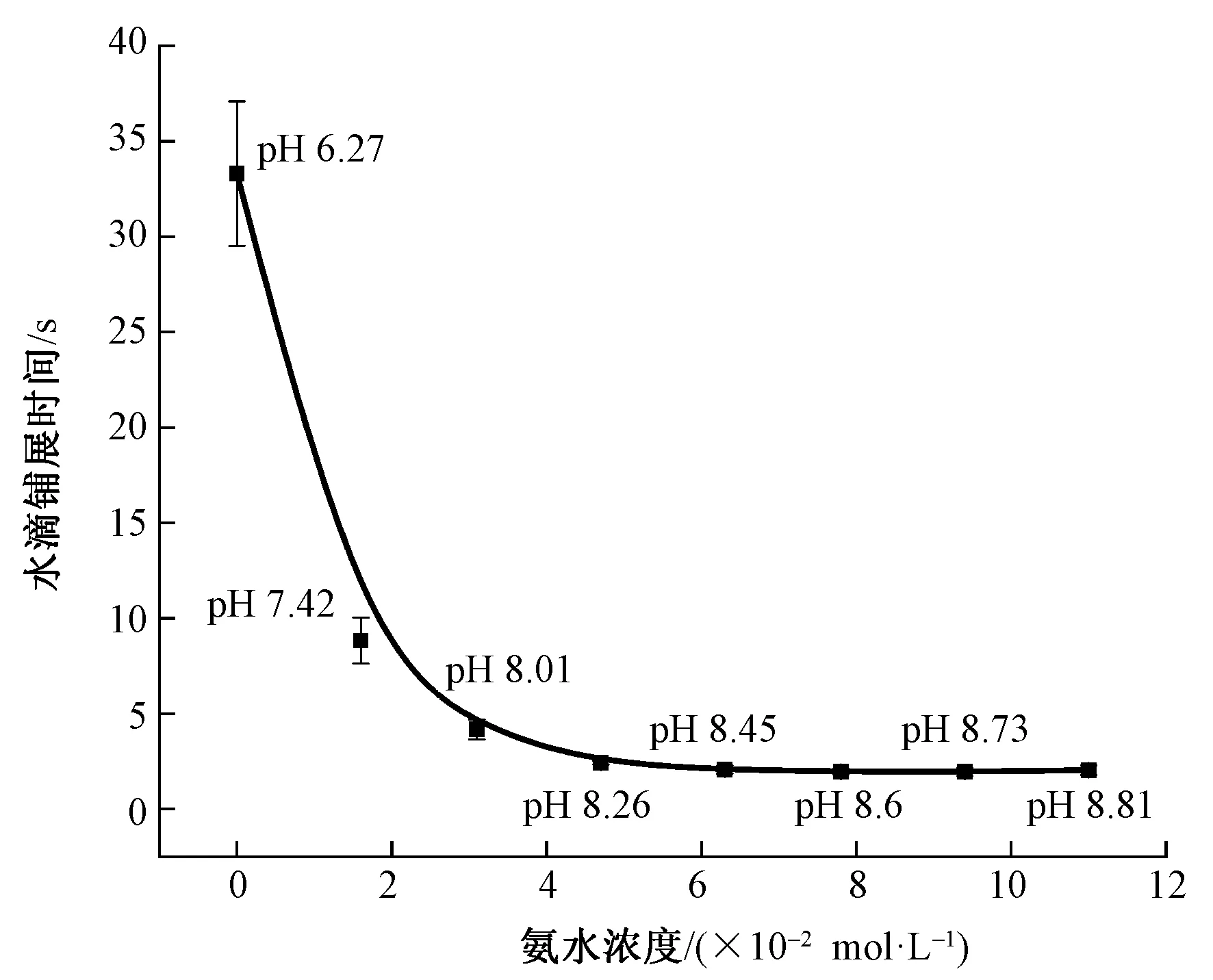
图8 L-半胱氨酸处理液pH值对织物润湿性的影响
2.3 纤维表观结构分析
羟胺/L-半胱氨酸处理对羊毛纤维鳞片层的损伤情况由图9所示。未处理羊毛纤维表面鳞片层清晰可见,改性后的羊毛鳞片层保持完整光洁,鳞片层边缘棱角分明,说明羟胺/L-半胱氨酸处理并不会损伤羊毛的表面。羊毛表面通过羟胺去除的结合脂质的厚度为2~7 nm,这在扫描电镜图片中是难以检测出来的。此外L-半胱氨酸在重组二硫键的过程中也不会降解羊毛蛋白质大分子。但在改性后,如图中箭头所指,羊毛角质细胞的间隙变小。原因可能是在羟胺/L-半胱氨酸改性过程中,细胞膜复合物中低交联的多肽和结合脂质可以被部分地溶出,最终导致角质细胞之间贴合得更加紧密。

图9 改性前后羊毛纤维表面形貌图
2.4 纤维的化学结构分析

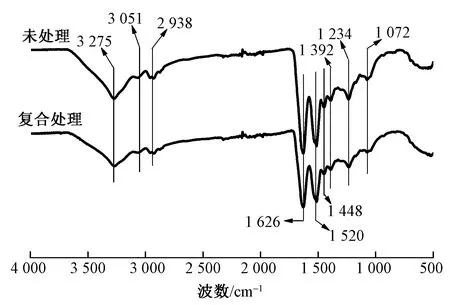
图10 改性前后羊毛纤维的红外谱图
2.5 处理织物的染色性能分析
分别用经过不同工艺处理的羊毛织物进行活性染料轧染染色,测定其L*、a*、b*、K/S值、固色率以及耐摩擦色牢度,结果如表1所示。未处理羊毛由于纤维表面类脂层的存在,浸轧后带液率仅为45%,轧染后的K/S值、固色率都比较低,干、湿耐摩擦色牢度也较差。羊毛织物单独通过羟胺处理后,共价结合的脂质被去除,亲水性得到提升。浸轧染液后织物带液率达77%,表观颜色深度(K/S值)得到提升。此外,羟胺处理削弱了纤维的扩散屏障,有利于染料的扩散,所以固色率和耐摩擦色牢度均得到一定改善。而单独通过L-半胱氨酸处理的羊毛织物浸轧染液后,带液率达73%,表观颜色深度得到提升。此外,L-半胱氨酸赋予纤维表面更多的极性基团,增加了羊毛纤维上的染座,固色率、耐摩擦色牢度也得到了一定程度的改善。但单独处理对于染色效果的提升有限。当织物经过羟胺/L-半胱氨酸复合处理后,浸轧染液后带液率高达99%,与未处理羊毛相比提升了120%,同时K/S值也提高了96%。复合处理不仅增加了纤维中的染座,提升了染料对于纤维的亲和力,而且削弱了羊毛纤维角质层对于染料扩散的屏障作用,导致固色率和耐摩擦色牢度均得到进一步提升。
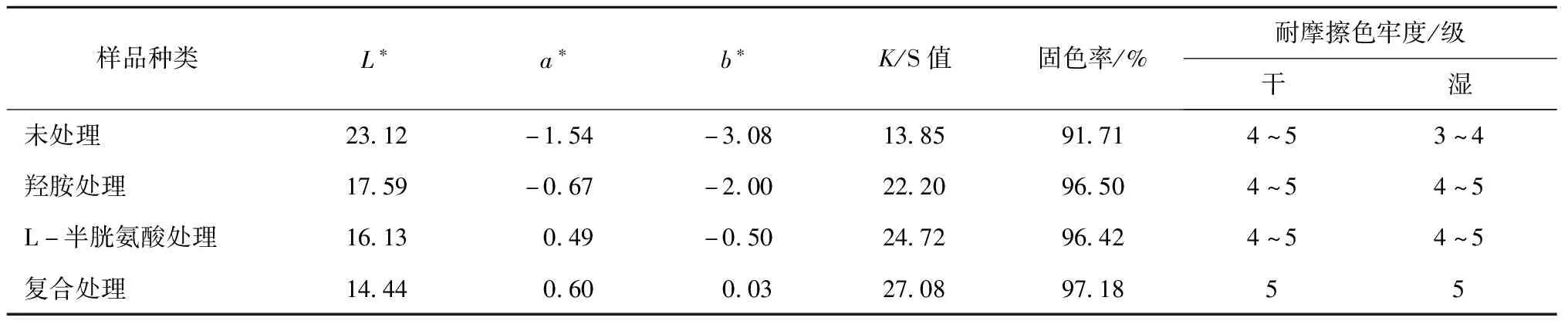
表1 不同工艺处理后羊毛织物的颜色信息
不同羊毛织物的染色截面如图11所示。可见,未处理羊毛纤维截面四周与中心具有严重的色差,是角质层对染料的屏障作用造成染料扩散不匀所致。羟胺或者L-半胱氨酸单独处理后,染料扩散不匀现象有一定的改善,但未消除。当经过羟胺/L-半胱氨酸复合处理后,染料扩散均匀且颜色较深,说明羟胺/L-半胱氨酸复合处理可极大地提升羊毛织物轧染的均匀性以及染深性。

图11 不同处理工艺下羊毛织物活性染料染色截面图
3 结 论
①采用羟胺、L-半胱氨酸对羊毛织物进行改性,极大地提升了织物的亲水性且对纤维表观形貌基本上没有影响。
②根据单因素实验的结果分析,羊毛织物最佳处理工艺为:盐酸羟胺用量7%(owf),氢氧化钠浓度16.7×10-2mol/L,60 ℃处理50 min;L-半胱氨酸用量20%(owf),氨水浓度4.7×10-2mol/L,60 ℃处理30 min。
③通过结合脂质的去除,二硫键的重建不仅增加了羊毛纤维表面的染座,而且削弱了角质层对于染料的扩散屏障作用,活性染料轧染后K/S值,固色率,干、湿耐摩擦色牢度均得到了显著的提高。
