胶质母细胞瘤中基质金属蛋白酶组织抑制物1、基质金属蛋白酶组织抑制物2的表达及与微血管密度的关系△
2021-07-20马建功王晓斌侯欣李明轩方树民刘亚虎何承
马建功,王晓斌,侯欣,李明轩,方树民,刘亚虎,何承#
河南大学第一附属医院1神经外科,2肿瘤科,河南 开封 475000
胶质母细胞瘤是星形细胞瘤中恶性程度最高的胶质瘤,病情发展迅速,预后差。胶质母细胞瘤多位于皮质下,生长在幕上大脑半球各处,可累及对侧大脑半球。调查指出,恶性胶质瘤在原发性恶性脑部肿瘤中的占比约为70%,年发病率约为5/10万,可随着年龄的增长不断升高,胶质母细胞瘤的发病例数也逐年增多。另有报道显示,胶质母细胞瘤在星形细胞瘤中的占比为60%~75%,复发率高,且5年生存率很低。目前人们对于胶质母细胞瘤的发病机制认识尚浅,有研究指出,胶质母细胞瘤患者的肿瘤组织中有大量新血管生成,微血管密度(microvessel density,MVD)显著增加,提示应将抗血管生成作为胶质母细胞瘤患者重要的治疗措施。但是目前针对胶质母细胞瘤患者的常用治疗方法效果并不理想,而与新血管生成相关的因素并未得到全面、有效地控制。基质金属蛋白酶组织抑制物1(tissue inhibitor of metalloproteinase 1,TIMP1)、基质金属蛋白酶组织抑制物2(tissue inhibitor of metalloproteinase 2,TIMP2)均属于基质金属蛋白酶的抑制酶,不仅能够抑制肿瘤细胞生长、浸润和转移,还具有抗纤维化作用,已有报道证实在多种恶性肿瘤组织中二者的表达水平偏高,如乳腺癌、肝癌、星形细胞瘤等。有研究指出,TIMP1、TIMP2表达水平越高,恶性肿瘤的恶性程度越高,预后越差。本研究探讨了胶质母细胞瘤中TIMP1、TIMP2的表达及其与MVD值的相关性,现报道如下。
1 资料与方法
1.1 一般资料
选择2017年1月至2019年12月河南大学第一附属医院收治的胶质母细胞瘤患者。纳入标准:①实施手术治疗,经术后病理检查确诊为原发性胶质母细胞瘤;②手术切除组织均以石蜡包埋存档;③组织学分级为Ⅲ级或Ⅳ级;④临床资料完整。排除标准:①其他类型脑胶质瘤患者;②胶质母细胞瘤复发患者;③手术切除组织切缘未见正常组织;④术前具有抗肿瘤治疗史。依据纳入和排除标准,本研究共纳入42例患者。其中,男22例,女20例;年龄42~75岁,平均(58.52±8.71)岁;组织学分级:Ⅲ级12例,Ⅳ级30例;肿瘤部位:额叶28例,顶叶5例,丘脑-基底节4例,颞叶2例,胼胝体1例,桥脑1例,小脑1例;最大肿瘤直径为8~75 mm,平均(35.52±5.85)mm。收集患者的胶质母细胞瘤组织42例和周围正常组织42例。
1.2 检测方法
采用蛋白质印迹法(Western blotting)检测胶质母细胞瘤组织和周围正常组织中TIMP1、TIMP2的相对表达量。取胶质母细胞瘤组织和周围正常组织,研磨、匀浆、裂解后对总蛋白进行定量,然后进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE),转膜。采用脱脂牛奶封闭,加入鼠抗人TIMP1、TIMP2单克隆抗体,室温孵育过夜;加入过氧化物酶标记的兔抗鼠TIMP1、TIMP2多克隆抗体,4℃孵育2 h。加入电化学发光(electrochemiluminescence,ECL)剂,暗室曝光。以β-肌动蛋白(βactin)为内参,目的蛋白的相对表达量=目的蛋白灰度值/内参蛋白灰度值。
采用免疫组化两步法检测胶质母细胞瘤组织和周围正常组织中的MVD。采用CD34抗体对微血管染色,可见棕褐色颗粒,为血管内皮细胞的细胞质。采用200倍光镜对整张切片扫视,确定3个热点,即微血管密集区域,然后用400倍物镜计算每个热点区域中的微血管数,计算3个热点的平均值记为MVD值。
1.3 观察指标
比较胶质母细胞瘤组织和周围正常组织中TIMP1、TIMP2的相对表达量及MVD值;比较不同组织学分级胶质母细胞瘤组织中TIMP1、TIMP2的相对表达量及MVD值;分析胶质母细胞瘤组织中TIMP1、TIMP2表达与MVD的相关性。
1.4 统计学分析
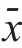
2 结果
2.1 胶质母细胞瘤组织和周围正常组织中TIMP1、TIMP2相对表达量及MVD值的比较
胶质母细胞瘤组织中TIMP1、TIMP2的相对表达量均明显低于周围正常组织,MVD值明显高于周围正常组织,差异均有统计学意义(P
<0.01)。(表1)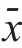
表1 胶质母细胞瘤组织和周围正常组织中TIMP1、TIMP2相对表达量及MVD值的比较(±s)
2.2 不同组织学分级胶质母细胞瘤组织中TIMP1、TIMP2相对表达量及MVD值的比较
Ⅳ级胶质母细胞瘤组织中TIMP1、TIMP2的相对表达量均明显低于Ⅲ级胶质母细胞瘤组织,MVD值明显高于Ⅲ级胶质母细胞瘤组织,差异均有统计学意义(P
<0.01)。(表2)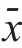
表2 不同组织学分级胶质母细胞瘤组织中-TIMP1、TIMP2相对表达量及MVD值的比较(±s)
2.3 胶质母细胞瘤组织中TIMP1、TIMP2的表达与MVD 的相关性
胶质母细胞瘤组织中TIMP1、TIMP2的表达均与MVD值呈负相关(r=-0.796、-0.815,P<0.01)。
3 讨论
原发性胶质母细胞瘤的分子改变以表皮生长因子受体扩增和过量表达为主,可导致表皮生长因子水平升高,新生血管大量生成,对脑组织产生浸润性损坏,还可导致头痛、偏瘫、失语、偏盲等。胶质母细胞瘤多呈浸润性生长,可侵犯几个脑叶和深部结构,对患者的身心健康造成严重危害。尽管目前临床上常用手术、放疗和化疗等方法治疗胶质母细胞瘤患者,但效果并不理想,主要原因如下:胶质母细胞瘤的恶性程度高,临床治疗难度大;胶质母细胞瘤可生成大量新生血管,导致肿瘤复发、浸润和转移,甚至危及患者的生命安全。然而目前人们对新生血管生成的机制认识尚浅,其治疗措施也缺乏针对性。因此该领域工作者应积极探索与胶质母细胞瘤患者新生血管生成相关的因素,以期为临床抗肿瘤治疗的研究提供新方向。
新生血管生成是一个涉及多种细胞和分子的复杂过程,主要包括激活期血管基底膜降解、血管内皮细胞激活、血管内皮细胞增殖和迁移、新生血管以及血管网重建等,还可形成小的血管分支。基质金属蛋白酶组织抑制物(tissue inhibitor of metalloproteinase,TIMP)对细胞生长、凋亡均具有直接作用,而TIMP1、TIMP2作为该家族的主要成员,不仅可参与细胞生长、增殖与凋亡的调控,还可影响新生血管生成,主要原因可能是影响细胞外基质金属蛋白酶的降解。研究指出,新生血管生成是从基底膜降解开始的,即邻近血管生成刺激因子的静脉基底膜降解,然后内皮细胞变形,生成血管芽伸入细胞外基质,与此同时细胞外基质金属蛋白酶增多,TIMP1减少,新生血管和基底膜生成,进而参与恶性肿瘤的发生和发展。另有报道显示,胶质瘤患者中细胞外基质金属蛋白酶/TIMP平衡受损,TIMP1和TIMP2减少,其中TIMP1可直接参与新生血管生成,TIMP2不仅可与整合素α3β结合,还可诱导基因表达将细胞周期阻滞于G期,抑制细胞迁移,抑制新生血管生成。本研究中,胶质母细胞瘤组织中TIMP1、TIMP2的相对表达量均明显低于周围正常组织,MVD值明显高于周围正常组织,差异均有统计学意义(P<0.01);Ⅳ级胶质母细胞瘤组织中TIMP1、TIMP2的相对表达量均明显低于Ⅲ级胶质母细胞瘤组织,MVD值明显高于Ⅲ级胶质母细胞瘤组织,差异均有统计学意义(P<0.01)。说明胶质母细胞瘤组织中TIMP1、TIMP2表达水平偏低,MVD值偏高,且恶性程度越高,上述指标异常程度越严重。
MVD是新生血管生成的重要标志,TIMP1和TIMP2的表达与神经微丝阳性的神经元均具有紧密相关性,且二者均可影响神经元由增生状态向最终分化状态转化。因此TIMP1和TIMP2均可直接影响胶质母细胞瘤的新生血管生成潜能和恶性程度,恶性程度越高,MVD值越高,而TIMP1和TIMP2表达水平越低。国外报道指出,血管内皮管腔的形成依赖于基质金属蛋白酶/TIMP平衡,各种因素加入后一旦打破二者的平衡关系,便可影响新生血管生成和肿瘤细胞的浸润与转移,使肿瘤组织的恶性潜能增加。既往报道显示,胶质母细胞瘤中TIMP1和TIMP2缺乏,基质金属蛋白酶高表达,前者可能与瘤周水肿无关,而后者与瘤周水肿密切相关。本研究结果与上述报道相符,胶质母细胞瘤组织中TIMP1和TIMP2的表达均与MVD呈负相关,提示TIMP1和TIMP2表达水平越低,MVD值越高,新生血管生成越多,肿瘤的恶性程度越高。
综上所述,胶质母细胞瘤组织中TIMP1和TIMP2的表达水平均明显低于周围正常组织,MVD值均明显高于周围正常组织,且恶性程度越高,TIMP1和TIMP2的表达水平越低,MVD值越高,TIMP1和TIMP2的表达与MVD均呈负相关。结合本研究结果,建议尝试将TIMP1和TIMP2作为胶质母细胞瘤临床治疗的新靶点,以降低MVD值,抑制新生血管生成。如何采取有效的措施提高胶质母细胞瘤患者中TIMP1和TIMP2的表达水平,降低MVD值应作为后期研究的重点。
