广州市2018年至2020年无偿献血者的HTLV感染及流行情况调查
2021-07-13陈翀单振刚游冉冉
陈翀,单振刚,游冉冉
(广州血液中心,广东 广州 510000)
人类嗜细胞病毒(human T-lymphocyte virus,HTLV)属于一种致瘤性RNA病毒,可分为4型,其中HTLV-Ⅰ抗体及HTLV-Ⅱ抗体主要用于献血者筛查。感染HTLV-Ⅰ型病毒后可导致成人T细胞白血病/淋巴瘤等疾病,使机体外周血中异常T细胞比例升高,并伴多种器官系统的损害,治疗效果及预后较差[1]。研究[2]发现,感染HTLV-Ⅰ型病毒易发生支气管扩张,严重时可危及患者生命安全。感染HTLV-Ⅱ病毒后可导致T多毛细胞/巨粒细胞白血病,可损害中枢神经系统,严重影响患者的生活质量。HTLV主要经母婴及血液传播,其中血液传播的常见途径为输血、器官移植等途径。输血是我国临床上补充血容量的主要方式,提示输血存在感染HTLV的风险,因此,需严格管控血制品的安全性。目前,尚无治疗感染HTLV病毒的疫苗或特效药等,一旦感染,后果难以想象。为保障血液制品的安全性[3-4],世界卫生组织建议筛查献血者HTLV感染及流行的情况,以便及时阻断通过血液制品传染疾病,同时可制定针对性的血液管理,加强血液管理的薄弱环节。本研究旨在探讨2018年至2020年无偿献血者HTLV感染及流行情况调查,旨在为临床提供参考依据,现报道如下。
1 资料与方法
1.1 临床资料 选取广州市2018年1月至2020年9月无偿献血者699 081例作为研究对象,其中男461 799例,女237 282例;年龄18~60岁。共收集699 081例血样标本,其中初筛阳性248例,确诊阳性8例。本研究经本院医学伦理委员会审核批准。
1.2 方法 所采血液标本均经酶联免疫吸附法测定(enzyme-linked immunosorbent assay,ELISA)初筛,若结果显示ELISA反应性的血样标本,均采用电化学发光法试剂盒检测HTLV抗体,若结果阳性,再使用确诊实验蛋白印迹法(western blot,WB)和/或实时荧光定量聚合酶链反应(real time polymerase chain reaction,RT-PCR)检测HTLV抗体。
1.3 检测 收集所有无偿献血者的血样标本静置于常温空气中30 min,置入4 000 r/min KUBOTA8420离心机(日本久保田)中高速离心10 min,置于-25℃冰箱中待测。采用ML-STAR全自动加样仪(瑞士哈密顿公司)、FAME全自动酶标分析系统(瑞士哈密顿公司)检测血清HTLV,采用双抗原夹心酶联免疫法,试剂盒由北京万泰生物药业股份有限公司提供。ELISA显示反应性的血样标本采用Roche Cobas 601全自动电化学发光免疫分析仪(瑞士Roche),试剂盒由罗氏诊断产品(上海)有限公司提供。采用全自动混样仪(HAMILTON Microlab STAR IVD,瑞士HAMILTON),核酸提取仪(cobasAmpliPrep)与分析仪(cobasTaqMan)检测ELISA及电化学发光法均显示反应性的血样标本,试剂盒由北京万泰生物药业股份有限公司提供。采用MP Diagnostics HTLV BLOT 2.4 Western Blot Assay(美国MP)、MagNA Pure LC DNA Isolation Kit-Laege Volume(瑞士Roche)、ABI7500 fast荧光定量PCR仪(美国Applied Biosystems)及罗氏MagNAPure LC 2.0 DNA自动提取仪(瑞士Roche)检测ELISA及电化学发光法均显示反应性的血样标本,所有指标检测均严格按照操作说明书进行。判断标准,①初筛阳性:ELISA显示反应性;②确诊阳性:经WB和RT-PCR显示阳性。
1.3 观察指标 ①比较2018年至2020年无偿献血者HTLV的初筛阳性率及确诊阳性率;②比较2018年至2020年无偿献血者HTLV初筛及确诊情况;③比较2018年至2020年无偿献血者HTLV阳性感染者的情况。
1.4 统计学方法 采用SPSS 21.0统计软件进行数据分析,计数资料以[n(%)]表示,比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 2018年至2020年无偿献血者HTLV的初筛反应性率及确诊阳性率比较 2018年至2020年无偿献血者HTLV初筛反应性率及阳性率比较差异无统计学意义,见表1。
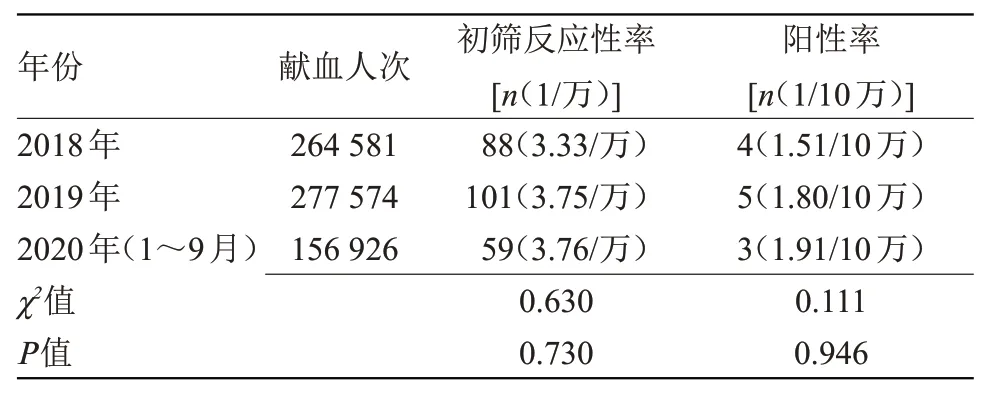
表1 2018年至2020年无偿献血者HTLV的感染情况比较
2.2 2018年至2020年无偿献血者HTLV初筛及确诊情况比较 无偿献血者HTLV ELISA反应性为248例,占比3.55/1万,HTLV阳性为12例,占比0.17/1万,见表2。

表2 2018年至2020年无偿献血者HTLV初筛及确诊情况比较[n(1/万)]
2.3 2018年至2020年无偿献血者HTLV阳性感染者的情况比较 HTLV阳性献血者主要以男性(11例,91.67%)为主,HTLV阳性献血者主要以36~45岁(5例,41.66%)年龄段为主,HTLV阳性献血者主要以首次献血人群(9例,75.00%)为主,HTLV阳性献血者主要以广东籍(7例,58.33%)为主,见表3。

表3 2018年至2020年无偿献血者HTLV阳性感染者的情况比较
3 讨论
HTLV属于逆转录病毒,具备较高的遗传稳定性,与其复制方式密切相关。感染HTLV不通过病毒本身复制,而是由感染细胞的克隆增殖所致。多项研究[5-6]发现,HTLV的流行情况与地区密切相关,如日本2006年至2007年首次献血者中HTLV-Ⅰ阳性率为31.7/1万;伊朗在2009年至2013年HTLV阳性率为9.87/1万,首次献血者中HTLV阳性率为29/1万,固定献血者中HTLV阳性率为0.1/1万;美国2000年至2009年献血者中HTLV阳性率为1.97/1万,2011年至2013年献血者中HTLV阳性率为0.34/1万。本市早于2019年为广州市献血者HTLV流行概况及基因分型展开报道[7],证实本市属于低流行地区,暂时发现HTLV-Ⅰ基因型的感染,并未发现HTLV-Ⅱ基因型的感染。目前,为保障血液制品的安全性,日本、中国香港及台湾地区已将献血群体检测血清学抗-HTLV-Ⅰ、抗-HTLV-Ⅱ列为常规项目,避免经血液传播途径感染HTLV。
目前,全球均未攻克HTLV预防性疫苗及特效药的研制。从病毒本身感染的特点考虑,存在自机体感染至产生抗体需51 d的窗口期,从而限制常规筛查献血群体的血清学抗-HTLV的准确度。陈海洋[8]等报道显示,HTLV病毒存在于淋巴细胞中,血清中很少存在HTLV,进而对血液制品应用白细胞过滤,滤白后血制品的病毒载量低于感染所需的病毒载量,且血液制品保存>14 d,极大降低感染HTLV的风险。为提高血液制品的安全性,可通过加强首次献血者的检测环节,及制定针对性群体招募策略,同时提倡临床输血时采用滤白血制品,一定程度上可降低感染HTLV的风险性。本研究结果显示,2018年至2020年无偿献血者HTLV初筛反应性率及阳性率无明显上升趋势,HTLV感染呈低流行趋势,本市流行情况与安庆[8]、东莞[9]、石家庄[10]等地区一致,表明采用血制品滤白等措施可降低HTLV感染的风险;HTLV阳性献血者主要以男性为主,以36~45岁年龄段为主,考虑与本市HTLV感染率低,献血人数过多等特点有关;HTLV阳性者以首次献血人群为主,表明严格管控首次献血人群的筛查环节至关重要。
综上所述,广州市2018年至2020年无偿献血者HTLV感染率无明显上升趋势,呈低流行趋势,严格筛查首次献血者的HTLV抗体,有助于降低血液传播途径HTLV感染的风险。
