总硬度测试中的影响因素分析
2021-06-21杨琳
杨 琳
(辽宁省丹东水文局,辽宁 丹东118000)
0 前言
水体总硬度即水中钙、镁离子的总浓度[1],也分为碳酸盐硬度和非碳酸盐硬度。碳酸氢盐硬度经加热之后生成沉淀物可从水中除去,故亦称为暂时硬度。非碳酸盐硬度主要是由钙镁的硫酸盐、氯化物和硝酸盐等盐类形成[2]。这类硬度加热后不能沉淀,即不能通过加热后沉淀去除,称为永久硬度[3]。
总硬度含量适中的饮用水口感清冽,对心血管系统、神经肌肉、人体骨骼和凝血过程有积极的影响[4],水硬度无论过高或过低都会对健康产生不利影响稀释后标准物质的标准浓度和不确定度[5],但由于检测过程中一些因素会影响总硬度的测定值,因此,本文将从多方面研究总硬度测试中的影响因素、解决办法以及注意事项。
1 实验室能力
辽宁省水环境监测中心丹东分中心,隶属于辽宁省水利厅,监测分中心设有综合业务室、分析检测室和质量保证室。中心拥有流动注射仪、原子吸收分光光度计、红外测油仪、紫外分光光度计、酸度计、浊度仪、电导率、离子色谱、原子荧光、电子天平及常规分析仪器设备(列入本监测分中心现有的大型仪器),总计22台(套),实验人员专业水平较高,最高学历硕士研究生毕业。
本监测分中心具有较雄厚的技术力量,具有承担水资源水环境监测和评价工作以及国内外委托检测、验证业务能力。主要从事水资源量、质监测工作,负责监测本省境内江河湖库的水质状况,审核水域纳污能力,负责水利工程建设水质监测、供水取水许可的水质监测,参与辖区内重大水污染事故和由水污染引起的水事纠纷的调查、仲裁,承担水资源论证勘测评价及第三方监测,即委托检测或仲裁检测等任务。认证的检测范围为地表水、地下水、生活饮用水(含引用天然矿泉水)、农田灌溉水、污废水、大气降水、水文要素等第二大类48个项目参数。
2 实验材料及原理
2.1 实验仪器及试剂
1)实验仪器:酸式滴定管(25 mL)、锥形瓶、天平。
2)实验试剂:a.缓冲溶液;b.EDTA二钠标准溶液;c.钙标准溶液;d.铬黑T指示剂。
2.2 实验原理
水中的钙镁离子与铬黑T指示剂生成紫红或者紫色溶液,在适当pH时,当使用EDTA二钠标准溶液进行滴定,游离的钙、镁离子先与EDTA反应,跟指示剂络合的钙、镁离子随后和EDTA发生反应,具体过程见式(1)~式(4)。
滴定前Ca2+,Mg2+与铬黑T反应,生成与铬黑T指示剂本身颜色不同的络合物:

逐滴加入EDTA标准溶液时,它首先与溶液中游离的Ca2+,Mg2+逐步发生络合反应,然后夺取已经与铬黑T指示剂络合的Ca2+,Mg2+,此时溶液的变化由红色逐渐变为蓝色。
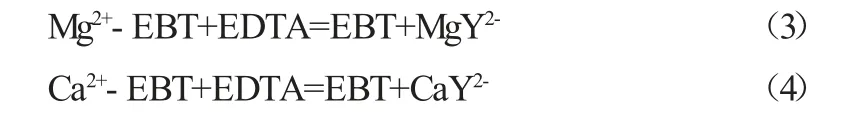
3 总硬度测试中的影响因素
3.1 总硬度测试时的pH
总硬度的测试原理是络合反应,而络合滴定中酸度的控制的原因见式(5):

1)pH值不同,溶液中EDTA二钠的离解平衡处于不同的阶段,见表1。

表1 EDTA的离解平衡
参加主反应的是Y4-,由于酸效应,即由于氢离子浓度不同,EDTA参加主反应的能力也不同,Y4-是参加主反应的离子,因此,综合考虑使用pH>10.34作为总硬度测试的最佳pH。
2)铬黑T指示剂需要在一定的酸度介质中使用。
铬黑T属于金属指示剂In,而金属指示剂本身就是有机酸或弱碱,能随着pH的改变而发生颜色变化,金属指示剂具有酸碱指示剂的性质,使用时应该注意金属指示剂的适用pH范围,为了明确测试的敏感度,铬黑T指示剂的颜色应该与它与钙镁离子络合反应的产物颜色有明显差别,铬黑T指示剂溶液中随着不同的pH下显示颜色见表2。

表2 铬黑T指示剂在不同pH下的颜色变化
由于铬黑T指示剂与钙镁离子络合物成红色,为了保证黑T指示剂的颜色与它与钙镁离子络合反应的产物颜色有明显差别,因此使用铬黑T作为指示剂测试总硬度时的pH选择范围为8<pH<11,实际上在pH(9~10.5)使用。
综合以上内容,总硬度的测试是在10.34<pH<10.5的条件下,乙二胺四乙酸二钠标准溶液与水中的钙及镁离子反应生成络合物。注意:测试结果表明pH对总硬度的测试有一定影响,因此若pH存在过高过低现象时,需要对其进行处理,可使用6 mol/L的盐酸溶液或是100 g/L的氢氧化钠溶液对pH值进行调节,调节至pH为7时再加入缓冲溶液后进行滴定测试。
3.2 铬黑T指示剂
3.2.1 指示剂
金属指示剂是一种络合剂,它能与金属离子形成与其本身明显不同颜色的络合物而指示滴定终点。铬黑T(EBT),属于金属指示剂的一种,黑色粉末,有金属光泽,其水溶液易发生聚合,不能长期保存。
指示剂与金属离子若稳定性太强,则终点时不能够被滴定剂置换出来,否则终点推迟甚至封闭;如果稳定性太弱,未到终点时游离指示剂出来,会导致提前确定了终点,铬黑T与钙镁金属离子生成适当稳定性的配合物。而且铬黑T指示剂与金属离子生成的配合物易溶于水,否则在滴定时,指示剂与EDTA的置换作用进行的过于缓慢从而导致终点的拖后变长。使用铬黑T指示剂,显色反应灵敏快速,并且有良好的变色可逆性。
3.2.2 指示剂铬黑T的封闭与处理
指示剂的封闭现象:化学计量点时不见指示剂变色。
1)产生原因
干扰离子:当铬黑T与除钙镁离子以外的金属离子生成了稳定的配合物而不能被EDTA二钠标准溶液置换出来,即当水中存在某些金属离子和铬黑T的化学反应常数较大,Cu2+、Co2+、Ni2+、Fe3+、AL3+等对铬黑T具有封闭作用,即它们与铬黑T指示剂发生反应,而它们属于干扰离子。
消除方法:配置时加入三乙醇胺掩蔽Fe3+、AL3+等离子,以消除其对EBT的封闭。
2)指示剂的氧化变质
铬黑T指示剂含有双键结构,易被日光、氧化剂及空气中的氧化还原性物质破坏,容易失效,尤其在水溶液中不稳定,变质后的铬黑T,一般滴定终点变色不敏锐。放置时间较长的铬黑T几乎不能够正常变色。
3)改善方法
可用NaCL固体稀释,配置成固体混合物或者加三乙醇胺或者无水乙醇配置。
3.3 滴定终点的确定
变色实质:EDTA置换与指示剂配位络合反应的金属离子释放指示剂,从而引起溶液颜色的改变,钙和镁总量C(mmoL/L)用式(6)计算:

式中:C1为EDTA二钠溶液浓度,mmol/L;V1为滴定中消耗EDTA二钠溶液的体积,mL;V0为试样体积,mL。
1 mmol/L的钙镁总量相当于100.1 mg/L以CaCO3表示的硬度。
选取水利部样品编号为170853的总硬度标准物质见表3。

表3 标准物质的标准浓度和不确定度
使用乙二胺四乙酸二钠标准溶液对标准物质进行3次滴定,并记录对应不同滴定值时溶液的变色情况(肉眼视觉下),最后根据滴定数计算总硬度值,汇总结果见表4。
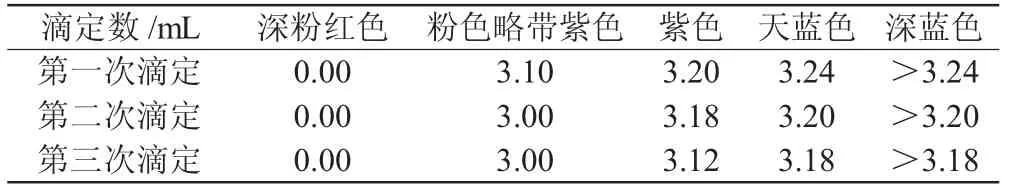
表4 不同标准溶液滴定数时溶液的颜色变化
滴定过程中,从原理角度来讲,锥形瓶中混合液的颜色随着乙二胺四乙酸二钠标准溶液滴定数量的增加红色逐渐褪去,蓝色逐渐显著,在视觉效果上呈现深粉红色溶液逐渐变淡,直到溶液变为淡粉色略带紫色,这个阶段的颜色对标准溶液十分敏感,很快由淡粉色略带紫色变为紫色,再由紫色变为天蓝色,再继续滴加,溶液颜色会加深。
将不同颜色对应的颜色值代入式(9)进行计算,并对应标准物质的标准值的不确定度范围,见表5。
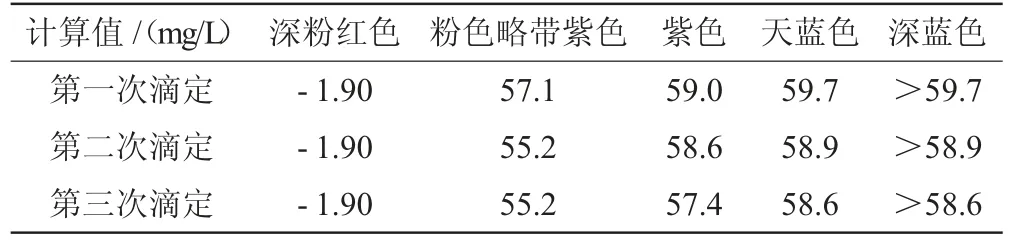
表5 溶液不同颜色时对应滴定量的计算值
由表4可知,标准物质的标准值为60 mg/L,于滴定时溶液由深粉红色到粉色带紫色到紫色,到天蓝色,最后再滴加会变为深蓝色对应的滴定量的计算值比较,当溶液颜色为天蓝色时与标准物质的标准值最为接近,且根据反应原理当红色全部退却,蓝色出现说明反应已完全,因此当溶液突变为天蓝色时即为滴定终点。
3.4 滴定速度
据总硬度的测试公式(9),标准溶液滴定的毫升数影响着总硬度的测试结果,因此滴定终点一定要准确,由于络合反应速度需要一定的反应显色时间,此时很容易在达到滴定终点后继续进行滴加导致过量,测试结果失真。
因此在滴定时应时刻注意混合液的颜色变化,在确定滴定终点实验中,根据滴定值与溶液颜色的对应情况,从开始滴定溶液会持续一段时间的由深粉红色到淡粉色(肉眼观察下)的阶段,此阶段可以匀速滴定,并不断摇晃,当锥形瓶中混合液突然出现微紫色时,说明接近滴定终点,此时滴定要放慢速度,每滴一滴摇晃均匀,大概2~3滴后,溶液会完全变成紫色。出现紫色即马上到达终点,此时要控制滴定速度,每一次滴定保持半滴到一滴,再摇晃,时刻观察溶液颜色,确定没有出现颜色变化后再滴下一滴,当溶液突然由紫色变为天蓝色时,停止滴定,记录使用的标准溶液量代入公式并计算。
3.5 滴定水样颜色的处理
测定水总硬度时,存在杂质多或者颜色较深的水样,会影响滴定终点颜色的判断或者干扰滴定,导致标准溶液的使用量无法准确确定。当杂质较多时,要对水样进行过滤,再取澄清水样进行测试;若发现水样颜色较深,则应立即用乙醚对水样进行萃取取色。如果还是难以满足测试条件,可使用水浴锅蒸干,再将蒸干后的残渣用1∶1的盐酸溶解,来有效去除杂质。
4 结论
1)总硬度的测试是在10.34<pH<10.5的条件下,乙二胺四乙酸二钠标准溶液与水中的钙及镁离子反应生成络合物。
2)针对化学计量点时不见指示剂变色,可通过添加三乙醇胺或者固体氯化钠消除现象。
3)溶液突变为天蓝色时即为滴定终点。
4)根据不同的颜色变化需要控制不同滴定速度。
