改性毛竹生物炭复合材料对水中磷的动态吸附试验
2021-06-05李艳红王国豪张立浩朱义年
李艳红, 王国豪, 张立浩, 梁 森, 朱义年
(1.桂林理工大学 a.环境科学与工程学院; b.广西环境污染控制理论与技术重点实验室; c.岩溶地区水污染控制与用水安全保障协同创新中心, 广西 桂林 541006; 2.青岛华高墨烯科技股份有限公司, 山东 青岛 266000)
0 引 言
磷是植物和其他生物所必须的营养元素之一, 同时也是水体富营养化的关键因子[1-2]。由于人类活动的影响, 水体P含量过高导致的水体富营养化已成为全球环境问题之一, 有效控制水体中P含量已成为解决全球水体富营养化问题的关键[3-4]。目前处理含P废水的方法有反渗透[5]、电渗析[6]、接触过滤法[5, 7]、生物法[2]和沉淀法[5], 但其所需成本均较高、操作工艺复杂, 不宜大规模应用。吸附法因其具有工艺简单、选择性好、经济性高的优点而被广泛应用于水体净化工程实践中, 吸附法处理水体中磷主要依赖于吸附剂对磷的作用。目前在吸附法中应用众多的吸附剂中, 生物炭具有可再生、来源广、成本低等优势而成为研究和工程应用的热点[8]。近年来, 利用金属氧化物对生物炭进行活化改性, 使生物炭能够更高效地从水中去除磷酸盐等污染物的研究引起了广大学者们的关注。Delaney等[9]研究了多孔材料耦合金属氧化物在化学工程中对于除磷的作用, 结果显示多孔材料耦合金属氧化物是磷酸盐的有效吸附剂, 在适当的条件下去除率高达100%; Kralchevska等[10]使用高铁酸盐(Ⅵ)诱导核壳纳米粒子进行原位吸附实验, 结果表明, 通过对核壳纳米粒子表面的吸附, 即可从水中去除磷酸盐; Fytianos等[11]建立了使用三价铁从废水中去除磷的模型, 该模型解释了加入三价铁之后, 对水溶液和城市污水中磷酸盐去除效果的差异; Zach-Maor等[12]建立了固化纳米磁铁矿固定磷酸盐的Thomas模型, 证明了Thomas模型可以拟合固化纳米磁铁固定磷酸盐的过程; Rafati等[13]使用含铁纳米粒子的树脂从水中去除磷酸盐, 当水体中磷酸盐初始浓度为6 mg·L-1时, 含铁纳米离子树脂对水体中磷酸盐的去除率可达73%左右; 刘桂凤等[14]以硝酸铁为改性剂, 对白果壳进行改性制备成白果壳遗态Fe2O3/Fe3O4/C复合材料, 研究了其对Sb(Ⅲ)的去除性能, 结果表明,在初始 Sb(Ⅲ)浓度为 50 mg·L-1时, 其吸附量达9.23 mg·g-1, 吸附过程主要发生配位交换表面络合反应。
中国是世界上的最大产竹国, 竹类资源丰富[15]。竹类的开采、加工和利用过程中会产生大量低价值的竹类废弃物, 其有效利用率仅有35%~40%[16]。毛竹是具有复杂多级结构的生物材料, 适合制备生物炭[17-18]。目前, 利用毛竹制作的生物炭吸附剂的种类众多[19-20], 但利用铁改性毛竹制生物炭进行动态吸附的研究鲜有报道。本研究以农林废弃物毛竹为植物模板, 利用铁氧化物对毛竹生物炭改性, 制备改性的毛竹生物炭复合材料(PMC-Fe/C-B)。首先对原材料进行氨水抽提预处理, 可以有效去除原始材料中堵塞导管孔的侵填体组织、油脂和树腊等, 浸提后的PMC-Fe/C-B可以完整地复制毛竹的分级多孔结构[21], 孔径分布为20~50 μm(梯纹导管)、3~10 μm(梯纹导管、螺纹导管)和0.1~1.3 μm(纤维孔)。铁溶液浸提后进行高温焙烧, 毛竹模板中的纤维素经过了脱氢、脱氧的过程, 所吸附的Fe(NO3)3在高温下分解为Fe2O3、NO2和O2。 在高温含氧环境下, 部分Fe2O3被进一步转化为磁性氧化铁(Fe3O4)。通过金属原位优化改性工艺, 成功负载了Fe2O3/Fe3O4铁氧化物功能基团。
本文以PMC-Fe/C-B为吸附剂进行P(Ⅴ)溶液的动态吸附试验, 研究初始浓度、流速、pH值、吸附剂投加量、吸附剂粒径以及吸附温度等因素对吸附过程的影响, 通过现代分析手段表征复合材料对水体中P(Ⅴ)吸附前后的变化, 探究吸附剂对水体中P(Ⅴ)的吸附行为和吸附机理。
1 实验部分
1.1 实验材料与仪器
实验材料:磷酸二氢钾、氨水、硝酸铁、乙醇, 以上试剂均为分析纯; 实验用水为去离子水。
仪器:真空管式马弗炉(RS120/750/11/P300, 德国纳博热仪器公司), 紫外分光光度计(UV2100, 尤尼柯上海仪器有限公司), 扫描电子显微镜(JSM-6380LV, 日本电子株式会社), 能谱仪(IE350, 英国牛津仪器国际市场有限公司), X射线光电子能谱仪(ESCALAB Mark II, 英国VG科学仪器公司), X射线衍射仪(X′Pert PRO, 荷兰帕纳科公司), 傅里叶变换红外光谱仪(470 FT-IR, 美国热电公司)。
1.2 实验方法
1.2.1 改性材料制备 以农林废弃物的毛竹旁枝为材料, 经抽提预处理、清洗、烘干、硝酸铁溶液中循环浸泡、焙烧等工艺制得吸附剂PMC-Fe/C-B[22]。具体制备方法:①将毛竹碎化, 放入5%稀氨水中浸煮(100 ℃,6 h), 用超纯水洗净后烘干(80 ℃, 1 d); ②称取硝酸铁溶于乙醇超纯水(V∶V=1∶1)混合溶剂中, 制备1.2 mol/L硝酸铁前驱体溶液, 水浴保温浸泡稀氨水浸煮烘干后的产物(60 ℃, 5 d)后取出烘干(80 ℃, 1 d); ③重复步骤②3次, 将水浴保温浸泡的产物置于马弗炉中焙烧(600 ℃, 3 h), 冷却至常温后研磨过筛, 获得不同粒径的PMC-Fe/C-B。
1.2.2 动态吸附试验 将磷酸二氢钾(KH2PO4)溶于超纯水配制模拟含P(Ⅴ)废水, 以PMC-Fe/C-B为吸附剂, 以含P(Ⅴ)废水初始浓度、pH值、流速、PMC-Fe/C-B投加量、粒径和温度为影响因素开展动态吸附试验, 研究PMC-Fe/C-B对P(Ⅴ)的动态吸附效果。采用动态吸附模型中较常用的Thomas模型探究改性吸附剂对P(Ⅴ)的吸附行为及其吸附机理。动态吸附试验在自制小型固定床吸附装置内进行(图1)。

图1 动态吸附实验装置图Fig.1 Dynamic adsorption experimental device①—进水槽; ②—蠕动泵; ③—温度调节池; ④—吸附柱; ⑤—温度调节器; ⑥—出水槽; ⑦—循环水泵
PMC-Fe/C-B吸附柱④的长度为200 mm, 外径为35 mm, 内径为12 mm(当吸附剂投加量为0.5 g时, 吸附剂的高度为12.3 mm, 吸附体容积BV为1.4 mL)。为避免动态吸附过程中吸附剂的流失, 吸附柱的底部和顶部各设有纤维玻璃膜, 用蠕动泵控制进水流速, 使含P(Ⅴ)废水自下而上进入吸附柱, 定时采集流出液, 运用过硫酸钾-钼锑抗分光光度法(GB 11893—1989)测定流出液中P(Ⅴ)的质量浓度。以《污水综合排放标准》(GB 8978—1996)规定的P(Ⅴ)一级排放标准质量浓度为穿透点(Cb=0.5 mg·L-1), 以占溶液初始质量浓度90%的流出液P(Ⅴ)质量浓度作为衰竭点。P(Ⅴ)平衡吸附量为
(1)
式中:qtotal为吸附剂对P(Ⅴ)的平衡吸附总量,mg;qe为单位质量吸附剂对P(Ⅴ)的平衡吸附量,mg·g-1;Q为进水流速,mL·min-1;t0为吸附起始时间,min;te为吸附达到平衡所需的时间,min;Cad为已被吸附的P(Ⅴ)质量浓度, mg·L-1;x为吸附剂投加量,g。
通过改变进水初始P(Ⅴ)浓度(5、10、20和30 mg·L-1)、进水流速(4.280、5.136、6.849和8.561 mL·min-1)、进水pH值(1.0、2.0、3.0、4.0、5.0、6.0、8.0、9.0和10.0)、吸附剂投加量(0.3、0.4、0.5和0.6 g)、吸附剂的粒径(20~40目(0.841~0.4 mm)、40~60目(0.4~0.25 mm)、60~80目(0.25~0.177 mm)、80~100目(0.177~0.149 mm)和>100目(<0.149 mm))和吸附温度(25、35和45 ℃)等条件对P(Ⅴ)动态吸附的影响因素进行研究。
1.2.3 动态吸附结果的模型 Thomas模型是一种常用的动态吸附模型, 用于预测吸附剂的吸附容量和描述吸附柱的穿透曲线[23-24]。该模型假设在吸附过程中不存在轴向扩散, 因此Thomas模型适用于预测外部和内部扩散阻力非常小的吸附过程。
(2)
式中:Ct、C0—出水、进水浓度, mg·L-1;kTh—Thomas模型常数, mL·(min·mg)-1;qe—吸附剂平衡吸附量, mg·g-1;x—吸附剂在吸附柱中的投加量, g;Q—进水流速, mL·min-1;t—吸附时间, min。
1.2.4 材料表征方法 利用SEM-EDS、FT-IR、XRD和XPS等技术手段对吸附前后的吸附剂进行固相表面元素及其形态的表征, 分析吸附前后PMC-Fe/C-B复合材料的表面元素、基团和价态的变化和分布特征, 从而为吸附过程和机制的研究提供微观信息和佐证。
2 结果与讨论
2.1 动态吸附结果
2.1.1 溶液初始浓度 当进水浓度为5、10和20 mg·L-1时, 达到穿透时(0.5 mg·L-1)的时间(处理水量)分别为96 min(352 BV)、75 min(275 BV)、21 min(77 BV), 达到衰竭时的时间(处理水量)分别为200 min(733 BV)、148 min(543 BV)、86 min(315 BV),qe分别为7.83、12.47和12.39 mg·g-1。表明随着溶液初始浓度的增加, PMC-Fe/C-B对P(Ⅴ)的吸附效果变差(图2)。吸附柱里面的吸附点位饱和较慢, 穿透和衰竭时间随之增加。随着进水浓度提高, 穿透和衰竭时间大大缩短, 出水浓度随之升高。

图2 溶液初始浓度对PMC-Fe/C-B吸附P(Ⅴ)的影响Fig.2 Effect of initial concentration of solution on the adsorption of P(Ⅴ) on PMC-Fe/C-B
2.1.2 进水流速 在低流速条件下吸附柱对P(Ⅴ)的吸附效果更好(图3)。在低流速下(4.280 mL/min-1)的穿透时间比高流速(8.561 mL·min-1)从12 min(4 BV)延长到了88 min(323 BV), 衰竭时间从70 min(257 BV)延长到了188 min(689 BV)。在较低流速下的qe相对较大, 在4.280、5.136、6.849和8.561 mL·min-1下, 分别为12.92、12.47、12.00和7.95 mg·g-1, 主要是因为流速越小, P(Ⅴ)与PMC-Fe/C-B上的活性位点接触时间更长更充分, 因此有更多的P(Ⅴ)被去除。当流速从4.280 mL·min-1增加到8.561 mL·min-1时, 总P(Ⅴ)去除率从76.43%降低至58.09%。

图3 进水流速对PMC-Fe/C-B吸附P(Ⅴ)的影响Fig.3 Effect of inflow velocity on the adsorption of P(Ⅴ)on PMC-Fe/C-B
2.1.3 溶液初始pH 如图4a、b所示, P(Ⅴ)的吸附受pH的影响较大, 低pH条件(2~3)下对P(Ⅴ)的吸附去除较为有效。pH为2、3时达到穿透点(0.5 mg·L-1)的时间分别为105 min(385 BV)、150 min(550 BV),qe分别为10.70 mg·g-1和12.47 mg·g-1, 去除率分别为70.63%和77.65%。而在其他的pH条件下,qe和去除率依次降低, 表明pH值对穿透曲线的影响较大。当pH从2上升到10时, 去除率从69.58%下降到43.40%。

图4 溶液初始pH值对PMC-Fe/C-B吸附P(Ⅴ)的影响Fig.4 Effect of initial pH on the adsorption of P(Ⅴ) onPMC-Fe/C-B
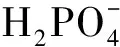
(3)

2.1.4 吸附剂投加量 吸附剂投加量(吸附剂层高)对吸附柱的穿透时间和性能存在较大的影响(图5)。当PMC-Fe/C-B投加量分别为0.3、0.4、0.5和0.6 g, 穿透时间分别为22 min(81 BV)、25 min(92 BV)、73 min(268 BV)和115 min(422 BV),qe分别为10.28、10.29、12.47和14.38 mg·g-1, 去除率分别为60.12%、63.42%、77.65%和81.23%。在较低的PMC-Fe/C-B投加量条件下, 吸附柱穿透和衰竭都较快, 穿透曲线较陡峭。当PMC-Fe/C-B投加量(吸附剂层高)增加时, P(Ⅴ)离子有更长的时间与吸附剂接触, 能降低出水中P(Ⅴ)的浓度, 同时可以有效地延缓吸附柱的穿透和衰竭。

图5 吸附剂投加量对PMC-Fe/C-B吸附P(Ⅴ)的影响Fig.5 Effect of adsorbent dosage on the adsorptionof P(Ⅴ) in PMC-Fe/C-B
2.1.5 吸附剂粒径 图6显示, 吸附剂粒径越小, PMC-Fe/C-B对P(Ⅴ)的吸附效果越好。当PMC-Fe/C-B粒径分别为60~80目、80~100目和>100目时,qe分别为7.14、10.80和12.47 mg·g-1。当吸附剂的粒径从20~40目下降到>100目时, 吸附剂比表面积从138.17 m2·g-1增加到186.66 m2·g-1, 平均孔径宽度从4.371 13 nm变化到3.289 67 nm, 总孔容从0.150 988 cm3·g-1增大到0.153 514 cm3·g-1, 表明随着粒径变小, PMC-Fe/C-B的比表面积增大, 微孔孔容增大, 可供吸附的点位增多且被缓慢结合, 穿透曲线变平坦, 穿透时间相应变长, 吸附能力也就越强。

图6 吸附剂粒径对PMC-Fe/C-B吸附P(Ⅴ)的影响Fig.6 Effect of particle size of adsorbent on the adsorptionof P(Ⅴ) in PMC-Fe/C-B
2.1.6 吸附温度 如图7所示, 温度越高, PMC-Fe/C-B对P(Ⅴ)的吸附效果越好。当吸附温度分别为25、35和45 ℃时, 对应的吸附容量qe分别为11.39、12.47和14.37 mg·g-1,τexp分别为112 min(411 BV)、123 min(451 BV)和143 min(524 BV)。可能是由于PMC-Fe/C-B对P(Ⅴ)的吸附属于吸热反应, 提高反应温度可以促进吸热反应向正反应方向移动, 促进PMC-Fe/C-B对水体中P(Ⅴ)的吸附, 达到更好的吸附效果。

图7 吸附温度对PMC-Fe/C-B吸附P(Ⅴ)的影响Fig.7 Effect of adsorption temperature on the adsorption of P(Ⅴ) in PMC-Fe/C-B
2.2 Thomas模型模拟动态吸附
Thomas模型可以拟合进水流速、溶液初始浓度、吸附剂投加量和环境温度对PMC-Fe/C-B动态吸附水中P(Ⅴ)性能影响, 拟合参数与误差分析结果如表1所示, 穿透曲线见图2~7。

表1 不同条件下PMC-Fe/C-B吸附 P(Ⅴ)的Thomas参数Table 1 Thomas parameters for column adsorption of P(Ⅴ) on PMC-Fe/C-B at different conditions
当进水浓度从5 mg·L-1增加到20 mg·L-1时, Thomas常数kTh呈降低趋势,qe, exp从7.98 mg·g-1增加到11.67 mg·g-1, 表明此阶段是质量传质主导的吸附过程, 浓度差是吸附反应发生的主要驱动力。 在较高的进水浓度下, 具有的反应驱动力相对较大, 吸附性能相应得到改善。当进水流速从4.280 mL·min-1增加到8.561 mL·min-1时,kTh从0.005 42 mL·(min·mg)-1升高到0.009 62 mL·(min·mg)-1,qe, exp从12.76 mg·g-1降低到7.46 mg·g-1。以上结果表明, 低流速、高进水浓度条件会促进PMC-Fe/C-B对P(Ⅴ)的吸附。同时, 在较低的流速下废水在吸附柱内具有较长的停留时间, 有利于P(Ⅴ)离子的扩散。当吸附剂投加量从0.3 g增加到0.6 g时, 吸附剂层高从0.98 cm增加到1.48 cm(由吸附剂投加量换算得到[25]),kTh降低,qe, exp从9.78 mg·g-1增加到14.26 mg·g-1。 当吸附剂粒径从60目到>100目时,kTh从0.007 24 mL·(min·mg)-1降低到0.006 33 mL·(min·mg)-1,qe, exp从6.92 mg·g-1增加到12.36 mg·g-1。当吸附剂的粒径>100目时, 吸附剂比表面积增加, 平均孔径宽度变小, 总孔容增大, 可供吸附的点位增多且被缓慢结合, 吸附能力增强。经测定, 吸附剂PMC-Fe/C-B的零点电位pHzpc约为3.3, 吸附剂表面带正电荷, 易于吸附带有负电荷的离子, 当pH=3时,qe, exp最大为12.36 mg·g-1, 吸附剂PMC-Fe/C-B对P(Ⅴ)的吸附效果最好。吸附时温度从25 ℃到45 ℃,kTh从0.006 48 mL·(min·mg)-1降低到0.005 97 mL·(min·mg)-1,qe, exp从11.30 mg·g-1升高到14.33 mg·g-1, 表明适当提高温度有利于PMC-Fe/C-B对P(Ⅴ)的吸附。
在给定的实验条件下, 通过Thomas模型计算出的相关系数(R2)较高, 如进水P(Ⅴ)浓度的影响(R2=0.967 8~0.991 2), PMC-Fe/C-B投加量的影响 (R2=0.977 5~0.990 8), 流速的影响(R2=0.948 4~0.990 8), PMC-Fe/C-B粒径的影响(R2=0.987 5~0.992 0), 温度的影响(R2=0.979 7~0.9875), pH的影响(R2=0.936 8~0.991 5), 表明Ct/C0和t之间的相关性显著,qe跟qe, exp存在很高的一致性, 揭示了Thomas模型能够很好地描述PMC-Fe/C-B对P(Ⅴ)的吸附过程。
2.3 动态吸附表征
2.3.1 SEM-EDS 对初始浓度为50 mg·L-1含P(Ⅴ)溶液吸附处理后的PMC-Fe/C-B进行SEM电镜扫描和EDS能谱分析(图8、表2)。吸附P(Ⅴ)后的SEM-EDS结果显示, PMC-Fe/C-B的螺纹导管上、维管束的蹄管内、纤维细胞腔的径向壁和横向壁上的纹孔内可见有成团的沉积物存在。同时, PMC-Fe/C-B的横、纵截面均存在目标元素P的检出, 且横、纵截面的P元素占比分别为1.26%和0.94%。O元素的比例下降, Fe元素比例上升, C元素变化不大。

表2 PMC-Fe/C-B吸附P(Ⅴ)后表面原子浓度的变化

图8 PMC-Fe/C-B吸附P(Ⅴ)前后的SEM-EDS表征结果Fig.8 SEM-EDS scan spectrogram of PMC-Fe/C-B before and after P(Ⅴ) adsorption
2.3.2 XRD 对PMC-Fe/C-B吸附P(Ⅴ)前后XRD表征结果显示(图9), PMC-Fe/C-B吸附P(Ⅴ)后2θ为24.50°、35.47°、49.53°、62.54°的Fe2O3特征峰消失, 2θ为33.21°、54.12°处的Fe2O3特征主峰明显减弱, 2θ为29.98°处的Fe3O4特征峰有所加强, 揭示了PMC-Fe/C-B吸附P(Ⅴ)后氧化铁晶型发生了改变, 可能是因为Fe2O3溶于水发生水合反应, 生成了FeOOH。

图9 PMC-Fe/C-B吸附P(Ⅴ)前后的XRD谱图Fig.9 XRD patterns of PMC-Fe/C-B after P(Ⅴ) adsorption
2.3.3 FT-IR PMC-Fe/C-B吸附P(Ⅴ)的FT-IR谱图(图10)结果显示, 在PMC-Fe/C-B吸附P(Ⅴ)后, 在波数3 437.33 cm-1处出现较宽的吸收峰, 对应于—OH的反对称伸缩振动和对称伸缩振动, 说明吸附后氧化铁表面出现—OH基团, 同时印证了PMC-Fe/C-B在吸附P(Ⅴ)过程中表面存在酸碱离解行为。

图10 PMC-Fe/C-B吸附P(Ⅴ)前后的FT-IR谱图Fig.10 FT-IR patterns of PMC-Fe/C-B after P(Ⅴ) adsorption

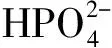

图11 PMC-Fe/C-B吸附P(Ⅴ)后的XPS全谱扫描图及Fe2p/C1s/O1s窄谱扫描图Fig.11 XPS full spectrum scan and Fe2p/C1s/O1s narrow spectral scan of the PMC-Fe/C-B after P(Ⅴ) adsorption

表3 PMC-Fe/C-B吸附P(Ⅴ)后Fe、O的结合能、电荷变化及电子转移方向
3 结 论
以铁改性毛竹生物炭复合材料为吸附剂, 当初始浓度为5 mg·L-1, 进水流速为5.136 mL·min-1, pH为3, 吸附剂投加量为1.0 g, 粒径>100目, 吸附温度为35 ℃, PMC-Fe/C-B对P(Ⅴ)的最大吸附容量qe, exp为14.26 mg·g-1, 去除率为77.65%,此时PMC-Fe/C-B作为吸附剂对水体中P(Ⅴ)的吸附效果最好。

Thomas模型能较好地拟合和预测不同实验条件下的P(Ⅴ)吸附试验数据, 相关性系数R2>0.9。当进水流速、吸附剂投加量(吸附柱层高)和原水P(Ⅴ)浓度增大时, 达到50%穿透所需的时间会有所降低。
