典型低阶煤热解过程中镉元素的释放规律
2021-06-02周玲妹王晓兵马茂林刘姣姣
周玲妹,王晓兵,马 晨,刘 爽,马茂林,刘姣姣
(中国矿业大学(北京)化学与环境工程学院,北京100083)
低阶煤在世界各地均有分布,如美国、澳大利亚和德国等,在中国主要分布于新疆、内蒙和云南等地[1]。低阶煤内水分、氧含量、挥发分较高,而碳含量低和发热量低以及易氧化、自燃等特性,给其储存、运输、加工、转化带来了许多困难[2]。
热解,作为热化学过程中的起始反应,对煤炭气化和燃烧至关重要[3]。低阶煤经热解后,水分明显降低,发热量大幅提高,不易自燃,更便于运输和储存,提高了可靠性和利用率,目前,热解技术在中国已得到不同程度的工业化应用[4,5]。但中国每年煤炭利用量巨大,在煤热解过程中因重金属元素及其化合物的迁移和转化产生的有害物质会对下游产品的生产和环保带来压力,当其在环境中积累到一定程度会对生态环境造成污染,进而危害人类的健康[6−8]。
目前,关于重金属元素释放行为的研究大多集中在动力煤燃烧过程,对于低阶煤热解过程中重金属元素的释放行为的相关报道较少[9]。热解过程是在无氧条件下进行,整个过程包括一系列复杂的裂解和缩聚反应,热解温度、停留时间以及升温速率都会对镉(Cd)的释放和迁移产生影响[10−14];同时研究表明,Cd在煤中的赋存形态也是造成其热解过程中挥发行为不同的原因,周玲妹等[15]研究表明,在一定的热解条件下与煤中有机组分伴生的Cd在较低的温度下便开始逸出,而与硅铝酸盐、碳酸盐等矿物伴生的Cd基本稳定存在于热解后的固体半焦中;高温时(750℃以后),由于所选煤种SiO2含量较高,高温下熔融硅酸盐可与气态Cd发生反应,导致煤中Cd的释放速率开始迅速下降,使得Cd的挥发率降低。魏晓飞等[16]发现,元素化学性质、热解温度和赋存状态是影响煤热解过程中Cd等重金属元素挥发的主要原因,赋存于煤中水溶态和可交换态的重金属元素随着煤热解第一阶段水分的挥发附着于煤颗粒表面,随着挥发分的大量逸出得以挥发;与煤中有机态结合的重金属元素会随着有机质的急剧热解而大量挥发;与硫化物结合的元素易在高温还原性条件下挥发;碳酸盐结合态和硅酸盐结合态的重金属元素则比较稳定,在热解过程中不易挥发。Chen等[17]发现,Cd与硅酸盐在高温条件下反应生成稳定的硅酸铝镉矿物,离子交换态和硫化物结合态Cd在热解过程中释放到气相中。从上述相关研究可以看出,Cd在热解过程中的释放与热解条件和其在煤中的赋存形态密不可分。目前,关于低阶煤中重金属元素在热解过程中的挥发行为鲜有报道,低阶煤具有较高的挥发分和反应活性,是煤化工领域较好的原料。因此,研究低煤阶煤热解过程中重金属元素的释放行为,对于低煤阶煤的开发利用具有重要意义。
针对目前低阶煤热解过程中Cd迁移行为研究不足这一现状,本研究利用卧式和立式管式炉分别对新疆淖毛湖煤和内蒙高硫煤进行慢速和快速热解实验,并结合热重分析和逐级化学提取,考察了赋存形态、热解终温、升温速率和热解停留时间对Cd释放规律的影响;最后利用FactSage热力学软件在理想条件下模拟Cd在低阶煤热解过程中的迁移和转化规律,以期为中国低阶煤热解制备高品质化学品和燃料时重金属元素的迁移和转化行为提供一定的科学依据。
1 实验部分
1.1 实验样品
实验所选取的低阶煤为新疆淖毛湖煤(NMH)和内蒙古高硫煤(GL)。实验前将煤样破碎、筛分至2 mm以下,然后80℃真空干燥24 h。煤样的工业分析和元素分析分别依照《煤的工业分析方法》(GB/T 212—2008)和采用Vario MACRO元素分析仪进行测定,使用硫分分析仪(YX-DL8300)测定煤中总硫含量,使用X射线荧光光谱(XRF-1800)对煤中灰成分进行分析,结果见表1。从表1可以看出,NMH的挥发分较高,而硫含量和灰分低于GL;NMH灰成分主要为SiO2、Al2O3和CaO,而GL灰成分主要为SiO2、Al2O3、CaO和SO3。使用马弗炉在250℃对原煤进行低温灰化60 h,对低温灰化样品进行X射线衍射分析(D/max2500PC),分析结果见图1。从图1可以看出,NMH中主要矿物质有高岭石、石英和方解石,而GL中主要矿物质为石英、石膏、方解石和黄铁矿。
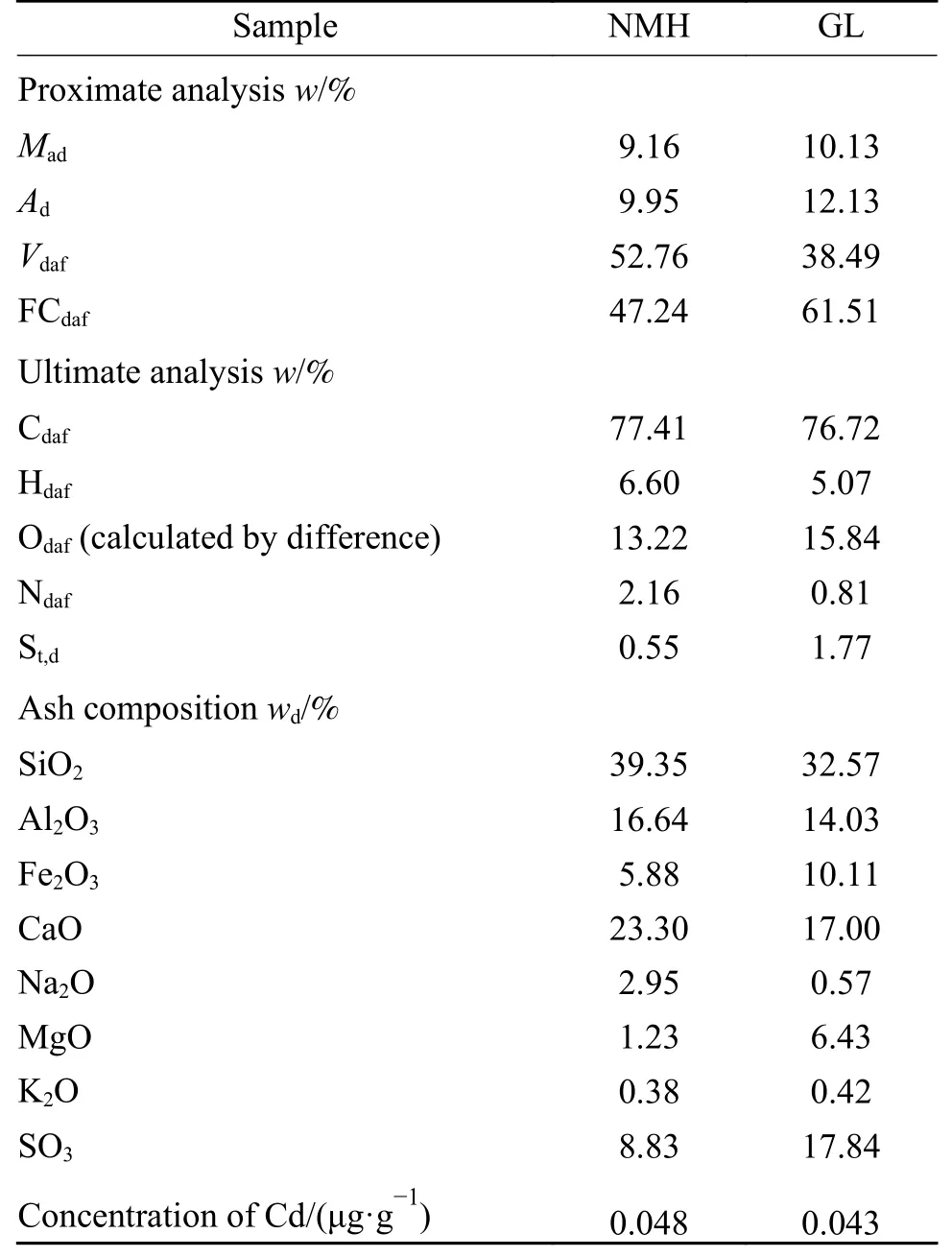
表1 原煤基本性质Table 1 Basic properties of NMH and GL raw coal
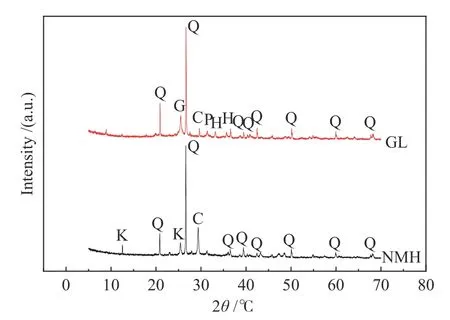
图1 原煤的XRD谱图Figure 1 XRD patterns of raw coal (Q-quartz (SiO2);Kkaolinite (Al4(Si4O10)(OH)8);P-pyrite(FeS2);S-Gypsum(CaSO4);C-calcite(CaCO3)
1.2 热重分析
热重分析在Mettler-Toledo公司的TAG/DSC1同步热分析仪上进行。实验气氛为高纯氮气,温度为30−900℃,升温速率为10℃/min,样品进料量约为10 mg。
1.3 固定床热解实验
使用如图2(a)所示的卧式管式炉和图2(b)所示的立式管式炉固定床反应器,对原煤分别进行慢速和固体热载体快速热解实验。
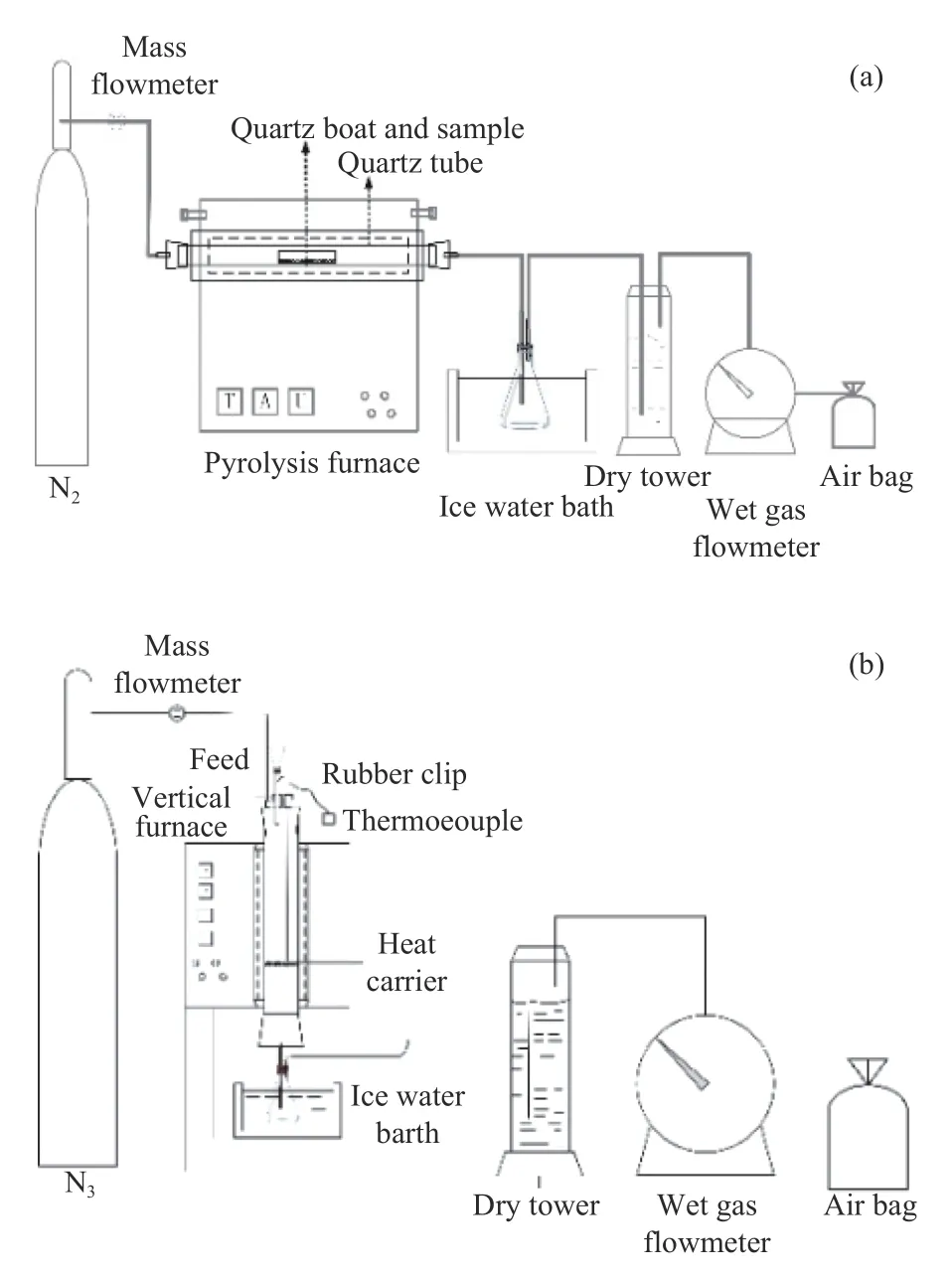
图2 (a)卧式管式炉和(b)立式管式炉示意图Figure 2 Schematic diagram of (a)horizontal tubular furnace and (b)vertical tubular furnace
实验前,需通入高纯氮气置换装置内空气。使用立式炉时,预先将适量固体热载体(刚玉)平铺于管内石英网,待炉温升至设定终温后将预先称量好的煤样与刚玉的混合物迅速倒入反应器内以达到快速升温的目的。实验条件如下:热解终温为400−800℃,终温间隔100℃,气体流量为100 mL/min,卧式炉升温速率为5℃/min,立式炉升温速率约为517℃/min。慢速热解终温停留时间为60 min,快速热解终温停留时间分别为10、30和60 min。
1.4 逐级化学提取
研究认为[18],盐酸能溶解煤中的碳酸盐、硫酸盐、磷酸盐和氧化物等矿物质;氢氟酸能溶解煤中铝硅酸盐类矿物质;上述两种溶剂无法溶解煤中的二硫化物(黄铁矿),而一定浓度的硝酸能溶解煤中的二硫化物;双氧水能分解煤中的有机质。因此,可利用上述特点,分别使用盐酸、氢氟酸、硝酸和双氧水对原煤进行逐级化学提取,即可分别得到碳酸盐(包括单硫化物、硫酸盐、磷酸盐及氧化物)结合态Cd、铝硅酸盐结合态Cd、二硫化物结合态Cd和有机质结合态Cd,逐级化学提取详细步骤见表2。

表2 逐级化学提取步骤Table 2 Sequential chemical extraction procedure
1.5 镉含量测试
利用微波消解仪(CEM MARS 5)对原煤和实验后的固体样品进行消解,使用电感耦合等离子体质谱仪(ICP-MS,NexlON300X)测定消解液和液体样品中Cd的含量,NMH和GL中Cd含量见表1。为尽可能降低背景值,实验过程中所用试剂均为优级纯,水均为超纯水。
1.6 Cd释放率
为评价Cd在慢速和快速热解过程中的挥发能力,本文引入挥发率的概念,定义为:

式中,RB为Cd的挥发率,%;C0为原煤中Cd的含量;C为半焦中Cd的含量;Y为半焦产率。
1.7 FactSage热力学计算
FactSage7.3热力学平衡模拟计算软件依据吉布斯自由能最小原则,结合软件DataSearch下的FactPS和Ftoxide数据库,计算化学热力学平衡态下的元素的存在形式。本文采用FactSage对煤热解过程中Cd的迁移转化行为进行模拟。计算时,假设使用1000 g煤样,将元素分析、灰成分分析和Cd的质量作为输入值,气体值按实际热解时通入的氮气量210 g,压力为1.013×105Pa,温度输入值为“100、800、100”,代表100−800℃反应,每隔100℃计算一次,煤中元素计算输入具体值见表3。

表3 计算时输入的参数Table 3 Parameters for calculation
2 结果与讨论
2.1 Cd赋存形态分布
成煤阶段由于受初始环境和地质活动的共同影响,导致不同地域和煤种中元素的赋存形态存在着较大差异[19,20]。研究表明,Cd主要与闪锌矿有关,在某些文献中也与硫铁矿或黏土矿有关[21−23]。图3比较了两种原煤中矿物质提取率和Cd提取率。NMH中32%的Cd、37%的矿物质能同时被HCl溶出,溶出的Cd称为碳酸盐结合态Cd;10%的Cd、60%的矿物能同时被HF溶出,溶出的Cd称为铝硅酸盐结合态Cd;12%的Cd、2.8%的矿物质能同时被HNO3溶出,溶出的Cd称为二硫化物结合态Cd。NMH经上述试剂提取后,残余物中矿物质含量仅为0.2%,残余物几乎全部为有机质。因此,NMH中Cd的赋存形态从主到次依次为有机质结合态(46%)> 碳酸盐结合态(32%)> 二硫化物结合态(12%)> 铝硅酸盐结合态(10%)。GL中24%的Cd、43%的矿物质能同时被HCl溶出,溶出的Cd称为碳酸盐结合态Cd;38%的Cd、53%的矿物质能同时被HF溶出,溶出的Cd称为铝硅酸盐结合态Cd;1%的Cd、3.7%的矿物质能同时被HNO3溶出,溶出的Cd称为二硫化物结合态Cd。GL经上述试剂提取后,残余物中矿物质含量仅为0.3%,残余物几乎全部为有机质。因此,GL中Cd的赋存形态从主到次依次为铝硅酸盐结合态(38%)> 有机质结合态(37%)>碳酸盐结合态(24%)> 二硫化物结合态(1%)。其他学者研究表明[22,24],烟煤等高阶煤中Cd主要以铝硅酸盐形式存在,高硫含量煤中Cd主要以硫化物形式存在,有机质结合态Cd含量较低。由此可见,两种低阶煤中有机质结合态Cd含量明显高于高阶煤。

图3 NMH和GL中矿物(a)和Cd(b)提取率Figure 3 Extraction rate of minerals(a)and Cd (b)in NMH and GL coal
2.2 原煤热重分析
图4 是NMH和GL的热解特性曲线。RT-300℃为第一阶段,低阶煤会发生轻微的热解,煤中吸附的水分和少量的CH4、CO2等气体在此阶段脱除。300−500℃为第二阶段(也称一次热解),此温度段以煤的分解、解聚为主,是煤的主要失重阶段;煤中侧链烷基和官能团发生剧烈分解,生成大量的相对分子质量较小的气体组分和焦油蒸气;NMH的失重率约为24%,约为GL失重率的两倍;由图4(b)可知,两种煤的最大失重峰约在440℃,对应图4(a)中440℃附近曲线急剧下降;在此阶段煤中与有机质伴生的Cd会随着有机质的裂解而挥发。500−900℃为第三阶段(也称二次热解),煤中大分子结构发生缩聚反应,产生少量的H2和CH4,两种煤的失重率分别为23%和17%。煤中矿物质(黄铁矿、碳酸盐和铝硅酸盐等)会在此温度段分解,与之伴生的Cd会随着矿物质的分解与转化而以不同形态挥发。整个热解过程中NMH和GL失重率分别为60%和40%,且NMH失重率一直大于GL主要是因为NMH中挥发分高于GL,灰分低于GL。

图4 NMH和GL原煤TG(a)和DTG(b)曲线Figure 4 TG (a)and DTG (b)analyses of NMH and GL coal
2.3 热解温度对Cd挥发性的影响
NMH和GL中Cd在卧式炉400−800℃热解过程中的挥发行为见图5(a)。热解温度对Cd的挥发性为影响显著,分别从400℃时37.2%与27.2%的挥发率到800℃时79.9%与85.7%的挥发率。除760−800℃之外,Cd在NMH中的释放率高于GL,是由于NMH中Cd主要以有机结合态和碳酸盐结合态为主,而GL中有较多的Cd与铝硅酸盐伴生。热重分析和文献[25]表明,煤中有机质会在低温度分解,硫化物(主要是黄铁矿)会在中温阶段分解(约500℃),与之伴生的Cd会随着这部分物质的分解而挥发。文献[3,16]表明,煤中铝硅酸盐矿物在700℃之后开始分解,在760℃之后GL中Cd释放率高于NMH是由于铝硅酸盐结合态Cd随这部分铝硅酸盐分解而释放。图5(b)比较了NMH和GL煤中Cd的释放速率。

图5 NMH和GL中Cd的挥发率(a)和反应速率(b)Figure 5 Volatility (a)and reaction rate(b)of Cd in NMH and GL coal
在400−650℃,GL中Cd的释放速率低于NMH,650−800℃时,与之相反。在650℃之前,NMH中Cd的释放速率始终高于GL,这是因为该阶段煤中低分子有机化合物受热分解,由逐级化学提取结果可知,NMH中有机结合态Cd含量高于GL,而且热重分析表明该阶段NMH的分解速率较GL更快,导致了此温度段NMH中Cd的释放速率更高。650−800℃时,以矿物结合态存在的Cd开始随着相关矿物逐渐分解而析出。该阶段GL中Cd的释放速率迅速增加,由相关文献[26]可知,煤中碱金属或碱土金属会与矿物成分一起形成低温共熔物,进而促进以相关矿物结合态赋存的Cd的释放,结合逐级化学提取结果发现GL中硅铝酸盐结合态Cd含量明显高于NMH,因此,可以推断700−800℃时GL中Cd的释放速率较高的原因很可能是煤中的含Na、Ca等元素的矿物与硅铝酸盐矿物形成的低温共熔物分解促进了Cd的释放。Wei等[12]对两种烟煤中Cd的挥发行为和赋存形态研究表明,在400−800℃,其挥发率为18%−35%,Cd主要以铝硅酸盐结合态为主;Guo等[24]研究表明,烟煤中Cd在400−800℃的挥发率为5%−30%,Cd主要赋存于铝硅酸盐矿物中。对比发现,在400−800℃,低阶煤中Cd挥发率明显高于高阶煤且其易于在低温阶段释放,这是由于低阶煤具有较多的有机质结合态和较少的无机矿物质结合态Cd。
2.4 升温速率对镉挥发性的影响
除温度外,升温速率对煤热解过程也会产生影响[27]。为进一步探究不同升温速率对Cd释放行为的影响,实验以NMH为研究对象,利用卧式炉和立式炉在400−800℃、60 min恒温时间条件下分别对其进行慢速和快速热解,Cd在两种煤中的挥发率见图6。NMH分别经慢速热解和快速热解后Cd的释放规律基本相同。同一温度下,慢速热解相较于快速热解Cd的释放率高约4%,是因为慢速热解时间较长,传质和传热较充分,有利于Cd的释放[28]。由曲线走势可知,热解温度范围内Cd在慢速和快速热解过程中的释放速率基本一致,这表明热解升温速率对Cd的释放速率几乎无影响。

图6 快慢速热解时NMH中Cd的释放率Figure 6 Volatility in Cd of NMH in mild and fast pyrolysis
2.5 停留时间对快速热解中Cd挥发性的影响
为了进一步探究不同停留时间对热解过程中Cd释放行为的影响,实验以NMH为研究对象,对其快速热解,实验结果见图7。停留时间从10 min延长至60 min,Cd在400−800℃释放率变化规律基本一致,增幅在1.2%−8.0%,延长停留时间利于Cd的挥发,这与其他相关研究结果一致[29]。由图5(b)可知,在600℃时30和60 min停留时间下Cd挥发速率开始增大,而750℃时,10 min停留时间下Cd的挥发速率开始增大,由于停留时间缩短造成Cd挥发存在“滞后现象”,表明过短的停留时间会造成元素释放不充分现象。
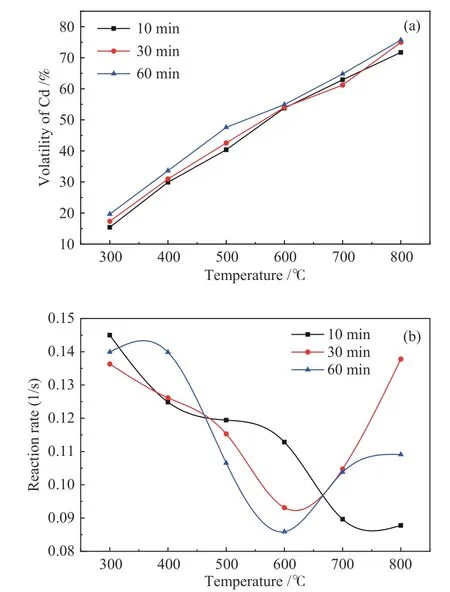
图7 快速热解Cd在不同停留时间时的释放率(a)和反应速率(b)Figure 7 Volatility (a)and reaction rate(b)of Cd with holding time of 10,30 and 60 min during fast pyrolysis
2.6 FactSage模拟计算
煤热解过程涉及的反应较复杂,为进一步研究煤热解过程中Cd在不同温度下的形态转化,本研究采用FactSage软件在理想条件下对NMH和GL中Cd的迁移转化规律进行模拟,模拟条件为100−800℃,模拟结果见图8。NMH和GL中Cd的气态产物主要有Cd、CdO、Cd(OH)x和CdS,分别见图8(a)、8(b)、8(c)和8(d)。由图8(a)可以看出,在300℃之后,气态Cd-NMH挥发量大于Cd-GL,挥发温度低于Cd-GL,是由于NMH挥发分和有机质结合态Cd均高于GL,导致其在低温阶段开始挥发,且挥发量较高。由图8(b)可以看出,在500℃之后,CdO-GL挥发量大于CdO-NMH,结合Cd在两种煤中赋存形态的分布状态可知,碳酸盐结合态Cd-GL含量低于Cd-NMH,导致NMH中较多的Cd残留在半焦中。由图8(c)可以看出,Cd(OH)x-GL挥发量大于Cd(OH)x-NMH,这可能是因为GL中铝硅酸盐结合态Cd较多,铝硅酸盐类矿物受热失水,与气态Cd反应生成Cd的氢氧化物,以此形态挥发;且最高峰对应温度高于NMH是由于NMH挥发分较高,具有较高的反应活性。由图8(d)可以看出,在400℃之后,CdS-GL挥发量大于CdS-NMH,主要是由于GL中具有较多的硫和黄铁矿,在热解时气态S与气态Cd反应生成Cd的硫化物,以此形态挥发。FactSage热力学模拟计算表明Cd的释放行为与热解温度、赋存形态分布以及煤阶密切相关,模拟与实验结果吻合较好。
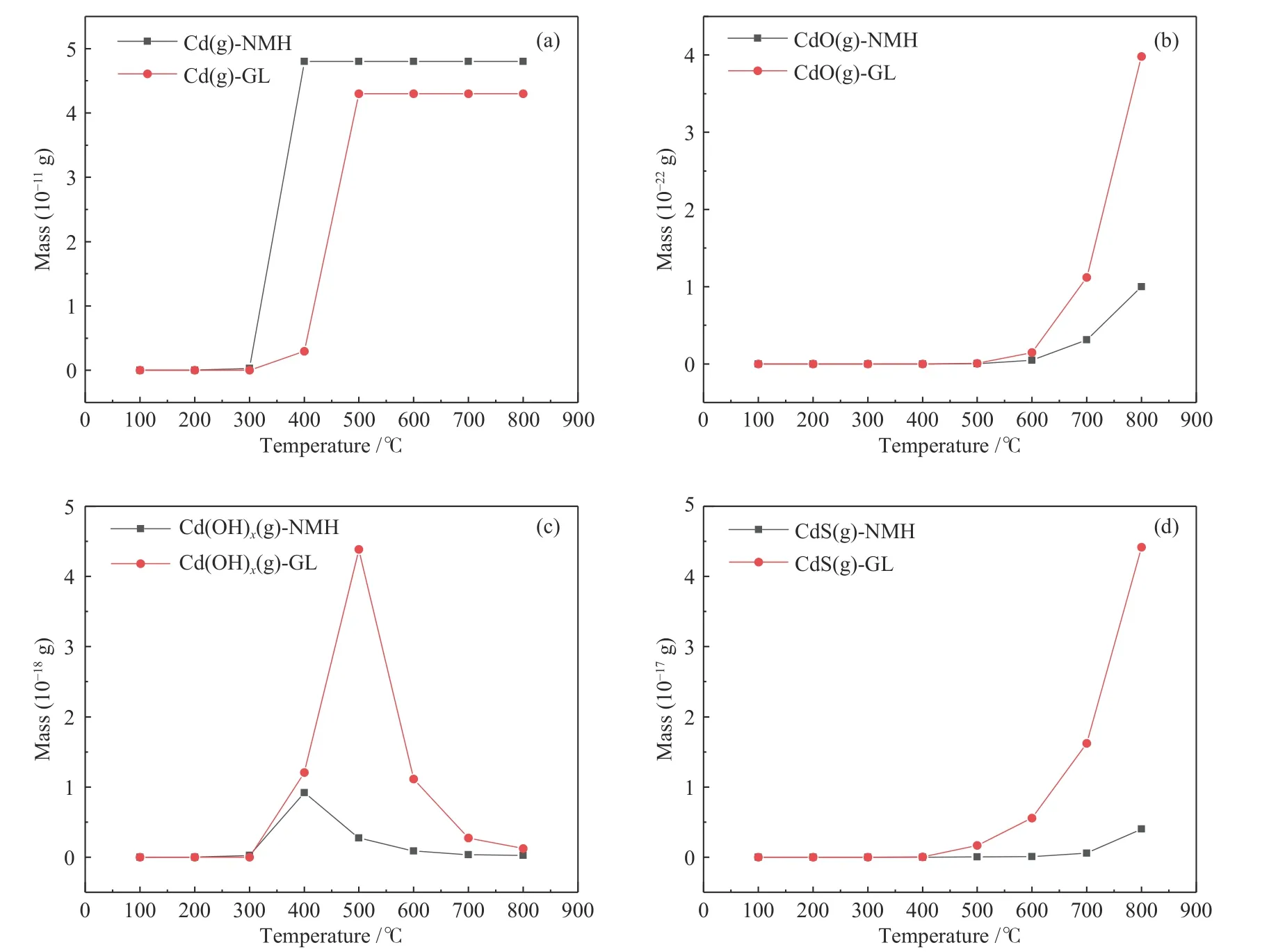
图8 FactSage热力学模拟计算Figure 8 FactSage thermochemical calculation
3 结论
两种低阶煤中矿物质分布类似,主要是铝硅酸盐类矿物和碳酸盐类矿物。Cd在NMH中的赋存形态分布依次是有机质结合态(46%)、碳酸盐结合态(32%)、二硫化物结合态(12%)、铝硅酸盐结合态(10%),而其在GL中的赋存形态分布依次为铝硅酸盐结合态(38%)、有机质结合态(37%)、碳酸盐结合态(24%)、二硫化物结合态(1%)。
慢速热解时,Cd在NMH和GL的挥发率分别为37.2%−79.9%和27.2%−85.7%,明显高于高阶煤中Cd的挥发率。Cd的赋存形态分布严重影响其挥发行为。有机质结合态Cd易在低温区挥发,导致在760℃之前,Cd在NMH中的释放率高于GL。碳酸盐、铝硅酸盐和硫化物结合态需在中高温区挥发。导致在760−800℃时GL中Cd的挥发率大于NMH。降低热解速率与延长停留时间都可以促进NMH中Cd的挥发,Cd在慢速热解时的挥发率比其在快速热解时的挥发率高约4%,在停留时间10−60 min时Cd的释放率增幅在1.2%−8.0%。
FactSage热力学计算表明模拟与实验结果吻合较好。NMH和GL中Cd的气态产物主要有Cd、CdO、Cd(OH)x和CdS,Cd在两种煤中挥发行为的差异主要由热解温度、赋存形态分布以及煤阶决定。
