Graves 甲亢131I 治疗后甲状腺功能的变化特点及其与治疗前抗体水平的关系
2021-05-27陈美言李雪娜李亚明
陈美言 李雪娜 李亚明
中国医科大学附属第一医院核医学科,沈阳 110000
131I 治疗在欧美发达国家已成为成人Graves 甲状腺功能亢进症(简称甲亢)的首选治疗方法[1],我国131I 治疗Graves 甲亢的临床应用频度明显低于国外[2],这与其治疗后可引起甲状腺功能减退症(简称甲减)密切相关。有研究结果表明,131I 治疗剂量与甲减的初期发生密切相关[3]。国内外报道的131I治疗Graves 甲亢患者甲减发生率的差异较大[4-6],131I 治疗后甲减的高发是临床及科研中不可忽视的问题。影响甲减发生的因素较多,国内外报道多不一致[7],这给临床医师的诊治及预后判断带来了困难。为了及早发现甲减并及时采取有效的治疗措施,早期的密切随访尤为重要。本研究分析131I 治疗 Graves 甲亢后1、3、6 个月甲状腺功能(简称甲功)的变化特点及治疗前抗体水平与临床疗效的关系,旨在帮助临床医师密切监测病情变化,及早发现甲减,为预后的判断提供依据。
1 资料与方法
1.1 一般资料
前瞻性分析2016 年3 月至5 月于中国医科大学附属第一医院核医学科首次行131I 治疗的80 例Graves 甲亢患者的临床资料,其中男性20 例、女性60 例,年龄19~70(40.5±12.8)岁。纳入标准:①年龄≥18 岁且根据《131I 治疗格雷夫斯甲亢指南(2013版)》[5]诊断为Graves 甲亢;②确诊Graves 甲亢后首次行131I 治疗;③131I 治疗剂量均按相同的方法确定;④患者治疗前有完善的血清学检查结果[游离三碘甲状腺原氨酸(free triiodothyronine,FT3)、游离甲状腺素(free thyroxine,FT4)、TSH、抗甲状腺球蛋白抗体(anti thyroglobulin antibodies,TgAb)、甲状腺过氧化物酶抗体(thyroid peroxidase antibody,TPOAb)、促甲状腺素受体抗体(thyrotrophin receptor antibody,TRAb)]及完整的相关临床检查;⑤允许随访,患者治疗后1、3、6 个月复查。排除标准:有甲状腺手术史或超声诊断甲状腺结节的患者。所有患者均在检查前签署了知情同意书。本研究获得中国医科大学附属第一医院医学科学研究伦理委员会的批准(批准号:科伦审[2020]387 号)。
1.2 研究方法
1.2.1 随访
电话嘱患者治疗后1、3、6 个月复查。随访时间6 个月,随访的内容包括患者的症状、体征和甲功复查情况。终止随访的标准:131I 治疗后1 个月内因不能耐受而口服抗甲状腺药物者。
1.2.2 分组标准
根据甲功变化情况,将治疗后1 个月和3 个月的患者分为4 组。①甲功升高组:血清FT3和FT4无明显降低甚至高于治疗前;②甲功好转组:血清FT3、FT4水平明显降低,但仍高于正常水平;③甲功正常组:血清FT3、FT4水平恢复正常;④甲减组:血清FT3、FT4水平低于正常。
根据《131I 治疗格雷夫斯甲亢指南(2013 版)》[5]将治疗后6 个月的患者分为4 组:①完全缓解组:患者甲亢症状和体征完全消失,血清FT3、FT4水平恢复正常;②部分缓解组:甲亢症状减轻,体征部分消失,血清FT3、FT4水平明显降低,但未降至正常水平;③无效组:患者的甲亢症状和体征均无改善或反而加重,血清FT3、FT4水平无明显降低;④甲减组:出现甲减症状和体征,血清FT3、FT4水平低于正常,TSH 水平高于正常。非甲减组包括完全缓解组、部分缓解组和无效组。治愈组包括完全缓解组和甲减组,非治愈组包括无效组、部分缓解组和再次治疗的患者。本研究将FT3和FT4水平降低幅度大于治疗前的10%定义为明显降低。
1.3 检测方法
血清甲功检验使用美国雅培公司i2000SR 化学免疫发光检测仪及相关专用试剂。甲状腺静态扫描仪使用德国 Siemens 公司生产的Symbia T2 SPECT/CT 仪,配低能高分辨平行孔准直器,矩阵256×256,采集计数400 K。显像剂为高锝99m酸钠(Na99TcmO4,放射化学纯度≥95%),由北京原子高科股份有限公司提供。碘化钠口服溶液由中核高通同位素股份有限公司(国药准字H10983121)和原子高科股份有限公司(国药准字H10960249)提供。甲功测定使用MN-6110 甲功仪(安徽中科中佳科学仪器有限公司)。
1.4 131I 治疗方法
131I 治疗前低碘饮食、停用抗甲状腺药物1~2周。完善常规体格检查及实验室检查,测定甲状腺2、4、24 h 的131I 摄取率,具体方法:患者空腹口服131I 溶液74~370 kBq 后继续禁食1~2 h,在服药后2、4、24 h 分别测量甲状腺部位的放射性计数,每次60 s。测量前先测定室内本底的计数及标准源计数,测量时间均为60 s。行甲状腺SPECT/CT显像评估甲状腺重量[甲状腺重量(g)=正面投影面积(cm2)×左右叶平均高度(cm)×k,k 为常数,介于0.23~0.32]。嘱患者相关注意事项;确定131I 治疗剂量,服药前至少空腹2 h,采用一次性口服给药,服药至少2 h 后方可进食。
1.5 统计学方法
采用SPSS19.0 软件对数据进行统计学分析。治疗前甲状腺抗体水平采用M(P25,P75)表示。采用卡方检验分析治疗后1 个月的4 组在3 个月后甲减发生率的差异,采用Kappa 检验分析治疗后3 个月甲功变化和治疗后6 个月疗效评价的一致性(Kappa值≥0.75 为两者一致性非常好,0.6≤Kappa值<0.75 为两者一致性较好,0.5≤Kappa值<0.6 为两者一致性中等,Kappa值<0.5 为两者一致性较差)。采用Wilcoxon 秩和检验分析治疗前抗体水平与疗效的关系。P<0.05 为差异有统计学意义。
2 结果
2.1 临床疗效
80 例甲亢患者的131I 治疗剂量为74.0~388.5(180.6±78.0) MBq。131I 治疗6 个月后,80 例患者中,15 例(18.75%)为完全缓解,13 例(16.25%)为部分缓解,24 例(30.00%)为发生甲减,2 例(2.50%)为无效,其余26 例(32.50%)在首次131I 治疗后3~5 个月行再次治疗。
2.2 131I 治疗后1 个月和3 个月的甲功变化
所有患者均无失访。治疗后1 个月的4 组患者例数分别为甲功升高组20 例(25.00%)、甲功好转组51 例(63.75%)、甲功正常组7 例(8.75%)、甲减组2 例(2.50%)。由于甲功正常组和甲减组例数较少,故合并为正常及甲减组。为突出说明1 个月后甲功的变化情况与3 个月后发生甲减的关系,又将治疗后3 个月的患者分为非甲减组56 例(70.00%)、甲减组24 例(30.00%)。
131I 治疗后1 个月与3 个月甲功变化的关系见表1。治疗后1 个月的各组在3 个月后的结果显示,甲功升高组[15.00%(3/20)]与正常及甲减组[88.90%(8/9)]甲减发生率的差异有统计学意义(χ2=14.39,P<0.01);甲功好转组[25.49%(13/51)]与正常及甲减组的甲减发生率的差异有统计学意义(χ2=13.52,P=0.001);甲功升高组与甲功好转组的甲减发生率的差异无统计学意义(χ2=0.91,P=0.529)。
2.3 131I 治疗后3 个月和6 个月甲功变化的一致性分析
因治疗后3~5 个月有26 例患者行二次治疗,故在此处剔除,不予讨论。治疗后3 个月的3 组患者在治疗6 个月后,甲减组发生甲减21 例(91.30%,21/23)、非甲减2 例(8.70%,2/23)(治疗后3 个月甲减组24 例患者中,其中1 例行二次治疗,此处不予讨论);非甲减组发生甲减3 例(9.70%,3/31)、非甲减28 例(90.32%,28/31)。甲功正常组完全缓解10 例(76.92%,10/13)、非完全缓解3 例(23.08%,3/13);非甲功正常组完全缓解5 例(12.20%,5/41)、非完全缓解36 例(87.80%,36/41)。甲功好转组部分缓解9 例(60.00%,9/15)、非部分缓解6 例(40.00%,6/15);非甲功好转组部分缓解4 例(10.26%,4/39)、非部分缓解35 例(89.70%,35/39)。
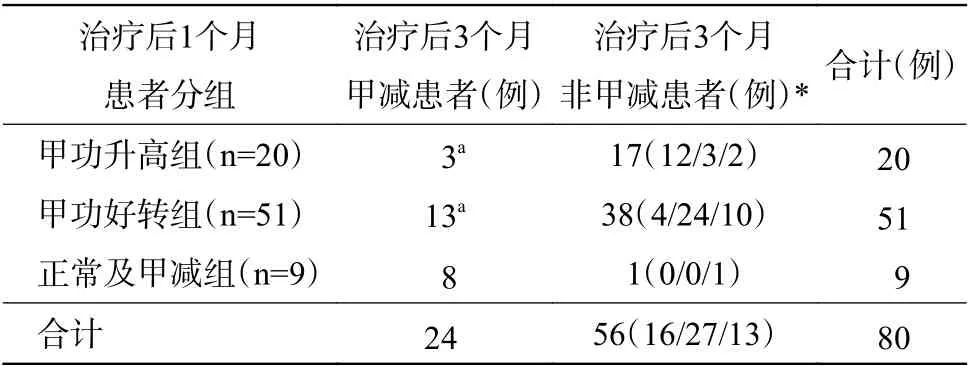
表 1 80 例Graves 甲亢患者131I 治疗后1 个月各组在3 个月后甲状腺功能的变化关系Table 1 Relationship of the thyroid function change between 1st and 3rd month after 131I treatment of 80 Graves hyperthyroidism patients
治疗后3 个月甲减和6 个月甲减的一致性非常好(Κappa值=0.812,P<0.01);治疗后3 个月甲功正常和6 个月完全缓解的一致性较好(Κappa值=0.615,P<0.01);治疗后3 个月甲功好转和6 个月部分缓解的一致性中等(Κappa值=0.519,P<0.01)。
2.4 131I 治疗前甲状腺抗体水平与疗效的关系
2.4.1 TgAb、TPOAb 水平与甲减的关系
治疗后6 个月甲减组和非甲减组间治疗前的TgAb[51.53(9.05,781.19)U/mL 对14.30(3.33,45.14) U/mL]和TPOAb[577.50(197.89,1000) U/mL对397.71(98.41,955.68)U/mL]的差异均无统计学意义(u=249.00、306.50,P=0.053、0.346)。
2.4.2 TRAb 水平与治愈的关系
治疗后6 个月治愈组和非治愈组间治疗前TRAb 水平[11.43(4.34,32.42) IU/L 对19.82(7.95,39.14) IU/L]的差异有统计学意义(u=557.50,P=0.02),且非治愈组的秩均值大于治愈组的秩均值(46.40 对34.29)。
3 讨论
131I 是欧美发达国家治疗成人甲亢首选的方法[1,8],但治疗后甲减的高发是不可忽视的问题[9-10]。有研究指出,131I 治疗的最终目标是使患者发生甲减,进而改善甲亢的状态[11]。我国甲减的发生率相对较低,这可能与我国治疗剂量较保守且根据患者病情积极调整剂量有关。本研究结果显示,80 例甲亢患者131I 治疗后1、3、6 个月甲减的发生率分别为2.50%、30.00%和30.00%。研究结果表明,部分早发甲减如不及时给予甲状腺激素替代治疗,可能会导致甲减症状加重,甚至发展成永久性甲减[12]。本研究结果显示,治疗后1 个月甲功正常及甲减患者在3 个月后甲减的发生率高达88.89%,明显高于甲功升高(15.00%)和甲功好转患者(25.49%)在3 个月后甲减的发生率,因此要缩短随访时间,以便及早发现甲减,及时给予替代治疗。131I 治疗后早期密切的随访尤为重要,临床医师可根据症状及时给予替代治疗。
本研究结果显示,131I 治疗后3 个月甲减和6 个月甲减的一致性非常好。早期鉴别一过性甲减和永久性甲减比较困难,且在本研究中,治疗后3 个月发生甲减的患者中15 例(62.50%)有临床症状,故在甲减初期,医师应根据患者的症状和体征积极给予替代治疗,如不及时给予替代治疗可能会导致甲减症状加重。由于本研究中在治疗后3 个月甲功升高组的患者中有13 例(81.25%)接受二次治疗,故无法对3 个月甲功升高和6 个月无效的患者进行统计学分析。本研究结果显示,通过131I 治疗后3 个月甲功变化的趋势可评估和预测6 个月后的临床转归。对于治疗后3 个月发生甲减的患者,可根据临床症状和体征适当给予替代治疗,并密切随访病情变化;治疗后3 个月甲功正常的患者在6 个月后临床痊愈的可能性较大;治疗后3 个月甲功好转的患者在6 个月后的转归变化相对较大,还需要进一步的监测和密切随访。
无论甲减发生的初期还是晚期,多数报道均认为与TgAb 和TPOAb 水平相关[13],而TRAb 水平则与疗效和复发相关[14]。本研究结果显示,治疗前TgAb 和TPOAb 水平的高低与治疗后甲减的发生无相关性,造成该差异的原因可能是甲减的发生与多方面因素相关,如甲状腺重量、131I 治疗剂量等。本研究结果显示,治疗前TRAb 水平的高低与甲亢的治愈有相关性,且未治愈组TRAb 水平的秩均值大于治愈组。有研究者认为,对于TPOAb、TgAb 水平超过标准值的患者可适当减少131I 治疗剂量,从而降低甲减的发生率[15]。在临床工作中,刻意降低甲减的发生率可能导致治愈率的下降,即无效、复发或需要二次治疗的比例会增加,因此,我们认为,131I 治疗Graves 甲亢的重点不应是降低甲减的发生率,而应是尽量提高治愈率,在治疗后密切监测甲功变化,及时给予二次治疗或替代治疗才能真正达到治愈的目的。但该方案在国内实施的难度相对较大,这就有赖于临床医师与患者进行充分细致的沟通,告知患者甲减发生后的注意事项,并签署知情同意书。对于TRAb 水平升高的患者,甲亢无法治愈的可能性较大,在临床工作中是否应该对TRAb 水平升高的患者适当增加131I 治疗的剂量仍需进一步研究。
本研究存在的局限性:131I 治疗剂量的计算受不同临床医师的经验和主观性影响较大,导致结果存在偏倚,有待进一步标准化治疗剂量;样本量相对较少,随访时间较短,无法行多因素分析甲减发生的相关因素,有待之后扩大样本量并长期密切随访观察。
利益冲突本研究由署名作者按以下贡献声明独立开展,不涉及任何利益冲突。
作者贡献声明陈美言负责研究过程的实施、数据的获得与分析、论文的撰写;李雪娜负责命题的完善、数据的分析、论文的修改;李亚明负责命题的提出及论文的审阅。
