索尔维纯碱氯化钙废液中氯化钠回收及高强石膏的合成
2021-04-30张晓娟段东平李志宝
蔡 超,张晓娟,段东平,李志宝
(1.中国科学院过程工程研究所绿色过程与工程重点试验室,北京 100190;2.中国科学院大学化学工程学院,北京 100049)
1 纯碱生产废液的处理方法
碳酸钠(俗名纯碱)[1,2],是一个重要的基础化工原料,在各个工业部门都有广泛的应用。据统计我国是纯碱生产的主要国家,年产能已达3 000万t[3]。纯碱的生产工艺选择取决于原料的获得,我国主要以海盐氯化钠和矿盐氯化钠为原料,还有以天然碱矿为主要原料。如果以氯化钠为原料制备纯碱,生产工艺有两种方法:索尔维方法[2]和侯德榜制碱方法。后者工艺需要配套合成氨厂,并副产氯化铵肥料。索尔维方法制纯碱一直是我国的主要方法,产量达到上千万吨。索尔维纯碱工艺主要有如下几个工段:1)盐水除钙镁净化;2)碳酸氢钠结晶;3)氯化铵分解氨气蒸馏;4)粗碳酸氢钠煅烧等。简单的工艺流程如图1所示。

图1 索尔维法碳酸钠生产工艺流程
索尔维纯碱工艺虽然已经有上百年的工业生产历史了,但高能耗、高污染并排放大量废水和固体废渣的环保问题一直存在,像日本、韩国等发达国家都已经不再利用此工艺生产纯碱,而是从美国或中国进口。随着我国环保要求的不断提高,纯碱企业面临着巨大的环境压力,只有解决纯碱企业的废水废渣外排问题,或者开发新的工艺取而代之。如果将废水废渣实现有价值的综合利用,不仅可以提升纯碱工业的绿色化,还会给企业带来可观的经济效益,这是一条优先发展可持续的道路。利用索尔维工艺每生产1 t纯碱,需要外排10 m3的废液。例如某年产150万t纯碱的厂家,产生的废液达1 500万m3。纯碱废液中含有7.8%的氯化钙和2.7%的氯化钠,其余为水分,如果采用多效蒸发的方法回收废液中的钠盐和钙盐,需要消耗大量能源[2]。为此,有的公司为了节约能源消耗,利用当地沿海土地建立盐田,利用太阳能浓缩氯化钙废液,达到一定饱和度后把卤水储存起来,再通过多效蒸发,由于共离子效应氯化钠结晶析出,过滤得到的盐送往盐水净化工段,氯化钙溶液继续高温蒸发,达到一定浓度后冷却直接得到二水氯化钙产品。此工艺能耗高操作时间长,设备的腐蚀也增加了操作成本,而产品氯化钙的用途十分有限,全球仅有500万t的销量,且价格低廉,中国仅一个纯碱厂就可以产生大量的氯化钙,可以看出这条工艺路线没有前途。只有在回收氯化钠的同时,将氯化钙转化为高附加值的钙产品,且用途广泛才是有前景的发展方向。
2 新工艺和理论基础
根据上面的描述,我们提出了一个新工艺,即利用硫酸钠沉淀二水硫酸钙分离纯碱废液中氯化钙,过滤得到二水硫酸钙结晶和氯化钠溶液,二水硫酸钙将通过高浓电解质介质在低温下转相为高强石膏,即阿尔法型半水硫酸钙,氯化钠盐卤将送往盐水净化工段作为纯碱原料,新工艺的流程图见图2,主要化学反应方程如下:

(1)

(2)
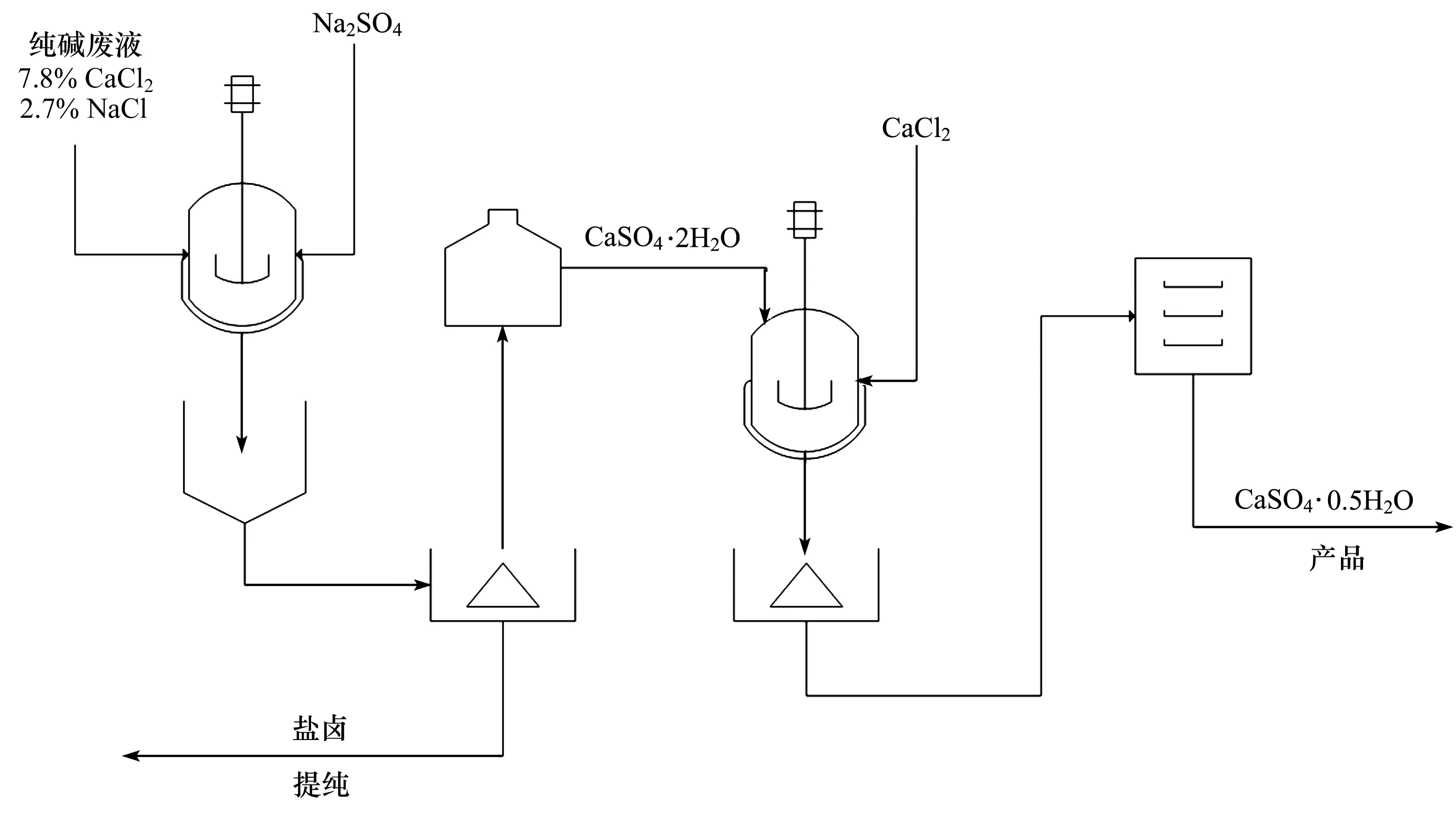
图2 纯碱氯化钙与硫酸钠反应制备高强石膏工艺流程
通过反应得到的二水硫酸钙固体,将加入到浓氯化钙溶液中并加入少量转相助剂,反应温度控制在80~100 ℃,反应3~5 h后,二水硫酸钙将转相为阿尔法型半水硫酸钙,过滤干燥可得高强石膏。高强石膏在市场上有广阔的前景,每吨售价1 500元不等,由于高强石膏主要用于建筑材料,巨大的需求量足可以消耗纯碱工艺废液中的氯化钙。
硫酸钙有三种形式的晶体:二水硫酸钙(DH), 半水硫酸钙(HH) 和无水硫酸(AH)。这三种硫酸钙在溶液中反生解离为离子可以用下面的方程表示[4,5]:
(3)
(4)
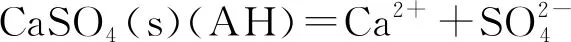
(5)
上述三个方程的溶度积常数分别表达为:
(6)
(7)
(8)
三个固相之间可以建立平衡关系,如二水硫酸钙-无水硫酸钙之间(DH-AH),和二水硫酸钙-半水硫酸钙之间(DH-HH),平衡方程如下:
CaSO4·2H2O(s)(DH)=CaSO4(s)(AH)+2H2O
(9)
CaSO4·2H2O(s)(DH)=CaSO4·0.5H2O(s)(HH)+1.5H2O
(10)
两个固相的转相平衡常数可以用每个相的溶度积常数表达:
(11)
(12)
方程(11)和(12)表明了,二水硫酸钙转相为半水硫酸钙和无水硫酸钙,仅取决于溶液中水的活度,也就是溶液中电解质浓度和溶液温度。因此,从二水硫酸钙制备半水硫酸钙可以在电解质溶液中转相得以实现,如果只用水作为介质,则需要很高的温度和压力,设备投资和操作费用大幅提高,这也是半水硫酸钙价格高的原因,由于使用加压反应装置或使用加压蒸汽,很难大规模生产。
3 试 验
3.1 材料与试剂
本研究试验所用试剂包括CaCl2(AR.96%)、NaCl(AR.99%)、MgCl2·6H2O (AR.98%)、 KCl(AR.99%)、 AlCl3·6H2O(AR.96%)、CaSO4·2H2O(AR.99%)、和无水乙醇(AR.99%)等,提供方均为国药集团化学试剂有限公司;Na2SO4·10H2O(AR.99%)和Na2SO4(AR.99%) 来自上海阿拉丁生化科技股份有限公司;纯碱氯化钙废液则由河北省某纯碱生产企业提供;去离子水试验室自行制作,所用试剂使用时没有进一步处理。
3.2 试验设备与分析仪器
本试验所使用的仪器包括:玻璃结晶反应釜(自行加工),磁力搅拌器(84-1A),由天津市华兴科学仪器厂提供;智能节能恒温槽(DC-3006),来自宁波新芝生物科技股份有限公司;电热恒温鼓风干燥箱(DHG-9053A),来自上海精宏试验设备有限公司;蠕动泵(BT100-1J),由保定兰格恒流泵有限公司提供;双层杯;分析天平等。利用XRD表征物相,利用SEM表征形貌。
3.3 试验方法
废液氯化钙和硫酸钠反应结晶在一个带有搅拌的反应器中进行,结晶反应器由恒温水浴控制温度在±0.1 K,搅拌速度在500 rpm,氯化钙和硫酸钠都用去离子水配置成一定的浓度,通过蠕动泵控制加料速度,就是控制过饱和度,以实现反应因素的考察,例如:温度,浓度,加料方式,老化时间等试验条件,确定最优的反应条件,制备晶型好的二水硫酸钙样品,作为转相制备阿尔法高强石膏的原料。
同样利用该装置进行二水硫酸钙在氯化钙溶液中的转相试验,不同的是不需要进料,试验步骤是,将一定浓度的氯化钙溶液加入到反应器中,升温到80~90 ℃后将一定量的二水硫酸钙放入反应釜中,在充分搅拌的情况下反应几个小时,中间可以相隔半个小时取样一次,洗涤干燥用来物相表征,以判断二水硫酸钙的转相进程。化学滴定方法测定钙离子的浓度。
4 结果与讨论
4.1 氯化钙和硫酸钠反应制备二水硫酸钙
首先考察温度对制备二水硫酸钙形貌的影响[6]。氯化钙和硫酸钠的进料浓度均为1 mol/L,反应的有效体积约为500 mL,考察温度分别为313 K,323 K和333 K三个温度,加料结束后静置老化时间为15 min。不同温度下得到的二水硫酸钙的电子扫描电镜(SEM)见图3。可以看出二水硫酸钙是片状形貌,三个温度下颗粒的大小随温度升高略有增长,平均粒径约43 μm,由于颗粒较大形状规整,已经具有良好的过滤性能,本工艺给工程放大带来了优势。

(a)40 ℃ (b)50 ℃ (c)60 ℃图3 温度对合成二水硫酸钙产品形貌的影响
从温度影响和操作实际出发,我们选择50 ℃为反应温度,进而考察停留时间对反应得到的二水硫酸钙在形貌,沉降速度和粒度分布的影响。反应停留时间分别为:15 min,27 min,43 min 和55 min。从图4的SEM图可以看出,随着停留时间延长,颗粒尺寸逐步增大从34 μm到87 μm,二水硫酸钙的形貌仍然为片状,但厚度逐步增加。在60 ℃温度下,如果将停留时间延长到95 min,则二水硫酸钙的颗粒尺寸可达158.2 μm。说明在较高温度下,延长停留时间二水硫酸钙会进一步重结晶,使颗粒逐步长大。

(a)15 min (b)27 min (c)43 min (d)55 min图4 不同停留时间制备二水硫酸钙产品SEM图
为了制备足够量的二水硫酸钙作为转相制备高强石膏,即α-半水硫酸钙的原料,本试验使用5 L的反应结晶器做了放大试验,在60 ℃反应温度下利用氯化钙和硫酸钠溶液加料反应得到二水硫酸钙。停留时间为60 min,得到的产品粒度达到112 μm。可以看出在一定进料浓度和停留时间下,温度决定了二水硫酸钙的颗粒尺寸。
4.2 半水硫酸钙的转相
由二水硫酸钙转相或重结晶合成α-半水硫酸钙,即高强石膏,研究人员几十年来做了很多工作[5],已经有成熟的工业生产装置,主要是处理烟煤发电脱硫石膏。烟煤锅炉排放的烟气需要脱硝脱硫,一般用石灰乳反应得到亚硫酸钙,然后氧化得到二水石膏,但脱硫石膏用途有限,也不能填埋或露天堆放。发达国家通常将脱硫石膏作为原料生产高强半水石膏作为建筑材料,只有这样才能处理如此大量的脱硫石膏。工业上使用高压水热法在一定助剂的条件下,二水石膏发生转相生成半水石膏,在水相中合成的半水石膏为阿尔法型,具有优良的建筑材料性能,已经在建筑业广泛使用,但我国对高强石膏的需求量更大,更有大量的脱硫石膏、磷石膏、钛白石膏等固体废弃物急需处理,因此将这些二水石膏转变为半水石膏是当务之急。但是由高压水热合成路线生产高强石膏,能量消耗和操作成本都很高。为此,科研人员提出了利用浓电解质溶液作为介质,来降低溶液中水的活度,在常压下实现二水硫酸钙到半水硫酸钙的转相,但反应温度在100 ℃以下。
本试验利用浓氯化钙溶液考察二水硫酸钙的转相行为,氯化钙的浓度为3~4 mol/kgH2O,转相温度是80 ℃,反应开始后间隔取样并做XRD分析,考察了反应时间和氯化钙浓度对最终产品的影响,见图5。从图中可以看到4 mol/L的氯化钙溶液需要20 h的反应时间,二水硫酸钙才能转变为半水硫酸钙,但在5 mol/L的氯化钙溶液中6 h就可以实现半水硫酸钙的完全转相。结果证明除温度外电解质溶液的浓度对转相起最关键的作用。

图5 氯化钙浓度和反应时间对转相产物影响
最后确定二水硫酸钙在氯化钙介质中转相操作条件为:温度85~105 ℃,氯化钙浓度为5 mol/L,反应时间2 h,反应结束后固体取样洗涤后做XRD和SEM检测,检测结果见图6, 图中显示最终产物都是晶体较大的棒状结晶,这种晶型可以得到高强的半水石膏,说明试验工艺和反应条件的可行性。
4.3 新工艺物料衡算和经济分析
一个年产150万t纯碱的工厂,产生的氯化钙废液1 500万m3[8,9],含有117万t氯化钙和41万t氯化钠。如果利用本论文提出的工艺将废液氯化钙制备成二水硫酸钙,然后转相为高强石膏,需要151万t硫酸钠,得到154万t的高强石膏,废液中氯化钠和硫酸钠反应生成的氯化钠共165万t,一起回用可生产纯碱150万t,完全实现了循环。实现了用硫酸钠作为原料而不改变索尔维工艺的目标。表1对整个工艺产品的价值增值做了计算,可以看出将产生巨大的经济效益。

(a)=85 ℃ (b)=90 ℃ (c)=95 ℃

(d)=95 ℃ (e)=95 ℃ (f)=105 ℃图6 转相产物高强石膏SEM图
5 结 论
本文着眼于纯碱废液中氯化钙的高质化利用和氯化钠的回收循环,提出的利用硫酸钠和废液中的氯化钙反应制备高强半水硫酸钙的新工艺是一个工业上可行的方案。不仅成功制备了合格的阿尔法型半水硫酸钙,即高强石膏,而且实现了废液中氯化钙的回收利用。温度是制备二水硫酸钙形貌的关键因素,足够的停留时间可以使得二水硫酸钙的形貌更加完整。利用高浓度氯化钙溶液成功将二水硫酸钙转相为半水硫酸钙,在这个反应过程中,电解质的浓度和温度是转相主要参数。对于现在生产纯碱的工厂而言,利用本文提出的纯碱废液制备半水石膏工艺,处理部分纯碱废液就可以产生很好的经济效益和环保效益。

表1 用纯碱废液和硫酸钠生产半水硫酸钙的效益分析
