人参黄连有效组分速崩片的质量标准研究
2021-04-16吕金朋李晶峰
高 旭,吕金朋,张 辉*,李晶峰*
(1.长春中医药大学吉林省人参科学研究院,长春 130117;2.吉林省东北亚生物科技有限公司,长春 130117)
中医学将糖尿病称为消渴,临床主要表现为多饮、多食、多尿、形体消瘦或尿有甜味。人参黄连有效组分速崩片由黄连总碱、人参总皂苷配伍,主要针对早期糖尿病肾病患者,其配伍充分显示了中医辨证施治与整体观念的思想[1]。为了更好地控制该药品的质量,本研究参照药典和相关文献资料,采用高效液相色谱法(HPLC)对人参黄连有效组分进行定性与定量检测。
1 材料与仪器
1.1 试药
人参黄连有效组分速崩片(批号:ZT191201、ZT191202、ZT191203), 黄 连 总 碱(20181101、20181104、20181107),人参总皂苷(20181102、20181108、20181115), 人 参 皂 苷Rg1(110703-201733)、Re(110703-201728)、Rb1(110704-201726)、Rd(111818-201603)、S-Rg3(18101302)、 盐 酸小檗碱(110713-201712,中国食品药品检定研究院,纯度>98%)、盐酸药根碱(110733-201609,中国食品药品检定研究院,纯度>98%),甲醇和乙腈为色谱纯,其余试剂均为分析纯。
1.2 仪器
Agilent 1260 高效液相色谱仪;SPECORD 200 plus 紫外检测器,德国耶拿分析仪器股份有限公司;PT104-55SY 十万分之一天平,福州华志科学仪器有限公司;BSA124S-CW 万分之一天平,赛多利斯科学仪器(北京)有限公司;液晶超声波清洗器,昆山洁力美超声仪器有限公司。
2 方法与结果
2.1 人参黄连有效组分速崩片人参皂苷的含量测定研究
2.1.1 测定依据 参照《中国药典》(2015 版)[2]人参含量测定项下选用的检测波长,色谱条件:以十八烷基硅烷键合硅胶为填充剂(色谱柱型号:Agilent Eclipse Plus-C18,4.6 mm×250 mm);柱温:30 ℃;以乙腈为流动相A,水为流动相B,按表1中洗脱表进行梯度洗脱;检测波长203 nm,流速为1.0 mL·mL-1。
2.1.2 对照品溶液的制备 按表2 所示分别精密称取人参皂苷 Rg1、Re、Rb1、Rd、S-Rg3 标准品,加入适量甲醇配成下表所示浓度的人参总皂苷混合标准品溶液。
2.1.3 供试品溶液的备 取人参黄连有效组分速崩片10 片,研磨,精密称取1 g,加甲醇30 mL 超声30 min,过滤,取续滤液,水浴蒸干,加30 mL 水使溶解,用水饱和正丁醇振摇提取3 次,每次30 mL,合并正丁醇液,用正丁醇饱和的水洗涤3 次,每次30 mL,弃去水洗液,正丁醇液蒸干,残渣加甲醇10 mL 使溶解,大孔吸附树脂上样,待样品液面与大孔树脂相水平后,加入70%乙醇100 mL洗脱,续滤液蒸干,30 mL 甲醇溶解,作为供试品溶液。

表1 流动相洗脱表
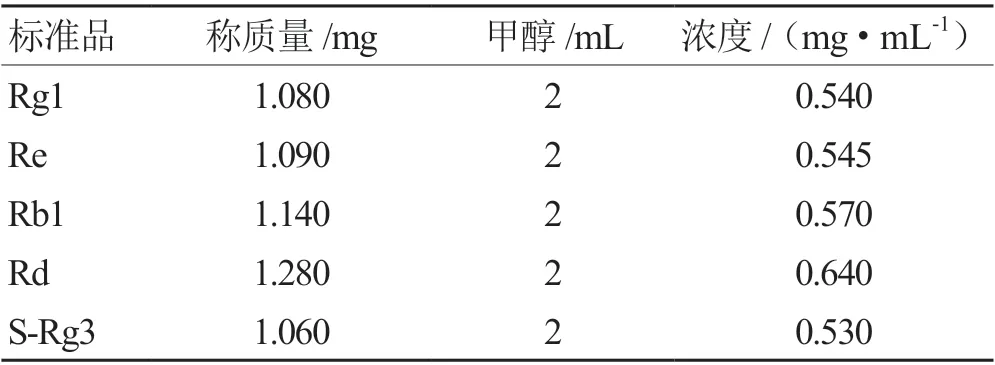
表2 人参皂苷混合标品统计表
2.1.4 方法学考察2.1.4.1 线性关系考察 分别以进样量为2、4、6、8、10、12 μL 的混合对照品溶液注入液相色谱仪中,以进样量(μL)为横坐标,峰面积为纵坐标,绘制人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 的标准曲线,各对照品的回归方程及线性范围为:Rg1:Y = 203.09X + 13.234(1.08 ~6.48 μg);Re:Y = 135.76X+62.095(1.09 ~6.54 μg);Rb1:Y = 72.308X + 5.6685(1.14 ~6.84 μg);Rd:Y =162.28X + 10.071(1.28 ~7.68 μg);S-Rg3:Y =197.36X + 19.989(1.06 ~6.36 μg)[3],见表3。
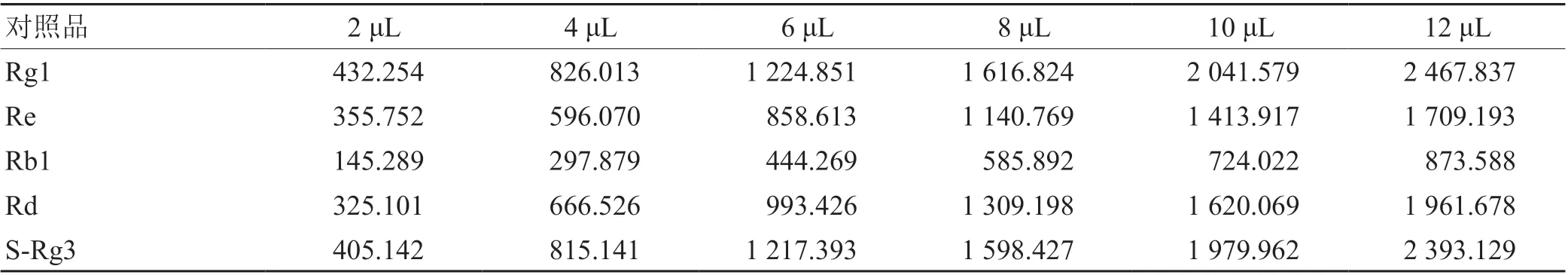
表3 线性考察数据(峰面积)
2.1.4.2 精密度试验 精密吸取人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 的混标对照品溶液10 μL,注入液相色谱仪,连续进样6 次,依2.1.1 方法测定,记录峰面积积分值,计算,考察精密度,见表4。
精密度考察结果显示:对照品溶液连续测定人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 的混标对照品的峰面积结果的RSD 均<2%,表明仪器、方法的精密度良好[4]。

表4 精密度试验实验结果(峰面积)
2.1.4.3 稳定性试验 精密吸取同一人参总皂苷供试品溶液5 μL,按0 h、4 h、8 h、16 h、18、24 h分别注入液相色谱仪,依2.1.1 方法测定。以人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 的峰面积测定结果为指标,测定其在24 h 内检测的稳定性,见表5。
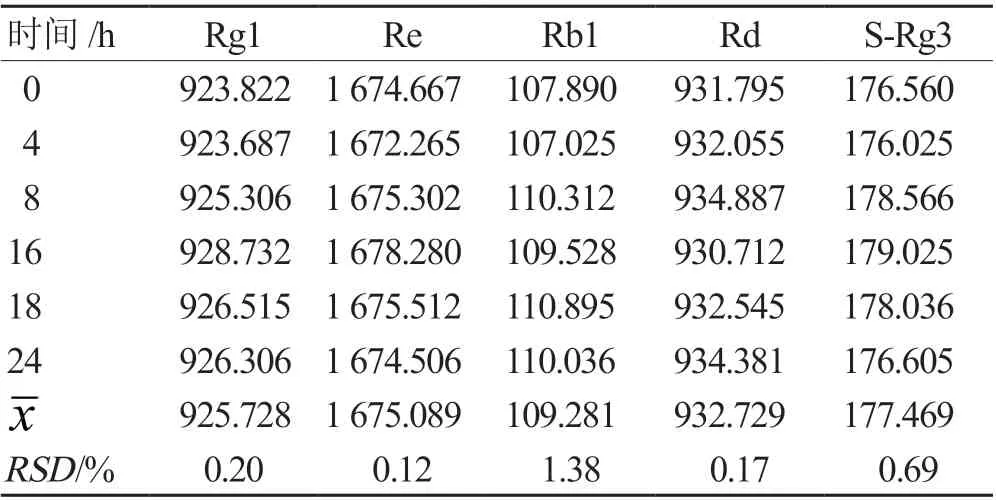
表5 稳定性试验结果(峰面积)
稳定性考察结果显示:在24 h 内测定供试品溶液中人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 的各标准品的峰面积的RSD 均<2%,表明人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 5个基准物24 h内测定结果可靠,稳定性良好。
2.1.4.4 重现性试验 精密量取同一人参总皂苷供试品共5 份,按供试品溶液项下制备方法制备,精密吸取5 μL,依2.1.1 方法测定,计算样品含量,以考察本法的重现性[5],见表6。
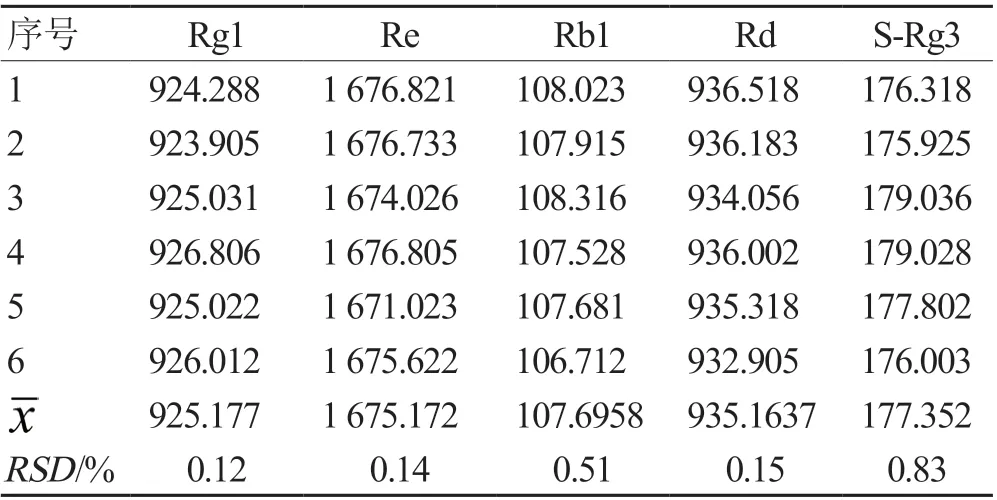
表6 重现性试验(峰面积)
以人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 为含量测定指标,考察本法的重现性,结果RSD 均<2%,表明该方法重现性良好。
2.1.4.5 加样回收率试验 取3 批次已知含量的人参黄连有效组分速崩片10 片,研磨后精密称定0.5 g,准确加人参皂苷Rg1、Re、Rb1、Rd 和S-Rg3适量混合标准品溶液,按2.1.3 方法制备样品溶液,每批样品均平行进样3 次,分别按这5 种人参皂苷的含量分别为80%、100%、120%的比例分别加入一定量的各人参皂苷标准品溶液,依2.1.1 方法测定,测定并计算各成分的加样回收率及RSD 值[6]。人参皂苷Rg1、Re、Rb1、Rd、S-Rg3 的加样回收率分别为 101.5%、100.03%、99.02%、101.5%、100.02%,RSD 值分别为1.2%、1.02%、1.30%、0.86%、1.20%表明该方法的准确度良好,结果可信。
2.1.5 3 批样品含量 根据外标公式计人参总皂苷Rg1、Re、Rb1、Rd、S-Rg3 的含量。样品含量由样品峰面积(A 样)、对照品浓度(C 标)、对照品进样量(Ⅴ标)三者的乘积比对照品峰面积(A 标)、样品浓度(C 样)、样品进样量(Ⅴ样)三者的乘积求得。取不同3 批次人参黄连有效组分速崩片,每批次中均平行检测3 个样品,色谱图见图1、图2。取平均值后,暂定人参皂苷Rg1、Re、Rb1、Rd 和S-Rg3 含量每片分别为2.92 mg、7.69 mg 、1.06 mg、4.42 mg 和0.56 mg。

图1 人参皂苷混合对照品色谱图

图2 人参总皂苷色谱图
2.2 人参黄连有效组分速崩片人参皂苷的含量测定研究
2.2.1 测定依据 参照《中国药典》(2015 版)[2]黄连含量测定项下选用的检测波长,色谱条件:以十八烷基硅烷键合硅胶为填充剂(色谱柱型号:Xcharge- C18,5 μm,4.6 mm×250 mm);柱温:30 ℃以乙腈为流动相A,万分之一三氟乙酸水为流动相B,按照表7 进行等度洗脱;检测波长为345 nm。流速为0.6 mL·min-1。

表7 流动相洗脱表
2.2.2 对照品溶液制备 称取盐酸小檗碱1.88 mg、盐酸药根碱1.18 mg 溶于适量的甲醇中,混匀,分别得到浓度为0.47 mg·mL-1和0.295 mg·mL-1的盐酸小檗碱及盐酸药根碱混合标准品溶液。
2.2.3 黄连供试品溶液制备 取10 片人参黄连有效组分速崩片,研磨,精确称定1 g,加入25 mL 甲醇并超声波30 min,过0.45 μm 滤膜,备用。
2.2.4 方法学考察
2.2.4.1 紫外检测波长确定 称取适量的盐酸小檗碱对照品,其相应的试剂作为空白,用紫外分光光度计(200 ~500 nm)进行全波长扫描,结果显示,在345 nm 处有最大吸收峰,因此将345 nm 确定为检测波长[7]。
2.2.4.2 线性关系考察 制备浓度分别为0.47、0.295 mg·mL-1盐酸小檗碱及药根碱的混合标准品溶液。进样量分别为1、3、5、7、9、12 μL,注入液相色谱仪。进样量(μL)为横坐标,峰面积积分值为纵坐标,分别绘制盐酸小檗碱和药根碱标准曲线,见表8。

表8 盐酸小檗碱及药根碱标准曲线数据(峰面积)
2.2.4.3 精密度试验 精密吸取3 μL 盐酸小檗碱和药根碱的混合标准品溶液,将其注入液相色谱仪中,连续进样6 次,依2.2.1 中方法测定,记录峰面积积分值,考察精密度[8],见表9。精密度考察结果显示:对照品溶液连续测定盐酸小檗碱和药根碱的混标对照品的峰面积结果的RSD 均<2%,表明该方法精密度良好。
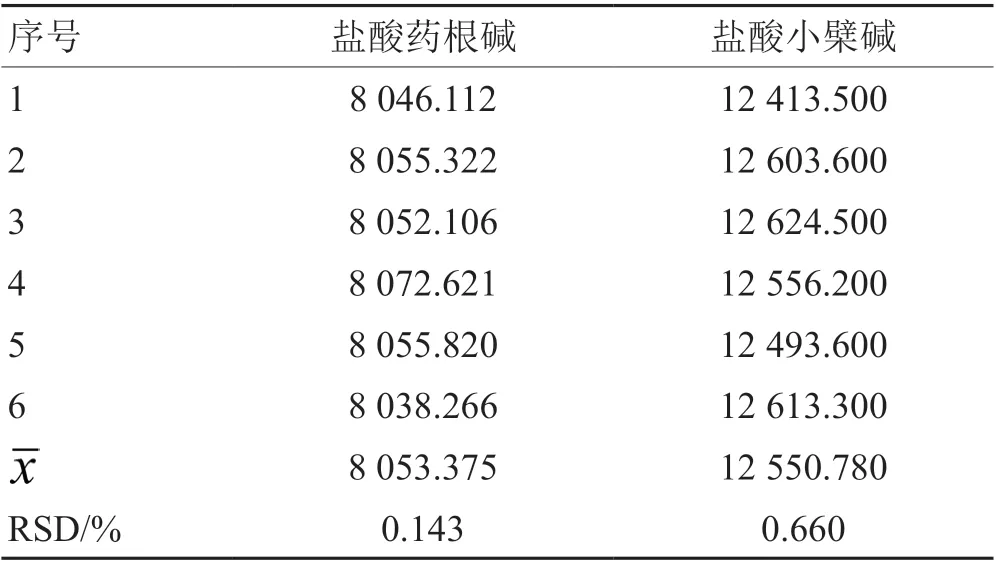
表9 精密度实验数据(峰面积)
2.2.4.4 稳定性试验 精密吸取10 μL 同一黄连总生物碱样品溶液,按一定时间分别注入液相色谱仪。依2.2.1 方法测定,以盐酸小檗碱及药根碱的混标对照品各成分的峰面积测定结果为指标,测定其在24 h 内检测的稳定性[9],见表10。

表10 稳定性实验结果(峰面积)
2.2.4.5 重现性试验 精密称定5 份同一黄连总生物碱样品,按供试品溶液项下制备方法制备样品,精密吸取10 μL,按照方法2.2.1 进行测量,并计算样品的含量,以研究该方法的重现性。见表11。

表11 重现性实验结果(峰面积)
2.2.4.6 加样回收率实验 精密称定已知含量的3批黄连总生物碱各2 mg,每批样品平行进样3 次,分别精密加入盐酸小檗碱和药根碱混合标准品溶液适量,每组分别按照盐酸小檗碱和药根碱总含量比例的80%,100%和120%,加入一定量的盐酸小檗碱和药根碱的标准品溶液,依2.2.1 方法测定,测定并计算各成分的加样回收率及RSD 值。回收率由加入对照品后测得的含有该成分的量与加入对照品前测得的含有该成分的量的差值比加入对照品的量求得。
盐酸小檗碱和药根碱的加样回收率分别为102.6%、99.6%和101.6%。RSD 值分别为101.3%,100.5%和99.6%。结果表明,该方法准确度高,结果可信。2.2.5 样品测定 取3批人参黄连有效组分速崩片,每批检测3 个平行样品,色谱图见图3、图4。取其平均值后,盐酸麻风次碱和小碱的含量每片分别为2.644 mg 和39.02 mg。

图3 混合对照品色谱图
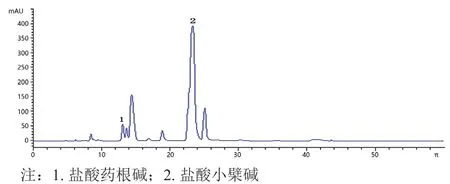
图4 黄连总生物碱色谱图
3 小结
人参在降糖方面有较好的活性,能够加速糖尿病性大鼠血糖和血脂代谢,并促进胰岛素分泌[10-11],黄连可降低患者血糖、血脂[12-13],人参黄连配伍后能够改善糖代谢,并能维持胰岛细胞身份[14],且经课题组前期研究结果表明人参黄连配伍后表现的降糖活性优于单味药。人参黄连有效组分速崩片具有使用剂量低、释放速度快、作用靶点多等创新性,对糖尿病肾病的治疗有重大意义[15]。本实验通过高效液相色谱法检测各成分的含量,操作简单可靠,灵敏度高,初步建立该制剂的质量标准,为后续试验研究提供理论基础。
