“双注射器组合装置”的制作与应用
2020-12-07魏海李德前
魏海 李德前

摘要: 将10mL塑料注射器与1mL塑料注射器巧妙组合,既保留了两个注射器的功能,又使仪器组合达到1+1>2的效果。介绍“双注射器组合装置”的构成和制作,应用于铜和硝酸反应的系列实验。该实验装置不仅能反复使用,操作简便,而且能应用于常温下块状固体与液体的反应,演示封闭环境中的液体化学反应也十分有效。
关键词: 双注射器; 组合装置; 实验装置设计和制作; 铜与硝酸反应
文章编号: 1005-6629(2020)11-0069-03
中图分类号: G633.8
文献标识码: B
塑料注射器透明度高,材质性能稳定,针筒的密封性好,活塞与筒壁之间的静摩擦力适中,尤其是其性价比远远高于常规化学仪器,因而塑料注射器已成为化学实验创新必不可少的替代品。
最近,我们基于化学实验创新技法的“同类组合”“等值替换”思维,将1mL注射器与10mL注射器巧妙组合,形成固定装置(如图3所示),可用于铜与硝酸反應等多个常温下的化学实验,并取得了显著的实验效果。
1 双注射器组合装置的制作
1.1 制作材料
主要是1mL塑料注射器(见图1-A),10mL塑料注射器(见图1-B),橡胶帽(在橡胶塞小头处挖一个半深的凹槽,见图3),强力胶水,胶带等。
1.2 制作过程
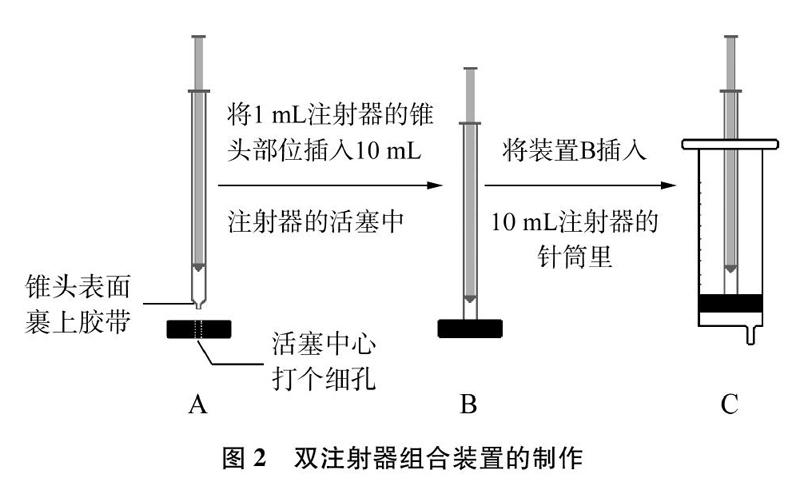
该实验装置的制作(如图2所示)并不复杂,其主要操作是将1mL注射器插入10mL注射器的活塞中(原芯杆废弃),通过这种内外组合,形成比较固定的实验装置。具体制作流程如下。
(1) 准备一个10mL注射器,抽出芯杆,取下套在芯杆顶端的活塞(芯杆废弃),在活塞中心打一个直径约3mm的细孔(见图2-A)。
(2) 准备一个1mL注射器,在针筒的锥头表面裹上几圈胶带(要裹成圆柱状,并且圆柱直径略大于活塞凹槽),然后在胶带表面涂抹一层胶水,随即将其插入活塞的凹槽中(见图2-B),并粘牢。
(3) 将1mL注射器与10mL注射器活塞的组合装置B,插入10mL注射器的针筒里(见图2-C)。
(4) 给10mL注射器吸入口配一个大小合适的橡胶帽,至此双注射器组合装置制作完成(见图3)。
1.3 装置构成
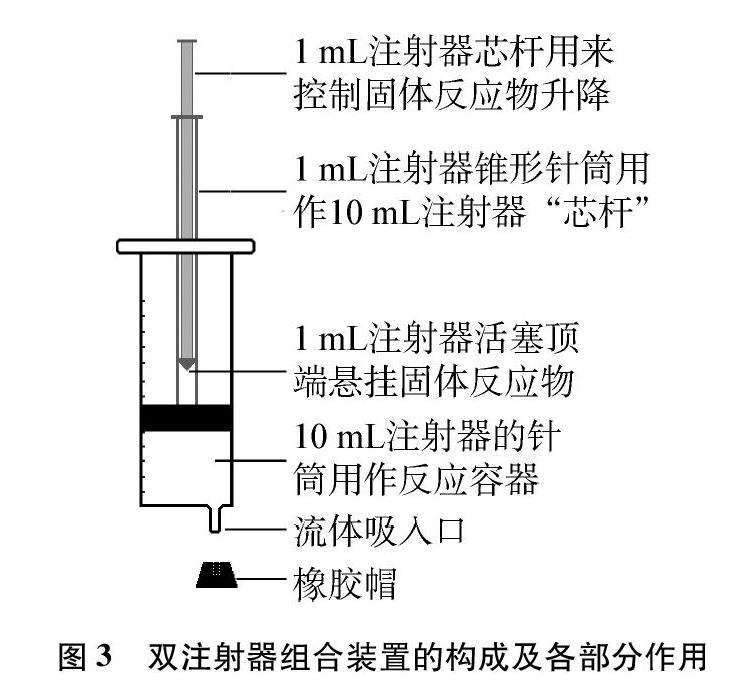
双注射器组合装置的构成及各部分作用,如图3所示。
(1) 10mL注射器的主要作用是盛装液体反应物,并作为常温下的反应容器。
(2) 1mL注射器的主要作用是承载固体反应物,并控制固体反应物的升降。
(3) 橡胶帽的作用是使反应容器封闭或开启。
(4) 上述实验用品按图3组合起来,就可以使反应随时发生或停止。
2 装置应用
下面以铜分别与稀、浓硝酸反应及NO、 NO2性质的系列实验为例,介绍该装置的使用方法。
2.1 铜与稀硝酸反应的实验操作
(1) 找一根2mm×50mm的铜丝,将其表面打毛(以增大铜与稀硝酸的接触面)。
(2) 抽出1mL注射器的芯杆,将铜丝固定在活塞的突出部位,再将芯杆放回锥形针筒里,并推至合适位置(对准活塞中间小孔,但确保铜丝不露出活塞表面)。
(3) 在10mL注射器针筒里吸入2~3mL刚冷却的蒸馏水,然后使注射器吸入口向上。缓缓上推活塞至零刻度处,以彻底排除针筒里的空气[1](见图4)。
(4) 在10mL注射器针筒里吸入5mL稀硝酸,随后将橡胶帽套在吸入口上,并保持注射器吸入口向下。通过1mL注射器的芯杆按下铜丝,使铜丝穿过活塞浸入稀硝酸中,两者立即发生化学反应(见图5),观察到铜丝表面产生无色气体,10mL注射器的活塞缓慢上移,溶液逐渐变为蓝色[2],有关反应的化学方程式是3Cu+8HNO33Cu(NO3)2+2NO↑+4H2O。待反应放出约5mL无色气体后,将铜丝拉回1mL注射器的锥形针筒里,反应立即停止。
(5) 使注射器吸入口向上,再拔掉吸入口上的橡胶帽,然后缓缓下拉活塞,吸入足量的空气,针筒内无色气体立即变为红棕色,说明一氧化氮气体极不稳定,易被空气氧化为二氧化氮气体,有关反应的化学方程式是2NO+O22NO2。
(6) 使注射器吸入口向下(此时针筒里下层是硝酸和硝酸铜的混合液、上层是含有二氧化氮气体的尾气[3],见图6),缓缓下推活塞,先排出针筒里的实验废液(用小烧杯接收)。继续缓缓下推活塞,将尾气直接推入饱和氢氧化钠溶液中将其吸收,有关反应的化学方程式是2NO2+2NaOHNaNO2+NaNO3+H2O。
(7) 实验结束,整理实验用品,回收实验废液(处理后可再利用)。
2.2 铜与浓硝酸反应的实验操作
(1) 抽出1mL注射器的芯杆,在活塞的突出部位固定一根2mm×50mm的铜丝,然后再将其放回1mL锥形针筒里。
(2) 在10mL注射器针筒里吸入5mL浓硝酸,然后用橡胶帽封闭吸入口,并保持注射器吸入口向下。通过1mL注射器的芯杆,将铜丝按下来,使金属铜与浓硝酸接触,两者立即发生化学反应;观察到铜丝表面快速产生红棕色气体,10mL注射器的活塞缓缓上移,溶液逐渐呈现绿色,有关反应的化学方程式是Cu+4HNO3Cu(NO3)2+2NO2↑+2H2O。待反应放出大约5mL红棕色气体后,将铜丝拉回1mL注射器的锥形针筒里,反应即刻停止。
(3) 拔掉吸入口上的橡胶帽,使注射器吸入口向下(此时针筒里下层是硝酸和硝酸铜的混合液、上层是二氧化氮气体),缓缓下推活塞,恰好完全排出针筒里的混合液(用小烧杯接收),二氧化氮气体仍然保留在针筒里。
(4) 在10mL注射器针筒里吸入5mL刚冷却的蒸馏水(此时注射器活塞约在10mL刻度处),然后用橡胶帽封闭注射器吸入口,再轻轻振荡注射器针筒几次,观察到红棕色气体逐渐消失,气体的体积明显减少,残留的气体为无色,这说明二氧化氮溶于水发生了化学反应,产生了无色气体,有关反应的化学方程式是3NO2+H2O2HNO3+NO;最终,整个针筒里混合物(主要是硝酸溶液和一氧化氮气体)的总体积约为7mL。
(5) 使注射器吸入口向上,再拔掉吸入口上的橡胶帽,缓緩下拉活塞,吸入足量的空气(使针筒内残留的一氧化氮气体变为能被氢氧化钠溶液直接吸收的二氧化氮气体),观察到无色气体很快变为红棕色气体。
(6) 将注射器吸入口向下(此时针筒里下层是硝酸溶液、上层是含有二氧化氮气体的尾气),缓缓下推活塞,先将针筒内的硝酸溶液排出(用小烧杯接收)。继续缓缓下推活塞,将尾气直接推入饱和的氢氧化钠溶液中以充分吸收[4]。
(7) 实验结束,整理实验用品,回收实验废液(处理后再利用)。
3 装置优点
(1) 上述实验装置还可以用来演示制取氢氧化亚铁的实验;如果改用大容积的塑料注射器,并将固体装入有孔小塑料瓶(悬挂在细铜丝上),该装置就可以用来制取氢气、二氧化碳气体、硫化氢气体等。并且这些化学反应可以随时发生和停止,有利于多个班级的连续授课,因此提高了实验教学效益。
(2) 上述实验装置用于中学化学实验,其操作非常简单,就是通过推拉注射器芯杆使反应发生或停止,因此有利于教师开展实验教学,也方便学生进行实验探究活动,尤其适用于教学装备条件相对落后的学校或地区。
(3) 上述实验装置属于整体固定的实验仪器,由于是塑料材质,不易损坏,可以反复使用,因此节约了装备资源、降低了实验成本。
(4) 该实验装置可以全程封闭,实现了有害气体的零排放。注射器针筒便于制造无氧环境,有利于防氧化实验(制取一氧化氮气体、氢氧化亚铁等)的顺利进行[5]。
总之,“双注射器组合装置”适用面较为广泛,实验教学效果明显,既能用于教师的演示实验,也方便学生动手操作,开展一系列实验探究活动,因此是优良且实用的化学实验装备资源。
参考文献:
[1]张玉勇. 铜与硝酸反应实验创新设计三例[J]. 实验教学与仪器, 2017, (7~8): 78~79.
[2]吴正帅, 郝海龙. 铜与硝酸反应及NOx性质实验的创新设计[J]. 中小学实验与装备, 2018, (3): 34~35.
[3]赵立胜, 李德前. 铜与浓、 稀硝酸反应实验的新设计[J]. 中国现代教育装备, 2017, (24): 47~48.
[4]李德前, 周梅华. “铜与稀硝酸反应”实验的改进[J]. 教育与装备研究, 2017, (10): 69~70.
[5]伍强, 方瑞光. 铜与硝酸反应实验的一体化设计[J]. 化学教学, 2016, (6): 60~63.