一种改良兔心房纤颤模型建立方法的研究
2020-10-29江燕白雪赵立志潘洪杨思进
江燕 白雪 赵立志 潘洪 杨思进


摘要:目的 尋找一种操作简便、可重复性高的房颤建模方法,为研究心房纤颤的发生机制以及治疗方案奠定基础。方法 将新西兰兔30只随机分为正常对照组、常规模型组、改良组,每组各10只,正常对照组仅暴露心房和分离肺静脉,J形双极起搏电极置于左心房,仅置入电极而不起搏;常规模型组暴露心房分离肺静脉后将起搏电极缝在左心房,高频起搏左心房起搏12 h;改良组暴露心房,分离肺静脉,然后在肺静脉主干任意处使用自制双电极电刺激,进行程序期前刺激12 h,比较三组存活情况、房颤诱发率、房颤发作的心室率及房颤持续时间,测量完毕后分离左心耳进行HE染色,观察三组左心耳纤维化程度。结果 三组死亡率均为10.00%,差异无统计学意义(P>0.05);正常对照组未诱发出心律失常,常规模型组房颤有诱发率为50.00%,改良组诱发率为80.00%,差异有统计学意义(P<0.05);常规模型组房颤发作时平均心室率为(121.00±15.35)次/min,低于改良组的(154.00±18.49)次/min,差异有统计学意义(P<0.05);常规模型组房颤持续时间为(425.40±49.51)s,低于改良组的(817.60±39.16)s,差异有统计学意义(P<0.05);改良组每倍镜下心肌纤维化及细胞空泡程度高于常规模型组及对照组。结论 兔心房纤颤时左心耳的纤维化程度较正常窦性心律时增加,房颤发生时心耳也出现结构重构,本次改良方法可成功建立心房纤颤模型,且成功率高、方法简单、重复性好,值得推广。
关键词:心房纤颤;兔;动物模型;改良
中图分类号:R541.75 文献标识码:A DOI:10.3969/j.issn.1006-1959.2020.18.016
文章编号:1006-1959(2020)18-0051-04
Study on an Improved Method for Establishing Rabbit Atrial Fibrillation Model
JIANG Yan,BAI Xue,ZHAO Li-zhi,PAN Hong,YANG Si-jin
(Department of Cardiology,the Affiliated Hospital of Traditional Chinese Medicine,Southwest Medical University,
Luzhou 646000,Sichuan,China)
Abstract:Objective To find a simple and reproducible atrial fibrillation modeling method to lay the foundation for the study of the mechanism of atrial fibrillation and treatment options. Methods 30 New Zealand rabbits were randomly divided into normal control group, conventional model group, and modified group, each with 10 rabbits. The normal control group only exposed the atrium and separated the pulmonary vein. The J-shaped bipolar pacing electrode was placed in the left atrium and only placed the electrode is inserted without pacing; the conventional model group was exposed to the atrium and the pulmonary vein is separated, the pacing electrode was sewn to the left atrium, and the left atrium was paced with high frequency pacing for 12 h; the modified group was exposed to the atrium, separates the pulmonary vein, and then use it anywhere in the pulmonary vein self-made dual-electrode electrical stimulation, performed pre-procedural stimulation for 12 h, compared the survival, atrial fibrillation induction rate, ventricular rate of atrial fibrillation and the duration of atrial fibrillation in the three groups. After the measurement, the left atrial appendage was separated for HE staining, and the three groups were observed The degree of left atrial appendage fibrosis.Results The mortality rate of the three groups was 10.00%,the difference was not statistically significant (P>0.05); the normal control group did not induce arrhythmia, the induction rate of atrial fibrillation in the conventional model group was 50.00%, and the induction rate of the modified group was 80.00%,the difference was statistically significant (P<0.05); the average ventricular rate during the onset of atrial fibrillation in the conventional model group was (121.00±15.35) beats/min, which was lower than that of the modified group (154.00±18.49) beats/min,the difference was statistically significant (P<0.05); The duration of atrial fibrillation in the conventional model group was (425.40±49.51) s, which was lower than (817.60±39.16) s in the modified group,the difference was statistically significant (P<0.05); The degree of muscle fibrosis and cell vacuolation was higher than that of the conventional model group and the control group.Conclusion The degree of fibrosis of the left atrial appendage in rabbits with atrial fibrillation was higher than that of normal sinus rhythm, and the structure of the atrial appendage was also remodeled when atrial fibrillation occurs. This modified method could successfully establish atrial fibrillation model with high success rate and simple method,good repeatability, worthy of promotion.
Key words:Atrial fibrillation;Rabbit;Animal model;Improvement
心房纤颤是临床上常见的心律失常之一,随着人口老龄化,房颤的发生率呈上升趋势,据不完全统计,大于80岁人群中,房颤发生率高达10%,高危心脏病患者人数可达30%[1]。房颤时心房的有效收缩消失,心排血量降低、血液瘀滞,容易形成附壁血栓,从而导致栓心力衰竭、栓塞等不良事件[2],使患者生活质量降低、死亡率升高,给社会带来巨大负担,此一直是心血管领域研究的热点和难点。很多疾病都可导致心房纤颤的发生,如心脏瓣膜病、缺血性心肌病、高血压、甲亢、糖尿病、缩窄性心包炎、慢性肺源性心脏病等[3],但也有少许患者为单纯性孤立性房颤。近年来随着新型口服抗凝药物的问世、房颤射频消融以及左心耳封堵术的推广[4],房颤的治疗取得了突破性进展,但心房纤颤的发生机制仍是基础和临床工作者共同面临的重大课题。以上工作的开展均离不开房颤模型的建立,如何建立一个简便、重复性高、成本低、容易推广应用的试验模型显得尤为重要。本文旨在通过对兔心房纤颤建模方法的改良,探寻一种操作简便、可重复性高的建模方法,以便后期为研究心房纤颤的发生机制奠定基础。
1材料与仪器
1.1实验动物 成年雄性新西兰大耳白兔30只,由西南医科大学实验动物中心提供,体重2~3 kg,按照随机数字表法分为正常对照组10只、常规模型组10只、改良组10只。
1.2仪器和器械
1.2.1主要仪器 RM6240BD多道生理信号采集处理系统(成都仪器厂)、BL-420E生物机能试验系统(成都泰盟科技有限公司)、心内膜电图引导电极(成都仪器厂)。
1.2.2实验器械及药品 镊子、止血钳、组织剪、眼科剪、大剪刀、动脉夹、注射器、烧杯、量筒、棉签、纱布等。盐酸利多卡因注射液(山东华鲁制药有限公司,批号1103034)、戊巴比妥钠(北京化学试剂公司,德国进口分装)。
1.3方法 用丙戊酸钠麻醉兔后,将其固定在解剖台上,止血钳撑开口腔后植入一口咽通气管用于安置食道刺激电极。然会将四肢和颈部的兔毛剪掉并清洁相应部位的皮肤,将心电图机上的红、黄、黑、绿四个电极线分别接于兔的右前肢、左前肢、右后肢、左后肢,选取最为清晰的Ⅱ导联监测心电情况,记录此时的心电图为正常窦性心律。
1.3.1正常对照组 在麻醉状态下,打开胸前皮肤及皮下组织,仅暴露静脉静脉、心房和分离肺静脉,穿刺植入2F电极导线,结扎远端颈外静脉,经超声证实,J形双极起搏电极置于左心房,仅置入电极而不起搏,稳定15 min后记录此时的心电图。
1.3.2常规模型组 兔麻醉后暴露心房分离右侧颈外静脉、肺静脉后,穿刺植入3F电极导线,结扎远端颈外静脉,经超声证实,J形双极起搏电极置于左心房,稳定15 min后采取连续单刺激模式,高频起搏左心房起搏12 h,起搏频率为500次/min,脉宽0.5 mv,强度3.5 v。
1.3.3改良组 同常规模型组,麻醉兔后暴露心房,分离右侧颈内静脉、肺静脉,然后在肺静脉主干任意处使用自制双电极电刺激,两根电极之间的距离为4 mm,稳定15 min后进行程序期前刺激12 h,心脏程序期前刺激法(S1S2),分别测量基础刺激间期(S1S1)分别为200 mS、150 mS。
1.4观察左心耳心肌纤维化程度 试验结束后,将兔处死,取其左心耳脱水、固定、切片后进行HE染色,观察左心耳心肌纤维化程度。
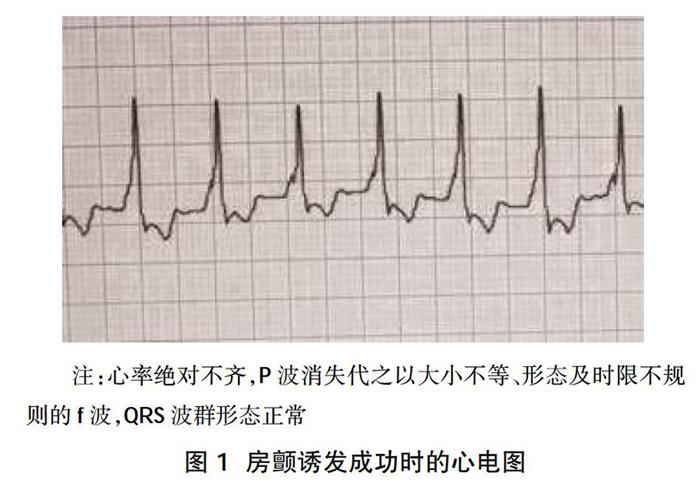
1.5指标判定 利用容积导体记录体表Ⅱ导联心电图(ECG)监测心房纤颤诱发的情况。当Ⅱ导联心电图记录到AF发生时,按下计时器记录房颤发作和中止时时间作为房颤的持续时间。AF诱发成功的标准必须满足以下三个条件:①AF发作时,Ⅱ导联心电图可见P波消失,代之以大小不等、形态及时限不规则的f波,f波频率为350~600次/min,R-R间期绝对不齐,QRS波群形态正常。②听诊时可闻及心率绝对不齐,第一心音强弱快慢不等,脉搏短绌。③房颤发作的持续时间须超过20 min。
1.6统计学处理 用SPSS20.0和Excel2000软件处理实验数据,计量资料采用(x±s)表示,组间比较行t检验;计数资料采用(%)表示,行?字2检验。P<0.05为差异具有统计学意义。
2结果
2.1三组动物存活及并发症情况 正常对照组死亡1只,死因为切口血肿,死亡率为10.00%;常规模型组死亡1例,死亡原因为诱发室颤后心力衰竭,死亡率为10.00%;改良组死亡1例,该例动物在诱发快速房颤后心脏驟停死亡,尸检未发现明显异常,考虑快速心室率诱发心力衰竭,改良组的死亡率也为10.00%,三组死亡率比较,差异无统计学意义(P>0.05)。
2.2三组心律失常发生情况比较 正常对照组无心律失常发生,常规模型组和改良组可见诱发心房纤颤,其中常规模型组还有频发室早、室性心动过速、室内阻滞发生,心律失常心电图见图1;改良组的心律失常类型少于常规模型组,主要以心房纤颤为主,其中仅1例频发室性早搏,无室速和室颤,心律失常的类型和发生率见表1。常规模型组和改良组发生心房纤颤的平均心室率以及房颤维持的平均时间见表2。
2.3各组兔左心房心肌纤维化程度 正常对照组未诱发出房颤的心肌纤维化程度不明显,常规模型组和改良组诱发出房颤的心肌纤维排列欠整齐,心肌细胞肿胀明显,部分心肌可见纤维化。改良组每倍镜下心肌纤维化及细胞空泡下程度明显高于常规模型组及对照组,见图2、图3。
3讨论
随着人口老龄化的加剧,房颤的发病率呈上升趋势,据不完全统计,中国大陆目前房颤患者人数超过1000万,而大于75岁人群中,房颤发生率高达10%,高危心脏病患者人数可达30%[5]。房颤发作时,由于心房无规律的跳动,使得心房失去了有效收缩,从而导致心排血量减少,严重影响心功能造成心力衰竭[6]。同时,由于血液在心房内瘀滞以及形成涡流,容易使心房或左心耳形成附壁血栓,栓子脱落可致栓塞事件,使患者生活质量降低、致残率、死亡率升高,给社会带来巨大负担,此一直是心血管领域研究的热点和难点。对心房纤颤的发生机制和治疗的研究,是基础和临床工作者共同面临的重大课题。
近年来,国内外众多学者为房颤研究进行了不懈努力,使得房颤发生过程中的电生理机制、结构重构、基因学、内分泌机制等方面研究都有了一定程度的研究,房颤三维射频消融术、左心耳封堵、外科迷宫手术等在临床上的应用,使得房颤的治疗成功率得到大大提高[7]。以上的成就的取得均离不开成功的房颤模型的建立,并在此基础上进行的大量基础研究,这些研究对于阐明和探寻房颤发生发展机制以及治疗方案起到了很多的作用。
目前成功建立的房颤模型中,使用的试验动物主要为犬、猪、大鼠和兔。如乌头碱注射入犬右心耳或肺静脉诱发心房纤颤[8];乙酰胆碱联合联合心房Brust刺激诱发犬心房纤颤模型;尽管近年来许多研究均成功建立了房颤的体内、体外试验模型,但大多存在科研成本高、试验动物存活率低、重复性低、技术难度高、操作复杂等特点,难以进行推广及应用。基于上述缺点,创立一种简便、可靠、重复性高且更好模拟人体房颤的模型显得尤为必要。
心房纤颤的发病原因复杂,且临床上可引起房颤的发病机制也不单一,目前尚无一种理想的模型能与临床上众多心房纤颤病因相对应。但目前已有资料证实兔快速心房起搏引起的电生理改变,与人类房颤发生时的电生理改变一致,因此利用兔进行房颤的发病机制研究比较合理。我们设计了改良兔心房纤颤模型,本研究通过微创技术分离右侧颈内静脉、肺静脉,然后在肺静脉主干任意处使用自制双电极电刺激,简化了手术操作步骤及降低了对试验动物的创伤,在保证了试验动物的存活率、降低了科研成本的前提下,更好地模拟了人类房颤发生的机制。采用单相动作电位记录技术和心脏程序期前刺激法,分别测量基础刺激间期分别为200 mS、150 mS时房颤诱发率、房颤平均持续时间等电生理指标,本实验利用电极持续刺激肺静脉,代替了将电极插入心房内,既保证了有效起搏,又减少了创伤和试验难度。
综上所述,心房纤颤时左心耳的纤维化程度较正常窦性心律时增加,房颤发生时心耳也出现结构重构,本次改良方法可成功建立心房纤颤模型,且成功率高、方法简单、重复性好,值得推广。
参考文献:
[1]Rahman F,Kwan GF,Benjamin EJ.Global epidemiology of atrial fibrillation[J].Nature Reviews Cardiology,2014,11(11):639-654.
[2]Michele M,Glukhov AV.Atrial Fibrillation and Fibrosis:Beyond the Cardiomyocyte Centric View[J].BioMed Research International,2015(2015):1-16.
[3]马长生.2019年心房颤动治疗新进展[J].临床心血管病杂志,2019,35(11):967-971.
[4]Park JW,Yu HT,Kim TH,et al.Atrial Fibrillation Catheter Ablation Increases the Left Atrial Pressure[J].Circ Arrhythm Electrophysiol,2019,12(4):e7073.
[5]Borlich M,Sommer P.Cardiac mapping systems[J].Card Electrophysiol Clin,2019,11(3):449-458.
[6]景远文,李海瑞,黄驰雄,等.超声引导经食管起搏电极定位建立大鼠快速心房起搏房颤模型的实验研究[J].临床超声医学杂志,2017,19(2):73-76.
[7]Hiram R,Naud P,Xiong F,et al.Right atrial mechanisms of atrial fibrillation in a rat model of right heart disease[J].J Am Coll Cardiol,2019,74(10):1332-1347.
[8]Huang CX,Zhang S,Huang JD.Current knavledge and management recommendations of atrial fibrillation:2018[J].Chin J Cardiac Anhyth,2018,22(4):279-346.
[9]Boddum K,Saljic A,Jespersen T,et al.A Novel SCN5A Variant Associated with Abnormal Repolarization,Atrial Fibrillation,and Reversible Cardiomyopathy[J].Cardiology,2018,140(1):8-13.
收稿日期:2020-06-15;修回日期:2020-06-27
編辑/王朵梅
