共挤出流体法制备功能化胶囊膜的研究进展
2020-10-27刘文英巨晓洁谢锐汪伟刘壮褚良银
刘文英,巨晓洁,2,谢锐,2,汪伟,2,刘壮,2,褚良银,2
(1 四川大学化学工程学院,四川成都610065; 2 四川大学高分子材料工程国家重点实验室,四川成都610065)
引 言
胶囊膜作为一种封装系统,由于具有内部空腔结构以及比表面积较大等特点,能够对活性物质进行封装保护而被广泛应用于药物控制释放[1−4]、酶固定 化[5−7]、物 质 包 封[8−11]以 及 细 胞 培 养[12]等 领 域。其中,利用具有优良的生物相容性和生物可降解性以及成本低廉等特点的海藻酸作为壁材构建的海藻酸钙(Ca−Alg)胶囊膜在生物医药及食品等领域受到了国际上越来越多的重视[13−14]。目前,Ca−Alg 胶囊膜的制备方法主要有同轴电喷射法[15−16]、乳液模板法[17−19]以及共挤出流体法[20−21]等。其中,共挤出流体法[22−24]由于具有制备过程简单、条件温和、胶囊粒径均一以及结构可控等特点而备受关注。利用共挤出流体法可以制备包含水溶性液核或油溶性液核以及薄壁结构的Ca−Alg 胶囊膜[22],为细胞培养[12]和物质包埋[8−11]等领域提供一种有效的新手段。
本文主要介绍了近年来共挤出流体法制备Ca−Alg 胶囊膜及其应用的研究进展,重点介绍了利用共挤出法制备单腔室和多腔室Ca−Alg 胶囊膜、Ca−Alg 胶囊膜的跨膜传质影响因素、胶囊膜用于包埋细胞构建研究肿瘤增长机制的模型,以及利用具有温度和pH 等响应特性的功能材料对胶囊膜进行功能化及其应用研究进展,以期为功能性Ca−Alg 胶囊膜的进一步设计制备及应用研究提供指导。
1 共挤出流体法制备胶囊膜的方法
1.1 单腔室胶囊膜的制备方法
1.1.1 共挤出毛细管装置制备胶囊膜 利用共挤出毛细管装置制备单腔室胶囊膜,其实际操作方法是在控制内外相流速比的条件下,将内核液体及海藻酸钠溶液分别通入如图1所示的由玻璃毛细管组装的简易共挤出装置的内外管中,在界面张力和重力的作用下,外相流体剪切内相流体从而在管口处形成稳定的双重液滴。该液滴在重力作用下滴入钙离子(Ca2+)溶液中,海藻酸钠中的钠离子迅速与Ca2+发生离子交换,从而导致外层通过交联反应发生溶胶−凝胶转换,形成具有核壳型结构的胶囊膜,其外层是具有微米级厚度的Ca−Alg 凝胶膜,内核可以是水溶性或油溶性的液体[22,24−25]。通过调控内外相流体的流率,可灵活调节胶囊膜的外径与芯核的比例。从双重液滴形成到外层溶液发生交联的过程中,为了成功制备出封装完整的Ca−Alg 胶囊膜,需要解决的关键问题是如何维持两种流体的流动稳定性并且防止它们之间发生混合。研究表明,通过调节内外相流体的界面张力[向外相流体中加入表面活性剂,如十二烷基硫酸钠(SDS)]以及两相流体的黏度等可以实现Ca−Alg 胶囊膜的成功制备[22]。通过对胶囊膜进行有机/无机杂化处理,可以提高囊膜的稳定性[7]。利用共挤出毛细管装置可以将相变石蜡Rbubitherm®R27 封装于Ca−Alg 胶囊膜内,构建具有良好球形度和单分散性以及致密囊壁结构的相变材料胶囊,该胶囊具有良好的调温性、稳定性及重复使用性能[24]。另外,将共挤出毛细管装置组装可以构建含有多核的Ca−Alg 胶囊膜用于疏水性药物的控制释放[26]。
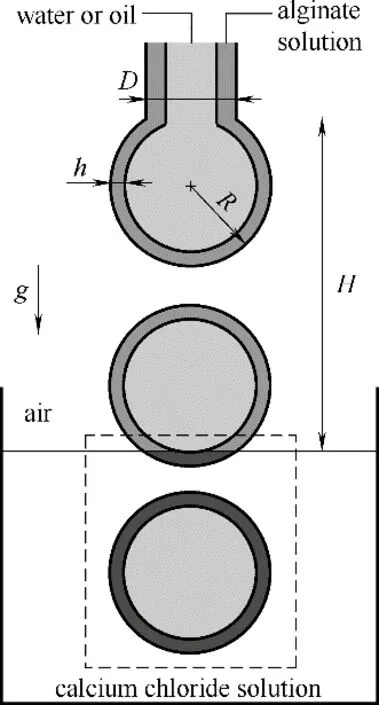
图1 共挤出流体法制备含有水溶性液核或油溶性液核的Ca−Alg胶囊膜的过程示意图[22]Fig.1 Schematic illustration of fabrication process of Ca−Alg capsule membranes containing aqueous or oil core by co−extrusion method[22]
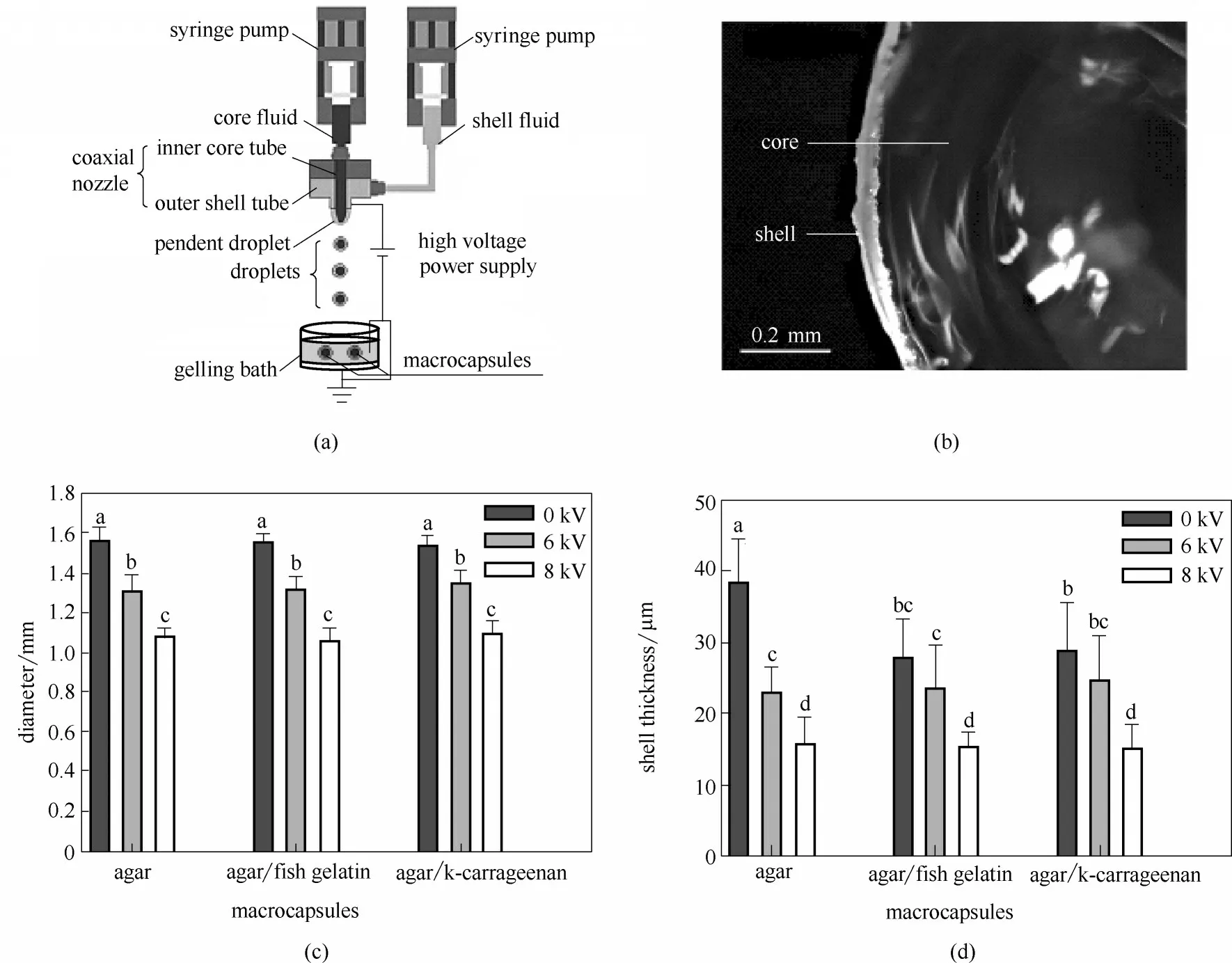
图2 利用电−共挤出工艺制备核壳结构Ca−Alg胶囊的示意图(a)及胶囊的光学图片(b)[27];在不同电压下利用电−共挤出工艺制备的三种微囊的直径(c)和壁厚(d)[28]Fig.2 Schematic illustration of electro−coextrusion process(a)and microscopic image(b)of core–shell structure of the calcium−alginate capsule fabricated by the process[27];Diameter(c)and shell thickness(d)of three types of capsules under different applied voltages[28]
1.1.2 电−共挤出制备胶囊膜 利用电−共挤出装置制备胶囊膜,其具体方法为:利用如图2(a)所示的装置,将内外相流体分别从注射管中注入共轴针的内外管中,在对针管进行加压的条件下,内外相流体在针出口处剪切形成复合液滴,该液滴下落进入能够使液滴外层固化的溶液中形成胶囊。以海藻酸钠作外相溶液封装含有苏丹Ш 的橄榄油,所制备的Ca−Alg 胶囊膜具有明显的核壳结构,如图2(b)所示[27]。基于琼脂构建核壳型胶囊的研究发现,只有当电压低于8 kV 时,才能产生稳定的核壳型胶囊。对比研究三种胶囊,即壳层材料分别为琼脂、琼脂/鱼凝胶混合物以及琼脂/卡拉胶混合物,发现从0~8 kV 增大电压时,三种胶囊的直径从1.6 mm 降低至1.1 mm[图2(c)],厚度也随电压的增大而在15.1~38.4 μm 范围内呈减小趋势,且在同一电压下,三种胶囊的壁厚几乎相同[图2(d)][28]。其原因为:在针上加正电压时,正电荷分子如H3O+等会聚集在针尖悬挂液滴的表面,随着电压的增大,更多的正电荷向液滴表面迁移,正电荷之间的强斥力会降低悬挂液滴的表面张力[29];除此之外,液滴表面的静电应力在高压下更强[30],随着外加电压的增加,具有较薄壳层的小尺寸液滴会以较高的频率从针尖滴落,从而形成具有薄壁结构的小尺寸胶囊。电−共挤出法能够制备微米级至毫米级范围内的核壳型胶囊,工艺简单,在大气条件下操作方便,为胶囊的制备提供了一种简易的策略。
1.1.3 共轴界面剪切制备胶囊膜 共轴界面剪切法制备胶囊膜,主要是基于交叉界面乳化机理[31−34],将内外相流体分别通入由共轴毛细管组装的共挤出装置的内外管中,通过振动穿过空气−液体界面的共轴毛细管而构建胶囊膜。调控振动频率和流体流率可以调控囊的尺寸,能够制备尺寸均一的胶囊,其过程可控,配置简单,在生物医学等领域具有广泛的应用[35−38]。当振动的毛细管垂直穿过空气−液体界面时,所产生的液滴垂直排列并最终沉积在收集容器的底部,若要实现胶囊的按需排列,该方式需要辅助额外的手段,例如介电泳法[39]、数字微流控技术[40]以及通过设计流体流动通道结构调控流场及液滴之间的相互作用[41−43]。为了简化液滴的产生和定位过程,Huang 等[44]基于上述手段开发了一种共轴斜界面剪切(COIS)技术,如图3(a)所示,利用一个同轴针来提供内外流体在气液界面上倾斜振动,从而产生复合液滴颈的夹点,液滴在接收相中以可调谐的横向位移移动,使得沿特定方向排列的胶囊可用于热和化学环境下的空间梯度释放[图3(b)]。研究发现,通过调节毛细管的振动频率和内外相流体的流率可以调控胶囊的形貌和尺寸,振动频率增大,产生的液滴尺寸随之增大,而当增大内相或外相流体的流率时,液滴的尺寸随之减小。并且,基于Stokes 漂移模型研究产生液滴的横向位移与过程参数之间的关系表明,随着振动频率的增大或者内相或外相流体流率的减小,液滴的最终横向位移均呈现增大的趋势。COIS 结合了共轴界面剪切与液滴侧向定位的优点,通过倾斜穿过空气−液体界面的周期性振动共轴毛细管装置实现了一步法产生胶囊及其空间梯度分布同步排序,并且基于Stokes 漂移模型可以准确预测胶囊的横向位移,利用该方法产生的具有不同形貌和尺寸的带有二维条纹结构的复合囊可以为构建具有热和化学物质刺激响应空间梯度控释的功能材料提供一种简易的方法。
1.2 多腔室胶囊膜的制备方法
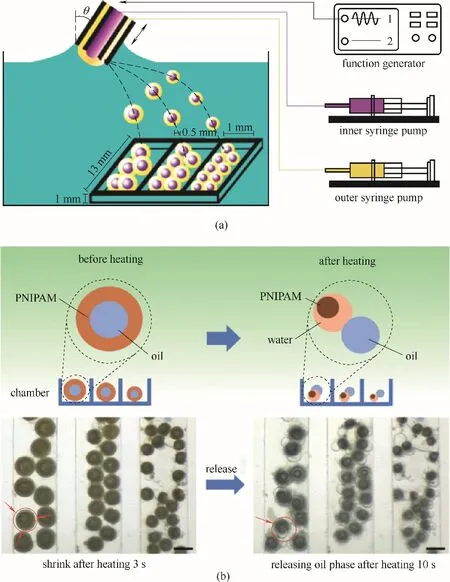
图3 利用共轴斜界面剪切(COIS)技术制备复乳及其热响应空间梯度释药[44]:利用COIS技术产生复乳并收集在带有三个矩形槽的石英池中(a);具有热响应性凝胶膜和油核的微囊膜的释放过程(比例尺:500 μm)(b)Fig.3 The coaxial oblique interface shearing(COIS)technique to generate the double emulsions and verification of thermal−responsive spatial gradient drug release[44]:schematic of the COIS technique for generation of double emulsions and colleting by a quartz pool with three rectangular grooves(a);schematic of the releasing process for microcapsules with a thermal−responsive hydrogel shell and an oil core(scale bar:500 μm)(b)
相比于具有单个腔室的胶囊,多腔室结构的胶囊具有更多功能,可实现在单个胶囊中同时包载互不相容的活性物质,并防止其发生交叉污染[45−47]。并且,在胶囊的囊膜中引入功能性组分,可实现对不同的包封组分在需要的情况下协同释放[48−49],也可实现将不同的反应物分别包载在不同的腔室中,一经触发便可发生反应等[50−51]。因此,多腔室结构胶囊具有更加广阔的应用前景。目前,制备多腔室结构的胶囊膜的方法主要是基于模板法来构建胶囊的内部腔室,包括固体模板法[52−53]、液滴模板法[54−55]以及微流控乳液模板法[56−59]等,利用这些方法制备的多腔室胶囊的研究虽然可实现上述效果,但这些胶囊中多个腔室外的囊壁是相同组分的,因此每个腔室外囊壁的渗透性能以及每个腔室内部包封物的释放行为不能够独立控制,这将会限制这些多腔室胶囊在控制释放及微反应等领域的应用。因此,He 等[60]通过将多套共挤出毛细管装置进行组装,开发了一种可升级式毛细管共挤出技术。利用探针巧妙地触发液滴在下落过程中的融合,能够可控制备用于物质协同释放的具有多组分液核及囊壁结构的Ca−Alg 胶囊。该技术的具体操作是将如图4(a)所示的两套共挤出装置按照图4(b)进行组装,两套装置接近垂直放置,通过控制内外相流体的流率,用羧甲基纤维素钠溶液作为内相流体1(IF1)和2(IF2)构建水包水(W/W)液滴的内核,海藻酸钠溶液作为外相流体1(OF1)和2(OF2)构建W/W 液滴的外层。在装置出口端同时产生两个不同的W/W 复合液滴在重力的作用下同时滴落,在下落过程中由一根水平放置的探针引发其融合,形成Janus 的θ 型液滴。θ型液滴落入硝酸钙[Ca(NO3)2]溶液中,使得Ca2+与θ 型液滴外层中的海藻酸发生交联,从而形成具有双腔室结构的Ca−Alg胶囊[图4(c)]。研究发现,利用组装后的共挤出装置成功制得的双腔室Ca−Alg胶囊具有良好的形貌及高度的均一性,具有Janus型囊壁的双腔室Ca−Alg 胶囊的示意图及光学照片如图4(d)、(e)所示。其中,胶囊内每个液核可作为独立的腔室用以同时包封不同的组分使其隔开而不发生混合,通过改变制备时的流速可实现对双腔室胶囊腔室液核体积及相应的壳层厚度进行灵活调控。并且,通过向双腔室胶囊Janus 型囊壁中添加不同功能性组分,可灵活控制每个腔室外囊壁的渗透性能,从而可实现各个腔室的包封物具有不同的控制释放行为,将两种控制释放模式在同一个胶囊中实现。另外,通过组装更多数量的毛细管共挤出装置,可实现对装置的进一步升级,制备具有更多不同组分液核腔室及囊壁的Ca−Alg 胶囊[如图4(f)所示的利用三套共挤出装置组装所制备的具有三腔室的Ca−Alg 胶囊],实现对物质的多样化包封及协同释放。因此,这种液核腔室及各腔室外的囊壁均为多组分的胶囊,在生物医学等领域具有更加广阔的应用前景。
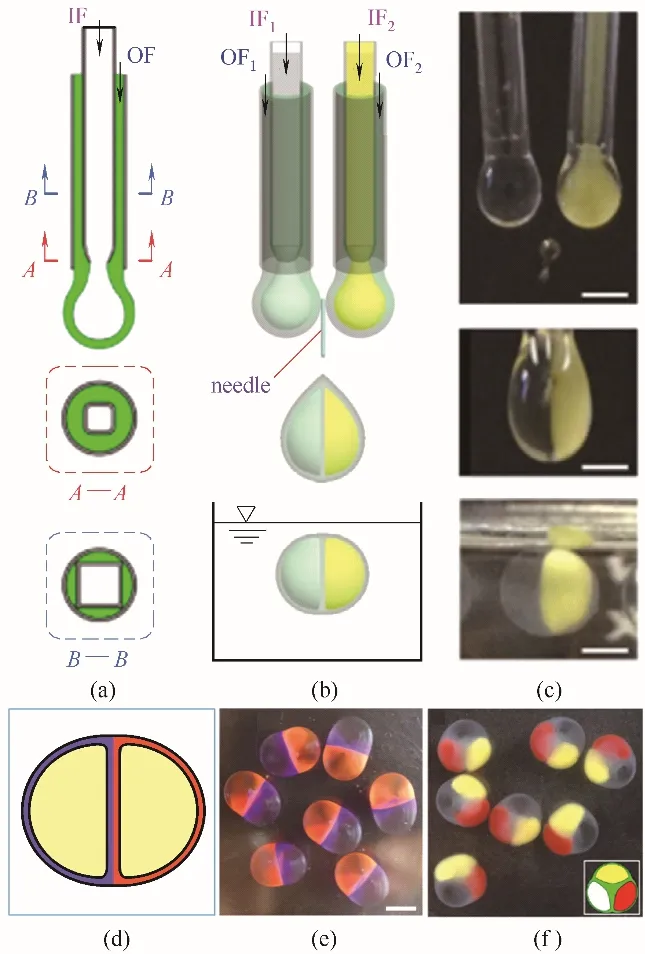
图4 共挤出装置制备具有多腔室的Ca−Alg胶囊[60]:共挤出装置构建W/W液滴示意图(a);两套共挤出装置组合构建具有双腔室结构的Ca−Alg胶囊示意图(b);在装置出口端产生的两个不同W/W液滴被不锈钢探针触发融合后在Ca(NO3)2溶液中形成具有双腔室结构Ca−Alg胶囊过程的光学图片(c);具有Janus型囊壁的双腔室Ca−Alg胶囊的示意图(d)及光学照片(e);具有三腔室的Ca−Alg胶囊的光学图片(f)[图(c)和(f)中的比例尺分别为2.5 mm和5 mm]Fig.4 Co−extrusion minifluidic devices for fabrication of multi−compartmental Ca−Alg capsules[60]:schematic illustration of the co−extrusion minifluidic device for fabricating W/W droplets(a);schematic illustration showing the combination of two co−extrusion minifluidic devices for fabricating the dual−compartmental Ca−Alg capsules(b);digital photos showing the generation of two different W/W droplets at the outlets of the devices with coalescence of the two W/W droplets triggered by the stainless steel needle,and the formation of dual−compartmental Ca−Alg capsules in the Ca(NO3)2solution(c);schematic illustration[(d),insert in(f)]and digital photos showing dual−compartmental(e)and triple−compartmental Ca−Alg capsules(f)[the scale bars in(c)and(f)are respectively 2.5 mm and 5 mm]
2 共挤出流体法制备胶囊膜的结构和性能影响因素
2.1 胶囊膜制备过程的影响因素
利用共挤出流体法制备胶囊膜,通常包含W/W复合液滴产生以及液滴囊壁凝胶化成囊膜两个过程。在产生W/W 液滴时,装置尺寸以及内外相流体的黏度、浓度、流率和界面张力等均会影响液滴的形成,只有这些影响因素控制在一定范围内才能形成稳定的W/W 复合液滴。在液滴囊壁凝胶化形成胶囊膜的过程中,液滴滴落高度(装置出口与Ca2+离子溶液液面之间的高度,H)、交联时间、凝胶剂浓度以及表面张力等均会影响胶囊膜的结构和性能。
产生W/W 液滴时,装置尺寸主要控制产生液滴的大小。内外相流体的流率、黏度和浓度等在装置中主要影响流体的流动特性,并与内外相流体间的界面张力协同作用,决定了在装置出口处是否能正常剪切形成W/W 复合液滴,以及所形成的液滴中内核流体与外壳流体的体积分率,从而影响囊壁的结构和厚度,进而影响跨囊膜传质速率。研究发现,以2%(质量)的海藻酸钠溶液作外相流体,15%的氯化钙作凝胶剂,当内相只有水时,通过控制内外相流体的流率以及液滴滴落高度,海藻酸在固化之前很容易与内核中的水混合,很难形成稳定的核−壳结构胶囊。而在外相溶液中添加表面活性剂SDS调节两相界面张力后,可成功制备出完整的胶囊膜,并且,通过调整H以及内外相流体的流率比等参数,可在0.6~150 μm 范围内灵活地改变所形成胶囊膜的厚度[22]。另外,以果汁作为水相液核,何帆[61]利用不同尺寸的共挤出装置制备了具有不同粒径的含有水相液核的Ca−Alg 胶囊,并系统研究了溶液黏度、制备过程中内外相流速等参数对胶囊膜形貌、胶囊膜中液核与囊壁体积的比值以及胶囊膜抗压强度的影响。研究发现,通过调节装置内外管的管径,可制备出外径在3.8~7.8 mm范围内且粒径均一的胶囊膜,实现对Ca−Alg 胶囊膜尺寸的调控。并且,通过增加溶液黏度及W/W 液滴下落的频率,可以制备具有良好形貌的包封有果汁液核的核壳型Ca−Alg 胶囊膜。此外,通过调节内外相流率的比值,可灵活调控每种尺寸胶囊中果汁液核的体积及胶囊的壁厚,从而可以根据需要准确控制果汁的包封含量及包封效果。通过向内外相中分别加入不同种类的果汁,可以实现内部水相液核及凝胶囊壁中含有两种不同种类的果汁,使得该胶囊对于果汁的包封更具多样性。胶囊受到挤压可发生形变直至破裂,使内部的果汁液核溢出,且对于每种尺寸的胶囊来说,随着液核与囊壁的体积比的增加,发生破裂时的最大应力应变均降低,囊壁越厚,果汁液核体积越小,胶囊被挤压破裂时所需的力就越大。
在W/W 复合液滴成囊膜过程中,液滴滴落高度H 主要影响胶囊膜的球形度,液滴滴落至凝胶剂中时,在空气/水界面会发生撞击导致复合液滴发生形变,从而影响液滴壳层凝胶化产生囊壁后所形成的胶囊膜的球形度。通过调节H使得液滴滴落的动能足够抵消凝胶剂溶液的表面阻力可以改善胶囊膜的球形度。另外,当凝胶剂溶液的黏度和表面张力增加时,胶囊的球形度下降,因此,也可以通过调节凝胶剂溶液的黏度和表面张力来调控胶囊的球形度[62]。交联时间以及凝胶剂浓度决定了囊壁的厚度和Ca−Alg 凝胶网络扩散通道的致密度[63]。研究发现,当海藻酸钠溶液与Ca2+溶液接触时,要想发生溶胶−凝胶转化,海藻酸钠与Ca2+的浓度匹配很重要,只有当海藻酸浓度高于0.8%(质量)时,海藻酸才能与Ca2+复合形成三维渗透凝胶网络,并且,当海藻酸浓度高于1.2%(质量)后,溶胶−凝胶转化过程便与Ca2+浓度没有关系[64]。另外,在研究海藻酸钠与Ca2+离子浓度对Ca−Alg 凝胶化的动力学的影响时发现,随着海藻酸浓度的增加,胶囊膜的壁厚减小,而随着Ca2+浓度的增大,胶囊膜的厚度增大[65]。由于海藻酸与Ca2+复合时,主要是海藻酸链中的古罗糖醛酸段(G)与Ca2+发生络合作用[13],因此,海藻酸链中的甘露糖醛酸段(M)与G 的含量比值会影响形成的Ca−Alg 凝胶的机械性能。Hecht 等[66]利用原子分子动力学模拟研究了不同海藻酸链在不同Ca2+离子浓度与不同海藻酸链组成下的缔合和聚集结构。研究发现,Ca2+离子通常会促进链聚集和凝胶化,而聚集主要受海藻酸单体组成(在确定溶液条件下与链的硬度有关)的影响,Ca−Alg 凝胶的硬度随着G 段含量的增高而增强,并且,链中G段的含量差异会导致如横向关联、拉链以及纠缠等不同的链间作用机理,而更多的M段能够增加杂聚物链的柔性,使得M段残留物可以作为一种促进链间相互作用的弹性调节剂。
2.2 胶囊膜的跨膜传质影响因素
胶囊膜在用作物质封装时,主要是基于液核和凝胶壳层的特殊结构,以实现封装物质的按需控释,其囊膜结构和特性对物质跨膜传输起关键性作用。囊膜结构和厚度、芯材性质及组分、环境溶液的pH 以及离子强度等对跨囊膜传输特性有重要的影响。根据扩散方程的基本原理可知,物质跨膜传输的渗透速率正比于推动力和扩散系数。对于外相仅为Ca−Alg 凝胶的胶囊膜,在溶质的跨膜传质过程中,胶囊膜的传质通道主要为Ca−Alg 凝胶网络间的空隙。胶囊膜的凝胶网络越致密,囊壁越厚,溶质跨膜传质阻力越大,渗透系数越低,因此,较薄的囊膜厚度可以减小跨膜传质阻力,但胶囊的机械性能会减弱。另外,胶囊的芯材性质及组分主要体现在渗透压的产生以及芯材释放等,环境溶液中的pH以及离子强度等主要影响囊膜的机械强度和稳定性。凝胶囊膜层的结构稳定性对其正常使用非常重要。Rolland 等[23]利用共挤出流体毛细管装置可控制备了封装不同溶质液核的Ca−Alg 凝胶囊膜,并研究了胶囊膜的物理化学特性。研究发现,当内外相流体的流率比为5~12时,所制备的胶囊膜厚度范围为45~100 μm,胶囊膜的壁厚与半径比值范围为0.026~0.06。当囊内的溶质不能完全渗透穿过囊膜时,囊膜内外产生的渗透压会驱使水分子持续进入囊内从而导致胶囊溶胀至饱和,囊膜厚度越薄,或者渗透压力越大,胶囊在溶胀的过程中会出现破裂[图5(a)]。分别对封装葡萄糖和摩尔质量Mw=2×104g·mol−1的葡聚糖以及Mw=2×106g·mol−1的葡聚糖的胶囊膜进行溶质释放动力学研究,结果发现,如图5(b)所示,分子摩尔质量高于临界尺寸的Mw=2×106g·mol−1的葡聚糖跨膜传输的质量分率在释放动力学特征时间t为100 h时仅为58%,而Mw小于临界尺寸的Mw=2×104g·mol−1的葡聚糖的t 仅为1 h,并比相同摩尔质量的葡萄糖大十倍,说明Mw=2×104g·mol−1的葡聚糖和葡萄糖均能自由渗透穿过胶囊膜,而Mw=2×106g·mol−1的葡聚糖跨膜传质会受限于海藻酸凝胶网络。胶囊的最大应力和渗透压随着囊内聚合物浓度的增大而增大,当渗透压一定时,应力随囊的壁厚或海藻酸的浓度减小而减小,胶囊的表观应力变软行为与其弹−塑性转化相关联,临界应变约为8%[图5(c)]。并且,由于胶囊的凝胶物理性质,在电解质的作用下,基于离子交换机理,囊内的包封物可以通过溶解囊膜而完全释放出来,囊壁的寿命与溶液的离子强度呈反比。
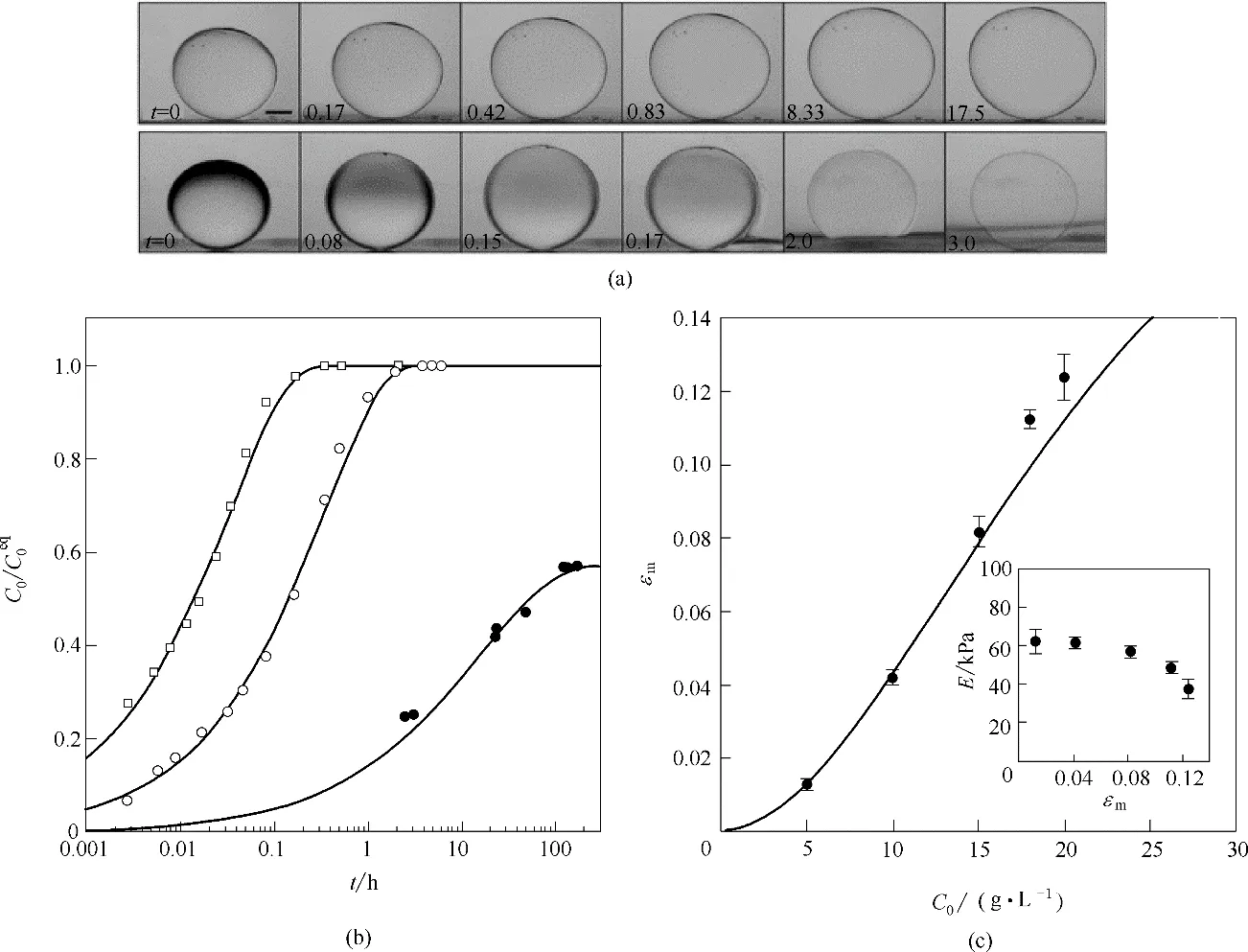
图5 胶囊膜的物理化学特性[23]:胶囊膜在渗透压下的溶胀(上)和饱和(下)变形过程光学图片(a);利用2%(质量)的海藻酸制备的胶囊膜对溶质葡萄糖(□)和Mw=2×104 g·mol−1的葡聚糖(○)以及Mw=2×106 g·mol−1的葡聚糖(●)的渗透扩散释放动力学(b);胶囊膜的最大应力与溶质液核中聚环氧乙烷初始浓度关系曲线(插图为弹性模量E与最大应力ɛm作用的胶囊应力变软行为)(c)Fig.5 Physicochemical properties of aqueous core hydrogel capsules[23]:time sequence of a capsule under osmotic stress that swells and whose deformation saturates(a);release kinetics of glucose(□),dextran with Mw=2×104g·mol−1(○),and dextran with Mw=2×106g·mol−1(●)from a capsule made with an alginate concentration of 2%(mass)(b);evolution of the maximal strain ɛm of stable capsules as a function of the initial poly(ethylene)oxide concentration C0(insert:elastic modulus E versus maximal strain showing a strain softening behavior)(c)
3 共挤出流体法制备胶囊膜的应用研究
3.1 胶囊膜包埋细胞研究肿瘤变化机制
基于多细胞球体(MCS)的细胞培养能够解决2D 细胞培养缺乏组织特异性而使肿瘤对治疗药物反应可预测性差的问题。目前,产生MCS 的方法如悬滴法、回旋法或者液体覆盖培养液法[67]等存在产量低以及细胞聚集体尺寸不可控等缺点,基于微尺度光刻技术的微阵列[68]、微波[69]以及微流体装置[70−71]等对MCS 进行自动化生产难以达到温和的细胞培养条件。因此,Alessandri 等[72]基于如图6(a)所示的微流体共挤出技术,提出了一种利用可渗透的弹性多孔微球封装细胞并使其增长用于大量生产尺寸可控的多细胞球的方法,并通过构建3D基细胞实验研究了肿瘤细胞的体外增长机制。利用荧光聚合物染色的海藻酸进行共聚焦成像,发现该胶囊具有明显的核壳结构[图6(b)]。利用小鼠结肠癌细胞系CT26,在标准培养条件下监测封装细胞形成MCSs的能力。为了研究弹性约束对生长球体外围细胞运动的影响,利用共聚焦活体成像技术,对由LifeAct−mCherry 稳 定 转 染 的CT26 的MCSs 的 生 长[图6(c)]以及用phalloidin−Alexa 488 (Hot LUT, cyan)染色的固定球体表面进行了成像。研究发现,细胞在生长过程中形成了长而薄的带有板状足和丝状足突起尖端,且在用荧光法染色的固定细胞中也可观察到板状足和丝状足[图6(d)],表明凝胶膜的渗透性可以使营养物质自由流进囊内,使得细胞在没有骨架的环境里也可以实现分裂增殖。另外,由于空心胶囊具有独特的几何形状和弹性性能,该胶囊能够作为定量测量因细胞球生长导致胶囊膜溶胀而产生的外部压力的机械传感器,使得胶囊膜的变形为外部压力的直接测量提供了策略。该研究将细胞封装在液核中并由凝胶膜层包围着,避免了油相环境,且制备过程中的装置剪切以及暴露在Ca2+溶液中均对细胞没有伤害。这种基于体外细胞实验的新方法,为新的抗癌疗法的开发以及研究肿瘤进化中力学和细胞增长的相互作用提供了一种新的策略。
3.2 胶囊膜的刺激响应性功能化及其应用研究
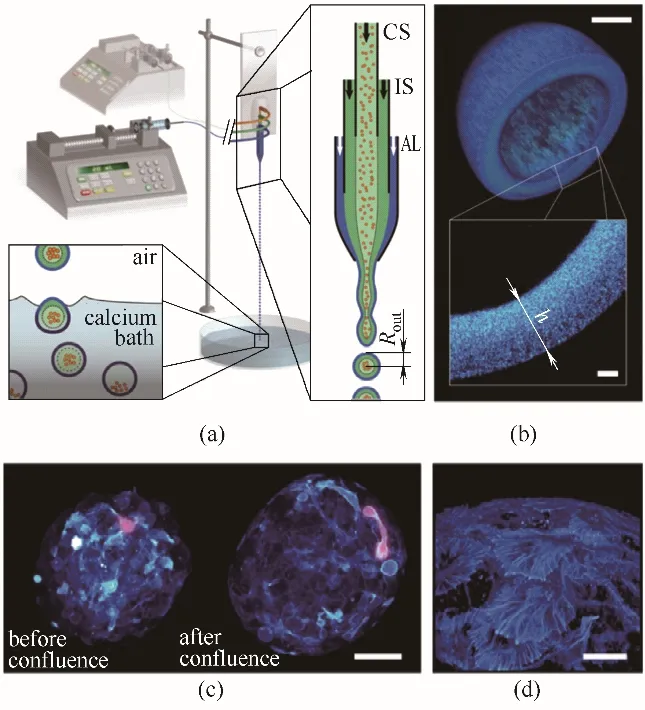
图6 构建封装细胞的胶囊膜的共挤出毛细管装置示意图(a);用荧光葡聚糖染色的胶囊膜的共聚焦图片(b);封装从LifeAct−mCherry稳定转染的细胞球体的生长共聚焦活体成像(c);用phalloidin−Alexa 488(Hot LUT,cyan)染色后的固定球体表面的共聚焦显微镜成像放大图(d)[比例尺:(b)50 μm;(c)50 μm;(d)10 μm][72]Fig.6 Schematic of the microfluidic platform used to fabricate capsule membranes encapsulated with cell suspension(a);confocal image of an alginate capsule stained with fluorescent dextran(b);confocal live imaging of an encapsulated spheroid grown from cells stably transfected with LifeAct−mCherry(c);enlarged view of the surface of a fixed spheroid imaged by confocal microscopy after staining with phalloidin−Alexa 488(Hot LUT,cyan)(d)[scale bars:(b)50 μm;(c)50 μm;(d)10 μm][72]
3.2.1 胶囊膜的pH响应特性 具有pH响应特性的胶囊膜主要是在胶囊膜的壳层中添加具有pH 响应特性的聚合物从而调控囊膜的渗透性能,进一步调控胶囊膜的控制释放特性。Mei 等[4]利用共挤出法可控制备了一种由Ca−Alg/精蛋白(CAP)复合膜层和封装有乳酸菌的海藻酸液核组成的具有pH 响应特性的藻酸钙基肠靶向智能化药物胶囊膜载体。该胶囊膜在pH 较低的胃中对乳酸菌具有保护作用,而在pH 较高的小肠中可以实现乳酸菌的快速释放。其pH 响应性能来源于Ca−Alg 与精蛋白之间的相互作用,当胶囊膜处于pH 较低的胃中时,胶囊膜的CAP 复合层中的Ca−Alg 凝胶网络由于羧基质子化使得扩散通道呈现“关”的状态,内核中的乳酸菌得以被保护,而当胶囊膜处于中性环境的小肠时,由于精蛋白与胰蛋白酶之间的相互作用,胶囊膜快速溶解使得内核中的乳酸菌被快速释放[图7(a)]。利用硅酸钠进一步对上述复合胶囊膜进行仿生硅化制得的Ca−Alg/精蛋白/二氧化硅(APSi)杂化胶囊膜具有更高的稳定性,可以用作酶的固定化载体[6−7,73]。研究发现,制备过程中pH条件对APSi杂化胶囊膜微观结构以及pH 响应性能均不会造成影响,在pH 为3~7 这一宽泛的范围内制备的胶囊膜渗透性能均在pH 4.5 附近有一个突变,均具有优良的pH 响应控制释放性能,并且APSi 胶囊膜只对溶质分子尺寸与胶囊膜中扩散通道尺寸相匹配的溶质展现出优良的pH 响应控制释放特性[73]。将胶囊膜用于仿生酶固定化载体的酶催化反应[6],Ca−Alg网络与精蛋白分子之间的静电作用提供的pH 响应特性可以通过改变环境pH 来调控固定化酶反应的速率。当环境pH 低于临界pH 时,Ca−Alg 凝胶网络呈电中性,带正电的精蛋白分子相互排斥地分布于凝胶网络的扩散通道内,此时通道呈现“关”的状态,酶催化反应的底物与产物的跨膜扩散受阻,胶囊膜内的酶催化反应停止;而当环境pH 高于胶囊膜临界pH 时,Ca−Alg 凝胶网络带负电,此时带正电的精蛋白分子由于静电作用被吸附到Ca−Alg 凝胶网络上而使扩散通道呈现“开”的状态,酶催化反应的底物和产物均可快速通过胶囊膜,使得胶囊膜内部的酶催化反应可顺畅进行,如图7(b)所示。另外,通过在APSi杂化胶囊膜表面接枝具有pH 响应特性的聚合物刷也可以赋予胶囊膜pH 响应特性[74]。用于酶固定化时,这种接枝了具有pH 响应特性聚合物刷的Ca−Alg 基囊膜对于酶催化反应具有良好的生物相容性以及优异的pH 响应性能[图7(c)]。利用毛细管共挤出装置制备的pH 响应胶囊膜无须使用任何模板,一步法即可形成胶囊膜,制备过程十分简单,为功能性胶囊膜的设计提供了高效策略。
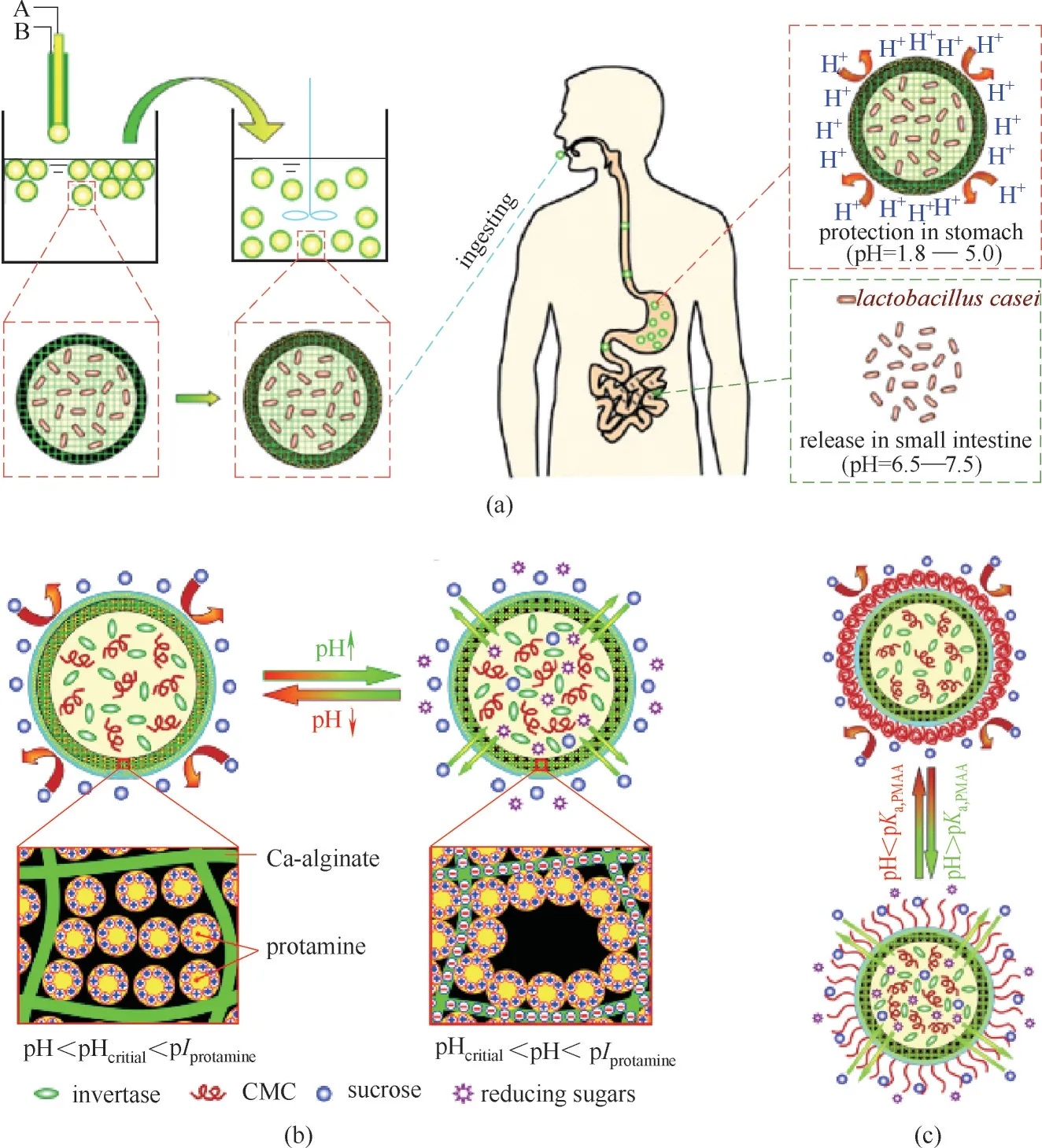
图7 基于pH响应特性保护和释放乳酸菌的肠靶向CAP胶囊膜载体的制备过程和概念设计示意图(a)[4];对海藻酸/精蛋白复合层进行仿生硅化后的胶囊膜用于酶固定化示意图(b)[6];接枝具有pH响应特性的聚合物刷的海藻酸钙胶囊膜用于酶固定化(c)[74]Fig.7 Schematic illustration of the preparation process and design concept of the intestinal−targeted capsule membrane for pH−responsive protection and release of lactic acid bacteria(a)[4];the enzyme−immobilized capsule membrane made of a Ca−alginate/protamine composite soft layer and the hard shell is silica surface rigid layer (b)[6];Ca−alginate capsule membrane grafted with pH−responsive brushes for controllable enzyme reaction(c)[74]
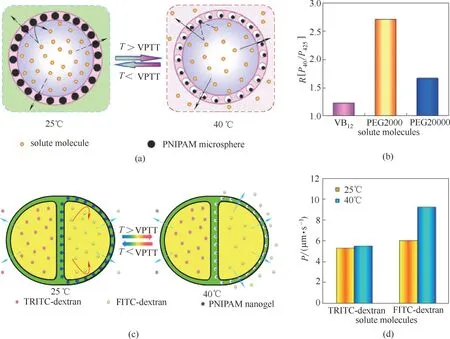
图8 具有热响应性能的Ca−Alg胶囊膜的热响应特性示意图(a);组成相同的Ca−Alg胶囊膜对不同溶质分子的热响应开关特性(b)[25];内核不同及一侧Janus囊膜含有热响应纳米凝胶的Janus型双腔室Ca−Alg胶囊膜的协同释放行为示意图(c);不同温度下溶质分子穿过Janus型双腔室囊膜的扩散渗透系数(P)(d)[60]Fig.8 Schematic illustration of the Ca−alginate capsule with thermo−responsive membrane (a);comparison of thermo−responsive gating characteristics of Ca−alginate capsule membranes for different solute molecules (b)[25];schematic illustration showing the synergistic release behaviors of the dual−compartmental Ca−Alg capsules with distinct cores and thermo−responsive nanogels embedded in one−half of the Janus membrane(c);diffusional permeability coefficient(P)of the solute molecules across the Janus membrane of the dual−compartmental capsules at different temperatures(d)[60]
3.2.2 胶囊膜的温度响应特性 在胶囊膜的壳层中添加具有温敏性的材料可以赋予胶囊膜温度响应特性,从而可通过改变温度来调控囊膜的渗透性能。Wang 等[25]利用共挤出微流体装置可控制备了一种具有液核和热响应性能的Ca−Alg 胶囊膜,该胶囊膜的热响应性来源于膜层中加入的具有温敏性的聚N−异丙基丙烯酰胺(PNIPAM)微球。当环境温度低于PNIPAM 微球在水中的体积相转变温度(VPTT)时,胶囊膜的Ca−Alg 凝胶网络中的PNIPAM微球处于溶胀状态,胶囊膜的渗透性能降低,此时溶质难以通过;当环境温度高于PNIPAM 微球在水中的VPTT时,胶囊膜中的PNIPAM 微球处于收缩状态,胶囊膜的渗透性能提高,此时溶质容易通过,如图8(a)所示。研究发现,随着胶囊膜中PNIPAM微球含量的增加,胶囊膜的温敏开关性能随之提高。在25℃时,随着胶囊膜中PNIPAM 微球含量的增加,PEG2000 溶质分子的扩散渗透系数(P)无明显变化;而在40℃时,P随着PNIPAM微球含量的增加而逐渐增大,且胶囊膜的温度响应渗透特性与溶质分子的大小有关,只有在溶质分子大小与胶囊膜扩散通道的尺寸相匹配时,胶囊膜才能表现出优良的温度响应渗透特性[图8(b)]。另外,通过在双腔室Janus 囊壁的一侧嵌入温度响应性纳米凝胶构建的双腔室囊膜具有不同渗透性能,能够在同一个胶囊中同时实现两种控释模式[60]。将分子量均为20×103的TRITC 标记的葡聚糖和FITC 标记的葡聚糖作为模型溶质分子分别包封在两个不同的液核腔室中,将具有温敏性的PNIPAM 纳米凝胶加入到包封有FITC 标记的葡聚糖一侧腔室外的壳层中作为功能开关。如图8(c)、(d)所示,当环境温度为25℃时(低于VPTT),纳米凝胶处于溶胀状态,该侧囊壁渗透性能较差;而当环境温度为40℃时(高于VPTT),纳米凝胶处于收缩状态,其体积缩小至小于25℃时体积的80%,使得该侧囊壁渗透性能提高,FITC 标记的葡聚糖可以比较容易地从该侧囊壁中扩散出去。另一侧囊壁中未添加具有温敏性的纳米凝胶功能组分,其渗透性能在高低温下没有明显变化,导致TRITC标记的葡聚糖在不同温度下通过该侧囊壁的速率几乎保持一致。该双腔室胶囊具有的Janus 型囊壁能够独立控制每种包封物的释放速率,实现灵活的协同释放。
3.2.3 胶囊膜的磁响应特性 在胶囊膜的内核或壳层中加入磁性颗粒,可以对胶囊膜进行磁响应功能化。He 等[60]通过将两套共挤出毛细管装置进行组装,在共挤出装置出口端同时形成两个水包水液滴,并在液滴下落过程中利用探针触发两个液滴的融合,从而制备了具有Janus 囊壁结构的双腔室胶囊。将磁性纳米颗粒加入到双腔室胶囊的其中一个液核腔室中,并将该双腔室胶囊放置于含有水的容器中,利用外加旋转磁场来对其进行远程操控,可以研究胶囊的磁响应性能。研究发现,如图9(a)所示,在旋转磁场的作用下,胶囊可进行相应的转动;并且,如图9(b)所示,在平行移动的磁场中,胶囊也可以迅速对磁场做出响应,并向该方向移动,表明一腔室内含有磁性纳米颗粒的双腔室胶囊具有优良的磁响应特性,可灵活进行转动及平行移动。此外,由于胶囊的磁响应特性主要取决于载入的磁性纳米颗粒的含量,因此可通过增加磁颗粒的含量来进一步提高磁响应性。这种具有磁响应性的双腔室胶囊用作不同包封物协同释放的载体时,通过外加磁场的操控可很容易地实现包封物的靶向运输及循环回收再利用。

图9 一腔室中含有磁纳米颗粒的双腔室Ca−Alg胶囊的磁性能调控[60]:磁诱导胶囊膜旋转运动的光学图片(a);磁诱导胶囊膜平行移动的光学图片(b)[图(a)、(b)的比例尺分别为2.5 mm和8 mm]Fig.9 Magnetic manipulation of dual−compartmental Ca−Alg capsules with magnetic nanoparticles dispersed in one of the compartments[60]:digital photos showing the magnetic−guided rotational motion of the capsules(a);digital photos showing the magnetic−guided translational movement of the capsules(b)[the scale bars in(a)and(b)are respectively 2.5 mm and 8 mm]
4 结 论
利用共挤出流体法制备海藻酸钙胶囊膜,主要优点有:制备过程简单、条件温和,胶囊膜的粒径均一以及结构和性能可控,可以制备包含水溶性液核或油溶性液核以及薄壁结构的胶囊膜;并且,通过对装置和方法进行改进设计,可以制备结构多样化的胶囊膜,实现物质的多样化包封,使其具有更多的功能和应用价值;另外,可以很方便地将具有温度或pH 等响应特性的功能性组分添加至装置的内外相流体中,赋予胶囊膜特定的功能,使其在细胞包埋以及酶固定化等领域具有更加广泛的应用。该方法的主要缺点是装置的共轴几何结构的共轴程度会受人为因素的限制,不利于制备对同心度要求极高的胶囊膜。利用共挤出毛细管装置可制备出外径在3.8~7.8 mm 范围内且粒径均一的海藻酸钙胶囊膜,其较大的内部空腔结构及优良的包埋能力有利于作为细胞和酶等物质的固定化载体,在生物化工、医药以及环境等领域具有广阔的应用前景。例如,基于胶囊膜独特的核壳结构,可以用于细胞包埋研究肿瘤增长机制。胶囊膜的结构和性能主要受装置尺寸、内外相流体的物化性质和流率、液滴滴落高度以及凝胶剂物化性质等的影响。为进一步拓展该方法制备胶囊膜在其他领域的应用,还需继续深入研究设计构建除物质装载型胶囊膜外的其他功能性材料,如简易制备功能性血管囊泡[75]拓展其在人造血管以及组织工程等领域的研究,以及进一步研究胶囊膜功能化的方法,将其他环境刺激响应性材料与该胶囊膜相结合,如与具有离子响应性功能材料相结合,用于重金属离子的检测和移除等领域。
