水凝胶材料在金属离子富集与分离领域的研究进展
2020-09-29文国宇汪伟谢锐巨晓洁刘壮褚良银
文国宇,汪伟,2,谢锐,2,巨晓洁,2,刘壮,2,褚良银,2
(1 四川大学化学工程学院,四川成都610065; 2 四川大学高分子材料工程国家重点实验室,四川成都610065)
引 言
水凝胶是一种以水为分散介质、具有三维网状结构的亲水性聚合物材料,其在智能传感器[1−3]、组织工程[4−6]、生物载药[7−8]、医用敷料[9−11]等领域广泛应用,因而受到了国内外越来越多的关注和重视。特别是在金属离子分离领域[12−15],相比诸如膜分离、化学沉淀、液−液萃取等传统分离手段,利用水凝胶材料作为吸附剂从环境中分离和富集特定金属离子,具有能耗低、分离效率高且不产生二次污染等优点。因此,水凝胶材料成为金属离子富集与分离领域非常有前景的载体。
目前研究人员已经制备了多种基于水凝胶材料的吸附剂,并展示了它们在金属离子富集和分离领域的作用。本文主要介绍了近年来水凝胶材料在金属离子富集和分离领域的研究进展,重点阐述了利用水凝胶材料富集放射性金属离子、稀土金属离子、贵重金属离子和重金属离子的研究现状,以期为进一步设计和研制新型水凝胶吸附功能材料提供指导。
1 用于放射性金属离子分离与富集的水凝胶材料
自然界中,能够自发地从不稳定原子核内部释放出α 射线、β 射线、β+射线或γ 射线的元素,被称为放射性元素。放射性元素所带来的放射性污染会不可避免地对环境和人体造成很多不可逆转的连锁性危害[16−20]。排放在环境中的放射性元素,可以通过水源和食物链在人体内部积累。研究表明,放射性元素的辐射对人体的血液循环系统、消化系统、神经系统等都将构成严重的损害[21−22]。特别是近年来,由于核武器爆炸、核电站泄漏、核动力装置爆炸或泄漏等事故的频繁发生[23−26],环境中的放射性物质不断增加。同时,核能发电领域的放射性原材料需求量也不断增加[27]。因此,对环境中放射性元素离子的富集与分离,不仅可以缓解严峻的环境形势,还可以为核能领域提供生产所需的原材料。
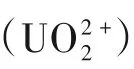
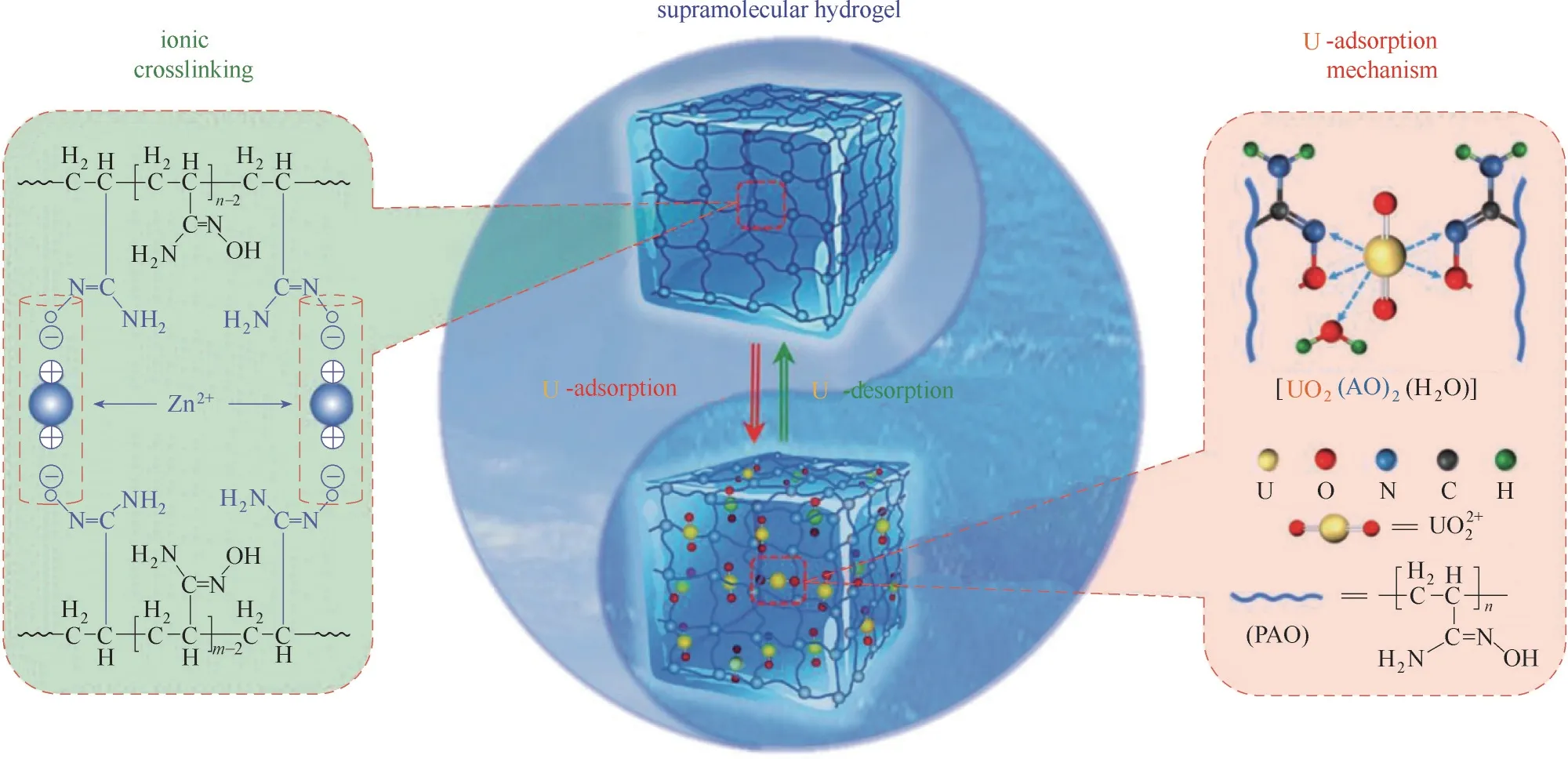
图1 Zn2+−PAO超分子水凝胶离子交联与选择性吸附铀的机理[31]Fig.1 The ionic crosslinking and selective uranium−adsorption mechanism of the Zn2+−PAO supramolecular hydrogel[31]
钍元素属于ⅢB 族锕系放射性化学元素,相比于应用广泛的铀元素,钍元素不仅含量更为丰富,而且在使用安全性方面也更优秀。所以,钍元素作为一种潜在的核燃料,已经引起了研究人员的广泛关注[32−34]。在核燃料加工过程中,钍元素是一种常见的且价态稳定的裂变产物,因此,吸附钍元素的研究具有十分重要的意义。Duan 等[35]提出以β−环糊精(β−CD)、丙烯腈(AN)和丙烯酸(AA)为原料,制备得到一种用于钍离子(Th4+)富集与分离的水凝胶。制备得到的β−CD(AN−co−AA)水凝胶内部含有丰富的β−CD,可以为Th4+的吸附提供理想的活性位点。在实际分离环境中,工业污水和海洋中存在的多种金属离子可能会影响吸附过程。但在多种干扰离子(如Pb2+、Mg2+、Ca2+等金属离子)存在的情况下,其吸附率并没有较大的下降,仍然能保持在77.08%~79.04%,证明了β−CD(AN−co−AA)水凝胶对于Th4+具有优异的吸附选择性。当环境pH 为2.95 时,该水凝胶对Th4+的最大吸附容量可以达到692 mg·g−1。以硝酸溶液作为洗脱液,经过4 h 的平衡时间,脱附效率可以达到87%。经过10 次吸附/脱附循环实验,该水凝胶的吸附容量与脱附效率并没有明显下降。所以同时具有较高吸附容量与优秀再生性能的β−CD(AN−co−AA)水凝胶具备较好的应用前景。但脱附过程的平衡时间相对超长,如果可以通过构建更疏松的凝胶骨架结构,便可以进一步降低平衡所需的时间,提高吸附剂的使用效率。
铯元素(Cs)属于ⅠA 金属元素,在自然界中仅以盐的形式极少分布于陆地和海洋中。然而,其同位素Cs−137 却是一种常见于核电站泄漏的放射性污染物。由于Cs−137放射性污染带来的巨大危害,因此如何有效地去除核污染中的放射性铯离子引起了研究人员的广泛关注[36−38]。目前,常用的分离方法有溶剂萃取法、共沉淀法、离子交换法等。但这些方法都存在如工艺烦琐、选择性较差等缺陷。如何高效、特异性地分离Cs+仍然是一个较大的挑战。Yu等[39]以苯并−18−冠−6−丙烯酰胺(B18C6Am)冠醚与丙烯酸(AAc)为原料,制备得到一种用于Cs+富集的水凝胶。如图2 所示,研究中以AAc 和B18C6Am 为单体,偶氮二异丁基脒二盐酸盐为引发剂,N,N−亚甲基双丙烯酰胺为交联剂,在高温下采用热引发自由基聚合的方法来制备聚(丙烯酸−共聚−苯并18 冠−6 丙烯酰胺)(P(AAc−co−B18C6Am))水凝胶。水凝胶内部的冠醚单元对Cs+具有良好的响应特性,当环境pH 高于AAC 的pKa时,AAc 由于去质子化作用使得原本电中性的羧酸基团脱去H+。此时,具有负电荷的羧酸基团就会因为静电吸引作用诱导Cs+进入水凝胶内部,而Cs+便会进一步地与B18C6 基团发生络合作用,形成稳定的2∶1“夹心”结构的主−客体配合物,以此来达到富集Cs+的目的。P(AAc−co−B18C6Am)水凝胶对Cs+的最大吸附容量为74.6 mg·g−1,同时其在30 min 以内就可以达到90%的吸附量。该水凝胶在混合离子溶液(Li+、Na+、K+、Cs+)中,对K+和Cs+都具有吸附能力,并且对Cs+的吸附能力大于K+。在实际应用场景中,对Cs+清除的需求往往较大,所以研究人员重点考察了该水凝胶的Cs+吸附容量和对水溶液Cs+的去除率。基于P(AAc−co−B18C6Am)水凝胶优秀的吸附性能和较高的吸附效率,其在核废料中Cs+的富集与分离领域具有较大的应用前景。
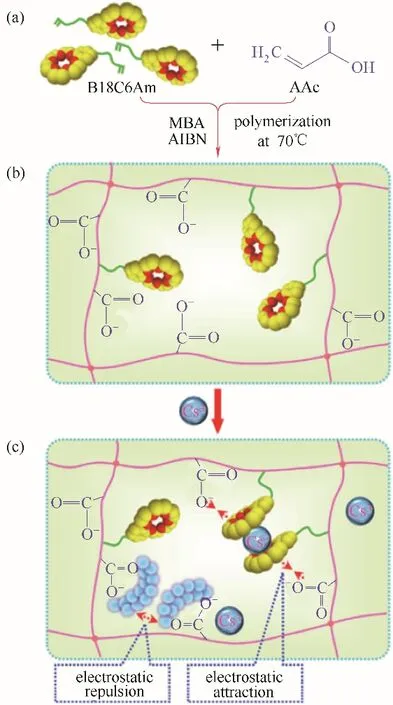
图2 P(AAc−co−B18C6Am)水凝胶的制备示意图(a)及其识别吸附铯离子的示意图[(b)、(c)][39]Fig.2 Schematic illustration of the preparation process(a)and cesium recognition and adsorption property[(b),(c)]of the P(AAc−co−B18C6Am)hydrogel[39]
2 用于稀土金属离子分离与富集的水凝胶材料
稀土元素是一种重要的战略资源。近年来,随着稀土元素在充电电池[40]、超导体[41]、催化剂[42]等领域的研究深入,其需求量也日益增长。而在稀土元素分离和后期加工处理的过程中,大量的稀土元素通过各种途径,在未经任何处理的情况下直接进入环境中,会带来资源极大的浪费[43−44]。因此,稀土元素的回收利用仍然是一个亟待解决的问题。
镧元素(La)属于ⅢB 族金属稀土元素,其在电池[45]、精密光学器件[46]、催化剂[47]等领域应用广泛。有效回收泄漏至环境中的镧元素,不仅是对自然的保护,更可实现稀土资源的回收利用[48−49]。Wu 等[50]提出以N−异丙基丙烯酰胺(NIPAM)、黏土(clay)和海藻酸钠(SA)为原料,制备得到一种用于镧离子(La3+)富集与分离的水凝胶。如图3 所示,首先将NIPAM、SA、clay 和光引发剂氧化锌(ZnO)充分混合后置于−15℃的环境中,在紫外光照引发的条件下,通过半导体纳米粒子引发的冷冻聚合技术,直接制备得到海藻酸−黏土−聚N−异丙基丙烯酰胺(alginate−clay−PNIPAm)水凝胶。当环境溶液中存在La3+时,该水凝胶内部的海藻酸高分子链上的α−L−古罗糖醛酸便会络合La3+,从而实现对于La3+的定向捕获。在双组分体系中进行的La3+与干扰离子(如K+、Zn2+、Al3+、Fe3+等)的竞争吸附实验表明,多数金属离子不会对La3+的去除率产生明显的影响。少量重金属离子(如Pb2+、Cd2+等)可能会使水凝胶对La3+的去除率下降至83%~86%,这展现了alginate−clay−PNIPAm 水凝胶对La3+具有较好的特异性吸附性能。同时,该水凝胶还具有较高的机械强度以及可逆的溶胀/收缩行为,可以实现对于La3+的高效吸附,其对La3+的最大吸附容量为182 mg·g−1。以浓盐酸作为洗脱液,经过6 次的吸附/脱附循环实验,该水凝胶仍然能够维持93.3%的吸附效率和92.4%的脱附效率。相比其他吸附材料,alginate−clay−PNIPAm 水凝胶不仅有着较大的吸附容量、较好的再生性能,而且吸附平衡时间短。作为一种成本低廉、高效的水凝胶吸附剂,alginate−clay−PNIPAm 水凝胶在La3+富集和分离领域具有很好的应用前景。
3 用于贵重金属离子分离与富集的水凝胶材料
以金、银和铂族金属为代表的贵重金属元素,因它们在艺术品、珠宝和硬币等方面的用途而闻名。同时,随着科学研究的不断深入,这类贵重金属元素在高效导体、精密电子元器件和催化剂等领域也展现了较高的应用价值。所以,从环境中富集和回收贵重金属元素十分重要[51−53]。
金元素(Au)属于ⅠB 族过渡金属元素,其单质通称为黄金,是一种广受欢迎的贵金属。同时,其在光纤通讯[54]、催化剂[55]、燃料电池[56]等领域都发挥着关键的作用。此外,随着全球经济的发展,对黄金的急剧需求造成了严重的供需关系失衡。加之,黄金本身的不可再生性,所以从环境中富集、分离黄金尤为必要。特别是从含金废水中回收金离子,引起了人们广泛的关注。Firlak 等[57]提出以季戊四醇四−3−巯基丙酸酯(Penta3MP4)、聚乙二醇丙烯酸酯(PEGDA)和甲基丙烯酸羟乙酯(HEMA)为原料,制备得到一种用于金离子(Au3+)富集的水凝胶。首先,将Penta3MP4、PEGDA 和HEMA 按照一定比例混合均匀,通过紫外光照引发的方式,制备得到聚(季戊四醇四−3−巯基丙酸酯/聚乙二醇丙烯酸酯/甲基丙烯酸羟乙酯)(P(Penta3MP4/PEGDA/HEMA))水凝胶。当环境溶液中存在Au3+时,水凝胶内部丰富的硫醇基团便会与Au3+发生络合反应,形成Au−S键,以此达到富集Au3+的目的。相比其他吸附剂材料,该水凝胶的制备方法简单,制备时间短(90 s),且吸附平衡时间也少于传统材料。但P(Penta3MP4/PEGDA/HEMA)水凝胶对Au3+的最大吸附容量仅为45.19 mg·g−1,较为紧致的水凝胶网络结构可能是导致离子吸附容量较低的原因之一。同时,研究人员对于干扰离子的影响探索也较少,缺乏对于实际应用体系的研究。以硫脲−盐酸作为洗脱液时,经过三次吸附/脱附循环实验,该水凝胶的脱附效率仍然超过96%,吸附容量略有下降,表现了较好的再生性能。总体来讲,该水凝胶可以实现对Au3+的特异性吸附,且制备过程更加高效、简单,可以用于含金废水中Au3+的富集。目前P(Penta3MP4/PEGDA/HEMA)水凝胶的吸附容量仍然有较大提升的空间,通过改变单体投料比,增加含硫组分占比,或许可以进一步提高其吸附容量。
银元素(Ag)属于ⅠB 族过渡金属元素,其在催化剂[58]、医用抗菌材料[59−60]和感光材料[61]等领域均有广泛的应用。虽然在低浓度情况下,Ag+具有较好的抗菌性,但随着浓度的增加,Ag+也会呈现一定的毒性。因此,富集和分离环境中的Ag+仍然十分必要。Wei等[62]提出以N−异丙基丙烯酰胺(NIPAM)和二硫化钼(MoS2)纳米片层为原料,制备一种用于Ag+富集和分离的水凝胶。如图4 所示,首先,将NIPAM、MoS2和交联剂MBA均匀混合,通过紫外光照引发的方式,制得二硫化钼/N−异丙基丙烯酰胺(MNH)水凝胶。其中,MoS2不仅是光引发剂,更是用于Ag+吸附的高硫添加剂。当环境溶液中出现Ag+时,水凝胶内部的MoS2会以Ag−S 键的形式与Ag+结合,从而实现对于Ag+的富集。当使用近红外光照射MNH水凝胶时,MoS2良好的光热转化效应会加速温敏性MNH 水凝胶的收缩,从而实现Ag+的脱附。MoS2的引入,赋予了该水凝胶对于Ag+特异性吸附的能力,更重要的是,通过高效率的光热转化操作,便可以实现Ag+的快速吸附与脱附,历经五次循环,其吸附效率仍能保持在90%以上。同时,根据软硬酸碱理论,MNH 水凝胶对含有Hg2+、Au+、Ag+等软酸金属离子都有一定的吸附能力,所以该水凝胶更适宜于针对Ag+含量相对较高的工业污水进行离子富集。该水凝胶对Ag+的最大吸附容量为40.5 mg·g−1,虽然吸附容量相对较小,但通过光热转化效应,便可以快捷、高效地脱附Ag+。其脱附过程更为简单,且无须洗脱液,作为一种高效的吸附剂有望应用于Ag+的快速富集与分离。
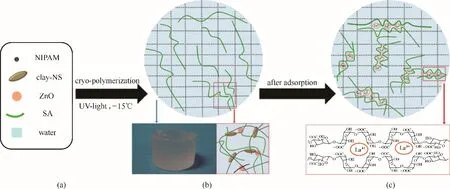
图3 PNIPAm−clay复合水凝胶制备过程和La3+吸附过程(a)预聚液中的所有成分(SA代表海藻酸钠);(b)PNIPAm−clay纳米复合晶胶的形成(−15℃),自立式晶胶(−15℃)的光学照片以及半互穿网络;(c)吸附后,由于La3+与海藻酸钠高分子链中的G组分的强螯合作用,两种聚合物网络相互交织,半互穿网络转变为互穿聚合物网络[50]Fig.3 Preparation process and La3+adsorption of PNIPAm−clay nanocomposite hydrogel(a)all of the components of the precursor solution(SA denotes sodium alginate);(b)formation of the PNIPAm−clay nanocomposite cryogel(−15℃),a photograph of a self−standing cryogel(−15℃),and a schematic diagram of the semi−IPN;(c)after adsorption,the two types of polymer networks are intertwined,semi−IPN changes to be an interpenetrating polymer network;demonstrated is a scheme of the strong chelating action between La3+and G blocks in the alginate chains[50]
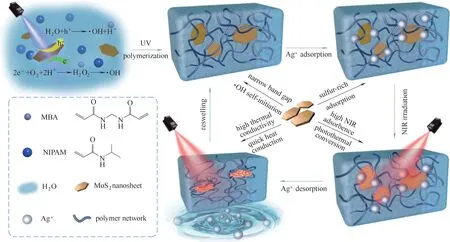
图4 充分利用多功能MoS2实现从水凝胶的制备到近红外光控制吸附−脱附循环的示意图[62]Fig.4 Schematic illustration of the utilization of multi−functional MoS2 from fabrication of the hydrogel to the NIR manipulated adsorption−desorption cycle[62]
4 用于重金属离子分离与富集的水凝胶材料
随着现代工业的不断发展,以铅、铬、汞、镉等为代表的重金属元素被大量排入土壤、湖泊和河流等水体中,最后汇入海洋,会对人体以及自然环境造成严重的危害。有效富集和分离水环境中的重金属离子,对于保护环境和人类健康具有相当重要的意义[63]。
铅元素(Pb)属于ⅣA 重金属元素,也是一种毒性较强的物质。研究表明,铅离子(Pb2+)对人体的神经系统、生殖系统、免疫系统等都会造成严重的伤害[64−65]。然而,铅在蓄电池、冶金、电焊等工业领域中被大量应用,导致每年都会有大量的含铅废水被排放到环境中[66−67],而其中的Pb2+就会通过水和食物链富集进入人体内。因此,去除环境中的Pb2+具有非常重要的意义。相比膜分离、化学沉淀、离子交换等方法,吸附由于其高效、易操作和吸附剂来源广泛等优点,成为一种简便且行之有效的方法。然而,大多数吸附剂对Pb2+并没有特异选择性,而实现Pb2+的选择性吸附不仅可以保护环境,而且可以对Pb2+回收再利用。所以,特异性地富集Pb2+具有重要意义。Ju 等[68]提出以苯并−18−冠−6 丙烯酰胺(B18C6Am)冠醚为功能基团,制备得到一种具有Pb2+吸附特性的水凝胶。以N−异丙基丙烯酰胺(NIPAM)和B18C6Am 为单体,N,N−亚甲基双丙烯酰胺为交联剂,偶氮二异丁基脒二盐酸盐为引发剂,在70℃的温度条件下,通过自由基共聚反应制备得到聚(N−异丙基丙烯酰胺−共聚−苯并18 冠−6丙烯酰胺)(P(NIPAM−co−B18C6Am))水凝胶。冠醚作为水凝胶中的活性位点,其能够选择性地与Pb2+形成稳定的B18C6Am/Pb2+络合物,从而实现对Pb2+的 特 异 性 识 别 和 吸 附。 此 外,P(NIPAM−co−B18C6Am)水凝胶还可以通过响应环境温度,实现Pb2+的智能捕获和释放。如图5所示,当环境温度低于LCST 时,水凝胶中的高分子网络处于舒展状态,水凝胶可以特异性吸附Pb2+;当环境温度高于LCST时,水凝胶内部的高分子网络急剧收缩、变得疏水,冠醚与Pb2+之间的结合常数显著下降,使得Pb2+解吸。通过响应环境温度,该水凝胶可以实现对Pb2+的特异性吸附与解吸,在23℃时,其最大吸附容量为142 mg·g−1。通过温度控制,便可以实现P(NIPAM−co−B18C6Am)水凝胶的吸附/脱附循环,无须使用其他洗脱液,智能化的响应过程简化了脱附过程。因此,其作为一种温度响应型Pb2+吸附材料,在Pb2+富集与分离领域具有较好的应用前景。
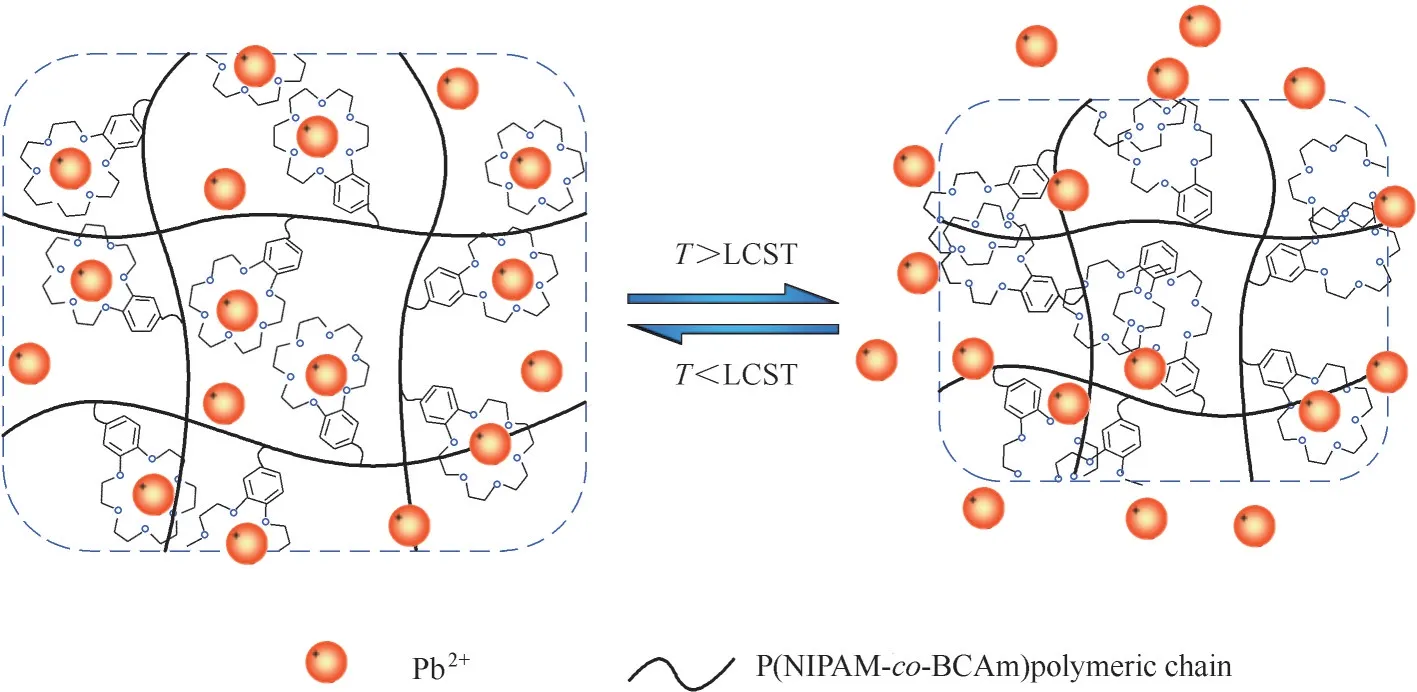
图5 P(NIPAM−co−BCAm)水凝胶针对Pb2+的温敏性吸附/解吸示意图:当温度低于LCST时吸附,当温度高于LCST时解吸[68]Fig.5 Schematic illustration of the thermo−responsive adsorption/desorption behavior of P(NIPAM−co−BCAm)hydrogel towards Pb2+ions,which exhibits adsorption at temperature lower than the LCST and desorption at temperature higher than the LCST[68]
汞元素(Hg)属于ⅡB 过渡金属元素,也是一种生活中常见的重金属元素。近年来,汞的高毒性以及长期存在于水溶液中的特点引起了研究人员的注意。清除存在于水环境中的汞离子(Hg2+),对环境保护具有重要意义[69−70]。Zhuang 等[71]利用二硫化钼(MoS2)和还原氧化石墨烯(rGO)的协同效应,制备得到一种对Hg2+具有特异性吸附能力的水凝胶。利用水热法,直接一步反应得到二硫化钼−还原氧化石墨烯(MoS2−rGO)水凝胶。在制备过程中MoS2会以氧化石墨烯表面的含氧组分为成核位点,从而形成异质界面的三维MoS2−rGO 水凝胶。当环境溶液中存在Hg2+时,MoS2与rGO会分别与Hg2+形成Hg−S 键与Hg−O 键,又由于协同效应的存在,水凝胶对Hg2+的吸附容量与效率会比单片层rGO 或MoS2更优。通过改变原料配比,可以调控水凝胶内部MoS2与rGO 的堆叠和聚集形式,导致异质界面面积的变化,从而影响Hg2+的吸附容量。在多金属离子(含Zn2+、Co2+、Pb2+等)溶液环境中,MoS2−rGO 水凝胶对Hg2+具有最高的移除率(接近100%),其对Hg2+的分配系数比其余金属离子高出4~5 个数量级,因此具有较好的选择性。不同于传统的吸附剂材料,该水凝胶可以被轻易地固定,由重力驱动的过滤过程可以完成水凝胶的吸附与脱附。六次吸附/脱附循环实验后,其仍能保持80%的吸附效率。MoS2−rGO水凝胶的最大吸附容量达到340 mg·g−1,同时对Hg2+具有较好的选择性,有望用于水环境中Hg2+的吸附。
离子吸附剂的吸附性能往往与环境中的pH 密切相关。表1列出了各种水凝胶吸附剂材料的最大吸附容量和与之对应的吸附条件,可为新型水凝胶吸附剂的开发与应用提供一定的参考
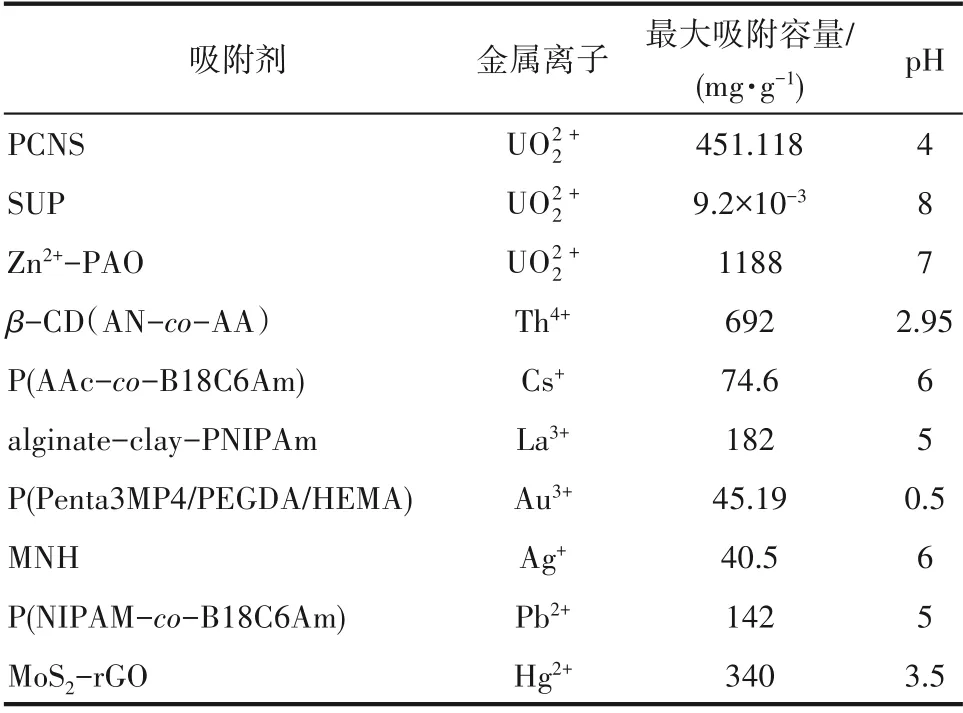
表1 水凝胶吸附剂对不同金属离子吸附容量及其吸附条件Table 1 Adsorption capacity and adsorption conditions of hydrogel adsorbent on different metal ions
5 结 论
水凝胶材料作为一种极具前途的吸附剂,在金属离子分离领域有着非常重要的应用。通过主客体分子识别作用或金属离子配位作用,水凝胶可以从环境中吸附特定的金属离子,从而实现对金属离子的分离与富集。它具有制备成本低、分离效率高且分离过程不产生二次污染等优点。目前,研究人员利用各种水凝胶材料,对放射性金属离子、稀土金属离子、贵重金属离子和重金属离子等实现了较好的分离效果;但是,目前仍然有一些问题亟需解决。例如,部分水凝胶材料对离子吸附/脱附的重复性较差,往往五次以后,吸附容量就会出现显著下降;部分水凝胶的吸附过程比较烦琐且耗时较长;一些水凝胶材料的制备过程相对复杂,工业化放大的难度较高;一些水凝胶吸附剂材料对在实际分离体系中的实验和探讨较少。因此,开发制备方法简单、重复性好、吸附/脱附效率高且易于工业化放大的水凝胶材料作为吸附剂,对于进一步促进环境的保护和实现资源的回收利用具有重要意义。而且,随着高强度、抗疲劳、自愈合水凝胶材料研究的不断深入,在保证离子吸附效率和吸附容量的前提下,提升水凝胶吸附剂的力学性能,对其在工业领域的应用大有裨益。
