超声弹性成像联合超微血流成像校正BI-RADS分类的临床价值
2020-09-04罗春月刘观成何广敏
李 涛 罗春月 刘观成 何广敏
目前,乳腺癌是威胁女性健康的首要恶性肿瘤,每年新发患者约27.9万[1]。超声作为诊断乳腺癌首选的医学影像学方法,现多采用乳腺影像报告和数据系统(breast imaging reporting and data system,BI-RADS)作为定性诊断的依据[2],但BI-RADS 是以超声二维图像特征作为主要分类标准,而组织硬度的变化及血供特点等反映肿瘤性质的重要指标并未纳入。超微血流成像(super microvascular imaging,SMI)是一种探测低速血流的新技术,可在无需造影剂的情况下对微血管进行成像,并对血流丰富程度进行精确分级。超声弹性成像(ultrasound elastography,UE)通过采集组织压缩时应变分布的变化差异,借助彩色编码来反映组织的硬度,从而可对乳腺肿块良恶性进行鉴别[3]。本研究应用UE 联合SMI 对BI-RADS 分类进行校正,探讨二者联合应用在提高鉴别诊断乳腺良、恶性肿块中的临床价值。
资料与方法
一、研究对象
选取 2018 年 12 月至 2019 年 9 月我院经手术病理诊断的乳腺肿块患者82例,均为女性,年龄17~76岁,平均(45.70±11.26)岁。单发78例,多发4例,共计86个病灶,最大径0.80~5.52 cm,平均(2.15±1.03)cm。其中良性病灶40 个,包括纤维腺瘤20 个,腺病13 个,炎性肉芽肿和导管内乳头状瘤各3 个,脓肿1 个;恶性病灶46 个,包括浸润性导管癌39个,髓样癌5个,导管内癌和小叶癌各1个。
纳入标准:①乳腺肿块在术前常规超声BI-RADS分类为3~5 类;②术后有明确的病理结果;③均行UE及SMI检查。排除标准:①哺乳期或妊娠期患者;②乳腺假体植入或探测区域有疤痕的患者;③检查前接受过穿刺活检、旋切手术或乳腺病灶局部切除的患者;④有全身性疾病不能耐受检查的患者。本研究经我院医学伦理委员会批准,所有患者均签署知情同意书。
二、仪器与方法
1.超声检查:使用日本东芝Aplio 500 彩色多普勒超声诊断仪,线阵探头,频率5~14 MHz;配备UE、SMI功能。常规超声检查记录乳腺肿块的二维及彩色血流特征,根据第5 版BI-RADS 对乳腺病灶分类;行UE检查,探头垂直皮肤,轻施压力,启动Elasto,取样框不小于病灶面积的2 倍,嘱患者屏气,待获取理想质控波形时冻结并存储图像;取乳腺肿块二维图像的最大切面,切换至SMI 功能,量程设定为1.0 cm/s,调高彩色增益至较好地显示小血管且不出现噪声,存储实时动态图像。
2.常规超声 BI-RADS 分类标准及 UE 联合 SMI 校正BI-RADS分类的标准
(1)为了保证常规超声BI-RADS 分类的一致性,参考 Kwak 等[4]提出的 BI-RADS 分类方法并结合本研究小组的既往经验制定本研究的BI-RADS 分类标准如下:将形态不规则、垂直位、边界高回声晕、边缘不光整、混合回声、后方回声衰减、周边组织受压改变、微钙化及导管扩张作为可疑恶性的征象。如果乳腺肿块出现上述特征中的1 项,判定为BI-RADS 4A 类;出现 2 项,判定为 BI-RADS 4B 类;出现 3 项,判定为BI-RADS 4C 类;出现 3 项以上,判定为 5 类;当肿块不属于2类、4类或5类时,判定为3类。
(2)UE 的诊断标准:根据罗葆明等[5]提出的改良UE 5分法进行评分,1~3 分诊断为良性,4~5 分诊断为恶性。
(3)SMI的诊断标准:血流丰富程度依照Adler等[6]制定的半定量标准进行评估:0 级,病灶内未见血流信号;Ⅰ级,少量血流,可见1~2 处点状血流;Ⅱ级,中量血流,可见1条主要血管,长度超过病灶的半径或几条小血管;Ⅲ级,丰富血流,可见4 条以上血管或血管相互连通,交织成网状。其中,0~Ⅰ级为良性病变,Ⅱ~Ⅲ级为恶性病变。
(4)UE 联合SMI校正BI-RADS 分类:当UE 与SMI均提示恶性,除5 类保持不变,其余分类则上调一级;当UE 与SMI 均提示良性,除3 类保持不变,其余分类则下调一级;当UE 与SMI 提示的良恶性不一致,则保持原分类不变。
乳腺的常规超声、UE及SMI检查均由同一具有10年以上乳腺超声诊断经验的医师独立完成;常规超声BI-RADS分类、UE评分及SMI分级均由两名中级以上乳腺超声研究方向的超声医师在未知病理结果的情况下共同完成,若结果不一致,则提交研究小组会诊后决定。
三、统计学处理
应用SPSS 19.0统计软件,计数资料以频数或百分比表示,组间比较行χ2检验;以病理结果为诊断金标准,绘制受试者工作特征(ROC)曲线,曲线下面积比较行Z检验。P<0.05为差异有统计学意义。
结 果
一、常规超声及经UE联合SMI校正后的乳腺肿块BI-RADS分类结果
1.良 性病 灶 40 个 ,经 UE 联合 SMI 校正 至 3 类20个,多于校正前;校正前4B类病灶12个,经UE 联合SMI 校正后减少至3 个;4A 类的病灶个数校正前后变化不明显,校正后较校正前少2个;4C 类和5类病灶个数校正前后未改变。
2.恶性病灶 46 个,校正前后均无 3 类病灶;9 个校正前4A类病灶经校正后7个升为4B类,致校正后4A 类病灶个数减少而4B 类病变个数增加;22 个校正前4C 类病灶校正后12 个升为5 类,致校正后5 类病灶个数增加至17 个而4C 类病灶个数减少。校正前后结果见表1和图1,2。

表1 常规超声及UE联合SMI校正后的乳腺病灶BI-RADS分类 个

图1 女,42岁,左侧乳腺病灶常规超声及经UE联合SMI校正后BI-RADS分类
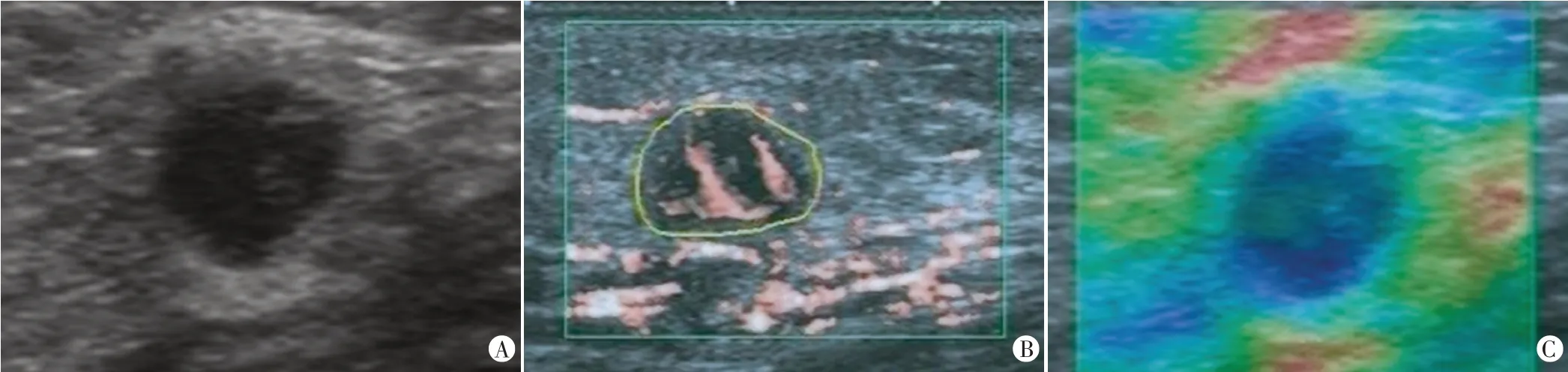
图2 女,53岁,右侧乳腺病灶常规超声及经UE联合SMI校正后BI-RADS分类
二、UE 联合SMI与校正前诊断乳腺病灶良恶性的诊断效能比较
以 BI-RADS 4B 类为诊断截断值,UE 联合 SMI 校正BI-RADS 分类诊断乳腺病灶良恶性敏感性、特异性、准确率、阳性预测值、阴性预测值及曲线下面积分别为95.65%、90.00%、93.02%、91.67%、94.74%、0.954,均高于校正前常规超声BI-RADS 分类的诊断效能(80.43%、67.50%、74.42%、74.00%、75.00%、0.853),差异均有统计学意义(均P<0.05)。见图3和表2,3。

图3 UE联合SMI校正前、后诊断乳腺恶性病灶的ROC曲线图

表2 常规超声BI-RADS分类鉴别乳腺病灶良恶性 个

表3 UE联合SMI校正BI-RADS分类鉴别乳腺病灶良恶性 个
讨 论
为了标准化乳腺超声诊断的报告,减少乳腺超声图像的误读,美国放射学会于2003 年提出BI-RADS,并于2013 年对BI-RADS 各分类恶性可能性的范围进行了改进。BI-RADS 可有效解决对超声操作者的依赖,较为客观地评估肿块,便于超声医师与临床医师进行沟通,有助于临床合理地处理乳腺病灶,因此近年来得到越来越广泛的应用。但BI-RADS 作为一种分类诊断,存在诊断跨度大(3~5 类恶性可能范围2%~95%)、易受医师主观影响[7]及无公认的具体分类标准等缺点。在对乳腺病灶进行分类的过程中,部分乳腺病灶良、恶性超声图像特征不典型,尤其是BI-RADS 3、4 类的良性及恶性病灶存在形态学表现重叠,可能使部分良性病变被高判或恶性病变被低判,导致不必要的活检或影响临床应对决策。因此,如何在BIRADS 分类基本原则的基础上引入新的诊断指标,进一步提高乳腺病灶鉴别诊断的准确性,是非常有意义和值得深入探讨的问题。
本研究使用SMI 的血流分级联合UE 对86 个乳腺病灶的BI-RADS分类进行了校正。研究发现,经UE联合SMI校正后,3类病灶由校正前的9个增加至20个,病理证实均为良性,多出的11 个病灶均为4A 类向下调类得到,因此可使某些4A 类病例的临床应对发生改变,将部分不必要的病理活检调整至定期复查。设定4B类为诊断截断值,校正前4A类27个,诊断准确率为66.67%(18/27),经校正后,9 个被低判的恶性病灶中7 个升为4B类,诊断准确率因此提升至88.89%(16/18)。校正前4B类的22个病灶中10个被高判的良性病灶校正后降至4A 类,由4A 类误升至4B 类的良性病灶仅1 个,导致4B 类病灶的诊断准确率由校正前的45.45%(10/22)上升至85.00%(17/20)。23 个校正前4C 类病灶有 52.17%(12/23)升为 5 类,虽在本研究中 4C 类病灶的分类调整不影响诊断准确率,但确诊乳腺高风险病灶无疑增强了临床处置的信心。86 个乳腺病灶经校正后BI-RADS 分类预测乳腺恶性病灶的ROC 曲线下面积为0.954,明显大于校正前的0.853(P<0.05),分析原因为良性病灶校正后调整至低一级病变个数及恶性病灶校正后调整至高一级病变的个数出现净增加,提示UE 联合SMI 有助于提高BI-RADS 分类的总体诊断效能。经UE 联合SMI 校正后乳腺病灶BI-RADS 分类的敏感性、特异性、准确性、阳性预测值及阴性预测值均高于常规超声BI-RADS 分类的诊断效能(均P<0.05),说明经UE联合SMI校正的BI-RADS分类不仅提高了总体诊断效能,在切点诊断中也具有更高的诊断准确率、更低的漏诊率和误诊率。
值得注意的是,本研究校正后BI-RADS 分类仍存在一些不足之处和容易误漏诊的因素,良性病灶中,有3 个病灶(1 个脓肿和2 个纤维腺瘤)常规超声BIRADS 分类提示恶性病灶未能被UE 联合SMI 有效校正为良性,有1 个(导管内乳头状瘤)常规超声BIRADS 分类良性的病灶却校正为恶性;恶性病灶中,有1 个浸润性导管癌常规超声BI-RADS 分类提示良性,但因乏血供未能被UE 联合SMI 有效校正为恶性。造成误判可能原因有[8-10]:①病灶成分具有多变性和复杂性,如炎性反应引起微血管数量增加及部分乳腺病灶因纤维成分比例较大致硬度偏高等因素会导致良性病灶被误判为恶性;部分恶性病灶因内部无血流信号的坏死区域占比较大,且该区域硬度偏低,使SMI的Adler血流分类及UE评分偏低,造成漏诊;②病灶的大小影响UE和SMI测量的准确性也不可忽视,较大的病灶会使UE 图像的质量下降,影响UE 定性诊断的准确性;另外因SMI评判病灶血流丰富程度采用的是Adler分类方法,病灶过大,会高估供血情况,而病灶过小,则会造成供血情况的低估;③UE 和SMI本身具有局限性。UE 的局限性之一在于假定了应力在弹性介质中是均匀分布的,与组织的实际硬度不均匀分布存在偏差,同时因高频超声探头宽度的限制,随深度的增加会产生应力分散,导致离探头较远的深部肿瘤组织被误认为较硬,增加了肿瘤硬度评判的误差;UE 的另一个局限性是对检查者和诊断者要求较高,在不同检查者之间也容易产生差异。本研究SMI的局限性主要体现在仅观察了病灶单切面的血供情况,并不能反映肿块整体的血供丰富程度,仅将血流分级情况纳入研究,未考虑血管的形态、走行、有无分支等形态学表现的意义,而且与UE 相同的是,SMI也需人为进行分级,存在着不可避免的主观性。 因此,要尽量降低UE 和SMI局限性对乳腺肿块诊断的影响,需标准化UE 检查手法,提高诊断医师UE评分和SMI分级的准确性及多切面采集UE 和SMI,获得比较全面的诊断数据,必要时应结合其他的影像检查手段或超声引导下穿刺活检,以提高诊断准确率。
综上所述,在二维声像图特征的基础上,UE 联合SMI 能显著提高乳腺肿块BI-RADS 分类的诊断效能;在增加诊断信心的同时,可以减少临床上不必要的活检和手术,具有较高的临床应用价值。
