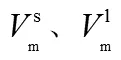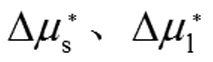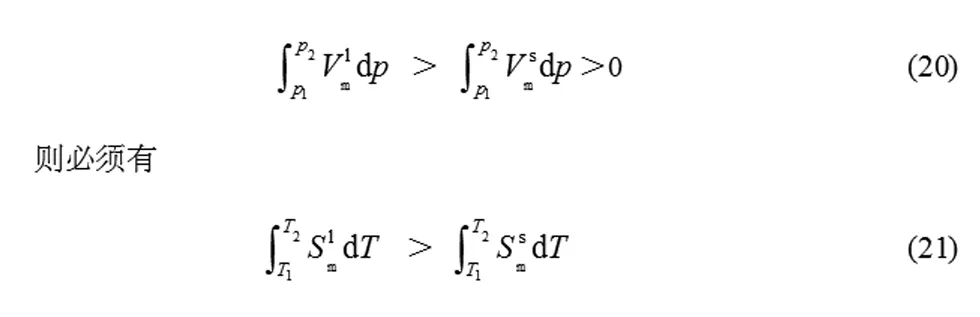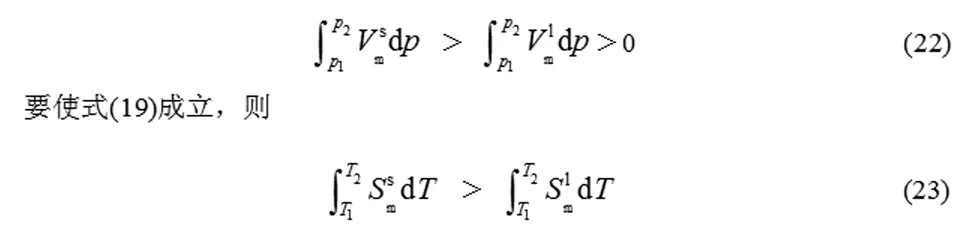纯物质固液平衡—压力对熔点的影响
2020-07-27李俊华曾荣英王成勇
刘 兴,李俊华,曾荣英,聂 雪,王成勇
(衡阳师范学院 化学与材料科学学院,湖南 衡阳 421008)
相平衡是热力学在化学领域中的重要应用。多相系统的相平衡理论在化学、化工的科研和生产中有重要的意义,如溶解、蒸馏、重结晶、萃取、提纯及金相分析等方面都要用到相平衡知识。
在所有相平衡体系中,纯物质(即单组分)体系是最简单的,也是学习和研究二组分及多组分体系相平衡的基础。对于单组分体系,根据相律:f(自由度) =C(组分数) -φ(相数) + 2 = 3-φ,由于相数φ至少为1,所以体系的自由度f最多为2,即体系状态可以由两个独立变量所决定,这两个变量就是T(温度)和p(压力)。纯物质的T-p相图比较简单,常温常压范围内主要由三条两相平衡线组成,这三条两相平衡线即气—液平衡、气—固平衡和固—液平衡,对于纯物质的两相平衡,有一个描述p、T之间关系的重要方程式—Clapeyron 方程,基于该方程现行物理化学教材一般对纯物质气—液平衡进行了比较多的介绍[1-2],包括Clasius-Clapeyron方程、外压对蒸汽压的影响等,我们知道,其它条件一定,当外压(通常是大气压)增大时纯物质的沸点会升高。熔点与沸点一样是物质的基本物理性质之一,关于压力对纯物质的熔点的影响,教材一般未作介绍,这里我们从Clapeyron 方程和化学势两个方面对纯物质熔点受压力的影响进行了理论上的推导和讨论。
1 从Clapeyron 方程讨论
由纯物质气—固平衡的Clapeyron 方程[3-6](以下下标“fus”代表“熔化过程”):

设在压力为p1、p2时,纯物质的熔点分别为T1、T2,ΔfusH、ΔfusV分别为熔化焓和熔化过程体积变化且ΔfusH、ΔfusV在T∈[T1,T2] 与温度T无关,积分上式,
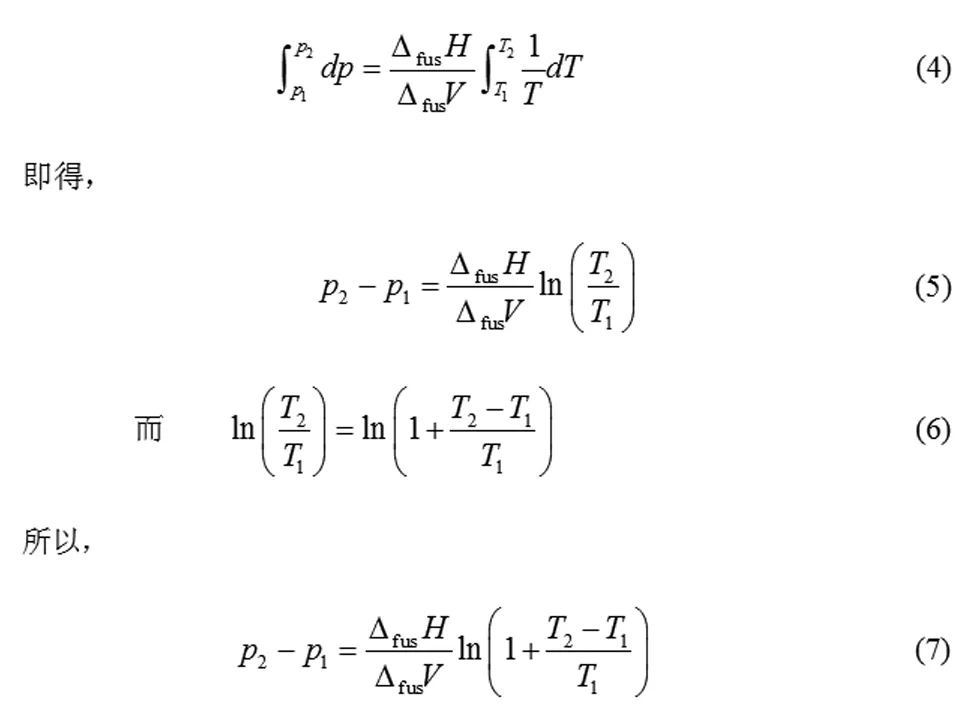
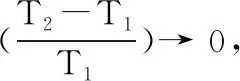
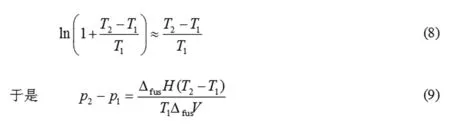


对于大多数纯物质而言,液态摩尔体积Vm(l) >固态摩尔体积Vm(s),即ΔfusV>0,且熔化过程ΔfusH>0。由式(10)可知,当p2>p1,T2>T1,即当体系的压力增大时,熔点升高。
对于Vm(l) 一定温度(T1)和压力(p1)下,固液两相平衡的纯物质(“*”表示纯物质),其固相和液相的化学势相等,即 下列分情况讨论: 以上与前面从Clapeyron 方程讨论的结果一致。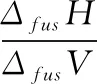
2 从化学势讨论[7]