中国南海海绵Ircinia sp.中化学成分的研究
2020-07-15王玲莉于欢张冬丽乔卫唐生安
王玲莉,于欢,张冬丽,乔卫,唐生安
(天津医科大学药学院天然药物学系,天津市临床药物关键技术重点实验室,天津300070)
海绵是一种进化了7 亿~8 亿年的古老多细胞动物,广泛分布在各种水域中。它作为一种静止不动的海洋生物,能产生多种次生代谢产物,作为对抗微生物及捕食者的化学防御物质[1]。寻常海绵纲的Ircinia属海绵能释放低分子量的挥发性化合物,使它们具有难闻的蒜臭味[2]。目前已经从该属海绵分离得到甾体、萜烯、内酯和生物碱等多种类型成分[3-5]。这些化学成分具有抗肿瘤、抗寄生虫和抗菌等多种生物活性[5-8]。本文采用多种现代分离纯化色谱技术及波谱解析方法,对采自中国广西涠洲岛海域的Ircinia属海绵进行提取分离和结构鉴定,通过与已报道的文献数据进行分析对比,确定了5 个化合物的结构信息。
1 材料与方法
1.1 仪器、试剂和材料 Brucker AV 400 核磁共振仪(TMS 内标);旋光仪:MC 241 digital polarimeter(PERKIN-ELMER);液质联用色谱仪:Alliance 2695,Quattro Micro TM ESI(Waters);半制备高效液相色谱仪:日本分光公司(JASCO),PU-2089(泵),RI-2031 和UV-2075(检测器);制备HPLC 色谱柱:YMC-Pack SIL SL12S05-2510WT(10 mm×250 mm);有机溶剂均为天津市化学试剂一厂分析纯产品;高效液相色谱所用试剂均为本实验室精馏自制;氘代试剂均为Cambrige Isotope Laboratories,Inc.USA 生产。
本文所用海绵采自中国广西壮族自治区涠洲岛海域,经天津医科大学药学院唐生安副教授鉴定为南海海绵Irciniasp.,样本编号为WZA-16,存放于天津医科大学药学院。
1.2 提取分离 将海绵Irciniasp.(干重463.0 g)粉碎,加95%乙醇进行回流提取(2 L×3),合并提取液并减压浓缩,得到总浸膏,加水混悬,依次用水饱和的二氯甲烷、正丁醇萃取,分别得到二氯甲烷萃取物19.0 g,正丁醇萃取物6.0 g。
将WZA-16 二氯甲烷萃取物用ODS-A 柱进行梯度洗脱,依次加入洗脱液为甲醇:水(5:5、6:4、7:3、8:2、9:1)、甲醇、乙酸乙酯、甲醇(加5%冰醋酸),得到14 个组分0101~0114。0109(5.0 g)组分经HW-40 凝胶柱,以二氯甲烷:甲醇=2:1 为流动相,得组分0201~0206。将0204~0206(4.0 g)合并,过正相硅胶柱,以二氯甲烷:乙酸乙酯:甲醇(8:0.3:0.1→8:1:0.5),二氯甲烷:甲醇(4:1),甲醇为流动相,得组分0301~0315。取0306(51.3 mg)经ODS-A 柱分离,以甲醇:水(9:1),甲醇为流动相,得组分0501~0509。将0305(308.3 mg)合并,经ODS-A 柱分离,以甲醇:水(85:15),甲醇为流动相,得组分0601~0612。
将0505~0506(28.0 mg)合并后经正相HPLC,以二氯甲烷:乙酸乙酯:甲醇(10:2:0.5)为流动相,得单体1、2 和3。将0603 和0605 经上述方法,分别得单体4 和5。
2 结果
从南海海绵Irciniasp. 提取物中分离得到5 个化合物,见图1。
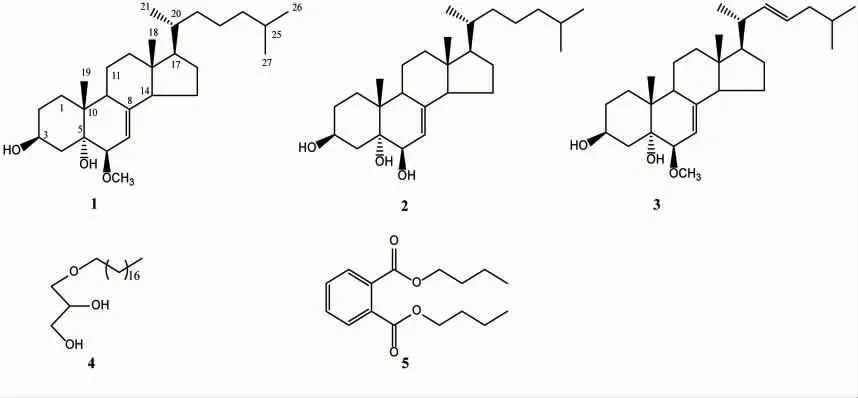
图1 从南海海绵Ircinia sp.中分离得到的化合物Fig1 Compounds 1-5 isolated from the South China Sea marine sponge Ircinia sp
2.1 化合物1,白色无定形粉末 EI-MS 给出分子离子峰为m/z:432 [M]+,结合1H NMR 和13C NMR 谱推测其分子式为:C28H48O3。分析1H NMR谱(CDCl3, 400 MHz),发现有1 个烯质子信号δH5.41(1H, br d,J=2.4Hz, H-7),1 个甲氧基质子信号[δH3.39(3H,s,6-OCH3)],2 个含氧次甲基质子信号[δH4.07(1H,m,H-3),3.18(1H,br d,J=4.4 Hz,H-6)],5 个甲基质子信号[δH0.59(3H, s, H-18),0.86(3H,d,J=6.8 Hz,H-27),0.87(3H,d,J=6.8 Hz,H-26),0.93(3H,d,J=6.4 Hz,H-21),1.00(3H,s,H-19)]。13C NMR(CDCl3, 100 MHz)谱和DEPT 谱给出了28个碳信号,其中有6 个甲基碳信号(δC12.1, 18.4, 18.8, 22.2,22.9, 58.3),10 个sp3杂化的亚甲基碳信号(δC22.2,23.0, 23.9, 27.8, 30.9, 32.8, 36.1, 39.5, 39.5, 39.6),2 个sp3杂化的含氧次甲基碳信号(δC67.9,82.5),5 个sp3杂化的次甲基碳信号(δC28.0, 36.2,43.9, 54.9, 58.2),1 个sp3杂化的含氧季碳信号(δC76.4),1 个sp2杂化的次甲基碳信号(δC115.0),1 个sp2杂化的季碳信号(δC143.7)。通过与文献报道的化合物的波谱数据进行比较,发现化合物1 与已知化合物cholest-7-en-6R-methoxy-3S,5R-diol 的结构一致,故化合物1 被鉴定为cholest-7-en-6Rmethoxy-3S,5R-diol[9]。
2.2 化合物2,无定形粉末 ESI-MS 给出准分子离子峰为m/z:419[M+H]+。1H NMR 谱(CDCl3,400 MHz)显示,1 个烯质子信号δH5.65(1H, br s, H-7),2 个含氧次甲基质子信号[δH4.06(1H, m, H-3), 3.50(1H, br s, H-6)],5 个甲基质子信号[δH0.59(3H, s,H-18), 0.86(3H, d,J=6.8 Hz, H-27), 0.87(3H, d,J=6.8 Hz,H-26),0.93(3H,d,J=6.4 Hz,H-21),0.95(3H,s, H-19)]。化合物2 的氢谱与碳谱与化合物1 基本一致,不同之处在于氢谱中化合物2 没有甲氧基的信号,并且H-6 的化学位移向低场位移至3.50;另外,碳谱中C-6 的化学位移由化合物1 的δC82.5,向高场位移至化合物2 的δC77.8,并且化合物2 的碳谱中也无甲氧基碳信号存在。因此,可以推断化合物2 的C-6 位为羟基取代,与文献报道的cholest-7-en-3S,5R,6R-triol 的结构一致,故化合物
2 被鉴定为cholest-7-en-3S,5R,6R-triol[10]。
2.3 化合物3,白色无定形粉末 ESI-MS 给出准分子离子峰为m/z:431 [M+H]+。1H NMR 谱(CDCl3,400 MHz)给出1 个甲氧基质子信号δH3.17(3H, s,CH3O-6)], 2 个含氧次甲基质子信号[δH4.08(1H, m,H-3), 3.01 (1H, br d, H-6)];5 个甲基质子信号[δH0.59(3H, s, CH3-18), 0.85(3H, d,J=6.4 Hz,H-27), 0.87(3H, d,J=6.8 Hz, CH3-26), 0.92(3H, d,J=6.8 Hz, CH3-21), 1.02(3H, s, CH3-19)];3 个烯质子信号[δH5.41(1H, br d, H-7), 5.19(2H, m, H-22, H-23)]。氢谱数据显示化合物3 与化合物1 非常相似,区别为在于化合物3 在H-22 和H-23 位为双键,多了两个烯质子。通过与文献报道化合物的波谱数据进行比较,发现化合物3 与已知化合物cholest-7-en-6R-methoxy-3S,5R-diol 的结构一致,故化合物3 被鉴定为cholest-7-en-6Rmethoxy-3S,5R-diol[9]。
2.4 化合物4,白色固体 EI-MS 给出分子离子峰为m/z:344 [M]+,结合1H NMR 和13C NMR 光谱推测其分子式为:C21H44O3。1H NMR 谱(CDCl3,400 MHz)数据显示16 个侧链次甲基质子信号δH1.26~1.57(32H, m),7 个连氧碳上质子信号[δH3.86(1H, m)和3.71(1H, dd,J=3.7, 11.4 Hz),3.62(1H, dd,J=5.4, 11.4 Hz), 3.52~3.45(4H, m)],2 个羟基质子信号δH2.67(2H, br s),1 个甲基质子信号δH0.88(3H, t,J=6.4 Hz)。13C NMR(CDCl3, 100MHz)谱给出了21 个碳信号,分别为:δC72.6(C-1),71.9(C-2),64.4(C-3),70.4(C-1’),29.4(C-2’),26.1(C-3’),29.7(C-4’~C-15’),22.7(C-16’),31.94(C-17’),14.1(C-18’)。通过与文献报道的化合物的波谱数据进行比较,发现化合物4 与已知化合物鲨肝醇的结构一致,故化合物4 被鉴定为鲨肝醇[11]。
2.5 化合物5,淡黄色油状物 ESI-MS 给出准分子离子峰为m/z:279[M+H]+,结合1H NMR 和13C NMR 光谱推测其分子式为:C16H22O4。1H NMR(400 MHz, CDCl3)谱给出4 个芳香氢质子信号[δH7.64(2H,m,H-3,H-6),7.46(2H,m,H-4,H-5)],4 个连氧碳上质子信号δH4.23(4H,t,J=6.7 Hz,H-1’,H-1”),8 个饱和碳上质子信号[δH1.64 (4H, m, H-2’,H-2”), 1.38 (4H, m, H-3’, H-3”)],2 个甲基信号δH0.89(6H, t,J=7.4 Hz, H-4’, H-4”)。通过与文献报道的化合物的波谱数据进行比较,发现化合物5与已知化合物邻苯二甲酸正丁酯的结构一致,故化合物5 被鉴定为邻苯二甲酸正丁酯[12]。
3 讨论
本实验运用各种色谱分离手段,包括硅胶柱色谱、凝胶柱色谱和半制备高效液相色谱等现代分离技术手段,从采集自中国涠洲岛海域的海绵生物Irciniasp.的二氯甲烷提取部位中获得5 个化合物。再经过核磁共振波谱、质谱等方法,确定了这5 个化合物的化学结构。通过与文献数据中的氢谱、碳谱数据对比分析,确定了Irciniasp.中分离的5 个化合物分别是cholest-7-en-6R-methoxy-3S,5R-diol(1),cholest-7-en-3S,5R,6R-triol(2),cholest-7,22-dien-6R-methoxy-3S,5R-diol(3),鲨肝醇(4)和邻苯二甲酸丁酯(5)。其中化合物1~3 为首次从该属海绵中分离得到。本文的研究成果使Ircinia属海绵的化学多样性得以丰富,尤其是扩充了甾体类化合物的结构内容,对进一步研究该属海绵的类似单体成分提供了理论支持,为寻找甾体类新药的先导化合物,开发海洋药物提供了结构依据。
