基于侧向磁泳的微流控芯片对两种磁性纳米球的同时分选
2020-07-06张作然张志凌
张作然, 张 利, 张志凌
(武汉大学化学与分子科学学院, 武汉 430072)
磁分选与微流控芯片技术相结合在生化分析中应用广泛, 目前已被用于细胞[1~10]、 细菌[11~13]、 核酸[14,15]及外泌体[16,17]等的分选. 增强被分选目标物受到的磁场力可缩短分选时间并提高分析通量. 借助微流控芯片平台, 目标物受到的磁场力可通过以下方式来增强: 使用电磁铁替代常规永磁体, 可提供更强且可控的磁场[18,19], 但由于线圈会产生大量焦耳热, 散热问题较难解决; 另一种策略是在微通道附近整合铁磁性微结构[8,20]. 由于磁性物质与缓冲相之间的相对磁导率相差很大[μr(Ni)≈200,μr(buffer)≈1], 施加外加磁场后, 铁磁性微结构局部可形成很高的磁场梯度. 其中, Ni带微结构已成功用于分选细胞[4,7,21]、 细菌[11]与RNA[14].
近年来, 随着微流控技术的发展, 多种目标物的磁分选受到广泛关注. 目前, 已逐步实现多种靶细胞分选, 如Adams等[21]通过精细设计芯片, 实现了2种靶细胞的磁分选. Kang等[22]通过掺杂Mn, Fe及Co元素优化磁性探针的磁响应性, 并将其分别特异性修饰在不同细胞上, 实现了芯片上不同类别靶细胞的同时磁分选.
由于单个细胞可结合大量磁性探针, 不同靶细胞间的磁响应性差异因磁性探针的增多而放大. 对于纳米尺度的目标物, 如蛋白质、 核酸及外泌体等, 单个目标物最多仅能结合一个磁性探针. 因此, 实现多种纳米尺度目标物分选的关键是在单颗粒水平上分选不同磁性的探针. 由于单个磁性探针之间的磁响应性差异较小, 对不同磁响应性探针的分选是研究的难点. 此外, 为实现多种磁性探针的磁分选, 需要更深入地探讨不同磁性探针在微通道内的运动差异. 然而, 目前关于芯片上磁分选的理论分析仍停留在单个磁球的受力分析上[11,21]. 多种磁性探针的磁分选仍然面临挑战.
本文提出了一种利用微流控芯片上侧向磁泳的策略, 成功分选了2种不同磁响应性的磁性纳米球. 首先提出了分析磁球侧向位移的理论(包括聚集与偏移), 可以更直观地分析磁球在芯片上的运动. 结合运动分析与实验现象, 获得磁响应性不同的磁性纳米球的侧向位移差异. 基于此, 设计微流控芯片系统, 实现了样品中2种磁球的依次分选, 二者的分选效果均可接受, 且实验操作简单. 该芯片系统被成功应用于乙型肝炎病毒(HBV)DNA与丙型肝炎病毒(HCV)反转录DNA的同时分选.
1 实验部分
1.1 试剂与仪器
光刻胶AZ 9260与SU-8 2015购自美国Electronic Materials公司; 聚二甲基硅氧烷(PDMS, RTV615)购自美国Momentive公司; 磁流体MF01购于中国华达臻远有限公司; 氧化铟锡(ITO)玻璃购自中国昱虹光电有限公司; 牛血清蛋白(BSA)购自中国瀚文生物公司; 1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC)、 正硅酸乙酯(TEOS)和3-氨丙基三乙氧基硅烷(APTES)均购自Sigma-Aldrich公司; 链霉亲和素(SA)购于美国VWR公司; 以上试剂均为分析纯. 分散于正己烷中的量子点(QDs)及链霉亲和素修饰的量子点(SA-QDs)购于中国武汉珈源量子点公司. 实验所用DNA购自中国生工公司, 其DNA序列见表1.

Table 1 Sequences of DNA
G-17型光刻机(Lithography), 中国成都鑫南光公司; TE2000-U型倒置荧光显微镜, 日本尼康公司; 铁铷硼(FeRbB)永磁体(60 mm×9 mm×2 mm, 60 mm×20 mm×4 mm), 中国宏昌磁电有限公司; BST200型高精度磁强计, 中国科力华电子有限公司; LSP02型微量恒流注射泵, 中国兰格有限公司; FL-3型荧光分光光度计, 法国Horiba公司.
1.2 实验过程
利用组装法合成磁性纳米球[23]. 磁响应性强的磁球通过组装5层磁性纳米颗粒获得, 根据组装磁性纳米颗粒的层数命名为5-MNs. 磁响应性弱的磁球通过组装1层磁性纳米颗粒获得, 命名为1-MNs(图S1, 见本文支持信息). 为了借助荧光信号考察磁球的分离效果, 同时制备了荧光磁性纳米球. 分别将红色荧光和绿色荧光量子点(QDs)通过组装法组装至磁球外层, 得到具有红色荧光的磁球5-RMNs与1-RMNs, 以及具有绿色荧光的1-GMNs. 然后, 用TEOS与APTES对这些磁球进行硅烷化处理. 最后, 将磁球分散于N,N′-二甲基甲酰胺(DMF)中, 并与琥珀酸酐反应2.5 h, 得到表面富含羧基的磁球. 用无水乙醇洗涤除去剩余的DMF后, 将磁球分散在超纯水中保存. 磁球的浓度约为 25 mg/mL.
将捕获DNA(Capture-DNA)通过链霉亲和素与生物素的特异性结合作用修饰在磁球上. 首先, 在磁球上修饰链霉亲和素. 取1-MNs与5-MNs各40 μL, 经磁分选后分散于400 μL 0.01 mol/L PBS缓冲液(pH=7.2)中. 向体系中加入4 mg EDC和10 μg的链霉亲和素(图S2, 见本文支持信息), 在37 ℃摇床(150 r/min)中反应4 h. 反应结束后, 用0.01 mol/L PBS缓冲液(pH=7.2)清洗磁球3次, 分散于PBS缓冲液中, 磁球表面即修饰上链霉亲和素. 表面修饰完成后, 在5-MNs体系中加入5 μL capture-HBV(100 mmol/L)制得capture-HBV-5-MNs体系; 在1-MNs体系中加入5 μL capture-HCV(100 mmol/L)制得capture-HCV-1-MNs体系(图S2). 置于37 ℃摇床(150 r/min)中反应40 min. 最后, 用0.01 mol/L Tris-HCV缓冲液(pH=8.0)重悬磁球3次, 除去过量的capture-DNA. 所得产物于4 ℃保存备用.
实验所用微流控芯片为PDMS芯片, 分为Ni带层与流体通道层. Ni带层的制作步骤如下: 在ITO玻璃的导电一侧旋涂一层12 μm厚的AZ9260光刻胶, 通过光刻与显影暴露出Ni带图案处的ITO玻璃导电层; 经电镀得到约12 μm高的Ni带微结构; 最后用无水乙醇洗去光刻胶层. 采用软光刻法制作流体通道层[24]. 旋涂一层极薄的PDMS层(4500 r/min, 30 s)封装Ni带结构; 置于75 ℃烘箱中3 h固化表面的PDMS, 然后与流体通道层键合.
借助荧光光谱技术考察了磁球的分离效果. 实验前, 将MNs用质量分数为1%的BSA蛋白溶液封闭30 min以避免非特异性吸附. 将含有质量分数为0.5%的BSA蛋白的Tris缓冲液(0.01 mol/L, pH=8.0)由缓冲入口(Buffer inlet)通入芯片系统(Scheme 1); 将1-GMNs与5-RMNs混合后从样品入口(Sample inlet)通入芯片系统40 min. 样品相、 缓冲相1与缓冲相2的流速分别为5, 30和5 μL/min. 实验条件下, 微通道中可形成稳定的层流, 当施加外加磁场时Ni带微结构会被磁化, Ni带的局部会形成很高的磁场梯度. 样品相中的5-MNs与1-MNs依次在芯片1(Chip 1)与芯片2(Chip 2)上磁偏移至缓冲相中. 经磁分离后, 在芯片系统的出口1(Outlet 1)与出口2(Outlet 2)处分别收集5-MNs与1-MNs. 将出口处收集物重悬成100 μL溶液, 分别用荧光分光光度计测定其荧光光谱.
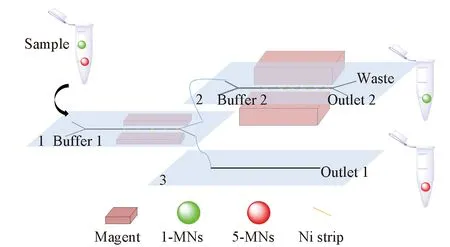
Scheme 1 Schematic of microfluidic chip system
作为方法展示, 将该芯片系统用于分选2种目标DNA. 用1% BSA溶液封闭capture-HBV-5-MNs与capture-HCV-1-MNs, 而后将2种捕获DNA修饰的磁球加入到混有HBV与HCV的样品中, 最终体系为30 μg/mL 5-MNs+60 μg/mL 1-MNs+200 mmol/L Tris缓冲液+300 mmol/L NaCl+5 mmol/L MgSO4+0.05%吐温20. 将该体系置于摇床中反应40 min后, 从芯片的样品入口通入40 min, 实验条件与上步相同. 从出口1, 出口2与废弃物出口流出的反应体系首先收集在一组试管中, 记为组1, 而后收集另一批, 记为组2. 将过量的probe-HBV加入组1中, 过量的probe-HCV加入组2中, 分别置于摇床中反应40 min. 去除过量probe-DNA后, 分别加入SA-QDs, 反应40 min. 最后测定组1和组2的荧光光谱, 以分析target-HBV与target-HCV在芯片各出口的分布.
2 结果与讨论
2.1 磁纳米球的表征
TEM照片表明, 2种磁球在样品中分散均匀, 且粒径均一[图1(A)和(D)]; 1-MNs与5-MNs的粒径均约为350 nm[图1(B)和(E)], 2种磁球的尺寸及体积基本一致. 由磁滞回线[图1(C)]可知, 1-MNs与5-MNs的饱和磁化强度分别为6.8与34.1 A·m2·kg-1, 二者的磁响应性差异较大, 并且在室温下均表现出超顺磁性. 由磁性纳米球的荧光光谱[图1(F)]可见, 1-GMNs与5-RMNs的荧光光谱峰形对称, 且荧光峰不重叠.
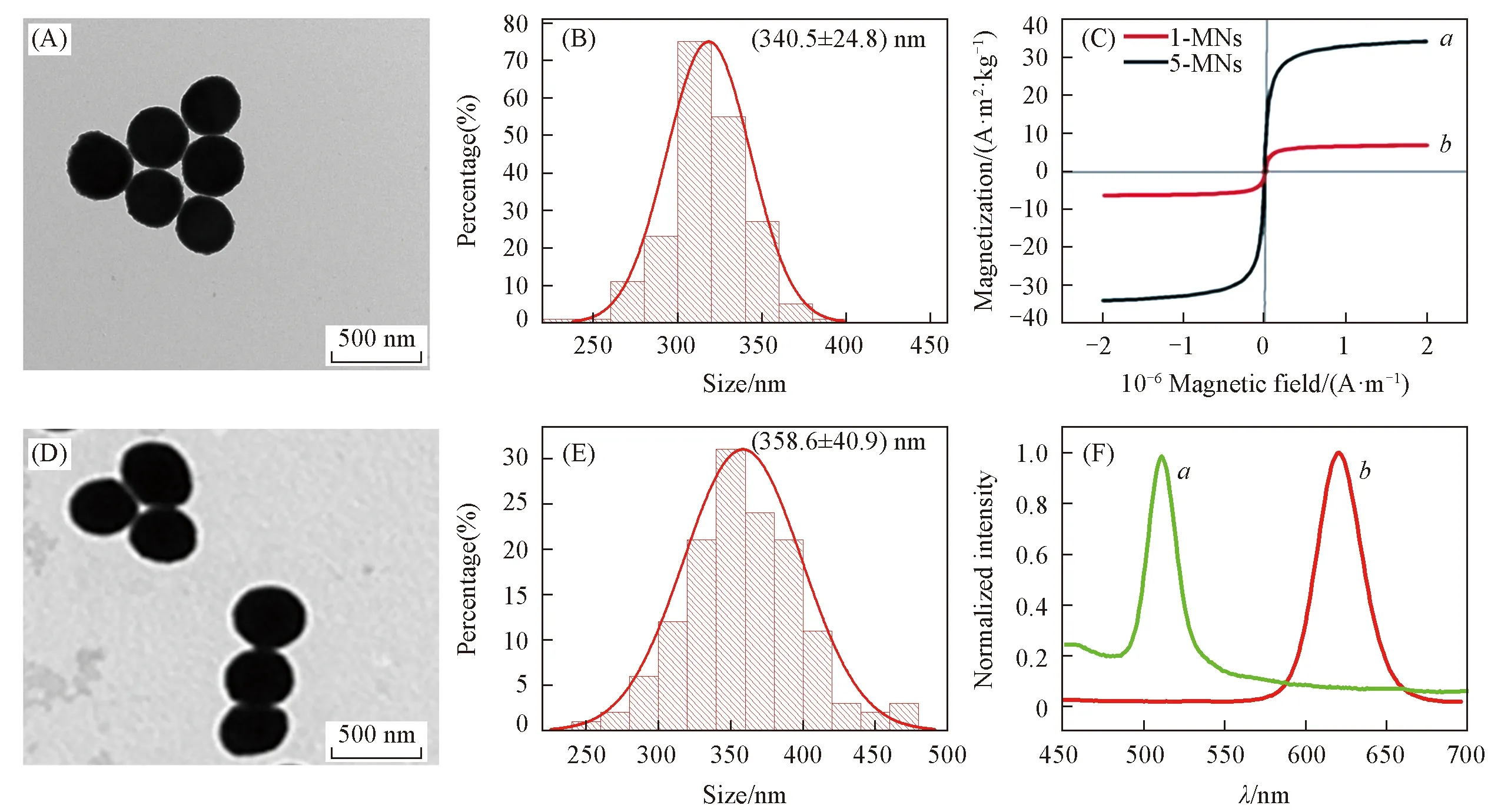
Fig.1 Characterization of beads with strong magnetic responsiveness(5-MNs) andweak magnetic responsiveness(1-MNs)(A, D) TEM images; (B, E) particle size statistics of 1-MNs(A, B) and 5-MNS(D, E); (C) magnetic hysteresis loops for 5-MNs(a) and 1-MNs(b); (F) fluorescence spectra of 1-GMNs(a) and 5-RMNs(b).
2.2 磁球在芯片上运动的理论分析
实验所用磁场通过芯片下方水平对置的2个尺寸相同的永磁体提供, 因此微通道内的磁场可近似为匀强磁场. 使用磁强计测得磁感应强度B约为0.48 T. 通过COMSOL Multiphysics 6.4软件模拟芯片中的磁场梯度(B)分布. 当施加外加磁场时, Ni带与缓冲液之间会形成很高的磁场梯度(图2).
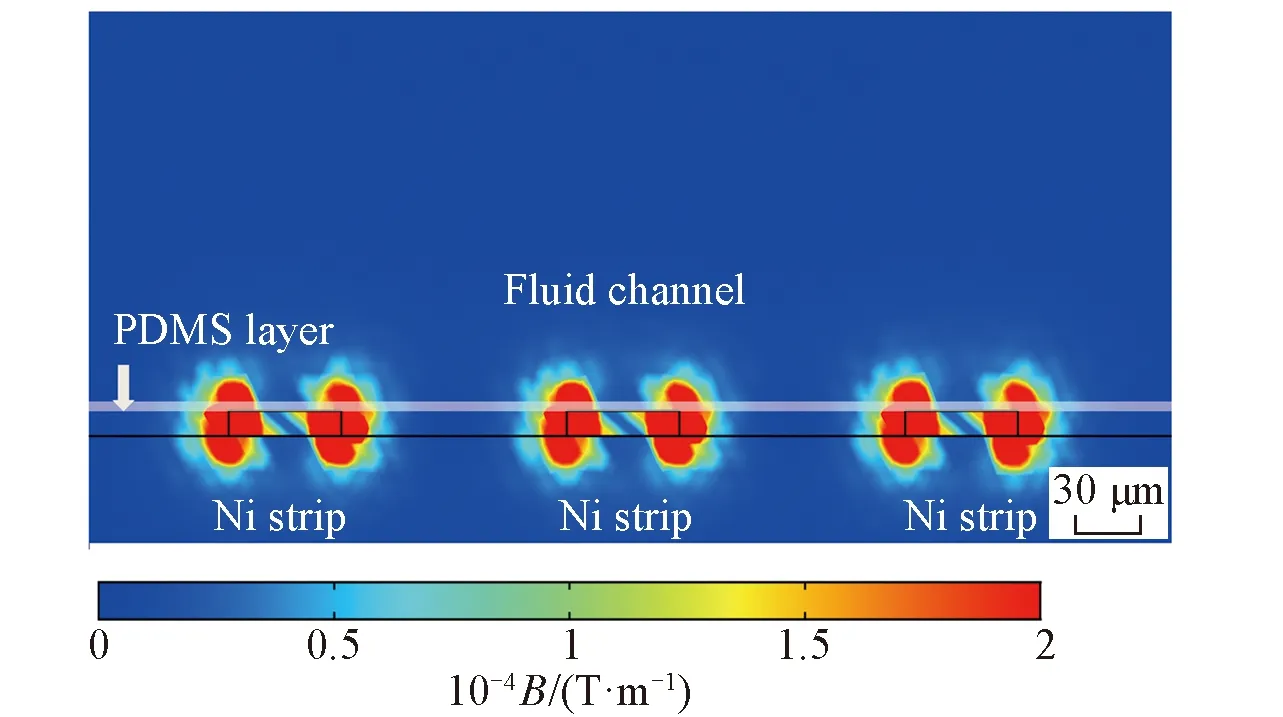
Fig.2 Simulation result of the magnetic fieldgradient(B) around Ni stripsEach Ni strips was 50 μm in width and 11 μm in height. The interval between Ni strips was 100 μm. The thickness of ITO glass under the Ni strips was 1.1 mm. Ni strips were covered by an extremely thin PDMS layer. The fluid channel was above the Ni strips.
微通道内的磁性颗粒分别受到磁场力Fm与流体黏滞力Fd的作用.Fm作用方向[25]与Ni带垂直, 计算公式如下:
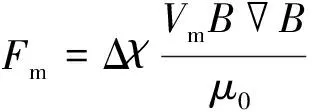
式中: Δχ为磁性颗粒与介质之间的磁化率差异;Vm(m3)为磁球体积;B(T)为磁感应强度;B(T/m)为磁场梯度;μ0(4π×10-7H/m)为真空磁导率. 流体黏滞力Fd可由斯托克斯力计算:
Fd=6πrηΔv=6πrη(v0-v) (2)
式中:r(m)为磁性颗粒的半径; Δv(m/s)为磁性颗粒与流体之间的速度差;v0(m/s)为流体的速度;ν(m/s)为磁性颗粒的速度;η(kg·m-1·s-1)为流体的表观黏度.
通过磁场力与流体黏滞力的共同作用, 磁球从样品相被推入缓冲相中. 当磁场力足够大时, 磁球会沿Ni带运动. 如图3(A)所示, 设Ni带与x方向夹角为β, 磁球与x方向夹角为α, 则0<α≤β.
微通道内的磁球会很快达到匀速运动, 于是Fdy=Fmy. 磁场力在y方向的分速度为Fmy=Fmcosβ, 因此磁球在y方向和x方向上的速度分别为
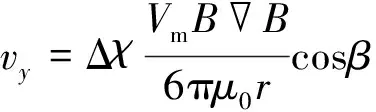
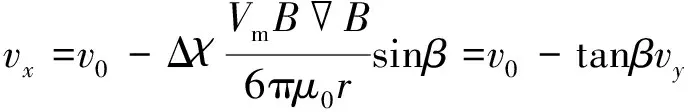
假定在一个极短的横向位移dx内, 磁球的速度不变, 于是:
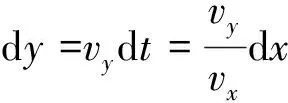
在对大量磁球进行磁分选时, 磁球磁化后会相互吸引而形成团簇[图3(B)]. 磁化形成的团簇与单个磁球的磁偏移性质差异非常大[26]. 下面通过一个简单的模型分析磁化形成团簇前后的性质差异.
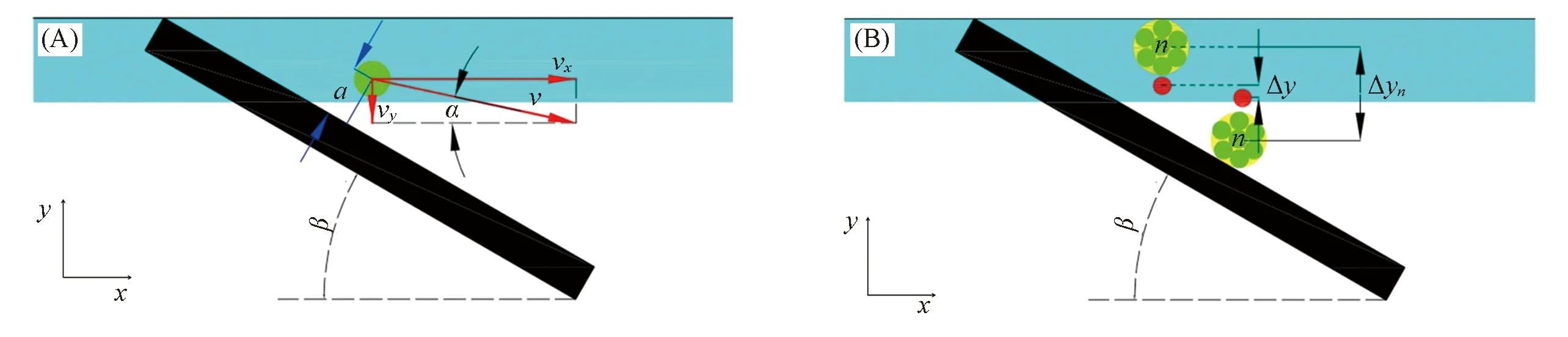
Fig.3 Motion analysis of MNs(A) Velocity analysis of a single MNs; (B) the motion of magnetic composited particles.
假设一个团簇由n个MNs组成, 那么:
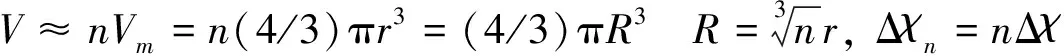
式中:R(m)是将团簇颗粒近似为球的半径;V(m3)是团簇颗粒近似为球的体积.
团簇颗粒的x与y方向速度计算方式与单个磁球类似, 即
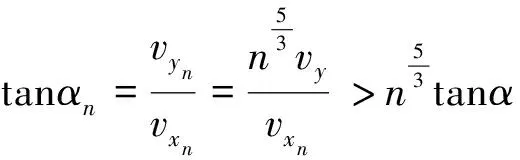
团簇颗粒与单颗粒侧向瞬时位移的差距为
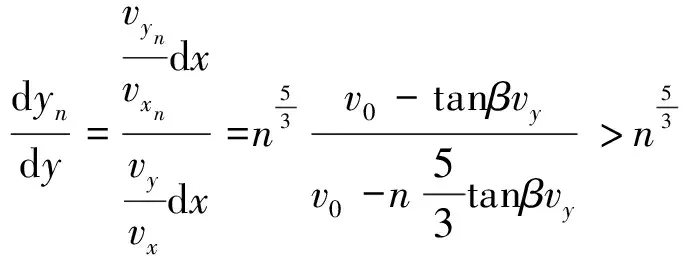
由式(7)可知, 磁化后团簇颗粒的偏移角度会随着n增大而迅速增加, 直至α=β. 越大的团簇颗粒越容易沿着Ni带偏移. 由式(8)可知, 聚集的MNs与单个MNs侧向位移差异非常大. 流体黏滞力的改变导致聚集前后MNs的侧向磁偏移存在差异. 相对于磁化前分散的磁球群体, 团簇所受的磁场力为各磁球所受磁场力的矢量和, 而流体黏滞力对磁球的作用则因聚集而降低. 磁球与流体之间会产生更大的速度差来维持流体黏滞力与磁场力的平衡, 于是团簇在x方向上的速度更慢, 在y方向上的速度更快, 磁球团簇与x方向的运动夹角也会增大, 从而更易沿着Ni带发生侧向磁偏移. 因此, 磁球的磁化聚集是磁分选中一个非常关键的因素.
利用侧向磁泳分离5-MNs与1-MNs, 需分析磁球在分选中的侧向磁偏移差异. 后续实验考察了2种磁球的侧向磁偏移. 施加外加磁场后, 磁球会相互磁化并形成微米级颗粒[图4(B)和(C)], 这些颗粒沿Ni带运动, 这与式(7)结论相同. 磁球磁化的聚集程度随流速增大而逐渐减小[图4(D)~(F)]. 但是, 1-GMNs与5-RMNs的聚集程度随着流速增大而减小的趋势却不同[图4(G)~(I)]. 当流速较低时, 1-GMNs与5-RMNs均聚集成微米颗粒沿着Ni带偏移, 而样品相流速升高至5 μL/min, 缓冲相流速升高至30 μL/min时, 5-RMNs仍然沿着Ni带偏移, 1-GMNs却未形成可见的微米级颗粒. 由图4(I)所示荧光图可知, 5-RMNs几乎完全偏移至出口1(Outlet 1)处, 而很少有1-GMNs出现在出口1处. 因此可以认为, 1个磁化颗粒中5-MNs的数量(n5)大于1-MNs的数量(n1).

Fig.4 On-chip movement of 5-RMNs and 1-GMN at different flow rates(A) Structure of the chip; (B)—(F) images were taken in a bright field; (B) without magnetic field, MNs did not move along the Ni strips; (C) when an external magnetic field was added, the MNs became magnetized and clumped into visible micro-sized particles; (D)—(F) images of the motion of MNs at different flow rates; (G)—(I) fluorescence field images and fluorescence spectra of the fluorescent MNs collected at each outlet.
结合上述讨论与结果分析了磁化对1-MNs与5-MNs侧向磁偏移的影响. 为简化分析, 理论上仅考虑5-MNs之间的磁化及1-MNs之间的磁化.
当流速约为35 μL/min时,n5>n1. 5-MNs与1-MNs磁响应性差异很大, 由式(3)可知,v5y>v1y, 由支持信息中的推导证明存在如下不等式:
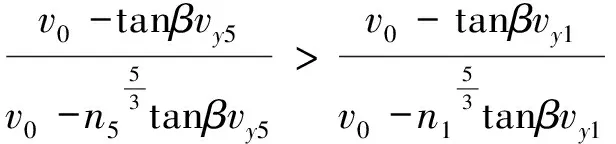
由式(8)与式(9)可得
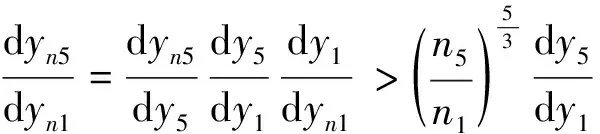
由式(10)可知, 在特定流速下5-MNs与1-MNs的侧向位移差异会因为磁化后聚集程度的不同而显著放大. 理论上5-MNs与1-MNs可以在含有Ni带结构的芯片上分离. 当流速更低时, 1-MNs会更加集中并沿着Ni带偏移[图4(G)和(H)]. 将5-MNs从样品相与1-MNs中分选后, 1-MNs可在更低流速下从样品相中分选出来.
2.3 芯片设计
基于以上分析结果设计了一个芯片系统用于分选5-MNs与1-MNs. 该芯片系统由3块芯片组成(见Scheme 1), 芯片1与芯片2含有Ni带结构, 分别用于5-MNs与1-MNs的分选, 芯片3用于平衡整个芯片系统的流体阻力.
芯片1与芯片2采用通用的连续磁分选芯片结构[8,11,14], 二者的Ni带结构相同(图S3, 见本文支持信息). 流体通道的高度均约为40 μm. 为了达到更好的分选效果, 芯片1宽度为1000 μm, 而芯片2设计在更低的流速下工作, 宽度为1500 μm.
2.4 不同磁响应性磁球的分选效果
将5-RMNs与1-GMNs混合作为样品通入芯片系统, 通过测定芯片出口处收集溶液的荧光光谱分析磁球的分离效果.
实验考察了1-MNs与5-MNs之间的相互磁化对分选的影响. 首先将1-RMNs作为样品通入芯片1并分选, 然后将5-MNs与1-RMNs按照质量浓度比1∶1混合后以相同流速通入芯片. 样品的荧光强度经荧光峰扣除背景后得到, 分离效率通过对应出口处样品的荧光强度与所有出口处样品的荧光强度之和的百分比进行估算. 由于磁球间的相互磁化, 约17%的1-RMNs被偏移至出口1[图5(B)]. 相互磁化对分选的影响可通过调控5-MNs与1-MNs的质量浓度比来降低[图5(B)~(D)]. 当5-MNs与1-RMNs的质量浓度比为1∶2 时, 仅有较少的1-RMNs偏移至出口1, 因此采用该条件进行后续实验.
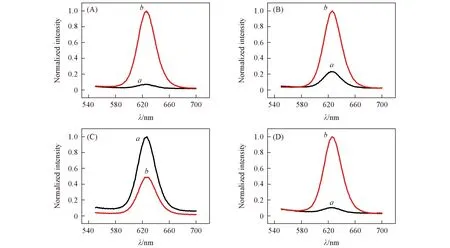
Fig.5 Fluorescence spectra of samplesThe flow rate of the sample was 5 μL/min and of the buffer was 30 μL/min. (A) Sample with only 1-RMNs; (B)—(D) samples with 5-MNs/1-RMNs mass ratios of 1∶1, 2∶1, 1∶2, respectively. a. Outlet 1; b. outlet 2.
采用芯片1分离5-RMNs与1-GMNs, 由图6(A)和(B)所示荧光光谱图可知, 5-RMNs与1-GMNs可被有效分离. 当样品流速为5 μL/min, 缓冲相流速为30 μL/min时, 会有约14%的1-GMNs偏移至出口1[图6(A)]. 随着缓冲相流速逐渐增加, 偏移至出口1的1-GMNs更少, 同时5-RMNs的分选效果下降. 其原因是随着流速升高, 磁球通过Ni带结构的时间减少, 并且磁化聚集程度减弱. 因此, 缓冲相流速为35 μL/min时, 5-MNs可在芯片1上得到有效分离[图6(C)]. 为了进一步将1-MNs从样品中分离, 设计了芯片2并考察1-GMNs在其上的分离效果. 图6(D)结果表明, 当样品流速为5 μL/min, 缓冲相流速为5 μL/min时, 1-GMNs可以得到有效分离.
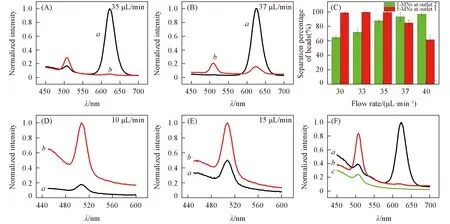
Fig.6 Separation efficiency of 5-RMNs and 1-GMNsOutlet 1 collected 5-MNs and outlet 2 collected 1-MNs. (A), (B) Separation efficiency of 5-RMNs and 1-GMNs by chip 1. (A) Flow rates: sample 5 μL/min, buffer 30 μL/min; (B) flow rates: sample 5 μL/min, buffer 32 μL/min; (C) relative separation percentages of 1-GMNs and 5-RMNs with flow rates by chip 1. Standard deviation was calculated from three experimental runs; (D), (E) separation efficiency of 1-GMNs by chip 2; (D) flow rates: sample 5 μL/min, buffer 5 μL/min; (E) flow rates: sample 5 μL/min, buffer 10 μL/min; (F) separation efficiency of 5-RMNs and 1-GMNs for the chip system. a. Outlet 1; b. outlet 2; c. waste.
为了将5-RMNs与1-GMNs同时从样品中分离, 连接芯片1与芯片2构成芯片系统, 考察了该系统对磁球的分离效果. 如图6(F)所示, 当样品流速为5 μL/min, 缓冲相1流速为30 μL/min, 缓冲相2的流速为5 μL/min时, 5-RMNs完全偏移至出口1处, 同时有18%的1-GMNs偏移至出口1, 出口2处基本为1-GMNs. 图6(F)所示荧光光谱中500~550 nm处的荧光峰表明, 有少量的1-GMNs未偏移至出口2而分布于废弃物出口.
总的来说, 所构建的基于微流控芯片的磁分选系统可实现对5-MNs与1-MNs的高效分选. 5-MNs可在出口1处收集, 1-MNs可在出口2处收集. 2种磁球的分选效果均可接受. 其中, 样品中的5-MNs可被完全分选, 从而减少珍贵样品在分选过程中的损失.
2.5 样品中HBV与HCV目标DNA的同时分选
将该磁分选系统用于乙型肝炎病毒(HBV)的DNA与丙型肝炎病毒(HCV)的反转录DNA的同时分选. 用2种磁响应性不同的磁球分别特异性捕获HBV的DNA与HCV的反转录DNA后, 通入芯片系统进行分选. 分选后, 收集各出口处的溶液并分别依次加入生物素修饰的探针DNA(Probe-DNA)和SA-QDs, 反应后测定溶液的荧光光谱, 可得到各出口处HBV与HCV目标DNA的荧光分布图. 如图7所示, HBV的目标DNA被分选于出口1处, HCV的目标DNA多数被分选于出口2, 少量的HCV出现在出口1, 2种目标DNA的分离效果均较好.
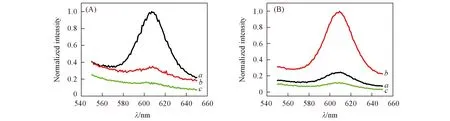
Fig.7 Separation of target DNA of HBV and HCV from the sampleDistributions of HBV DNA(A) and HCV complementary DNA(B) at outlet 1(a), outlet 2(b) and the waste outlet(c).
3 结 论
利用侧向磁泳实现了在微流控芯片上分选强磁响应性(5-MNs)与弱磁响应性(1-MNs)的磁性纳米球. 提出基于磁球侧向位移差异的理论用以解释实验现象. 分选实验操作简易, 且2种磁球的分选效果均可接受, 其中强磁响应性的球可被完全分选, 能减小分选中珍贵样品的损失. 将该芯片分选系统成功用于分选HBV与HCV的目标DNA. 这个多种目标物分选芯片系统在蛋白组学、 基因组学等领域有着广阔的应用前景.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/cjcu20200080.
